Количественная масс-спектрометрия в диагностике гриппа и контроле действия лекарственного препарата "Триазавирин"
Автор: А. В. Протасов, Р. А. Бубляев, О. А. Миргородская
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Системный анализ приборов и измерительных методик
Статья в выпуске: 1 т.30, 2020 года.
Бесплатный доступ
Для совершенствования методов диагностики и лечения заболевания гриппом в настоящей работе проведены количественные масс-спектрометрические исследования активности двух основных карбоксипептидаз — ангиотензинпревращающего фермента и карбоксипептидазы-N. Проведены сравнения уровней активности этих пептидаз для здоровых и инфицированных вирусом гриппа A/Aichi/2/68 (H3N2) мышей, а также для мышей, пролеченных экспериментальным противогриппозным препаратом "Триазавирин". Анализ, подобный продемонстрированному в данной работе, может быть с успехом использован при сравнительной оценке эффективности и других антигриппозных препаратов, а также для понимания направления их воздействия на инфицированный организм.
Ангиотензин I, ангиотензинпревращающий фермент, карбоксипептидаза N, брадикинин, количественная масс-спектрометрия,
Короткий адрес: https://sciup.org/142221539
IDR: 142221539 | УДК: 543.51: 577.1: 66.096.3 | DOI: 10.18358/np-30-1-i5561
Фрагмент статьи Количественная масс-спектрометрия в диагностике гриппа и контроле действия лекарственного препарата "Триазавирин"
ВЫВОДЫ
Наиболее значимые изменения активности пептидаз происходят в бронхиальных смывах, нежели в сыворотках крови больных животных. Введение препарата здоровому животному приводит к увеличению активности АПФ, но в значительно меньшей степени по сравнению с инфицированными животными. При введении препарата больным животным происходит заметное снижение активности АПФ до уровня, соответствующего здоровым животным. Это говорит об избирательности воздействия препарата на ренин-ангиотензиновую систему. По результатам работы можно сделать общий вывод о том, что подобный скрининг может быть с успехом использован при сравнительной оценке эффективности и других антигриппозных препаратов, а также для понимания направления их воздействия на инфицированный организм.
Quantitative mass spectrometry in diagnostics of influenza and control of action of the medicinal product "Triazavirine"
To improve the methods for diagnosing and treating influenza, we performed quantitative mass spectrometric studies of the activity of two main carboxypeptidases — angiotensin-converting enzyme and carboxypeptidase-N. The comparison of activity levels of these peptidases was carried out for mice both healthy and influenza A/Aichi/2/68 (H3N2) virus infected, as well as for treated with the experimental triazavirin anti-influenza drug. An analysis similar to the fulfilled in this work can be successfully used in a comparative assessment of the effectiveness of other anti-influenza drugs, as well as to understand the direction of their effect on the infected organism.
Текст научной статьи Количественная масс-спектрометрия в диагностике гриппа и контроле действия лекарственного препарата "Триазавирин"
Грипп в различных его формах в виде сезонных вспышек или пандемий остается серьезной проблемой общественного здравоохранения. Инфекция гриппа у человека может протекать по-разному: от бессимптомной инфекции до осложненных форм, включая тяжелую вирусную пневмонию и обострение имеющихся хронических заболеваний. Сезонные эпидемии гриппа ежегодно могут поражать до 15 % населения. Это указывает на важность создания новых и улучшения существующих вакцин и лекарств.
Вирус гриппа заражает в основном эпителиальные клетки верхних дыхательных путей, распространяясь затем и на клетки нижних дыхательных путей. Значительное число пораженных клеток, возникающее при недостаточном иммунном ответе организма, собственно, и приводит к нарушению функции органов и систем органов, в первую очередь нервной и сердечно-сосудистой систем. Эти нарушения проявляются в общих и локальных изменениях в регуляции кровоснабжения органов и тканей.
В регуляции кровяного давления и водно-солевого баланса принимает участие ренин-ангио-тензиновая система, которая является наиболее важной и достаточно хорошо изученной. Участником этой системы является ангиотензин II — конечный продукт каскада протеолитических процессов. Свое влияние ангиотензин II оказывает через ангиотензиновые рецепторы, являющиеся медиаторами основного сосудосуживающего эф- фекта, включающего вазоконстрикцию, синтез и секрецию альдостерона, секрецию вазопрессина, запуск норадренергической активности и регуляцию синтеза ренина в почках. Рецепторы ангиотензина II обнаружены в сердце, кровеносных сосудах, почках, надпочечниках, легких и головном мозге. Ангиотензин II образуется из ангиотензина I в результате отщепления двух C-концевых аминокислот ангиотензинпревращающим ферментом (АПФ).
Помимо ангиотензина I, АПФ гидролизует и другие пептиды плазмы крови, а также инактивирует пептид, обладающий сосудорасширяющим действием, — брадикинин [1]. Брадикинин играет важную роль в регуляции кровообращения в условиях острых воспалительных реакций различного патогенеза [2]. Он является одним из самых сильных сосудорасширяющих средств в организме, повышает проницаемость капилляров и способствует выходу жидкости из кровеносного сосуда (вызывает отек). С этой точки зрения брадикинин вместе с гистамином и простагландинами относят к медиаторам воспаления.
В метаболизме брадикинина, помимо АПФ, участвуют еще по крайней мере две протеиназы — аминопептидаза P и неприлизин (карбоксипептидаза N), которые отличаются продуктами гидролиза. АПФ расщепляет связь (7–8), а аминопептидаза и карбоксипептидаза отщепляют соответственно N и C концевые аминокислоты.
Таким образом, активность протеиназ, участвующих в метаболизме ангиотензина I и брадикинина в тканях дыхательных путей, будет отражать развитие патологического процесса при гриппе, что и являлось предметом изучения в настоящей работе.
Оптимальным материалом для исследования можно считать бронхиальный смыв — лаваж. Традиционно активность пептидаз измеряют с использованием хромогенных или флюорогенных субстратов, а также в условиях сложных смесей в присутствии ингибиторов. Однако выбор и синтез специальных субстратов и ингибиторов сам по себе является сложной задачей [3]. Кроме того, упомянутые протеиназы относятся к металлопротеиназам, что указывает на то, что можно ожидать перекрестного действия ингибиторов. Поэтому в данной работе использовались нативные субстраты, активность во времени которых измерялась методом количественной масс-спектрометрии, ранее разработанным и опробованным авторами [4, 5].
МАТЕРИАЛЫ И МЕТОДЫ
Тестируемые препараты
Исследуемый препарат "Триазавирин", предоставлен ООО "Завод Медсинтез".
Экспериментальные животные
Белые беспородные мыши предоставлены питомником Рапполово, Ленинградская область. Вес животных 16–18 г.
Животных содержали в стандартных условиях в соответствии с методическими документами, используемыми при работе. Все процедуры с животными в исследовании были рассмотрены и утверждены Комиссией по биоэтике ФГБУ "НИИ гриппа им. А.А. Смородинцева" Минздрава России на предмет соответствия регулирующим актам.
Вирусы гриппа
Для работы был использован штамм вируса гриппа A/Aichi/2/68 (H3N2), адаптированный к мышам, полученный из рабочей коллекции вирусов ФГБУ "НИИ гриппа им. А.А. Смородинце-ва" Минздрава России.
Введение препарата животным
Препарат "Триазавирин" был использован в дозировке 200 мг/кг, вводился перорально в объеме 0.2 мл один раз в сутки по лечебно-профилактической схеме (за 24, за 1 ч и через 24, 48 и 72 ч после заражения).
Заражение животных и забор проб
Мышей заражали интраназально под легким эфирным наркозом вирусом в дозе 1 МЛД50 на мышь в объеме 50 мкл (МЛД — мышиная летальная доза). На 3-й день после заражения, через 2 ч после введения препарата животных подвергали эвтаназии, забирали кровь и бронхиальный смыв (лаваж).
Получение стандарта из ангиотензина II и брадикинина
Стандарты подготавливались из ангиотензина II и брадикинина ("Sigma-Aldrich"). Навеску 2.1 мг пептида растворяли в 20 мкл 10 % трифторуксусной кислоты (ТФУ, "Sigma-Aldrich") в H 2 18O (97 % 18O, "Cambridge Isotope Laboratories
Andover", MA, USA) и инкубировали в твердотельном термостате при 70 °С в течение 90 мин для протекания изотопного обмена, после чего высушивали в вакуумном испарителе SpeedVac ("Eppendorf"). Содержимое пробирки растворяли в воде и использовали в качестве стандарта для определения концентрации пептидов.
MALDI-TOF масс-спектрометрия
Исследуемые образцы смешивали с матрицей HCCA ("Bruker", Германия), наносили на мишень GroundSteel ("Bruker", Германия) и анализировали на масс-спектрометре MALDI-TOF / TOF ultrafleXtreme ("Bruker", Германия) в режиме обнаружения положительных ионов. Для каждого спектра было суммировано 5000 лазерных импульсов. Идентификация белков проводилась с использованием MASCOT ( для доступа к базе данных NCBI (Национальный центр биотехнологической информации, , в параметрах в качестве переменных модификаций было указано окисление метионинов. Ошибка определения массы была ограничена до 50 ppm.
Условия гидролиза пептидазами
Растворы пептидов ангиотензина I и брадикинина смешивались с сывороткой (разбавление в 25 раз) и лаважем (без разбавления). Смеси инкубировались при 37 °С в течение 15, 40 и 60 мин. Реакция останавливалась добавлением аликвот в 2 % ТФУ. В анализируемые пробы вносился стандарт ожидаемого продукта гидролиза 18О-ангиотен-зин II для ангиотензина I или 18О-брадикинина для брадикинина.
Р ЕЗУЛЬТАТЫ ЭКСПЕРИМЕНТА И ИХ ОБСУЖДЕНИЕ
Общая характеристика
В настоящей работе исследовались образцы сыворотки крови и бронхиальных смывов здоровых и больных мышей. Выбор этих двух биологических сред для сравнительных исследований обусловлен тем, что они позволяют выявить изменения как в составе крови, так и в легких. В результате экспериментов на животных анализировались изменения активности протеаз, которые характеризуют состояние животных при развитии инфекции и в процессе лечения гриппа препаратом "Триазавирин".
В данной работе для нормировки активности ферментов в бронхиальных смывах использовался альбумин, количество которого было определено по указанной методике [4, 5], а для измерения активности карбокспептидаз использовались природные субстраты — ангиотензин I и брадикинин.
Масс-спектрометрический контроль за гидролизом ангиотензина I ангиотензинконвертирующим ферментом в сыворотке и лаваже
На рис. 1 представлены масс-спектры начального гидролиза ангиотензина I в бронхиальных смывах. Показано образование ангиотензина II ( m / z = 1046.6) из внесенного в сыворотку ангиотензина I ( m / z = 1296.8) под действием АПФ. Видно, что при этом в образце отсутствуют продукты гидролиза, не характерные для АПФ.
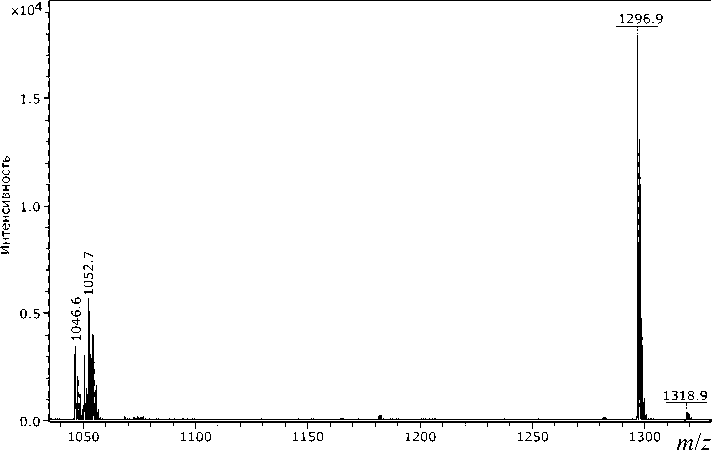
Рис. 1. MALDI-MS ангиотензина I ( m / z = 1296.8) через 40 мин гидролиза пептидазами в лаваже мыши при 37 °С в присутствии стандарта ( m / z = = 1052.7) к ангиотензину II ( m / z = 1046.6)
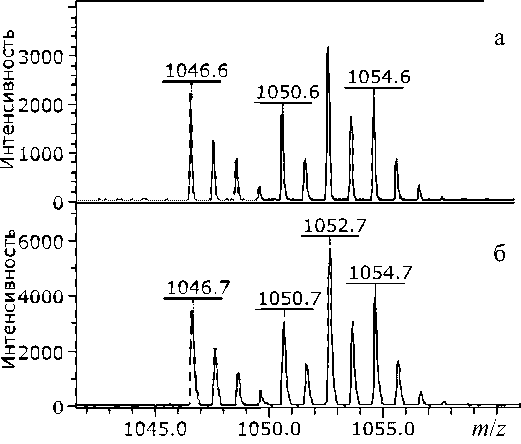
Рис. 2. Фрагменты масс-спектров для ангиотензина II и его стандарта в биологических средах.
а — в сыворотках, б — в бронхиальных смывах
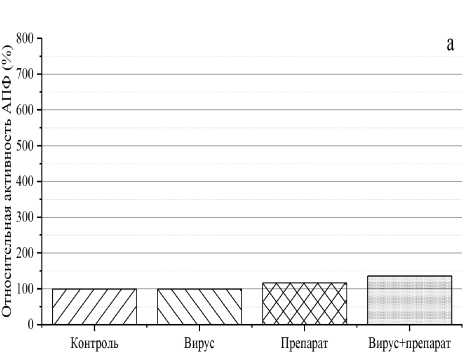
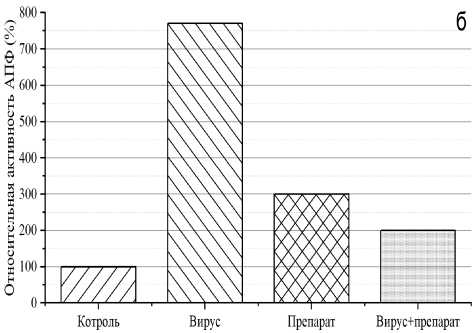
Рис. 3. Активность АПФ в сыворотках (а) и бронхиальных смывах (б) мышей. За 100 % взята активность АПФ у здоровых мышей
На рис. 2 представлены фрагменты масс-спектров гидролизатов для сыворотки (а) и лаважа (б), из которых было рассчитано количество образующегося ангиотензина II, согласно описанной в работе [5] методике.
Полученные данные использовались для вычисления относительной активности АПФ. Результаты этих вычислений представлены на рис. 3. Из рисунка видно, что разница в активности АПФ в сыворотке не столь существенна (разница между здоровой и зараженной особью не превысила 20 %) в отличие от результатов, наблюдаемых на бронхиальных смывах (увеличение активности АПФ в 8 раз у инфицированных мышей и существенное снижение при приеме препарата практически до нормальных значений).
Масс-спектрометрический контроль за гидролизом брадикинина в сыворотке и лаваже
Количественный масс-спектрометрический контроль за концентрацией брадикинина, привнесенного в сыворотку крови и в лаваж, позволил оценить изменение протеолитической активности при вирусной инфекции по сравнению с контролем.
Аналогично описанному выше исследованию по ангиотензину I проведены исследования активности пептидаз в отношении брадикинина. На рис. 4 и 5 представлены результаты исследований гидролиза брадикинина (продукты гидролиза представлены в таблице) в сыворотке и в лаваже.
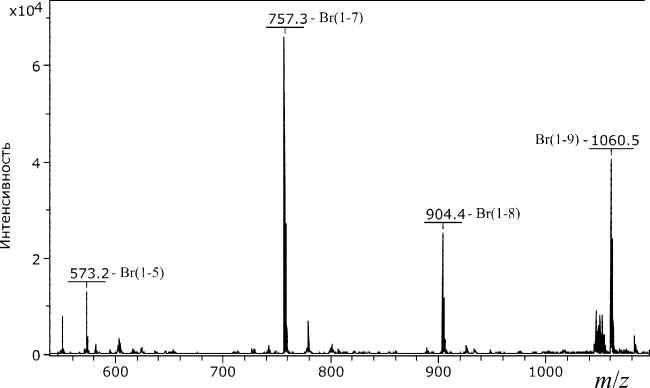
Рис. 4. MALDI-MS брадикинина через 15 мин гидролиза пептидазами в сыворотке крови при 37 °С
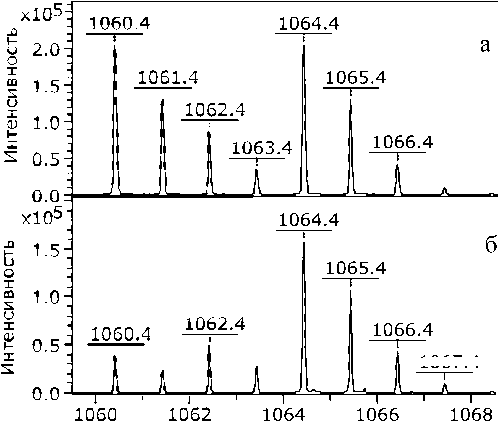
1067.4
m / z
Рис. 5. Фрагменты масс-спектров для брадикинина и его стандарта в биологических средах.
а — в сыворотках, б — в бронхиальных смывах
Аминокислотные последовательности продуктов гидролиза брадикинина
|
Пептид |
Аминокислотная последовательность |
|
Br(1–9) — брадикинин Br(1–8) Br(1–7) Br(1–5) |
Apг-Про-Про-Гли-Фен-Сер-Про-Фен-Apг Apг-Про-Про-Гли-Фен-Сер-Про-Фен Apг-Про-Про-Гли-Фен-Сер-Про Apг-Про-Про-Гли-Фен |
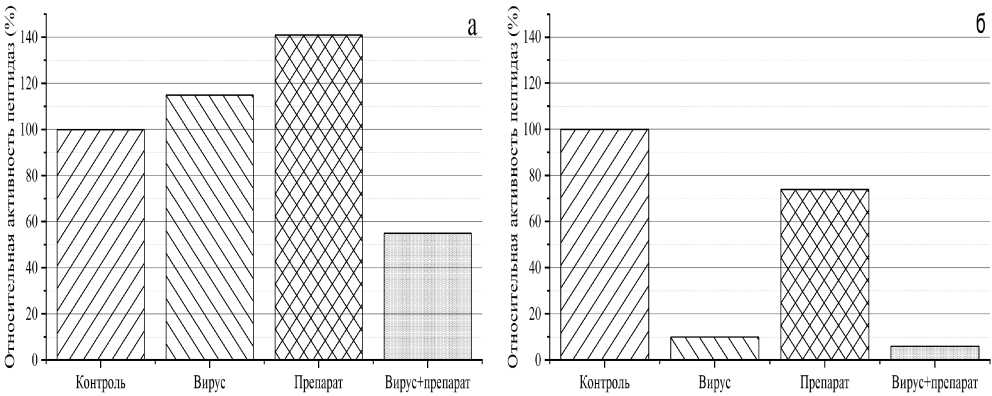
Рис. 6. Активность пептидаз в сыворотках (а) и бронхиальных смывах (б). За 100 % взята активность пептидаз у здоровых мышей
Из данных экспериментов прежде всего следует, что при гидролизе брадикинина (Br(1–9)) образуется несколько продуктов. Пептид Br(1–8) может быть образован исключительно под воздействием карбоксипептидазы N. В то же время пептиды Br(1–7) и Br(1–5) могут быть продуктами гид- ролиза брадикинина ангиотензинпревращающим ферментом.
Относительная активность пептидаз по отношению к брадикинину представлена на рис. 6. Концентрация брадикинина оценивалась с использованием в качестве стандарта 18О-брадикинина.
ВЫВОДЫ
Наиболее значимые изменения активности пептидаз происходят в бронхиальных смывах, нежели в сыворотках крови больных животных.
Введение препарата здоровому животному приводит к увеличению активности АПФ, но в значительно меньшей степени по сравнению с инфицированными животными.
При введении препарата больным животным происходит заметное снижение активности АПФ до уровня, соответствующего здоровым животным. Это говорит об избирательности воздействия препарата на ренин-ангиотензиновую систему.
По результатам работы можно сделать общий вывод о том, что подобный скрининг может быть с успехом использован при сравнительной оценке эффективности и других антигриппозных препаратов, а также для понимания направления их воздействия на инфицированный организм.
Авторы заявляют, что у них нет конфликта интересов, в том числе и финансовых.
Данная работа частично выполнена в рамках НИР 0074-2019-0009, входящей в состав гос. задания № 07500780-19-02 Министерства науки и высшего образования Российской Федерации для ИАП РАН.
Список литературы Количественная масс-спектрометрия в диагностике гриппа и контроле действия лекарственного препарата "Триазавирин"
- Pellacani A., Brunner H.R., Nussberger J. Plasma kinins increase after angiotensin-converting enzyme inhibition in human subjects // Clin Sci. 1994. Vol. 87, no. 5. P. 567– 574. DOI: 10.1042/cs0870567
- Chandrasoma P., Taylor C.R. Concise Pathology. 3rd ed. Appleton & Lange, 1997. 990 p.
- Гуреева Т.А., Кугаевская Е.В., Позднев В.Ф., Прозоровский В.Н., Елисеева Ю.Е., Соловьева Н.И. Исследование специфичности нового пептидного субстрата эндотелин-превращающего фермента // Биомедицинская химия. 2007. Т. 53, № 2. С. 172–180.
- Бубляев Р.А., Козьмин Ю.П., Краснов Н.В., Манойлов А.В., Миргородская О.А., Новиков А.В. Способ получения изотопно-модифицированных пептидов и белков. Патент РФ № 2399627. 2008.
- Козьмин Ю.П., Манойлов А.В., Серебрякова М.В., Миргородская О.А. Прямое введение изотопов 18О в пептиды и белки для количественного анализа методом масс-спектрометрии // Биоорганическая химия. 2011. Т. 37, № 6. С. 793–806.


