Количественное хромато-масс-спектрометрическое определение валсартана и гидрохлоротиазида в плазме крови
Автор: Толкачев Б.Е., Доценко А.М., Стрыгин А.О., Магницкая О.В.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Фармакология токсикология
Статья в выпуске: 4 (52), 2016 года.
Бесплатный доступ
В рамках настоящего исследования была проведена разработка и валидация метода количественного определения валсартана и гидрохлоротиазида в плазме крови человека с помощью хромато-масс-спектрометрии. Использование масс-спектрометрического детектора позволило повысить селективность и чувствительность метода без использования трудоёмких методов пробоподготовки.
Биоанализ, вэжх-мс/мс, валсартан, гидрохлоротиазид
Короткий адрес: https://sciup.org/142149201
IDR: 142149201 | УДК: 616.12-005.4-085.224
Quantitative lc-ms/ ms determination of valsartan and hydrochlorothiazide in human plasma
Development and validation of the highly selective and sensitive LC-MS/MS method to detect valsartan and hydrochlorothiazide in human plasma were performed. Mass spectrometriy detection made it possible to enhance analytical performance without time- and labor consuming sample preparation procedures, thus improving the overall bioanalytical productivity in the course of the bioequivalence study.
Текст научной статьи Количественное хромато-масс-спектрометрическое определение валсартана и гидрохлоротиазида в плазме крови
Требования, предъявляемые к современным биоаналитическим исследованиям непрерывно повышаются, что подчёркивает важность разработки высокочувствительных и селективных методов, позволяющих проводить высокопроизводительный анализ биологических проб в рамках различных этапов изучения лекарственных средств, включая исследования биоэквивалентности [3].
ЦЕЛЬ РАБОТЫ
Определение оптимальных условий одновременного количественного ВЭЖХ-МС/МС определения валсартана и гидрохлоротиазида в плазме крови для последующего использования в фармакокинетических исследованиях.
МЕТОДИКА ИССЛЕДОВАНИЯ
Для приготовления маточных и стандартных растворов валсартана и гидрохлоротиазида использовались сухие навески соответствующих сертифицированных стандартов веществ, которые впоследствии растворяли и разводили в смеси ацетонитрил/вода в объёмном соотношении 80/20.
Для калибровки методики количественного определения была использована плазма крови добровольцев, не принимавших исследуемые препараты.
Калибровочные образцы готовились в диапазоне концентраций от 4 до 1 000 нг/мл для валсартана и от 0,5 до 250 нг для гидрохлоротиазида.
В качестве опытных образцов были использованы образцы плазмы крови здоровых добровольцев, принимавших комбинированный препарат в рамках проведения исследования биоэквивалентности.
Пробоподготовка калибровочных и опытных образцов плазмы крови проводилась методом преципитации белков путём добавления к 200 мкл каждой из проб 600 мкл ацетонитрила, последующим центрифугированием в течение 15 минут при 3 000 об./мин и отбором 100 мкл надосадочной жидкости для анализа.
Хроматографическое разделение компонентов проводилось с использованием ВЭЖХ системы Agilent 1260 с бинарным насосом и термостатируемым автосемплером на колонке Poroshell 120 C18 (4,6 x 50 мм, 2,7 мкм).
Для детекции аналитов использовалась гибридная масс-спектрометрическая система Sciex QTRAP 5500.
Регистрация хромато-масс-спектров проводилась с использованием программного обеспечения Analyst 1.6. Интеграция пиков, расчёт количественного содержания исследуемых соединений и статистическая обработка данных проводилась с помощью программы MultiQuant 2.4.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Разработка метода количественного ВЭЖХ-МС/МС определения валсартана и гидрохлоротиазида включала определения оптимальных параметров хроматографического разделения, а также последующей масс-спектрометрической детекции. В качестве метода ионизации был использован электроспрей (ESI). Детекция ионов проводилась в режиме отрицательной полярности [2].
Ионы-«предшественники» валсартана соответствовали частицам с m/z 434,2, ионы-«предшественники» гидрохлоротиазида – m/z 295,9. Для построения метода мониторинга множественных реакций (MRM) использовались ионные переходы, соответствующие наибольшей интенсивности ионов-«продуктов». Было установлено, что оба вещества в ходе диссоциации в камере соударений дают по два наиболее интенсивных иона-«продукта»: m/z 179,0 и m/z 350,2 для валсартана; m/z 268,9 и 204,9 для гидрохлоротиазида.
При создании количественного МRM-метода с целью повышения специфичности были использованы оба ионных перехода.
В ходе оптимизации условий хроматографического разделения был выбран изокра-тический режим элюирования. Мобильная фаза представляла собой смесь ацетонитрил/ вода в соотношении 80/20 при скорости потока 0,3 мл/мин. В качестве модификатора мобильной фазы использовался ацетат аммония в концентрации 10 мкмоль/л, добавляемый к водной составляющей мобильной фазы. Использование данного модификатора позволяет повысить степень ионизации изучаемых соединений, тем самым увеличивая чувствительность анализа (рис. 1).
При этих условиях время удерживания валсартана составило 1,43 мин, время удерживания гидрохлоротиазида – 1,69 мин, что позволяло сократить суммарное время анализа каждой пробы до 2,5 минут (рис. 2, 3).
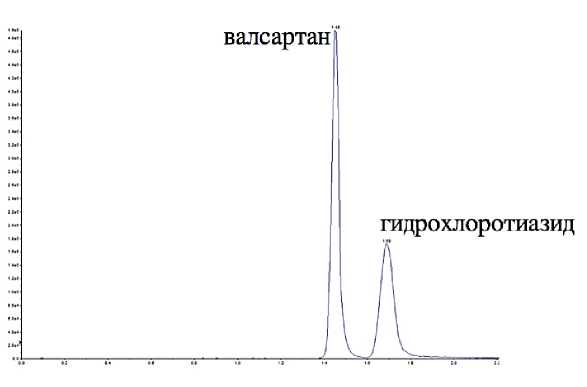
Рис. 1. Хромато-масс-спектрограмма опытного образца плазмы крови здорового добровольца после перорального приема комбинированного препарата «Валсартан-гидрохлоротиазид»: по оси абсцисс – время (мин), по оси ординат – интенсивность сигнала
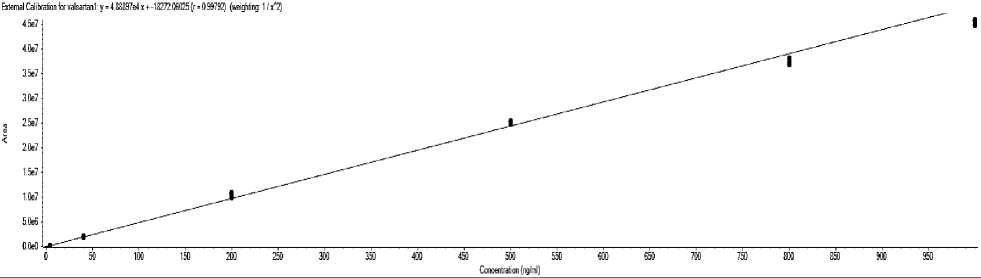
Рис. 2. Калибровочная кривая для валсартана: по оси ординат – площадь хромато-масс пика, нг/мл; по оси абсцисс – концентрация препарата
External Cali bration for hydrochlorotiazidel: у=4.76133e4 x+-8310.55060 (r=0.99818) (weighti ng: 1 / x^)
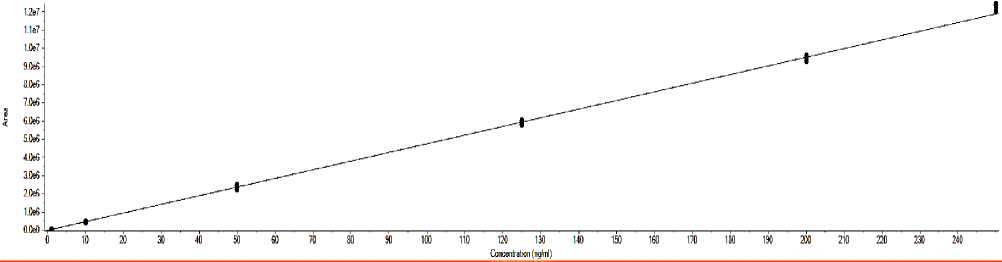
Рис. 3. Калибровочная кривая для гидрохлортиазида: по оси ординат – площадь хромато-масс пика, нг/мл; по оси абсцисс – концентрация препарата
В ходе валидации разработанного метода были установлены основные валидационные параметры: линейность, точность, правильность, чувствительность (нижний предел количественного определения), селективность.
Разработанная методика количественного определения подтвердила свою линейность в рассматриваемом диапазоне концентраций: при использовании взвешенного коэффициента 1/x2 для обоих аналитов r2 > 0,98 (рис 4, 5).
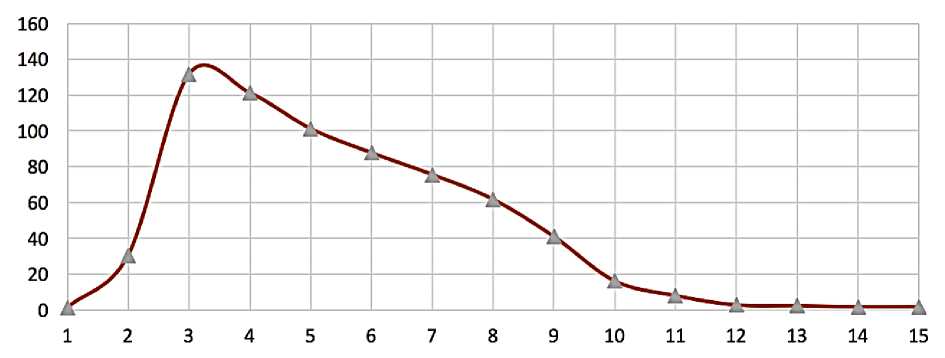
Рис 4. Фармакокинетическая кривая изменения концентрации валсартана после однократного перорального приёма комбинированного препарата «Валсартан/гидрохлортиазид»: по оси ординат – концентрация препарата, нг/мл; по оси абсцисс – порядковый номер пробы
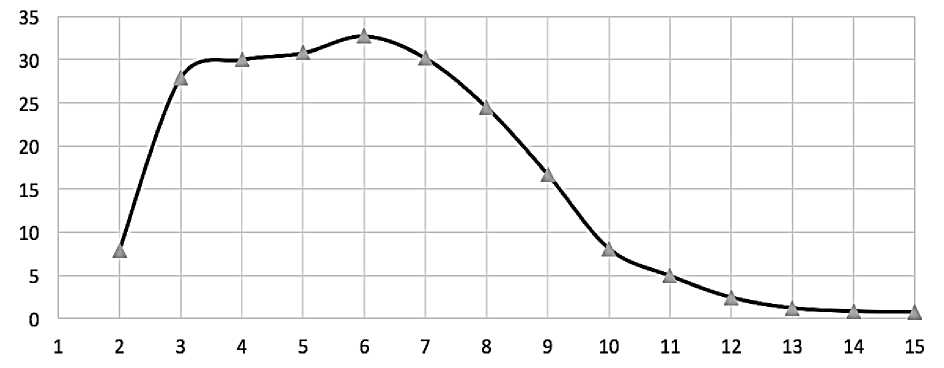
Рис. 5. Фармакокинетическая кривая изменения концентрации гидрохлортиазида после однократного перорального приёма комбинированного препарата «Валсартан/гидрохлортиазид»: по оси ординат – концентрация препарата, нг/мл; по оси абсцисс – порядковый номер пробы
Коэффициент вариации (%CV), рассчитываемый при определении меж- и внутридневной точности определения обоих препаратов не превышал 5 % для основного диапазона концентраций и 10 % для концентраций, соответствующих нижнему пределу количественного определения.
Отсутствие аналитической интерференции препаратов собой было достигнуто за счёт полного хроматографического разделения исследуемых веществ, а также использования несколько ионных MRM-переходов, обеспечивших высокую селективность биоанализа.
ЗАКЛЮЧЕНИЕ
Таким образом, в ходе проведённого исследования были установлены оптимальные условия высокочувствительного и селективного количественного ВЭЖХ-МС/МС определения валсартана и гидрохлоротиазида в плазме крови добровольцев, проведена его валидация и апробация в рамках биоаналитического этапа исследования биоэквивалентности.
Список литературы Количественное хромато-масс-спектрометрическое определение валсартана и гидрохлоротиазида в плазме крови
- Особенности количественного определения аторвастатина в плазме крови пациентов с ишемической болезнью сердца/А. Ф. Рябуха, К. А. Кузнецов, О. В. Магницкая и др.//Вестник Волгоградского государственного медицинского университета. -2011. -№ 1 (37). -С. 53-55.
- A liquid chromatography/tandem mass spectrometry method for the simultaneous quantification of valsartan and hydrochlorothiazide in human plasma/H. Li, Y. Wang, Y. Jiang, et al.//J. Chromatogr B. -2007. -№ 852. -P. 436-442.
- Simultaneous Determination of Hydrochlorothiazide and Valsartan in Human Plasma by Liquid Chromatography/Tandem Mass Spectrometry/F. Liu, J. Zhang, et al.//Analytical Letters. -2008. -№ 41 (8) -P. 1348-1365.


