Количественное содержание суммы фенольных соединений в траве володушки двустебельной (Bupleurum bicaule helm)
Автор: Тыхеев Жаргал Александрович, Тараскин Василий Владимирович, Раднаева Лариса Доржиевна
Журнал: Вестник Бурятского государственного университета. Медицина и фармация @vestnik-bsu-medicine-pharmacy
Статья в выпуске: 1, 2021 года.
Бесплатный доступ
Разработана методика количественного определения суммы флавоноидов и суммы фенолкарбоновых кислот в надземной части володушки двустебельной. Оптимальными параметрами экстракции данных групп БАВ являются: экстрагент - спирт этиловый 70%; степень измельчения - сырье, проходящее сквозь сито с диаметром отверстий 1 мм; время экстракции - 60 мин; соотношение сырье: экстрагент - 1:100 (использование данного соотношения является оптимальным и соответствует исчерпывающей экстракции). Подобраны оптимальные условия комплексообразования со спиртовым раствором алюминия хлорида - для полной реакции достаточно 2 мл 2%-ного спиртового раствора AlCl3. Впервые установлено содержание суммы флавоноидов, фенолкарбоновых кислот и дубильных веществ в траве B. bicaule из разных мест произрастания. Содержание суммы флавоноидов составило от 3,49±0,09% до 3,54±0,12%. Содержание суммы фенолкарбоновых кислот в травеB. bicaule составило от 4,02±0,11 до 4,13±0,15%. Содержание суммы дубильных веществ - от 10,27±0,36 до 11,28±0,38%.
Флавоноиды, фенолкарбоновые кислоты
Короткий адрес: https://sciup.org/148323404
IDR: 148323404 | УДК: 615.074+615.322 | DOI: 10.18101/2306-1995-2021-1-40-51
Quantitative content of the total phenolic compounds in the herb of Bupleurum bicaule helm
In the article we present a method for quantitation of the total flavonoids and phenolcarboxylic acids content in the aerial part of Bupleurum bicaule Helm. Optimal parameters for the extraction of these groups of biologically active substances are extractantethyl alcohol 70%; grinding degree - raw materials passing through a sieve with a hole diameter of 1 mm; extraction time - 60 min; the ratio of raw materials: extractant - 1:100 (this ratio is optimal and corresponds to exhaustive extraction). We have found optimal conditions for complexation with an alcoholic solution of aluminum chloride: 2 ml of a 2% alcohol solution of AlCl3 is sufficient for a complete reaction. For the first time, we have revealed the total content of flavonoids, phenolcarboxylic acids and tannins in the aerial part of B. bicaule from different growing areas. The content of the total content of flavonoids ranged from 3.49±0.09% to 3.54±0.12%. The total content of phenolcarboxylic acids in the B. bicaule herb is from 4.02 ± 0.11 to 4.13 ± 0.15%. The total content of tannins ranged from 10.27 ± 0.36 to 11.28 ± 0.38%.
Текст научной статьи Количественное содержание суммы фенольных соединений в траве володушки двустебельной (Bupleurum bicaule helm)
Введение. Растения природной флоры остаются одними из основных источников биологически активных веществ (БАВ), используемых во всем мире в целях профилактики и лечения различных заболеваний. В составе природной флоры важным и широко известным источником БАВ являются растения рода Bupleurum L., с давних времен используемые в традиционной медицине как средства, обладающие гепатопротекторной, желчегонной, противовоспалительной, иммунорегуляционной, антибактериальной и противовирусной активностями [1] . Однако представители этого рода до сих пор остаются практически не изученными с ботанической, химической и фармакологической точек зрения. Особенно это касается видов ( B. longifolium, B. sibiricum, B. bicaule и B. scorzonerifolium ) и их популяций из относительно малоосвоенных семиаридных и аридных районов, к каковым относятся значительные территории регионов Внутренней Азии (Бурятия, Забайкальский край, Монголия). Соединения фенольной природы, в частности флавоноиды и фенолкарбоновые кислоты, являются действующими веществами надземной части растений рода Bupleurum L. Именно они обусловливают спектр фармакологической активности травы воло-душки, такой как желчегонная, противовоспалительная и др.
Ранее Д. Н. Оленниковым определено содержание и состав флавоноидов и фенилпропаноидов в надземных частях B. bicaule, B. longifolium, B. multinerve, B. scorzonerifolium и B. triradiatum [2] . Также для надземных частей B. scorzonerifolium и B. longifolium разработаны и предложены методики количественного определения фенольных соединений и показатели доброкачественности сырья [3; 4] . Не менее перспективным видом для внедрения в медицинскую практику является володушка двустебельная ( Bupleurum bicaule Helm.), широко используемая в восточной традиционной медицине. Это многолетнее поликар-пическое растение 15‒35 см высотой с разветвленными каудексами [5] . В надземной части, корнях и плодах B. bicaule обнаружены кверцетин, изорам-нетин, рутин; в надземной части и плодах — изокверцитрин, нарциссин; в корнях — кемпферол [6] . Таким образом, разработка методик количественного определения суммы флавоноидов и суммы фенолкарбоновых кислот является важным этапом стандартизации нового вида лекарственного растительного сырья с целью его внедрения в отечественную фармакопею.
В настоящей работе представлены результаты разработки методик количественного определения суммы флавоноидов и фенолкарбоновых кислот и их содержание в траве B. Bicaule .
Материалы и методы
Объектами исследования служили образцы володушки двустебельной травы, собранные в ходе экспедиционных работ в 2018–2019 гг. на территории России (Республики Бурятия) в период массового цветения.
Качественные реакции проводили на спиртовом извлечении общепринятыми методами [7] , а также с использованием высокоэффективного жидкостного хроматографа «Милихром А-02» (ЗАО «ЭКОНОВА»). Разделение осуществляли с помощью колонки «ProntoSil-120-C18 AQ» (2*75 мм, 5 мкм). Подвижная фаза: элюент А — 0,1; раствор трифторуксусной кислоты; элюент Б — ацетонитрил. Скорость потока: 100 мкл/мин. Детектирование проводили с помощью УФ-детектора при длине волны 210–300 нм. Температура колонки — 35 °С.
Измерение оптической плотности исследуемых растворов проводили на спектрофотометре «СФ-46» в кварцевых кюветах с толщиной поглощающего слоя 1 см. Количественное определение дубильных веществ проводили методом окислительно-восстановительного титрования по методу 1 ОФС.1.5.3.0008.15 «Определение содержания дубильных веществ в лекарственном растительном сырье и лекарственных растительных препаратах» Государственной фармакопеи Российской Федерации XIV издания.
Результаты и обсуждение
Качественное обнаружение соединений фенольной природы
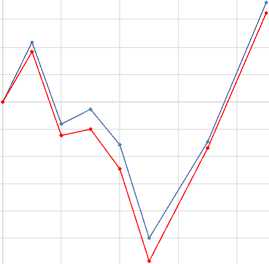
В результате проведенных общепринятых качественных реакций в надземной части володушки двустебельной обнаружены флавоноиды и дубильные вещества. Методом ВЭЖХ подтверждено наличие хлорогеновой кислоты и рутина. Идентификацию хлорогеновой кислоты и рутина осуществляли при сравнении с растворами СО по спектрам поглощения и времени удерживания (рис. 1–4).
—•— Пик
• • Компонент
1,3
1,2
1,1
0,9
0,8
0,7
0,6
0,5
0,4
0,3
0,2
0,1
330 350
190 210 230 250 270 290 310
Длина волны, нм
Рисунок 1. УФ-спектры хлорогеновой кислоты растворов СО и спиртового извлечения надземной части B. bicaule
0,9
0,8
0,7
0,6
0,5
0,4
0,3
0,2
0,1
-—*— Пик
— ♦ — Компонент
190 210 230 250 270 290 310 330 350
Длина волны, нм
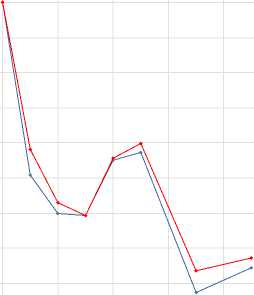
Рисунок 2. УФ-спектры рутина растворов СО и спиртового извлечения надземной части B. bicaule
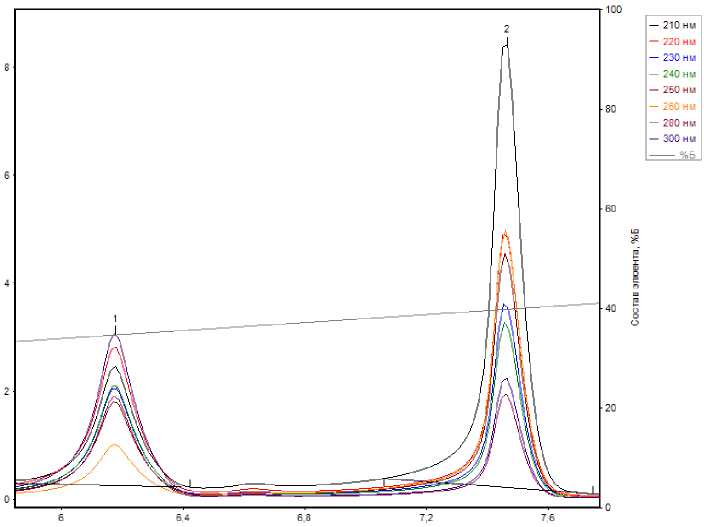
Время, мин
Рисунок 3. Фрагмент хроматограммы смеси растворов СО хлорогеновой кислоты и рутина
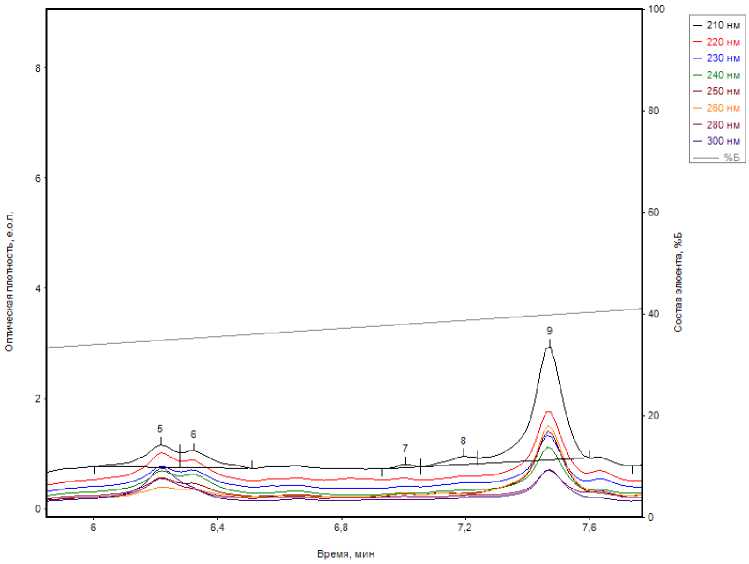
Рисунок 4. Фрагмент хроматограммы спиртового извлечения надземной части B. bicaule (Хоринский район, Бурятия)
Разработка методик количественного определения суммы флавоноидов и суммы фенолкарбоновых кислот
При изучении спектров поглощения спиртового извлечения из володушки двустебельной травы и комплекса алюминия хлорида с спиртовым извлечением из володушки двустебельной травы установлено наличие максимумов поглощения при 325 нм и 410 нм соответственно, что, в свою очередь, совпадает с максимумами поглощения раствора стандартного образца хлорогеновой кислоты и комплекса стандартного образца рутина с алюминием хлоридом.
Подбор условий при разработке методик количественного определения фенольных соединений проводили в зависимости от типа экстрагента, степени измельчения сырья, соотношения сырье — экстрагент, времени экстракции. При подборе наилучшего экстрагента использовали сырье, проходящее сквозь сито с отверстиями размером 1 мм. В качестве экстрагента брали спирт этиловый разной концентрации. Соотношение сырье — экстрагент — 1:100. Полученные данные представлены в таблице 1.
Таблица 1
Содержание суммы флавоноидов в пересчете на рутин и суммы фенолкарбоновых кислот в B. bicaule herba в зависимости от типа экстрагента
|
№ |
Экстрагент |
Сумма флавоноидов в пересчете на рутин, % |
Сумма фенолкарбоновых кислот |
|
1 |
Вода очищенная |
0,98±0,04 |
1,73±0,08 |
|
2 |
Спирт этиловый 10% |
2,26±0,09 |
2,28±0,05 |
|
3 |
Спирт этиловый 20% |
2,69±0,05 |
2,62±0,10 |
|
4 |
Спирт этиловый 30% |
3,38±0,10 |
2,85±0,13 |
|
5 |
Спирт этиловый 40% |
3,31±0,15 |
3,40±0,10 |
|
6 |
Спирт этиловый 50% |
3,22±0,07 |
3,56±0,10 |
|
7 |
Спирт этиловый 60% |
3,47±0,17 |
3,76±0,10 |
|
8 |
Спирт этиловый 70% |
3,49±0,06 |
4,02±0,17 |
|
9 |
Спирт этиловый 80% |
3,45±0,09 |
3,73±0,14 |
|
10 |
Спирт этиловый 90% |
3,07±0,04 |
3,72±0,17 |
|
11 |
Спирт этиловый 95% |
2,90±0,07 |
3,41±0,12 |
Оптимальным экстрагентом, позволяющим извлечь наибольший выход суммы флавоноидов: 3,47, 3,49 и 3,45%, является спирт этиловый в концентрации 60, 70 и 80% соответственно. Наибольший выход суммы фенолкарбоновых кислот наблюдается при экстракции 70%-ным спиртом этиловым — 4,02%. Таким образом, нами предложено использовать спирт этиловый 70%, при котором наблюдается наибольший выход как флавоноидов, так и фенолкарбоновых кислот.
Было использовано сырье, проходящее сквозь сито с диаметром отверстий 0.5, 1.0, 2.0, 3.0, 5.0 мм для выбора оптимальной степени измельчения (табл. 2). В качестве экстрагента использовали спирт этиловый 70%. Соотношение сы-рье:экстрагент — 1:100. Наибольший выход суммы фенольных соединений наблюдался для сырья, проходящего сквозь сито с диаметром отверстий 1,0 мм: сумма флавоноидов —3,50%; сумма фенолкарбоновых кислот — 4,02%.
Таблица 2
Содержание суммы флавоноидов в пересчете на рутин и суммы фенолкарбоновых кислот в B. bicaule herba в зависимости от степени измельчения сырья
|
№ |
Сырье, проходящее сквозь сито с отверстиями размером, мм |
Сумма флавоноидов в пересчете на рутин, % |
Сумма фенолкарбоновых кислот |
|
1 |
0,5 мм |
3,21±0,06 |
3,74±0,05 |
|
2 |
1,0 мм |
3,50±0,09 |
4,02±0,06 |
|
3 |
2,0 мм |
3,23±0,14 |
3,71±0,06 |
|
4 |
3,0 мм |
3,18±0,08 |
3,63±0,10 |
|
5 |
5,0 мм |
2,91±0,10 |
3,14±0,11 |
Для выявления оптимального времени экстракции сырье экстрагировали в течение 30, 60, 90 и 120 мин. В качестве экстрагента использовали спирт этиловый 70%. Соотношение сырье — экстрагент — 1:100 (табл. 3).
Таблица 3
Содержание суммы флавоноидов в пересчете на рутин и суммы фенолкарбоновых кислот в B. bicaule herba в зависимости от времени экстракции
|
№ |
Время экстракции, мин |
Сумма флавоноидов в пересчете на рутин, % |
Сумма фенолкарбоновых кислот |
|
1 |
30 |
3,30±0,16 |
3,62±0,07 |
|
2 |
60 |
3,49±0,12 |
4,02±0,12 |
|
3 |
90 |
3,49±0,15 |
4,00±0,10 |
|
4 |
120 |
3,48±0,10 |
3,99±0,13 |
Наибольший выход суммы флавоноидов и суммы фенолкарбоновых кислот наблюдается при экстракции в течение 60 мин. Дальнейшая экстракция до 120 мин не приводит к увеличению выхода фенольных соединений.
Следующим этапом мы подобрали оптимальные условия выхода основных биологически активных веществ при разных соотношениях сырье — экстрагент (табл. 4).
Таблица 4
Содержание суммы флавоноидов в пересчете на рутин и суммы фенолкарбоновых кислот в B. bicauli herba в зависимости от соотношения сырье — экстрагент
|
№ |
Соотношение сырье — экстрагент |
Сумма флавоноидов в пересчете на рутин, % |
Сумма фенолкарбоновых кислот |
|
1 |
1:25 |
2,54±0,09 |
3,04±0,14 |
|
2 |
1:50 |
3,12±0,10 |
3,54±0,15 |
|
3 |
1:75 |
3,36±0,08 |
3,87±0,13 |
|
4 |
1:100 |
3,49±0,09 |
4,02±0,11 |
|
5 |
1:150 |
3,49±0,14 |
4,01±0,12 |
|
6 |
Вариант экстракции (трехкратная экстракция при соотношении сырье ‒ экстрагент ‒ 1:30 и времени экстракции: 60, 30, 30) |
3,46±0,17 |
4,00±0,08 |
Полученные данные свидетельствуют о том, что оптимальным соотношением сырья и экстрагента является 1:100. Использование данного соотношения является оптимальным и соответствует исчерпывающей экстракции (№ 6, табл. 4; в шроте после исчерпывающей экстракции пробой Синода флавоноиды методом ТСХ и фенолкарбоновые кислоты не были обнаружены).
Для разрабатываемой методики количественного определения суммы флавоноидов нами подобраны оптимальные условия комплексообразования со спиртовым раствором алюминия хлорида (табл. 5).
Таблица 5
Содержание суммы флавоноидов в пересчете на рутин в B. bicauli herba в зависимости от объема и концентрации AlCl 3
|
Объем |
||
|
№ |
Объем AlCl 3 , мл |
Сумма флавоноидов в пересчете на рутин, % |
|
1 |
1 |
3,38±0,02 |
|
2 |
2 |
3,49±0,09 |
|
3 |
3 |
3,49±0,11 |
|
4 |
4 |
3,39±0,08 |
|
5 |
5 |
3,43±0,14 |
|
Концентрация |
||
|
№ |
Концентрация AlCl 3 , % |
Сумма флавоноидов в пересчете на рутин, % |
|
1 |
1 |
3,38±0,04 |
|
2 |
2 |
3,49±0,09 |
|
3 |
3 |
3,48±0,11 |
|
4 |
4 |
3,23±0,10 |
|
5 |
5 |
3,34±0,12 |
Показано, что для полной реакции комплексообразования достаточно использовать 2%-ной спиртовой раствор алюминия хлорида в количестве 2 мл. Таким образом, разработаны методики количественного определения суммы флавоноидов и суммы фенолкарбоновых кислот в B. bicauli herba .
Методика определения суммы флавоноидов:
Приготовление растворов. Раствор стандартного образца (СО) рутина: около 0,05 г (точная навеска) рутина, предварительно высушенного при температуре 130–135 °С в течение 3 ч, растворяют в 40 мл 96%-го спирта этилового в мерной колбе вместимостью 100 мл. В мерную колбу вместимостью 25 мл помещают 1 мл полученного раствора и доводят его объем до метки 50%-ным этиловым спиртом и перемешивают.
2%-ный спиртовой раствор алюминия хлорида: 2 г алюминия хлорида растворяют в 50 мл 95%-го спирта этилового в мерной колбе вместимостью 100 мл и доводят объем раствора тем же растворителем до метки и перемешивают.
Пробы сырья измельчают до величины частиц, проходящих сквозь сито с отверстиями размером 1 мм. Около 1,0 г (точная навеска) измельченного сырья помещают в плоскодонную колбу с притертой пробкой вместимостью 250 мл и прибавляют 100 мл 70%-го этилового спирта. Колбу с содержимым присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 60 мин. После охлаждения извлечение фильтровали через бумажный фильтр, отбрасывая первые 10 мл фильтрата (раствор А).
В мерную колбу объемом 25 мл вносят 1,0 мл раствора А, прибавляют 2 мл спиртового раствора алюминия хлорида 2% (раствор Б) и доводят 95%-ным этиловым спиртом до метки. Оптическую плотность измеряют на спектрофотометре при длине волны 410 нм в кювете с толщиной слоя 10 мм через 40 мин после добавления реактива. В качестве сравнения используют раствор, состоящий из 1,0 мл раствора А, капли уксусной кислоты 10%, помещенный в мерную колбу вместимостью 25 мл и доведенный 95%-ным этиловым спиртом до метки. Парал- лельно измеряют оптическую плотность раствора СО рутина, приготовленного аналогично испытуемому раствору.
Содержание суммы флавоноидов в пересчете на рутин и абсолютно сухое сырье в % вычисляют по формуле:
D X т0 X 100 X 100
X Do x m x (100 - WZ)J где D — значение оптической плотности испытуемого образца (раствор Б); D0 — значение оптической плотности рутина; m — масса сырья, г; m0 — масса рутина, г; W — потеря в массе при высушивании сырья в %.
Методика определения суммы фенолкарбоновых кислот:
Пробы сырья измельчают до величины частиц, проходящих сквозь сито с отверстиями размером 1 мм. Около 1,0 г (точная навеска) измельченного сырья помещают в плоскодонную колбу с притертой пробкой вместимостью 250 мл и прибавляют 100 мл этилового спирта 70%. Колбу с содержимым присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 60 минут. После охлаждения извлечение фильтровали через бумажный фильтр, отбрасывая первые 10 мл фильтрата (раствор А).
В мерную колбу объемом 50 мл вносят 0,5 мл раствора А и доводят 95%-ным этиловым спиртом до метки (раствор Б). Оптическую плотность полученного раствора измеряют в кюветах с толщиной слоя 10 мм на спектрофотометре при длине волны 325 нм. Раствором сравнения служит спирт этиловый 95%.
Содержание суммы фенолкарбоновых кислот в пересчете на абсолютно-сухое сырье в % вычисляют по формуле:
D X 100 X 50 X 100 у =______________________ m x 504,425 x 0,5 x (100 - W)'
где D — значение оптической плотности испытуемого раствора (раствор Б); m — масса сырья; W — потеря в массе при высушивании сырья, %; 504,425 — удельный показатель поглощения 3-О-кофелхинной (хлорогеновой) кислоты (при 325 нм).
Метрологическая характеристика результатов количественного определения представлена в таблице 6.
Таблица 6
Метрологическая характеристика результатов количественного определения суммы флавоноидов и суммы фенолкарбоновых кислот в B. bicauli herba
|
f \ |
̅х̅, % |
S 1 |
Sх̅ 1 |
P, % |
t(P, f) |
Δx |
E, % |
|
сумма флавоноидов |
|||||||
|
8 \ |
3,49 |
0,06954 |
0,02318 |
95 1 |
2,3 1 |
0,05 |
±1,53 |
|
сумма фенолкарбоновых кислот |
|||||||
|
8 \ |
4,02 |
0,13812 |
0,04604 |
95 1 |
2,3 1 |
0,11 |
±2,64 |
Ошибка методики количественного определения суммы флавоноидов составила ±1,53% при 9 независимых определениях; суммы фенолкарбоновых кислот, — ±2,64% при 9 независимых определениях.
Разработанными методиками проведено количественное определение суммы флавоноидов и суммы фенолкарбоновых кислот в пяти сериях полупромышленных партий сырья. Рекомендуемая норма содержания суммы флавоноидов в траве володушки двустебельной составляет не менее 2%; суммы фенолкарбоновых кисло — не менее 2,5%.
Данные методики валидны и соответствуют параметрам: специфичность, прецизионность, правильность и линейность. Они рекомендуются для включения в проект фармакопейной статьи «Володушки двустебельной трава — Bupleuri bicauli herba ».
Количественное определение суммы фенольных соединений
Впервые с использованием разработанных нами методик установлено содержание суммы флавоноидов и фенолкарбоновых кислот в траве B. bicaule из разных мест произрастания, а также содержание суммы дубильных веществ стандартной методикой (табл. 8).
Характеристика объектов исследования, суммарное содержание фенольных соединений в B. Bicaule
Таблица 8
|
Места сбора образцов |
Сумма флавоноидов, % |
Сумма фенолкарбоновых кислот, % |
Сумма дубильных веществ, % |
|
B. bicaule |
|||
|
РФ, РБ, Хоринский район, окр. с. Удинск |
3,49±0,09 |
4,02±0,11 |
11,22±0,32 |
|
РФ, РБ, Еравнинский район, окр. с. Можайка |
3,54±0,12 |
4,13±0,15 |
11,28±0,38 |
|
РФ, РБ, Мухоршибирский район, окр. с. Хошун-Узур |
3,53±0,07 |
4,07±0,08 |
10,27±0,36 |
Содержание суммы флавоноидов составило от 3,49±0,09% до 3,54±0,12%. Содержание суммы фенолкарбоновых кислот в траве B. bicaule составило от 4,02±0,11 до 4,13±0,15%; дубильных веществ — от 10,27±0,36% до 11,28±0,38%.
Согласно полученным данным не выявлено принципиального различия в содержании фенольных соединений надземной части володушки двустебельной, собранной в разных местах произрастания. Однако относительно высокое содержание данных БАВ было обнаружено в сырье, собранном в Еравнинском районе Республики Бурятия, что, вероятно, связано с условиями произрастания вида.
Выводы. В результате проведенных исследований показано, что трава воло-душки двустебельной является богатым источником флавоноидов, фенолкарбоновых кислот и дубильных веществ и может быть использована как дополнительное сырье к траве володушки козельцелистной, володушки золотистой и во-лодушки многожильчатой, используемых в традиционной медицине в качестве гепатопротекторных и желчегонных средств.
Список литературы Количественное содержание суммы фенольных соединений в траве володушки двустебельной (Bupleurum bicaule helm)
- A systematic review of the active saikosaponins and extracts isolated from Radix Bupleuri and their applications / B. Yuan, R. Yang, Y. Ma [et al.] // Pharmaceutical biology. 2016. Vol. 55, No 1. P. 620-635.
- Olennikov D. N., Partilkhaev V. V. Flavonoids and phenylpropanoids from several species of Bupleurum growing in Buryatia // Chemistry of Natural Compounds. 2013. Vol. 48, No. 6. P. 1078-1082.
- Канунникова Ю. С. Фармакогностическое изучение и стандартизация травы и экстракта сухого володушки золотистой (Bupleurum aurei Fisch.): автореферат диссертации на соискание ученой степени кандидата фармацевтических наук. Москва, 2014. 22 с. Текст: непосредственный.
- Петухова С. А. Фармакогностическое исследование володушки козельцелистной (Bupleurum scorzonerifolium Willd.) травы и разработка на ее основе экстракта сухого: автореферат диссертации на соискание ученой степени кандидата фармацевтических наук. Улан-Удэ, 2018. 22 с. Текст: непосредственный.
- Пименов М. Г., Остроумова Т. А. Зонтичные (Umbelliferae) России. Москва: Товарищество научных изданий КМК, 2012. 477 с. Текст: непосредственный.
- Растительные ресурсы России. Дикорастущие цветковые растения, их компонентный состав и биологическая активность. Т. 3. Семейства Fabaceae-Apiaceae / отв. ред. А. Л. Буданцев. Санкт-Петербург; Москва: Товарищество научных изданий КМК, 2010. 601 с. Текст: непосредственный.
- Гринкевич Н. И., Сафронович Л. Н. Химический анализ лекарственных растений. Москва, 1983. 176 с. Текст: непосредственный.


