Комбинированный остеосинтез при лечении диафизарных переломов большеберцовой кости
Автор: Клышников К.А., Сазонова Н.В., Попков А.В.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 6 т.29, 2023 года.
Бесплатный доступ
Введение. Использование биоактивных имплантатов (эластичных титановых стержней и деградируемых внутрикостных имплантатов) представляет собой перспективный подход к решению проблем регенерации костной ткани, сокращающий сроки лечения.Цель. Оценить эффективность сочетания чрескостного остеосинтеза с интрамедуллярным армированием эластичными титановыми стержнями, покрытыми гидроксиапатитом (НА-стержнями), при лечении переломов длинных трубчатых костей.Материалы и методы. Проанализированы истории болезни 40 пациентов в возрасте от 18 до 55 лет с закрытыми диафизарными переломами большеберцовой кости типа A1-A3 (по классификации AO/ASIF), прооперированных методом чрескостного остеосинтеза по Илизарову в сочетании с интрамедуллярными эластичными спицами, покрытыми гидроксиапатитом.Результаты. В среднем, демонтаж аппарата Илизарова проводили через 45,3 ± 14,7 дня после операции. Рентгенологические признаки консолидации перелома (наличие незрелой костной мозоли, периостальных и эндостальных наслоений, перекрывающих линию перелома) были видны на 3-4-й неделе.Обсуждение. Сочетание аппарата наружной фиксации и интрамедуллярных эластичных спиц с HA-покрытием позволяет преодолеть недостатки как внешних, так и внутренних устройств. Наружный остеосинтез обеспечивает все преимущества метода Илизарова: сохранение кровообращения, отсутствие повреждения мягких тканей, функция сустава и нагрузка в ранние сроки. Эластичные интрамедуллярные спицы не повреждают a. nutricia и механически стимулируют эндостальное и периостальное костеобразование.Заключение. Преимущества комбинированного остеосинтеза заключаются в сокращении времени фиксации в аппарате Илизарова, уменьшении количества спиц и стержней- шурупов в аппарате наружной фиксации, стимуляции образования костной мозоли и предупреждении вторичных смещений костных фрагментов.
Илизаров, интрамедуллярные эластичные спицы, гидроксиапатит
Короткий адрес: https://sciup.org/142240034
IDR: 142240034 | УДК: 616.718.5-001.5-089.227.84 | DOI: 10.18019/1028-4427-2023-29-6-635-639
Combined osteosynthesis for tibial shaft fracture treatment
Introduction Widespread use of intramedullary and extramedullary implants, as well as external fixation devices, has demonstrated that current surgical methods are not always successful.The study aimed to assess the efficiency of a combination of transosseous osteosynthesis with intramedullary reinforcement using elastic titanium hydroxyapatite-coated rods (HA-rods) in long bone fracture treatment.Material and methods Medical records of 40 patients aged from 18 to 55 years with closed diaphyseal tibia fractures of A1-A3 type (AO/ASIF) treated with the Ilizarov transosseous osteosynthesis method combined with intramedullary elastic HA-coated wires were analysed. Result Ilizarov fixator removal was performed on average 45.3 ± 14.7 days after surgery. Radiological signs of bone union (immature callus, patterns of periosteal and endosteal stratifications overlapping the fracture line) were visible by week 3 to 4.Discussion Combination of the external fixator and intramedullary elastic HA-coated wires overcomes shortcomings of both external and internal means of fixation. External osteosynthesis provides advantages of the Ilizarov method: preservation of blood supply, absence of soft tissue injury, joint function and early weightbearing. Elastic intramedullary wires do not injure a. nutricia and mechanically stimulate endosteal and periosteal bone formation.Conclusion The advantages of combined osteosynthesis provide reduction of Ilizarov apparatus fixation time, reduction in the number of wires and half-pins in the frame assembly, stimulation of bone callus formation and prevention of secondary bone fragment displacement.
Текст научной статьи Комбинированный остеосинтез при лечении диафизарных переломов большеберцовой кости
Проблема оказания неотложной помощи пациентам с повреждениями опорно-двигательной системы с каждым годом приобретает всё большее значение в связи с ростом количества пострадавших и последующей инвалидностью, особенно у лиц трудоспособного возраста [1-4].
Широко распространённое использование внутрикостных и накостных имплантатов, а также аппаратов наружной фиксации показало, что далеко не всегда современные хирургические методы являются успешными. Несостоятельность лечения связана с ятрогенной травматичностью оперативного вмешательства, значительной продолжительностью наружной фиксации, замедленной костной консолидацией, нарушениями комфортности при использовании аппаратов наружной фиксации [5, 6].
Следует признать, что использование биоактивных имплантатов (эластичных титановых стерж-
ней и деградируемых внутрикостных имплантатов) представляет собой перспективный подход к решению проблем регенерации костной ткани, связанных с сокращением сроков лечения переломов длинных трубчатых костей [7-9].
Цель – оценка эффективности сочетания чрескост-ного остеосинтеза с интрамедуллярным армированием эластичными титановыми стержнями, покрытыми гидроксиапатитом (НА-стержнями), при лечении переломов длинных трубчатых костей.
МАТЕРИАЛЫ И МЕТОДЫ
Ретроспективное исследование проводилось в Национальном медицинском исследовательском центре травматологии и ортопедии им. академика Г.А. Илизарова (Курган, Россия). Были проанализированы истории болезни 40 пациентов в возрасте от 18 до 55 лет с закрытыми диафизарными переломами большеберцовой кости типа A1-A3 (по классификации AO/ASIF).
Критериями для включения в исследование являлись взрослые лица трудоспособного возраста, прооперированные комбинированным методом остеосинтеза аппаратом Илизарова. Мы исключили из исследования пациентов других возрастных групп, а также пациентов с открытыми или осложнёнными переломами.
После получения одобрения экспертного совета учреждения были собраны данные о клинических и рентгенологических особенностях переломов, послеоперационном периоде, заживлении костей и функциональном восстановлении. Также оценивали частоту, тяжесть осложнений и исходы.
Особенности оперативного вмешательства. пера-цию проводили под эпидуральной анестезией во всех случаях. Стандартное скелетное вытяжение позволяло ликвидировать смещения костных отломков. Фиксацию интрамедуллярными спицами выполняли одновременно при наложении аппарата, используя две изогнутые спицы. В метафизе большеберцовой кости (проксимальном или дистальном – ближайшем к перелому) формировали наклонные отверстия, сообщающиеся с костномозговым каналом, с помощью сверла диа- метром 3-4 мм [10]. Изогнутые спицы с биоактивным покрытием (гидроксиапатитом-НА) легко вводились через отверстия в костномозговой канал под контролем эктронно-оптического преобразовпаателя (ЭОП). Мы использовали спицы диаметром 1,8 мм из титанового сплава с покрытием из гидроксиапатита (ортопедиа-трические спицы, модифицированные Metis Ltd, Томск, Россия). Биоактивное покрытие толщиной 20-40 µм и пористостью 2-8 % были получены методом анодного оксидирования в дуговом режиме [11]. Такой тип покрытия представляет собой ультрапористую систему, состоящую из макро- и микропор диаметром от 50-100 нм до 1-2 μм.
После фиксации интрамедуллярными спицами проводили монтаж аппарата Илизарова (Экспериментальный завод НМИЦ ТО им. академика Г.А. Илизарова, Курган, Россия) по технологии чрескостного остеосинтеза. Следует подчеркнуть, что интрамедуллярные спицы не мешали проведению спиц или стержней-шурупов аппарата наружной фиксации (АНФ).
Рентгенографию в двух стандартных проекциях проводили перед операцией, в день проведения операции и далее через каждые 2-3 недели до костной консолидации. Оценивали также и рентгенограммы после снятия аппарата.
Статистический анализ проводили, используя программное обеспечение AtteStat 12.0.5. Для описания непрерывных переменных использовали средние значения и стандартные отклонения.
РЕЗУЛЬТАТЫ
В исследование были включены сорок пациентов (9 женщин, 31 мужчина), средний возраст которых составлял 29,6 года (в пределах 18-55 лет). Тридцати трём пациентам (82,5 %) провели антеградное интрамедуллярное армирование, а семи пациентам (7,5 %) провели анте-ретроградное армирование (рис. 1). В семнадцати случаях (42,5 %) изогнутые интрамедуллярные спицы обеспечили возможность полной репозиции перелома, поэтому не было необходимости проводить дополнительные спицы с упорной площадкой в область костных концов в зоне перелома на уровне промежуточных колец наружного фиксатора. С первых дней после операции все пациенты самостоятельно ходили, опираясь на костыли, сначала с частичной нагрузкой на повреждённую ногу, затем – с полной. Послеоперационный отёк повреждённой конечности проходил через 2-3 недели. Послеоперационный болевой синдром, связанный с переломом, был умеренным и сохранялся до конца второй недели. Он купировался нестероидными противовоспалительными препаратами.
Через 14 суток после операции контуры концов отломков были размытыми. Эндостальная костная мозоль была видимой и хорошо выраженной в участ- ках костномозгового канала рядом с линией перелома и на протяжении всей длины интрамедуллярного имплантата. Периостальные наслоения были отчётливо видны и определялись на обеих проекциях рентгенограмм костных фрагментов. Толщина их составляла 2,8 ± 0,2 мм, длина – 14,7 ± 1,3 мм. В 24 случаях периостальная костная мозоль не прерывалась и перекрывала линию перелома, соединяя проксимальные и дистальные концы через 2 недели после операции.
Через четыре недели на рентгенограммах просматривались признаки костного сращения: размытое изображение концов переломов, едва различимая линия перелома, высокий уровень оптической плотности непрерывной периостальной кости на переднезадних и боковых проекциях. В этот период 32 пациента начали ходить с 50 % или даже полной нагрузкой на повреждённую ногу без вспомогательных средств опоры.
Двумя неделями позже костное сращение отмечалось во всех случаях: едва определяемая линия перелома, большое, плотное и компактное изображение периостальной костной мозоли. Ходьба с нагрузкой не ассоциировалась с болью. Во всех случаях отмечалось удовлетворительное восстановление объёма движений в голеностопном суставе. Таким образом, обосновывалось решение о демонтаже аппарата, и эту процедуру проводили в период 32-62 дней (в среднем, 45,3 ± 14,7 дня) после операции всем пациентам без иммобилизации в гипсовой повязке. Через месяц после снятия аппарата на рентгенограммах просматривалось ремоделирование костной мозоли с проходимостью костномозгового канала, анатомически правильным положением сегмента. Случаев миграции интрамедуллярных спиц не было. Их удаляли без затруднений через 4-7 месяцев после демонтажа аппарата во всех случаях.
Что касается осложнений, то наблюдаемое воспаление мягких тканей вокруг спиц аппарата Илизарова – в 9 случаях (22,5 %) успешно лечили локально антисептиками в 7 случаях, а применение антибиотиков и удаление спиц потребовалось двум пациентам. Дооперационный объём движений в коленном или голеностопном суставе восстановился у всех пациен- тов до последнего контрольного осмотра. В этой серии наблюдений у наших пациентов не было неврологических или сосудистых осложнений.
Клинический пример . Пациент 47 лет поступил с закрытым винтообразным переломом дистальной трети диафиза правой большеберцовой кости (рис. 1, a). Операция: остеосинтез костей голени аппаратом Илизарова и интрамедуллярное армирование большеберцовой кости эластичными спицами с HA-покрытием (рис. 1, б). Рентгенологические признаки костного сращения были отчётливо видны на 30-й день (рис. 1, в). В связи с этим аппарат был снят без какой-либо последующей иммобилизации (рис. 1, г). Пациенту была разрешена полная нагрузка через 2 недели после демонтажа аппарата. При контроле (через 3 месяца и 1 год после снятия аппарата) определялось ремоделирование костной мозоли и нормальные рентгенологические параметры большеберцовой кости (рис. 1, д, е).
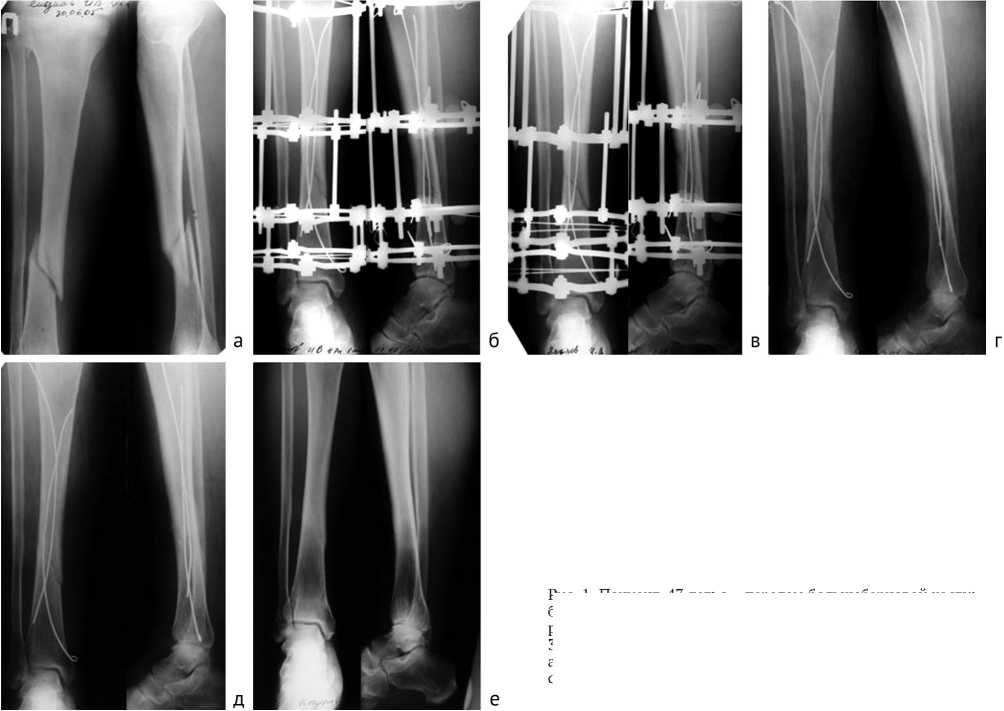
Рис. 1. Пациент, 47 лет: а – перелом большеберцовой кости; б – операция; в – рентгенограммы через 30 дней после операции; г – 32-й день после операции, аппарат снят; д – через 3 месяца, признаки неправильного сращения отсутствуют, анатомически правильное положение; е – через 1 год после снятия аппарата, костное ремоделирование
ОБСУЖДЕНИЕ
Диафизарные переломы большеберцовой кости являются самыми распространёнными переломами длинных трубчатых костей и происходят у 4 процентов взрослого населения, составляя от 11,3 до 41,2 % всех переломов костей скелета [12, 13]. Несмотря на улучшение технологии хирургических методов ле-чениятребуется, при переломах большеберцовой кости могут встречаться случаи замедленного костного сращения и неудовлетворительных результатов. Конечно, результаты лечения зависят как от характера перелома, так и от метода лечения [14-17].
При накостном остеосинтезе обычно требуется большой по протяжённости оперативный доступ, что приводит к увеличению кровопотери и дополнительной травматизации окружающих перелом мягких тканей, а, следовательно, к ухудшению кровоснабжения зоны перелома [14-16]. Основным недостатком интрамедуллярного остеосинтеза является значительное нарушение внутрикостного кровообращения, разрушение костного мозга и эндоста. Это потенциально снижает репаративную регенерацию кости [16, 17].
Метод наружной фиксации по Илизарову, в его классическом виде, довольно широко используется для хирургического лечения переломов большеберцовой кости. Но его применение осложняется большой продолжительностью (3-9 месяцев) фиксации аппаратом и, в связи с этим, высокой частотой случаев инфекций в области спиц. Это некомфортно для пациентов [18-20].
Сочетание аппарата наружной фиксации и интрамедуллярных эластичных спиц с HA-покрытием позволяет преодолеть недостатки как внешних, так и внутренних устройств. Наружный остеосинтез обеспечивает все преимущества метода Илизарова: сохранение кровообращения, отсутствие повреждения мягких тканей, функция сустава и нагрузка в ранние сроки [19-21]. Эластичные интрамедуллярные спицы не повреждают a. nutricia и механически стимулируют эндостальное и периостальное костеобразование [22]. Мы предполагаем, что HA-покрытие обеспечивает биологическую поддержку костного сращения [23]. Морфологические экспериментальные исследования, проведенные в НМИЦ травматологии и ортопедии им. академика Г.А. Илизарова, продемонстрировали формирование дополнительных структур костной ткани, окружающих интрамедуллярные спицы по всей их длине, что сохраняется до конца эксперимента и обеспечивает полную стабильность костных фрагментов [24]. Тонкие эластичные спицы не мешают губчатой костной ткани в костномозговом канале. Пучки остеоидных коллагеновых волокон прочно прикреплены к шероховатой наноструктурированной поверхности покрытия спиц и соединяются с эндостальной поверхностью кости, улучшая стабильность костных фрагментов. Такое покрытие из наноструктурированного высокопористого слоя гидроксиапатита обеспечивает высокую биосовместимость и остеоинтеграцию имплантатов в окружающую кость, предотвращая развитие фиброзной соединительной ткани [25, 26]. В нашей небольшой серии продемонстрировано, что такое сочетание стабильности фиксации костных отломков и биологической стимуляции костной регенерации обеспечивает удовлетворительные результаты при переломах большеберцовой кости с сокращением времени наружной фиксации.
ЗАКЛЮЧЕНИЕ
Результаты исследования выявили эффективность наружной фиксации с применением эластичных интрамедуллярных спиц с HA-покрытием. Можно предположить, что комбинированный метод обеспечивает благоприят- ные механические и биологические условия для костного сращения. Это позволяет рекомендовать его для лечения переломов диафиза большеберцовой кости, при которых, как считается, нарушена костная регенерация.
Список литературы Комбинированный остеосинтез при лечении диафизарных переломов большеберцовой кости
- Milstrey A, Baumbach SF, Pfleiderer A, et al. Trends of incidence and treatment strategies for operatively treated distal fibula fractures from 2005 to 2019: a nationwide register analysis. Arch Orthop Trauma Surg. 2022;142(12):3771-3777. doi: 10.1007/s00402-021-04232-0
- Ylitalo AAJ, Dahl KA, Reito A, Ekman E. Changes in operative treatment of tibia fractures in Finland between 2000 and 2018: A nationwide study. Scand J Surg. 2022;111(3):65-71. doi: 10.1177/14574969221111612
- Alhadhoud MA, Alsiri NF. The epidemiology of traumatic musculoskeletal injuries in Kuwait: Prevalence and associated risk factors. J Taibah Univ Med Sci. 2022;17(4):685-693. doi: 10.1016/j.jtumed.2022.01.006
- Мироманов А.М., Гусев К.А., Усков С.А. и др. Современные подходы к диагностике нарушений консолидации при переломах. Гений ортопедии. 2017;23(1):12-15. doi: 10.18019/1028-4427-2017-23-1-12-15
- Jayaraju U, Rammohan R,Awad F, et al. Tibial Intramedullary Nailing by SuprapatellarApproach: Is It Quicker and Safer? Cureus. 2022;14(10):e29915. doi: 10.7759/cureus.29915
- Bhanushali A, Kovoor JG, Stretton B, et al. Outcomes of early versus delayed weight-bearing with intramedullary nailing of tibial shaft fractures: a systematic review and meta-analysis. Eur J Trauma Emerg Surg. 2022;48(5):3521-3527. doi: 10.1007/s00068-022-01919-w
- Shikinami Y, Matsusue Y, Nakamura T. The complete process of bioresorption and bone replacement using devices made of forged composites of raw hydroxyapatite particles/poly l-lactide (F-u-HA/PLLA). Biomaterials. 2005;26(27):5542-5551. doi: 10.1016/j.biomaterials.2005.02.016
- Костив Р.Э., Матвеева Н, Калиниченко СГ. Биоактивные покрытия на металлических сплавах и стимуляция восстановления костей после перелома. Тихоокеанский медицинский журнал. 2021;(2):31-36. doi: 10.34215/1609-1175-2021-2-31-36
- Popkov AV, Popkov DA, Kononovich NA, et al. Biological activity of the implant for internal fixation. J Tissue Eng Regen Med. 2018;12(12):2248-2255. doi: 10.1002/term.2756
- Lascombes P, Haumont T, Journeau P. Use and abuse of flexible intramedullary nailing in children and adolescents. J Pediatr Orthop. 2006;26(6):827-834. doi: 10.1097/01.bpo.0000235397.64783.d6
- Bolbasov EN, Popkov AV, Popkov DA, et al. Osteoinductive composite coatings for flexible intramedullary nails. Mater Sci Eng C Mater Biol Appl. 2017;75:207-220. doi: 10.1016/j.msec.2017.02.073
- Cao L, Han SM, Wu HZ, et al. Lower Tibial Shaft Spiral Fracture Concurrent with Distal Tibial Triplane Fracture. Curr Med Imaging. 2022;18(3):322-326. doi: 10.2174/1573405617666210716170213
- Hemmann P, Friederich M, Körner D, et al. Changing epidemiology of lower extremity fractures in adults over a 15-year period - a National Hospital Discharge Registry study. BMC Musculoskelet Disord. 2021;22(1):456. doi: 10.1186/s12891-021-04291-9
- Patel I, Young J, Washington A, Vaidya R. Malunion of the Tibia: A Systematic Review. Medicina (Kaunas). 2022;58(3):389. doi: 10.3390/ medicina58030389
- Ding P, Chen Q, Zhang C, Yao C. Revision with Locking Compression Plate by Compression Technique for Diaphyseal Nonunions of the Femur and the Tibia: A Retrospective Study of 54 Cases. Biomed Res Int. 2021;2021:9905067. doi: 10.1155/2021/9905067
- Radaideh A, Alrawashdeh MA, Al Khateeb AH, et al. Outcomes of Treating Tibial Shaft Fractures Using Intramedullary Nailing (IMN) versus Minimally Invasive Percutaneous Plate Osteosynthesis (MIPPO). Med Arch. 2022;76(1):55-61. doi: 10.5455/medarh.2022.76.55-61
- Upfill-Brown A, Hwang R, Clarkson S, et al. Rates and timing of short-term complications following operative treatment of tibial shaft fractures. OTA Int. 2021;4(4):e158. doi: 10.1097/0I9.0000000000000158
- Пичхадзе И.М., Кузьменков К.А., Жадин А.В. и др. Лечение переломов длинных костей конечностей методом чрескостного остеосинтеза на основе биомеханической концепции. Вестник травматологии и ортопедии им. Н.Н. Приорова, 2006;(4):12-17.
- May JD, Paavana T, McGregor-Riley J, Royston S. Closed Tibial shaft fractures treated with the Ilizarov method: A ten year case series. Injury. 2017;48(7):1613-1615. doi: 10.1016/j.injury.2017.05.019
- Cibura C, Ull C, Rosteius T, Lotzien S, et al. The Use of the Ilizarov Fixator for the Treatment of Open and Closed Tibial Shaft and Distal Tibial Fractures in Patients with Complex Cases. Z Orthop Unfall. 2022. English. doi: 10.1055/a-1910-3606
- Makhdoom AU, Shaikh BJ, Baloch RA, et al. Management Of Segmental Fracture Of Tibia Treated By Ilizarov External Fixation. J Ayub Med Coll Abbottabad. 2020;32(3):291-294.
- Popkov DA, Popkov AV, Kononovich NA, et al. Experimental study of progressive tibial lengthening in dogs using the Ilizarov technique. Comparison with and without associated intramedullary K-wires. Orthop Traumatol Surg Res. 2014;100(7):809-14. doi: 10.1016/j.otsr.2014.06.021
- Popkov AV, Gorbach EN, Kononovich NA, et al. Bioactivity and osteointegration of hydroxyapatite-coated stainless steel and titanium wires used for intramedullary osteosynthesis. Strategies Trauma Limb Reconstr. 2017;12(2):107-113. doi: 10.1007/s11751-017-0282-x
- Ирьянов ЮМ, Кирьянов Н.А., Попков А.В. Заживление перелома в условиях интрамедуллярного введения спиц с покрытием из гидрокси-апатита. Вестник РАМН. 2014;(7-8):127-132.
- Fini M, Cigada A, Rondelli G, et al. In vitro and in vivo behaviour of Ca- and P-enriched anodized titanium. Biomaterials. 1999;20(17):1587-1594. doi: 10.1016/s0142-9612(99)00060-5
- Попков А.В., Попков Д.А., Кононович Н.А. и др. Остеоинтеграция биоактивных имплантатов при лечении переломов длинных трубчатых костей: учебное пособие. Томск: Изд-во Томского политехнического университета; 2017:304 с.


