Комплексная лучевая оценка церебропротективной эффективности антигипертензивной терапии средствами МР-томографи и перфузионной СРКТ головного мозга
Автор: Федоренко Е.В., Wittsack H.-J., Русина А.М., Гуляев В.М., Шелковникова Т.А., Афанасьева Н.Л., Книпенберг Н.В., Мордовин В.Ф., Усов В.Ю.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4-2 т.23, 2008 года.
Бесплатный доступ
Проведено комплексное лучевое исследование го- ловного мозга у 22 пациентов с артериальной гипер- тензией (среднесуточное АДсист=152,8±7,6 мм рт. ст., среднесуточное АДдиаст=94,6±5,2 мм рт. ст.), без признаков сосудистых катастроф головного мозга в анамнезе, в динамике шестимесячной антигипер- тензивной терапии. При поступлении и через 6 ме- сяцев лечения выполнялись магнитно-резонансная томография (МРТ) и контрастированная динами- ческая спиральная рентгеновская компьютерная томография (ДинРКТ). По данным МРТ и ДинРКТ проведена оценка выраженности перивентрикуляр- ного отека, объемов ликворной системы и расчет ре- гионарного мозгового кровотока в абсолютных фи- зиологических единицах (как мл/мин/100 г ткани). Показатели анализировались в аспекте соотноше- ния положительной динамики картины МРТ и ДинРКТ и степени изменения артериального дав- ления. Установлено, что перивентрикулярный отек снижается, а кровоток в области базальных ядер улучшается у пациентов при снижении систоличе- ского АД на 12-28 мм рт. ст. В то же время меньшее или большее снижение АД не сопровождается досто- верным улучшением лучевой картины состояния го- ловного мозга. Таким образом, МРТ головного моз- га и перфузионная ДинРКТ могут быть использова- ны для оценки церебропротективной эффективнос- ти антигипертензивной терапии.
Перфузионная рентгеновская томография головного мозга, артериальная гипертензия, оценка лечения
Короткий адрес: https://sciup.org/14918966
IDR: 14918966 | УДК: 616.12-008.331.1-073.756.8
Complex radial assesment of cerebroprotective efficacy of antihypertensive therapy using MR-tomography and perfusion HRCT of the brain
A multimodal MRI-DynCT study of the brain was performed in 22 patients with arterial hypertension (mean systolic arterial pressure = 152,8±7,6 mm Hg, mean diastolic arterial pressure = 94,6±5,2 mm Hg) without history of coronary or cerebral infarctions signs. Significantly decreased periventricual oedema and improved perfusion of basal ganglii area were revealed in patients who demonstrated decreased systolic apterial pressure by 12-28 mm Hg. MRI and DynCT in patients who demonstrated decrease in systolic arterial pressure over or below of the interval were seen after treatment essentially the same as at admission. Thus we conclude that the brain MRI and perfusion DynCT data can be employed for evaluation of cerebroprotective efficacy of antihypertensive therapy.
Текст научной статьи Комплексная лучевая оценка церебропротективной эффективности антигипертензивной терапии средствами МР-томографи и перфузионной СРКТ головного мозга
В настоящее время методы функциональной оценки мозгового кровообращения при контрастированных рентгенологических исследованиях сосудов брахиоцефального бассейна у пациентов с наиболее распространенной патологией сердечно-сосудистой системы – артериальной гипертензией практически не применяются. Функциональные методы исследования мозгового кровотока в повседневной практике ограничиваются ультразвуковыми допплеровскими методиками [1, 2] и различными модификациями перфузионной однофотонной эмиссионной компьютерной томографии (ОЭКТ) головного мозга [3]. Контрастированная рентгеновская компьютерная томография (РКТ) и спиральная рентгеновская компьютерная томография (СРКТ) используются, как правило, для визуализации стенозов крупных сосудов [4, 5]. Между тем возможность точного количественного определения концентраций рентген-контрастного препарата в сосудах и тканях, присущая ДинРКТ, в сочетании с высоким временным и пространственным разрешением этого метода и использованием количественных моделей внутрисосудистой и внесосудистой кинетики индикаторов позволяет оценить тканевой кровоток в физиологических единицах (т.е. как мл/мин/100 г ткани) [6], не ограничиваясь простым контрастированием гемодинамического просвета артерий. Общепризнанными методами количественной оценки мозгового кровотока являются различные радионуклидные методы исследования, такие, как однофотонная эмис- сионая компьютерная томография (ОЭКТ) с 99mTc-ГМПАО или 99mTc-ЭЦД, либо позитронная эмиссионная томография с H215O [7]. Однако в аспекте широкого практического клинического применения ОЭКТ и ПЭТ оказываются малодоступны для больных с артериальной гипертензий и экономически неподъемны для бюджета больниц и клиник ввиду высокой себестоимости, малой распространенности установок и довольно большой временной длительности собственно исследования.
Между тем количественное исследование кровотока головного мозга у пациентов с артериальной гипертензией является исключительно важным, поскольку, как давно доказано, именно мозговой инсульт представляет собой одну из главных причин инвалидизации больных с хронической АГ при недостаточно эффективном контроле артериального давления [8, 9]. У пациентов с артериальной гипертензий в настоящее время изучаются возможные ранние маркеры нарушения мозгового кровообращения и оценки церебральной гемодинамической эффективности антигипертензивной терапии. Одним из таких маркеров или ранним признаком дисциркуляторных нарушений на уровне микроциркуляции является перивентрикулярная отечность белого вещества головного мозга [10]. В последнее время было показано, что у пациентов с артериальной гипертензией и микроциркуляторными нарушениями в области перивентрикулярного отека по данным МРТ головного мозга чаще отмечаются лакунарные и кортикальные инфаркты мозга, в том числе с летальными исходами [11, 12]. Однако их изменения в ходе антигипертензивной терапии остаются практически неизученными, хотя контрастированная ДинРКТ позволяет проводить рутинную оценку мозгового кровотока по всем бассейнам кровоснабжения, благодаря хорошо разработанным методикам и общедоступным полуавтоматическим пакетам обработки данных перфузионной ДинРКТ.
В группе пациентов с артериальной гипертензией мы попытались изучить количественно выраженность перивентрикулярного отека, показатели мозгового кровотока в области перивентрикуляр-ной отечности, в области базальных ядер и по бассейнам кровоснабжения передней, средней и задней мозговой артерии (ПМА, СМА, ЗМА соответственно) при первичном обследовании пациента и на фоне проводимой терапии через шесть месяцев клинического наблюдения, в аспекте сопоставления динамики артериального давления и показателей комплексного лучевого исследования головного мозга
МАТЕРИАЛ И МЕТОДЫ
Исследование было выполнено у 22 пациентов c неосложненной эссенциальной артериальной гипертензией II стадии (среднесуточное АДсист=152,8± 7,6 мм рт. ст., среднесуточное АДдиаст=94,6± 5,2 мм рт. ст.), без признаков перенесенных острых 31
нарушений коронарного и мозгового кровообращения, и в частности геморрагий или ишемических инфарктов головного мозга в анамнезе. Диагноз артериальной гипертензии был установлен по результатам комплексного лучевого исследования, с использованием ультразвукового исследования почек, рентгеновской катетерной ангиографии аорты и почечных артерий и/или контрастированной ДинРКТ-ангиографии почечных артерий и почек и комплексного эндокринологического исследования, позволивших исключить симптоматический характер патологии.
Всем пациентам при поступлении и через 6 мес терапии и наблюдения выполнена контрастированная динамическая перфузионная спиральная РКТ (ДинРКТ) головного мозга с количественным расчетом показателей мозгового кровотока. Собственно перфузионная ДинРКТ выполнялась как последовательность ежесекундных томосрезов толщиной по 5 мм на уровне тел боковых желудочков и базальных ядер в течение 40-45 с после болюсного введения рентгенконтрастного препарата (Визи-пак, «Никомед-Амершам» или Ультравист-370, «Шеринг-Байер»). При этом рентгеноконтрастный препарат вводился в объеме до 50 мл со скоростью 4-6 мл/с. Непосредственно вслед за этим немедленно выполнялась статическая РКТ – для оценки кровенаполнения, не меняя положения тела, на 60-й– 75-й с после введения контрастного препарата. На динамическом исследовании выделялась передняя мозговая артерия, обычно видимая на этих срезах из артериальных стволов лучше всего, и по изменению рентгенплотности (РП, ед. Хаунсфильда) изображения в ней строилась зависимость {РП-время}, которая затем при количественных расчетах мозгового кровотока использовалась в качестве входной артериальной функции. Кривые {РП-время} затем автоматически строились по всем точкам изображения. По результатам свертки входной артериальной функции и повоксельно полученных таким образом кривых {РП-время} были получены карты пространственного распределения регионального мозгового кровотока (рМК, в абсолютных физиологических единицах как мл/мин/100 г ткани).
В частности, региональный мозговой кровоток (рМК, мл/мин/100 г ткани) рассчитывался, исходя из очевидного соотношения среднего времени прохождения (СВП, с) болюса контраста через исследуемую область мозга и ее кровенаполнения и кровотока: СВП=рМОК/рМК. Поскольку в то же время величина рМОК соотносится с входной артериальной функцией как:
+∞
J tCcer (T)dT / р М О К = -∞ +∞ ,
/ J Ca (T)dT
-∞ а среднее время прохождения рентгенконтраста в области ткани мозга по определению представляет собой отношение:
CBΠ =
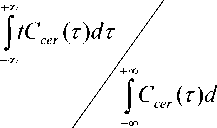
τ
то по имеющимся данным оказывается возможным автоматически рассчитать величину рМК.
Расчет величин РМК выполнялся с помощью специально разработанного пакета программ обработки данных перфузионной ДинРКТ в формате Dicom3.0 StrokeTool (разработка, кодирование и оптимизация пакета прикладных программ – [13], . Показатели кровотока анализировались раздельно для белого и серого вещества по артериальным бассейнам кровоснабжения головного мозга и отдельно – для области базальных ядер и области перивентрикулярной отечности.
Также всем пациентам при первичном обследовании и через 6 месяцев наблюдения была выполнена магнитно-резонансная томография (МРТ) головного мозга в Т1-взвешенном (TR=450 ms, TE=15 ms, a=70°) и в Т2-взвешенном (TR=6000 ms, TE=117 ms) режиме. Исследования проводились с получением изображений в аксиальной(параллельно орбитомеатальной линии) и сагиттальной плоскостях. Толщина срезов составляла 5 мм.
По данным МРТ исследования, помимо клинической визуальной верификации структурных изменений головного мозга была проведена количественная оценка показателей размеров ликворной системы и выраженность перивентрикулярного отека белого вещества головного мозга (ПВО). В частности рассчитывались такие показатели, как: поперечник боковых желудочков на уровне тела, мм, линейный размер зоны перивентрикулярного отека, мм; кровоток в области базальных ядер, мл/мин/100 г; мозговой кровоток, в области бассейнов артерий мозга (СМА, ПМА, ЗМА с расчетом отдельно кровотока в коре головного мозга и белом веществе), мл/мин/100 г; кровоток в области зоны перивентрикулярного отека, мл/мин/100 г; объем боковых желудочков, куб. см.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ.
Нормальные величины кровотока в физиологических абсолютных единицах, (как мл/мин/100 г), полученные у контрольных здоровых лиц без повышения артериального давления и без установленной соматической патологии методом перфузионной ДРКТ, составили в частности по бассейнам: бассейн передней мозговой артерии: кора головного мозга – 68,2±7,6 мл/мин/100 г ткани, белое вещество – 20,1± 7,2 мл/мин/100 г ткани; бассейн средней мозговой ар- терии: кора головного мозга – 76,2±9,6 мл/мин/100 г ткани, белое вещество – 19,4±8,9 мл/мин/100 г ткани; бассейн задней мозговой артерии: кора головного мозга – 95,3±9,3 мл/мин/100 г ткани, белое вещество 26,3±5,4 мл/мин/100 г ткани. Кровоток в области базальных ядер у пациентов с интактной тканью головного мозга составил в нашей контрольной группе 98± 2 мл/мин/100 г.
Величины мозгового кровотока рМК в физиологических абсолютных единицах (как мл/мин/100 г) при первичном обследовании у наших пациентов составили в среднем: бассейн ПМА: кора головного мозга – 48,2±7,6, белое вещество – 20,1±7,2; бассейн СМА: кора головного мозга – 56,2±9,6, белое вещество – 19,4±8,9; бассейн ЗМА: кора головного мозга – 55,3±9,3, белое вещество 26,3±5,4. Кровоток в области базальных ядер составил: 98±22 мл/мин/100 г, кровоток в области перивентрикулярного отека: 22,4±10,3 мл/мин/100 г.
При первичном МР-исследовании показатели ликворной системы составляли: линейный размер (ширина) переднего рога боковых желудочков – 5,2±2,5 мм, тела – 7,0±3,0 мм, заднего рога – 9±3,4 мм; линейная протяженность перивентрикулярного отека составила 2,2±2,8 мм.
По результатам контрольных исследований спустя 6 мес лечения анатомические показатели ликворной системы, выраженность перивентрикулярного отека, показатели кровотока и кровенаполнения ткани головного мозга в целом по группе обследован- ных не имели какого-либо однородного характера изменений. В нескольких случаях отмечалось увеличение линейных размеров желудочков мозга и пери-вентрикулярного отека, а также уменьшение показателей кровотока и кровенаполнения; у ряда пациентов верифицировано отсутствие какой-либо динамики по данным МРТ и СРКТ. Поэтому, основываясь на результатах контрольного обследования через 6 мес после начала лечения, нами были выделены две группы пациентов: 1-я – с положительной динамикой исследуемых параметров ликворной системы в виде уменьшения линейных размеров желудочков мозга и выраженности перивентрикулярного отека (типичная картина представлена на рис. 1 (см. обложку 3)); и 2-я группа – с отсутствием или отрицательной динамикой состояния ликворной системы головного мозга, у этих пациентов, как правило, отмечалось также отсутствие улучшения рМК как в области базальных ядер, так и в области лейкоареоза (перивентрикулярного отека) – рис. 2 (см. обложку 3). Детальные результаты исследования этих групп представлены в таблице.
При анализе клинических данных оказалось, что у пациентов первой группы в ходе проводимой терапии было достигнуто умеренное снижение САДсист от 138±8 мм рт. ст. до 126±6 мм рт. ст. Кроме того, у пациентов 1-й группы происходило увеличение кровотока в области базальных ядер. Во 2-й группе у пациентов на фоне терапии стойкого снижения артериального давления достигнуто либо не было, ли-
Таблица
Показатели кровотока и размеров боковых желудочков ликворной системы в динамике наблюдения пациентов с артериальной гипертензией
|
Показатели лучевого исследования головного мозга |
Исходно, в целом по группе обследованных, n=22 |
Через 6 мес терапии |
|||
|
1-я группа, n=12 (адекватное снижение АД в ходе терапии) |
2-я группа, n=10 (отсутствие динамики АД или избыточное его снижение) |
||||
|
Поперечник боковых желудочков на уровне тела, мм |
7±0,5 |
6,0±0,57 * |
7,2±1,04 |
||
|
Линейный размер зоны перивентрикулярного отека, мм |
2,2±0,46 |
2,2 ±0,34 |
2,18±0,86 |
||
|
Кровоток в области базальных ядер, мл/мин/100 г |
88±0,61 |
98±6,34 * |
87,6±6,84 |
||
|
Мозговой кровоток, в области кортикальных бассейнов артерий мозга, мл/мин/100 г |
ПМА |
Серое в-во |
85±0,61 |
84±6,63 |
83±6,65 |
|
Белое в-во |
27±1,16 |
26±2,59 |
27±2,53 |
||
|
СМА |
Серое в-во |
98±3 |
100±5,19 |
99±6,33 |
|
|
Белое в-во |
28±1,33 |
28±2,02 |
27±2,85 |
||
|
ЗМА |
Серое в-во |
80±3,16 |
81±6,05 |
81±6,65 |
|
|
Белое в-во |
25±1,5 |
24±3,46 |
25±2,85 |
||
|
Кровоток в области зоны перивентрикулярного отека, мл/мин/100 г |
22,1±1,72 |
22,9±2,97 |
22,3±3,26 |
||
|
Объем боковых желудочков, куб. см |
12±0,83 |
11±1,01 * |
12±1,58 |
||
– p < 0,05 при сравнении величин показателей после лечения с исходным значением.
бо, напротив, имело место выраженное снижение цифр САД от 154 до 123 мм рт. ст. [таблица, рис. 1, 2 (обложка 3)].
Таким образом, поскольку динамическая СРКТ с контрастированием при артериальной гипертензии и сопутствующем повреждении головного мозга позволяет рассчитать мозговой кровоток с высоким пространственным разрешением, обеспечивая точную оценку показателей рМК в абсолютных физиологических единицах [6, 13], в нашем случае она позволила показать, что при адекватной антигипертензивной терапии достигается улучшение кровоснабжения в области базальных ядер головного мозга (таблица). При этом величина снижения систолического артериального давления составляет от 10 до 22 мм рт. ст.
В то же время, как можно видеть по 2-й группе, достижение более выраженного снижения артериального давления у пациентов с артериальной гипертензией не ведет к улучшению мозгового кровотока. На фоне снижения артериального давления по сравнению с исходным САД более чем на 25% в ходе антигипертензивной терапии наблюдаются отрицательные изменения показателей ликворной системы, сопровождающиеся отеком белого вещества головного мозга в перивентрикулярной зоне, а также ухудшением кровотока и кровенаполнения головного мозга.
Таким образом, синхронное с благоприятной динамикой АД изменение показателей перфузии головного мозга и анатомических размеров ликворной системы позволяет говорить о самостоятельном значении томографических исследований головного мозга для оценки церебральной гемодинамики у пациентов с АГ. Действительно, ранее многократно и с использованием различных методов исследований (динамической сцинтиграфии [14], перфузионной ОЭКТ [15], перфузионной МРТ [16]) было доказано, что при артериальной гипертензии не происходит заметного снижения кровотока мозга в кортикальных отделах, но в значительной доле пациентов отмечается гипоперфузия в базальных ядрах [17], в перивентрикулярном белом веществе и в вертебробазилярном бассейне [18]. По данным проспективного инструментального наблюдения средствами МРТ за пациентами с артериальной гипертензией, не принимавшими регулярной адекватной терапии, как раз при наличии перивентрикулярных зон гиперинтенсивного Т2-взв. изображения отмечается повышенный риск мозгового инсульта, в том числе летального [12]. Наши данные вполне согласуются с этим. Именно при уменьшении перивентрикуляр-ного отека в ходе эффективной антигипертензивной терапии происходила практически полная нормализация кровотока в базальных структурах . В то же время в области собственно перивентрикулярной отечности не отмечалось заметного приращения кровотока. Вероятно, нарушения локальной микро-34
циркуляции в этих отделах носили стойкий характер, возможно, сопровождаясь органическими изменениями глиальных структур как при различных экспериментальных компрессионных моделях [19].
В то же время при отсутствии гипотензивного эффекта или, наоборот, при чрезмерном снижении артериального давления улучшения кровотока и положительных изменений со стороны ликворной системы не происходило. Это согласуется, в первую очередь, с отмеченной выше повышенной частотой мозговых инсультов у таких лиц [11, 12].
До сих пор МРТ головного мозга не включается в список методов исследований, проведение которых обязательно или весьма важно у лиц с артериальной гипертензией. Представленные здесь данные позволяют говорить, что именно МРТ головного мозга позволяет выявить изменения ликворных пространств и перивентрикулярных областей, сопровождающиеся повыщенным риском мозгового инсульта, с одной стороны, а с другой, – визуализировать положительную динамику в виде регресса перивент-рикулярной отечности в результате эффективной антигипертензивной терапии. В ближайшей перспективе, очевидно, при проведении клинических исследований эффективности антигипертензивных препаратов обоснованно включать в состав используемых методик технологии МРТ и перфузионной СРКТ головного мозга, как наиболее адекватно отражающих терапевтически существенные изменения в важнейшем из органов-мишенй АГ – головном мозге.
Список литературы Комплексная лучевая оценка церебропротективной эффективности антигипертензивной терапии средствами МР-томографи и перфузионной СРКТ головного мозга
- Гусев Е.И. Методы исследования в неврологии и нейрохирургии. -М.: Нолидж, 2000. -C. 222-236.
- Лелюк С.Э., Джибладзе Д.Н., Никитин Ю.М. Оценка состояния цереброваскулярного резерва у больных с сочетанной атеросклеротической патологией магистральных артерий головы с использованием функциональной нагрузочной пробы с ацетазоламидом//Ангиол. Сосуд. хир. -1995. -№ 3. -С. 7-23.
- Усов В.Ю., Плотников М.П., Шипулин В.М. Количественная томосцинтиграфическая оценка объема ишемического повреждения головного мозга: выбор оптимального радиофармпрепарата и техника расчета. ОЭКТ в исследованиях мозгового кровотока.//Мед. радиология. -1997. -№ 3. -C. 5-12.
- Калмин О.В. Ангионеврология. С-Пб.: СпецЛит, 2004.
- Meyer F.B., Sundt T.M.,Jr, Piepgras D.G., Sando B.A., Forbes B. Acute carotid occlusion//in: Occlusive Cerebrovascular disease. Diagnosis and surgical management (ed. by T.M. Sundt), Philadelphia, WB Saunders Co., 1987, P. 269-279.
- Marks M. P., Katz D. A. Spiral CT angiography of the cerebrovascular circulation//in: Fishman E.K. Jeffry R.B. Spiral CT: Principles, Techniques and Clinical Applications. -New York, 1995. -P. 671-682.
- Лишманов Ю.Б. Радионуклидная диагностика для практических врачей. Томск: STT, 2004, 394 с.
- Верещагин Н.В., Моргунов В.А., Гулевская Т.С. Патология головного мозга при атеросклерозе и артериальной гипертонии. М.: Медицина, 1997, 392 с.
- Auer L. The pathogenesis of hypertensive encephalopathy//Acta Neurochir.Wien. -1978. -V. 27. -P. 111-125.
- Lechner H., Schmidt R., Bertha G. et al. Nuclear magnetic resonance image white matter lesions and risk factors for stroke in normal individuals//Stroke. -1988. -V. 19. -№ 2. -P. 263-265.
- Шахматов М.А. Суточное мониорирование артериального давления и поражение органовмишеней у больных артериальной гипертонией. автореф. дисс… канд.мед. наук. -Томск, 1999. -26 с.
- Мордовин В.Ф., Семке Г.В., Афанасьева Н.Л., Лукъяненок П.И., Карпов Р.С. Церебральная патология у больных с артериальной гипертонией. Диагностика и лечение. Томск.: Изд-во ТГУ, 2007, 125 с.
- Wittsack H.-J. StrokeTool-CT. Manual. Koeln.: Digital-ImageSolutions, 2006, 45 P. www. digitalimagesolutions.de.
- Lassen N., Cristensen M. Physiology of cerebral blood flow//Brit. J. Anaesth. -1976. -Vol. 48. -P. 719-734.
- Seiderer M., Krappel W., Moser E., Hahn D., Schmiedek P., Buell U., Kirsch C.M., Lissner J. Detection and quantification of chronic cerebrovascular disease: Comparison of MR imaging, SPECT, and CT.//Radiology. -1989. -V. 170. -№ 2. -P. 545-548.
- Беличенко О.И., Федина И.Д., Арабидзе Г.Г., Беленков Ю.Н. Магнитнорезонансная томография в диагностике сосудистых поражений у больных артериальной гипертонией//Кардиология. -1987. -№ 2. -C. 67-71.
- Pantoni L.,Garcia J.H., Gutierres J.A. Cerebral white matter is highly vulnerable to ischemia//Eur.Neurol. -1996. -V. 27. -P. 16411647.
- Sacco R., Chair M., Emelia J. et al. Risk factors//Stroke. -1997. -V. 28. -P. 1507-1517.
- Hossmann K.A., Wechsler W., Wilmes F. Experimental peritumorous edema. Morphological and pathophysiological observations.//Acta Neuropathol (Berl). -1979. -Bd. 45. -S. 195-203.


