Комплексная NO- и лимфатическая терапия в лечении перитонитов различной этиологии
Автор: Вторенко В.И., Есипов А.В., Мусаилов В.А., Шишло В.К.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 6 (28), 2012 года.
Бесплатный доступ
В работе представлены результаты лечения пациентов с перитонитом, вызванным заболеваниями и повреждениями мочевыводящих путей. При сочетании лимфотропного введения амикацина и NO-обработки брюшной полости наблюдается максимально достижимый уровень содержания антибиотика в тканях брюшины с пролонгированием площади его фармакокинетической кривой до 48 часов, что определяет существенное увеличение продолжительности антибактериального эффекта используемых антисептических средств. Доказано, что лимфотропное введение антибиотиков сопряжено с пролонгированной их циркуляцией в крови.
Перитонит, лимфотропная терапия, no-терапия
Короткий адрес: https://sciup.org/142211067
IDR: 142211067 | УДК: 616.351-006.6-085
Текст научной статьи Комплексная NO- и лимфатическая терапия в лечении перитонитов различной этиологии
Методы клинической лимфологии успешно зарекомендовали себя в лечении перитонитов различного генеза. Одним из главных направлений в лечении данной патологии явилась эндолимфатическая антибактериальная терапия. Большой вклад в развитие исследований по этой проблеме внесли: Выренков Ю.Е., 1983–2012; Ярема И.В., 1999–2010; Ярема В.И., 2009; Вторенко В.И., 1986–2004; Евдокимов О.В., 1991; Карандин В.И., 2009; Шевхужев З.А., 2002; Лукьяненко Е.В., 2006; Колобов С.В., 2001; Ефименко Н.А., 2001; Чер-неховская Н.Е., 2011; Шишло В.К., 2011; Мартюшев А.В., 1999; Мержвинский И.А., 2002; Попов Ю.П., 1998.
Перитониты различной этиологии имеют свои особенности. В частности, перитонит, вызванный заболеваниями и повреждениями мочевыводящих путей. Частота перитонита, вызванного заболеваниями и травмами мочевой системы, составляет 10–15% от общего числа перитонитов, и летальность достигает 15% (Мартюшев А.В., 1999). Причи- нами такого перитонита являются: закрытая травма живота с внутрибрюшинным разрывом мочевого пузыря – 60,4%; перфорация мочевого пузыря инструментом – 6,25%; интраоперационное повреждение мочевого пузыря – 4,2%; самопроизвольный внутрибрюшинный разрыв мочевого пузыря на фоне гангренозного цистита или туберкулезного повреждения мочевого пузыря – 12,5%; самопроизвольный внутрибрюшинный разрыв мочевого пузыря на фоне распада опухоли мочевого пузыря – 10,4%; пионефроз с перфорацией в брюшную полость – 6,25% (Мартюшев А.В., 1999).
В настоящее время в хирургии особой популярностью и исследовательским интересом пользуется экзогенный монооксид азота. Он широко используется при лечении инфекции мягких тканей (Москаленко В.И., 2006; Ользе-ев И.С., 2004; Гостищев В.К. и др., 2004; Дарвин В.В. и др., 2007; Allen M.S., 2005), перитонита (Новиков К.В., 2003; Лукьяненко Е.В., 2006; Muller. B. et al., 2002) и остеомиелита (Беспалько В.И, 2000; Столяров Е.А. и др., 2007; Anaya D. et al., 2005; Fa-Si-Oen P.R., 2005).
В хирургической практике большое значение имеет участие эндогенного монооксида азота в развитии воспалительных реакций. Это определяется антимикробным эффектом NO за счет стимуляции макрофагов, индукции цитокинов, Т-лимфоцитов и ряда иммуноглобулинов, а также за счет его взаимодействия с кислородными радикалами, оказывая регулирующее влияние на микроциркуляцию, а также обеспечивая цитотоксический или цитопротективный эффект в зависимости от конкретных условий (Григорьян А.С. и др., 2001; Гундорова Р.А. и др., 2001; Laube S., 2004).
Кроме эндолимфатического введения лекарственных препаратов, был предложен способ лимфотропного введения препаратов, по фармакокинетике сходный с эндолимфатическими инфузиями. Особенно актуальными являются предложения использовать лимфотропное введение антибактериального средства, фармакокинетика которого приобретает «специфические» черты под влиянием экзогенного монооксида азота. Создание повышенной концентрации антибиотика в лимфатических узлах, а также в тканях оперируемой зоны, которая изначально подвержена патологическому процессу, обеспечивает потенцированный антибактериальный эффект. Основой их результирующейсоставляющейстановитсяуменьшениеколи-чества раневых инфекционно-воспалительных осложнений (Есипов В.А., 2011).
Актуальность проблемы
Установлено, что неадекватная антибактериальная терапия даже на фоне успешно выполненного оперативного вмешательства повышает вероятность летального исхода с 6,0% до 71,0% (Козлов Р.С., Голуб А.В. 2010). Антибактериальная терапия позволяет снизить летальность при перитоните только до 20%, однако неадекватное применение антибиотиков в послеоперационном периоде существенно ухудшает результаты лечения, увеличивая смертность, даже при адекватной и своевременно выполненной операции (Гельфанд Б.Р., Гологорский В. А., Бурневич С.З. с соавт., 2000; Шпигель А.С., 2004).
Несмотря на прогресс и успехи современной медицины, перитониты, вызванные заболеваниями и травмами мочевой системы, остаются актуальными. В улучшении результатов лечения данной категории больных могут помочь методы лимфотропного введения антимикробных препаратов, разрабатываемые Выренковым Ю.Е. и соавт. (1982–2005).
Цель исследования
Поиск критериев целесообразности применения комбинированной лимфатической и NO-терапии при с перитонитах, вызванных заболеваниями и повреждениями мочевыводящих путей.
Материал и методы
Настоящее исследование основано на анализе материалов историй болезни и клинических наблюдений 117
пациентов с перитонитом, вызванным заболеваниями и повреждениями мочевыводящих путей, которые находились на лечении в Филиале №1 ФГКУ «Главный военный клинический госпиталь имени академика Н.Н. Бурденко» Министерства обороны Российской Федерации. Москвы в 2000–2012 годах.
Проанализированы результаты диагностики и лечения этих пациентов. Для этого все пациенты были разделены на две группы.
Контрольную группу составили 65 человек, которым для лечения перитонита применяли только общепринятые методы лечения.
В основную группу вошли 52 пациента с перитонитом, у которых, кроме общепринятых методов лечения, проводилось лимфотропное введение амикацина и обработка брюшной полости экзогенным монооксидом азота. Пациентов данной группы лечили в три этапа. На первом этапе, во время предоперационной подготовки, проводилось лимфотропное введение амикацина. Интраоперационно проводилась обработка брюшной полости экзогенным монооксидом азота с помощью аппарата «Плазон» в режиме стимуляции-коагуляции из расчета 5–7 сек. на 1 см2. Третьим этапом, в послеоперационном периоде, продолжена лимфотропная антибактериальная и имммунотерапия, проводилась обработка брюшной полости через дренажные трубки аппаратом «Плазон» в режиме стимуляции «холодной плазмой» из расчета 15 сек/см2.
Возраст пациентов колебался от 18 до 62 лет. Средний возраст пострадавших составил: в основной группе 36,79±0,78 лет, в контрольной – 37,81±0,65 лет. Подавляющее число пострадавших – лица наиболее трудоспособного возраста: от 25 до 55 лет – 64,47% в основной группе и 65,29% в контрольной группе.
Наиболее часто в обеих группах встречались повреждения мочевого пузыря в виде его внутрибрюшинных разрывов (у 21,54% контрольной группы и 19,23% основной группы). Повреждения мочеточников с одной стороны имелись у 38,46% пострадавших контрольной группы и у 42,31% основной группы. Повреждения мочеточников с двух сторон – у 27,69% пострадавших контрольной группы и 26,92% основной группы. Ятрогенные повреждения мочевого пузыря имелись у 3,08% пострадавших контрольной группы и у 3,85% основной группы Ятрогенные повреждения мочеточников имелись у 9,23% пострадавших контрольной группы и у 7,69% основной группы.
Проведенный анализ результатов лечения показал достоверно значимые различия летальности в основной и контрольной группах (3,52% и 17,28% соответственно, p<0,05).
Средний койко-день в основной группе составил 15,45± ±1,07; в контрольной группе – 23,46±1,34, p<0,001. Это различие обусловлено достоверно более высокой летальностью первых трех суток послеоперационного периода в контрольной группе и наличием в контрольной группе таких пострадавших, у которых койко-день составил от 40 до 90 суток, что было обусловлено имеющейся сочетанной травмой с переломом таза и повреждением органов брюшной полости.
В основной группе пациенты со сроками лечения более 30 суток составили 26,94%, а в контрольной – 17,57%.
Оперативные вмешательства в обоих группах выполнялись по традиционной методике (лапаротомия) с привлечением урологов.
Перитонеальную жидкость получали у больных с перитонитом в послеоперационном периоде из дренажных трубок в течение трех суток от момента операции. Выпот из брюшной полости брали на исследование во время оперативного вмешательства – лапаротомии. В дальнейшем, в послеоперационном периоде, выпот брали на исследование через дренажные трубки, установленные в брюшную полость во время операции. Такую манипуляцию проводили ежедневно в течение всего периода пребывания дренажей в брюшной полости.
Критериями целесообразности предлагаемой терапии выбраны исследования клеточного состава перитонеальной жидкости и определение фармакокинетики амикацина. Определение концентрации амикацина осуществляли с помощью микробиологического метода – диффузии в агар с инокулированной культурой Staphylococcus aureus (штамм 209).
Полученные от больных мазки перитонеальной жидкости фиксировали спиртом и окрашивали селективным красителем тулоидиновым синим, являющимся самым специфичным для выявления тучных клеток. Другие пре-
После этого образцы замораживали в жидком азоте и раскалывали. После оттаивания в 96% этаноле процесс обезвоживания продолжался, препараты высушивали путем перехода через критическую точку в СО2 и напыляли золотом или платиной. Анализ препаратов проводили сканирующим электронным микроскопом Phillips PSEM – 500х со съемкой на коммерческую широко- и узкоформатную пленку.
Результаты и обсуждение
Анализ полученных данных показал, что после внутривенного введения концентрация амикацина в перитонеальной жидкости больных с перитонитом, вызванным заболеваниями и травмами мочевых путей через 3 часа от момента введения составила 5,8±0,4 мг/мл. Через 6 часов – 0,9±0,1 мг/мл. Через 9 часов препарат в перитонеальной жидкости не обнаружен. При лимфотропном введении через 3 часа концентрация амикацина в перитонеальной жидкости составила 4,7±0,6 мг/мл. Через 6 часов – 7,1±0,5 мг/мл; через 9 часов – 6,1±0,4мг/мл; через 12 часов – 3,7±0,2 мг/мл; через 18 часов – 2,1±0,3 мг/мл; через 24 часа – 1,6±0,2 мг/мл; через 36 часов – 0,8±0,1 мг/мл. Через 48 часов в перитонеальной жидкости определялись следы препарата. Таким образом, наивысшая концентрация препарата при лимфотропном его введении определялась через 6 часов. Период полувыведения (Т1/2) составил 12 часов. Общая площадь фармакокинетической кривой составила 36 часов.
В условиях лимфотропного введения антибиотика на фоне NO-терапии пик концентрации амикацина наблюдается к 6 часу от момента эксперимента. Такое содержание антибиотика сохраняется до 12 часов исследования, и только затем его концентрация постепенно снижается. Препа- параты окрашивали моноклональными антителами типа PCNA для определения пролиферативной активности популяции лимфоцитов и макрофагов. Часть препаратов готовили для исследования с помощью сканирующей электронной микроскопии нативных препаратов (СЭНП). Для приготовления нативных препаратов перитонеальную жидкость отмывали от крови с помощью гепаринизированной среды 199 и фиксировали перфузией 2,5% раствором глютарового альдегида на среде 199, обрабатывали 1% раствором осмиевой кислоты, обезвоживали в этаноле
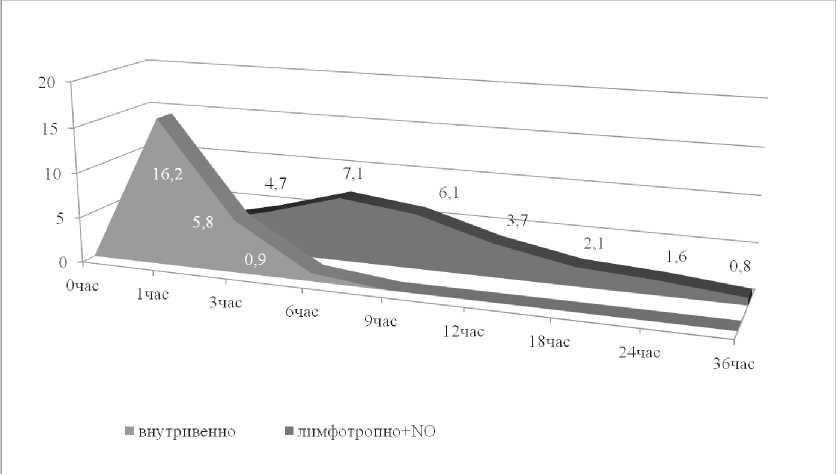
Рис. 1. Фармакокинетическая кривые при внутривенном и лимфотропном введении амикацина
восходящей концентрации.
рат определяется в крови до 36 часов опыта, и на всех этапах исследования его содержание было в 4 раза выше по сравнению с теми больными, которым NО-терапия не проводилась. Более того, амикацин пусть и в минимальном количестве определяется в перитонеальной жидкости даже через 48 часов от начала эксперимента.
Изложенное свидетельствуют о том, что лимфотропное введение амикацина сопряжено с пролонгированной его циркуляцией в перитонеальной жидкости. Несмотря на то, что максимальное содержание антибиотика при внутривенном введении выше (почти в 2 раза), быстрая его элиминация оставляет рану без нужной защиты от бактериальной интервенции. В свою очередь лимфотропное введение антибиотика на фоне обработки брюшной полости экзогенным монооксидом азота накладывает позитивный отпечаток на фармакокинетические характеристики амикацина. Важнейшей среди них является значительная «задержка» медикаментозного средства в перитонеальной жидкости, что пролонгирует распределение антибиотика в организме в терапевтической концентрации.
Комплексное воздействие на покровные ткани в зоне предстоящей операции, включающее традиционную обработку, лимфотропное введение амикацина за 30 минут до выполне-

Рис. 2. Клетки перитонеальной жидкости, взятые до начала лечения (в ходе операции, до применения NO- и лимфатической терапии). На данном препарате показаны полностью дегранулирующие тучные клетки и различные формы видоизмененных эритроцитов (эхино-циты, сфероциты) как результат эндотоксикоза. (Э – эритроцит, ТК – тучная клетка, ЛЦ – лимфоцит). СЭМ НП х 4800

Рис. 3. Клетки перитонеальной жидкости, взятые из дренажных трубок на третьи сутки после комплексной NO- и лимфатической терапии. Заметно депонирование биологически активных ингридиентов (биоаминов) в тучных клетках, отсутствие патологических форм эритроцитов и обилие лимфоцитов. СЭМ НП х 4800
ния разреза и превентивную обработку операционного поля экзогенным монооксидом азота, сопровождается ощутимым «антисептическим» эффектом. В 94% наблюдений мазки, взятые с поверхности кожи, стерильны, в остальных случаях микроорганизмы высеваются в минимальном количестве – менее 102 КОЕ/см2 кожного покрова. Выделенная микрофлора являет собой моногамный спектр бактерий (Staphylococcus aureus, Esherichia coli, Streptococcus epidermidis), которые обладают исходной чувствительностью к антибактериальным средствам, которая регистрируется при бактериологической оценке состояния операционного поля до производства хирургического вмешательства.
Микробиологическое исследование, при котором забор материала осуществляли перед зашиванием операционной раны после воздействия на нее экзогенным монооксидом азота, показывает, что стартовые потенции раневого процесса в данном случае имеют весьма благоприятный статус. Микрофлора высевается лишь в 5% клинических наблюдений и только в виде монокультуры Staphylococcus aureus, Esherichia coli, Streptococcus epidermidis с минимальными количественными характеристиками (в пределах 2,2× Х 10 2 КОЕ/см2) В качественном же отношении выделенные микроорганизмы не отличаются от тех, что высевались перед операцией при заборе материала непосредственно перед рассечением тканей передней брюшной стенки. Данное обстоятельство позволяет сделать заключение о том, что антисептический эффект использованного комплекса превентивных мер сохраняется, по крайней мере, до конца оперативного вмешательства.
При сравнении методов введения отмечено явное преимущество лимфотропного метода, на что указывают данные фармакокинетики.
Исследование перитонеальной жидкости в послеоперационном периоде показало увеличение площади фармакокинетической кривой до 48 часов с сохранением рабочей терапевтической концентрации, которая составила 1,2±0,1 мг/ мл. Эти данные не противоречат исследованиям Москаленко В.И (2007), проведенным в раневом экссудате у раненых.
В первые сутки у обеих групп больных тучные клетки (перитонеальные лаброциты) в основном находились в состоянии дегрануляции и фактически цитоплазма их была пустая, т.е. не содержала гранул с биологически активными веществами (гистамин, гепарин, серотонин).
Ко вторым суткам после операции гистологическая картина у больных первой группы оставалась без изменений. Во второй группе заметно увеличение в клеточной популяции тучных клеток в стадии депонирования, причем к третьим суткам количество депонирующих клеток значительно преобладало над дегранулирующими, чего не наблюдалось у больных первой группы.
При изучении пролиферации лимфоцитов и макрофагов в мазках перитонеальной жидкости выявлено присут- ствие как «малых активных» лимфоцитов, так и «больших» лимфобластов и макрофагов. В первые сутки у обеих групп отмечено нарастание пролиферативной активности, которое во второй группе к третьим суткам была значительно выше, чем в первой группе. Данные морфометрические критерии перитонеальной жидкости отражают состояние местного иммунного статуса и изменяются в зависимости от методов лечения и от проводимой в послеоперационном периоде терапии.
Заключение
При сочетании лимфотропного введения амикацина и NO-обработки брюшной полости наблюдается максимально достижимый уровень содержания антибиотика в тканях брюшины с пролонгированием площади его фармакокинетической кривой до 48 часов, что определяет существенное увеличение продолжительности антибактериального эффекта используемых антисептических средств. Благодаря подобному «тандему» NO-обработки раны и лимфотропной антибиотикопрофилактики в совокупности со способностью экзогенного монооксида азота «материально обеспечивать» реакции репаративной регенерации, достигается возможность оптимального управления раневым процессом, при котором отмечается максимальное уменьшение частоты развития послеоперационных инфекционновоспалительных осложнений.
Доказано, что лимфотропное введение антибиотиков сопряжено с пролонгированной их циркуляцией в крови. Несмотря на то, что максимальное содержание антибиотика при внутривенном введении выше (почти в 2 раза), быстрая его элиминация оставляет рану без нужной защиты от бактериальной интервенции. В свою очередь лимфотропное введение антибиотика на фоне обработки брюшной полости экзогенным монооксидом азота накладывает позитивный отпечаток на фармакокинетические характеристики амикацмна. Важнейшей среди них является значительная «задержка» медикаментозного средства в плазме крови, что пролонгирует распределение антибиотика в организме в терапевтической концентрации.
Выводы
-
1. Проведенное исследование концентрации амикацина при различных методах введения показывает преимущество лимфотропного введения антибиотиков на фоне воздействия воздушно-плазменными потоками.
-
2. На фоне лимфатической антибиотикотерапии степень обсемененности отделяемого из брюшной полости нормализовалась раньше, чем при использовании традиционных методов введения.
-
3. Морфометрические показатели клеточных популяций перитонеальной жидкости могут отражать динамику изменений в системе местного иммунитета и позволяют прогнозировать течение послеоперационного периода.
-
4. Необходимость дальнейшего целенаправленного изучения всех аспектов перитонита, вызванного заболеваниями и травмами мочевой системы, совершенствование известных и разработка новых методов его лечения с использованием комбинированной терапии монооксидом азота и лимфотропным введением антибиотиков определили актуальность настоящего исследования. Доказана необходимость проведения комбинированной терапии в комплексе лечения больных мочевым перитонитом, что позволяет улучшить результаты лечения, снизить летальность, количество послеоперационных осложнений, добиться экономии денежных средств и улучшения качества жизни у данной категории больных.
Список литературы Комплексная NO- и лимфатическая терапия в лечении перитонитов различной этиологии
- Сажин В.П., Бодрова Н.Г., климов д.Е. и др. Антибиотикотерапия при гнойных хирургических заболеваниях органов брюшной полости и мягких тканей//Хирургия. 2010. С. 4-10.
- Под ред. Волковой О.В., Шахламова в.А., А.А. миронова А.А. Атлас сканирующей электронной микроскопии клеток, тканей и органов. М.: Медицина, 1987. 464 с.
- Вторенко В.И. Клинико-экспериментальное обоснование применения лимфогенных методов в комплексном лечении перитонита. Автореф. дисс..д-ра мед. наук. М., 2002. 64 с.
- Вторенко В. И., городов С.Ю., богодаров м.Ю. Восстановление специфической иммунной защиты при лимфогенных методах терапии перитонита//Вестн. лимфологии. 2007. №3. С. 17-23.
- Евдокимов В.В. Патогенетические критерии диагностики комплексного лечения распространенного перитонита с включением лимфологических методов. Автореф. дисс.. д-ра мед. наук. М., 2002. 42 с.
- Карандин В.И. Эфферентная терапия в лечении тяжелых хирургических эндотоксикозов (клинико-экспериментальное исследование). Автореф. дисс.д-ра мед.наук. М., 2009. 50 с.
- Выренков Ю.Е., Есипов А.В., москаленко в.И., Шишло в.к. Комплексная NO-и лимфатическая терапия в клинической практике. М., 2011. 286 с.
- Лукьяненко Е.В. Использование NO-содержащих воздушно-плазменных потоков в комплексном лечении перитонита. Автореф. дисс.канд. мед. наук. М., 2006. 22 с.
- Под ред. Савельева В.С. Перитонит. Практическое руководство. (Серия: «Практические руководства»). М.: Литтера, 2006. 208 с.
- Попов Ю. П. и др. Лечение мочевого перитонита с использованием эндолимфатической антибиотикотерапии//Материалы научно-практической конференции, посвященной 100-летию Московской городской больницы №40. М., 1998.
- Страчунский Л.С., белоусов Ю.б., козлов С.н. Практическое руководство по антиинфекционной химиотерапии. Смоленск: МАКМАХ, 2007. 350 с.
- выренков Ю.Е. и др. Применение лимфологических методов в хирургии и интенсивной терапии. Учебно-методическое пособие. Краснодар, 2007. 62 с.
- Мартов Ю.Б. и др. Распространенный перитонит. Основы комплексного лечения. М.: Издательство «Триада-Х», 1998. 144 с.
- Ефименко Н.А., чернеховская н.Е., выренков Ю.Е. Руководство по клинической лимфологии. М., 2001.
- Djakovic N., Plas E., Martinez-Pineiro L. et al. Травматические повреждения органов мочевыделительной системы. Перевод В.А. Черняев. Европейская ассоциация урологов, 2010. 86 с.
- Ярема И. В. и др. Метод лекарственного насыщения лимфатической системы//Хирургия. 1999. №1. С. 14-16.


