Контрастированная магнитно-резонансная томография у пациентов с перенесенным инфарктом миокарда и предсердными тахиаритмиями
Автор: Усов Владимир Юрьевич, Бабокин Вадим Егорович, Мочула Ольга Витальевна, Лукьяненок Павел Иванович, Шелковникова Татьяна Александровна, Попов Сергей Валентинович, Бородина Елена Евгеньевна, Курлов Игорь Олегович, Оферкин Александр Иванович
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4 т.29, 2014 года.
Бесплатный доступ
Представлены результаты использования магнитно-резонансной томографии (МРТ) сердца с парамагнитным контрастированием для визуального выявления очагов повреждения миокарда, провоцирующих развитие предсердных нарушений ритма у пациентов с перенесенным обширным инфарктом левого желудочка. Показано, что объем левого предсердия более 75 см 3 и накопление контраста-парамагнетика в миокарде предсердий с индексом усиления в Т1-взв. спин-эхо режиме более 1,27 являются прогностическими факторами в отношении развития наджелудочковых тахиаритмий, а МРТ сердца с контрастированием является важным дополнительным методом исследования у пациентов с предсердными нарушениями ритма сердца.
Магнитно-резонансная томография сердца с контрастным усилением, наджелудочковые тахиаритмии
Короткий адрес: https://sciup.org/14919977
IDR: 14919977 | УДК: 616.12-008.318-073.86
Contrast-enhanced magnetic resonance tomography in patients with myocardial infarction and supraventricular tachyarrhythmias
Contrast-enhanced MRI of the heart was employed for visual detection of risk as well of anatomic locations of atrial arrhythmias in patients with previous myocardial infarction. Data showed that pathologic uptake of paramagnetic to the atrial myocardium with enhancement index over 1.27 (in T1-weighted spin-echo mode) and concomitant increase of left atrial volume over 75 mL provided prognostic factor for manifestation of atrial tachyarrhythmias and endocardial destruction procedure in the nearest future. Therefore the contrast-enhanced MRI can be included to the diagnostic algorithm for patients with ischaemic heart disease and risk of supraventricular tachyarrhythmias.
Текст научной статьи Контрастированная магнитно-резонансная томография у пациентов с перенесенным инфарктом миокарда и предсердными тахиаритмиями
Магнитно-резонансная томография (МРТ) сердца с парамагнитным контрастированием стала на сегодня наиболее чувствительным и специфичным и к тому же широко доступным методом выявления как ишемического, так и воспалительного повреждения миокарда [6, 8]. Однако применение парамагнетиков в диагностике патологии сердца до сих пор ограничивается использованием при поражении желудочков, тогда как визуализация повреждений предсердий не внедрена в повседневную кардиологическую практику. В то же время средства МР-ангиографии предсердий давно и широко используются для оценки топографии легочных вен и дальнейшего планирования транскатетерных аблационных вмешательств [11]. Хотя повреждение миокарда предсердий механически влияет на развитие сердечной недостаточности слабо, предсердные пароксизмальные тахиаритмии приводят к достоверному прогрессированию сердечной недостаточности за счет нарушений сократимости и расслабления миокарда желудочков на фоне аритмии [5]. В особенности это клинически важно для пациентов с одновременным повреждением сократительного миокарда левого желудочка (ЛЖ) [7].
Морфологически причиной развития аритмий, как правило, является значительная неоднородность ультраструктуры предсердий за счет чередования зон поврежденного и сохранного миокарда [4]. Повреждение миокарда наиболее эффективно оценивается средствами МРТ с контрастным усилением. Поэтому важно оценить, насколько признаки повреждения миокарда предсердий, выявляемые при МРТ с контрастированием парамагнетиками, могут быть использованы для оценки риска наджелудочковых тахиаритмий у пациентов, перенесших острый инфаркт миокарда (ОИМ).
Материал и методы
МР-томографическое исследование сердца с парамагнитным контрастированием было выполнено у 20 пациентов (18 мужчин, 2 женщины, возраст 57±6 лет) с распространенным атеросклерозом аорты и коронарных артерий и перенесенным ОИМ ЛЖ в ходе их рутинного инструментального кардиологического исследования.
Из 20 обследованных у 8 (группа 1) отмечались единичные наджелудочковые и желудочковые экстрасистолы или эпизоды фибрилляции предсердий, купировавшиеся спонтанно. У 12 впоследствии в течение 2–4 мес. после перенесенного ОИМ отмечались эпизоды частых пароксизмальных наджелудочковых тахиаритмий, причем 9 пациентам потребовалось выполнение операции радиочастотной аблации – изоляции устьев легочных вен либо истмической области правого предсердия. Эти 12 пациентов составили группу 2.
Контрольную группу составили пациенты с патологией органов грудной клетки и позвоночника без при- знаков клинически значимого атеросклероза (9 мужчин в возрасте 58±8 лет), которым контрастированное исследование грудной клетки и грудного отдела позвоночника выполнялось по ортопедическим показаниям. В аспекте настоящего исследования им дополнительно выполнялась лишь ЭКГ-синхронизация записи изображений грудной клетки.
МРТ с контрастным усилением была выполнена с полным охватом области сердца и средостения в аксиальной плоскости. Введение парамагнетика осуществлялось в дозе 0,1 ммоль/1 кг массы тела. До и спустя 12–15 мин после введения парамагнетика были записаны Т1-взве-шенные спин-эхо изображения, при TR=450–700 мс, TE=15–20 мс, в матрицу 256х256 пикселей, при размере области исследования до 250х250 мм и толщине томос-реза 7–8 мм (МР-томограф Magnetom Open, Siemens Medical).
Анализ изображений осуществлялся визуально двумя независимыми рентгенологами, не информированными о деталях клинической картины пациента. Рассчитывались следующие показатели:
– объем левого предсердия, см3;
– индекс усиления Т1-взв. спин-эхо МРТ сердца при ПМ контрастировании, по наибольшему очагу в левом предсердии. (ИУ), как отношение интенсивностей на контрастированном и исходном МРТ-исследовании;
– объем включения парамагнетика в наибольшем очаге поглощения ПМ, см3;
– суммарный объем включения парамагнетика в очагах в левом предсердии, см3.
Проводились также исследования по протоколам Т2-взвешивания, инверсия-восстановление и исследования сократимости миокарда в кино-режиме.
Статистическая обработка результатов была проведена с использованием как параметрических (t-критерий), так и непараметрических (Манна–Уитни, Вилкоксона) критериев.
Результаты
У пациентов контрольной группы индекс усиления интенсивности Т1-взв. спин-эхо изображений МРТ в области стенки левого предсердия составил при контрастировании 1,03±0,4, а значимых очагов усиления интенсивности не выявлялось.
Сравнение результатов МР-томографического и кате-теризационного электрофизиологического исследования у пациентов с тахиаритмиями (группа 2) показало, что достоверной детальной топической корреляции между локализациями очагов патологического включения парамагнетика и расположением путей ре-энтри или эктопического очага нет – прямое анатомическое соответствие имело место лишь в 3 случаях из 12. Однако электрофизиологический субстрат аритмии, как правило, в 10 случаях из 12 выявлялся все же на стороне очага наибо-
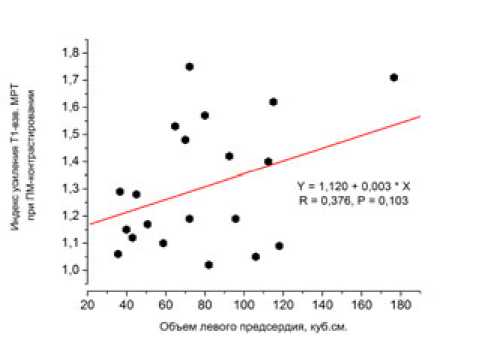
Рис. 2. Взаимоотношения показателей объема левого предсердия (а) и объема очагового включения парамагнетика в наиболее интенсивном очаге в левом предсердии (б) у обследованных пациентов. Очевидно отсутствие взаимозависимости этих показателей
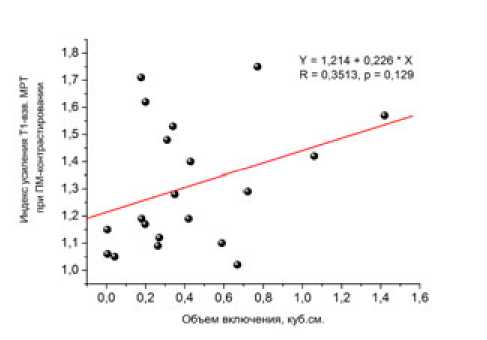
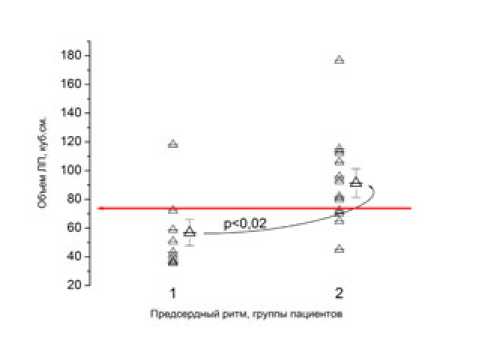
Рис. 3. Величины объема левого предсердия в группах с синусовым ритмом (1) и наджелудочковыми тахиаритмиями (2). Представлены как распределения индивидуальных значений, так и среднегрупповые величины. Горизонтальной линией со стрелкой отмечена величина объема левого предсердия, в 75 мл выше которой располагались лишь случаи пациентов с наджелудочковыми тахиаритмиями
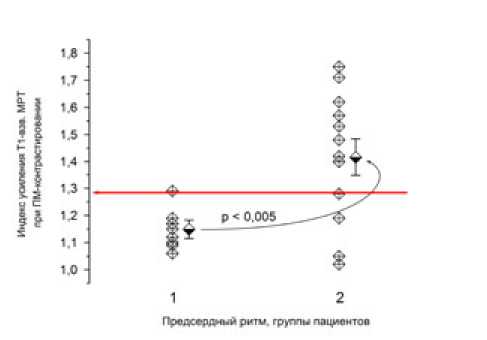
Рис. 4. Показатели индекса усиления Т1-взв. изображения МРТ в группах с синусовым ритмом (1) и наджелудочковыми тахиаритмиями (2). Представлены распределения индивидуальных значений и среднегрупповые величины. Горизонтальной линией со стрелкой отмечена величина ИУ=1,27, выше которой располагались лишь случаи, включающие пациентов с наджелудочковыми тахиаритмиями
лее интенсивного накопления парамагнетика в левом предсердии.
Среди пациентов с сохранным предсердным ритмом лишь у одного включение носило многоочаговый характер, тогда как при предсердных тахиаритмиях – у половины (6 из 12, p<0,05 по критерию χ 2). По расположению очага наиболее интенсивного включения парамагнетика, для “тахиаритмической” группы в случае сочетания двух очагов, оно, как правило, состояло из включений в нижней части перегородки с распространением вправо в область истмической зоны возле впадения нижней полой вены и также очагового включения в области устьев легочных вен левого легкого (рис. 1, см. 3-ю стр. обложки).
Количественные показатели, полученные при анализе картины контрастированной МРТ сердца в области предсердий в режиме Т1-взвешенного спин-эхо для групп пациентов с синусовым ритмом (группа 1) и с наджелудочковыми тахиаритмиями, не купировавшимися спонтанно и потребовавшими затем проведения транскатетерного аблационного вмешательства (группа 2), представлены в таблице.
При сопоставлении между собой показатели индекса усиления интенсивности Т1-взв. изображения предсердий и объема предсердий (рис. 2а), а также и объема собственно включения (рис. 2б) достоверно не коррелировали.
В целом, как можно видеть, показатели, характеризовавшие объем предсердий и собственно включение контраста-парамагнетика в анатомические структуры предсердия, не были взаимозависимыми.
В группе 2 – у лиц с наджелудочковой тахиаритмией
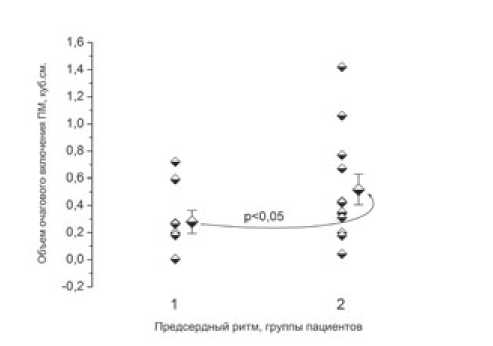
Рис. 5. Показатели объема включения парамагнетика в наиболее интенсивном очаге (а) и в целом по предсердию (б) в группах с синусовым ритмом (1) и наджелудочковыми тахиаритмиями (2). Представлены распределения индивидуальных значений и справа от них среднегрупповые величины
8 25 S

£
1 2
Предсердный ритм, группы пациентов
Таблица
Количественные показатели оценки состояния предсердий при контрастированной МРТ сердца у пациентов с синусовым ритмом (в т.ч. с эпизодами фибрилляции предсердий или наджелудочковой экстрасистолией) и пациентов с наджелудочковой тахиаритмией (как среднее±ошибка среднего)
Сходное высоко достоверное межгрупповое различие отмечалось и по величине индекса усиления Т1-взв. спин-эхо МРТ сердца при ПМ контрастировании, оцениваемом по наибольшему очагу в левом предсердии (рис. 4). Для этого показателя разброс в группе пациентов с синусовым ритмом был существенно меньше, так что величина ИУ>1,27 означала достоверную принадлежность к группе 2, “тахиаритмической”.
Как величина объема включения парамагнетика в наибольшем очаге поглощения, так и в особенности суммарный объем включения парамагнетика по левому предсердию в целом, были достоверно и значительно выше в группе 2 (рис. 5а, б).
Таким образом, пациенты с предсердными тахиаритмиями характеризовались при контрастированной Т1-взвешенной МРТ сердца более интенсивным и распространенным включением парамагнетика в стенку предсер- дия, а также достоверно большей степенью дилатации левого предсердия.
Обсуждение
Визуализация повреждения предсердий средствами контрастированной МРТ или с помощью различных модификаций Т2-взвешенного спин-эхо исследования используется в кардиологии достаточно давно, но почти исключительно для характеристики повреждения миокарда при различных электродеструкционных процедурах в ходе аблации предсердных аритмий [13, 14]. Такой подход, безусловно, важен и неоспорим, поскольку методы контрастированной МРТ обладают исключительной, практически безальтернативной чувствительностью в выявлении всех форм повреждения миокарда [9].
В последнее время МРТ удачно используется для текущего мониторирования расположения электродов при проведении внутрисердечных электрофизиологических исследований и аблации источников аритмий [10].
Однако в кардиологической клинике не менее важна задача своевременной ранней оценки риска развития пароксизмальных наджелудочковых тахиаритмий на воз- можно ранних стадиях их проявления, в частности у пациентов, перенесших острый инфаркт миокарда. Такие задачи, как правило, решаются средствами внутрисердечного электрофизиологического исследования [1], тем более что оно всегда может быть расширено до терапевтического вмешательства – проведения локальной электродеструкции ткани для подавления патологического очага автоматизма или разрыва путей циркулирующего возбуждения [2, 3]. К сожалению, средства контрастированной МРТ для такого прогноза практически не используются. В то же время методически средства МРТ, безусловно, заняли место стандарта в оценке как ишемического, так и некоронарного повреждения [6]. Поэтому представлялось рациональным опробовать МРТ сердца для оценки риска наджелудочковых аритмий.
В наших группах оказалось, что с развитием наджелудочковых тахиаритмий связаны изменения объема левого предсердия. Геометрические размеры и объем левого предсердия являются одним из существенных предикторов предсердных нарушений ритма, в частности наиболее опасных тахиаритмий [1, 4, 12]. Поскольку при ЭКГ-синхронизированной МРТ сердца количественный расчет объема левого предсердия относительно нетруден, а представленные здесь данные достоверно доказывают взаимосвязь его с развитием тахиформ предсердных аритмий, целесообразно предлагать оценивать объем левого предсердия во всех случаях проведения МРТ-ис-следования сердца у постинфарктных больных.
Абсолютным преимуществом МРТ перед другими методами исследования сердца является возможность с высоким, субмиллиметровым и миллиметровым, пространственным разрешением выявлять очаги повреждения миокарда с помощью парамагнитного контрастирования [9] и визуализации тканевого накопления контраста либо в Т1-взвешенном спин-эхо режиме, либо с помощью дополнительного использования протоколов с инверсией и адаптивным подбором времени инверсии – минимизацией интенсивности изображения здорового миокарда и максимумом поврежденного. Последний метод наиболее эффективен в исследованиях поражения миокарда желудочков [7], но не предсердий. По нашему опыту, представленному здесь, Т1-взвешенное спин-эхо исследование является вполне информативным в оценке визуальной картины предсердного накопления парамагнетика и его интенсивности. При этом объем и интенсивность включения достоверно выше у пациентов с тахиаритмиями, а сочетание признаков расширения предсердия более 75 см3, показателя ИУ более 1,27, а также множественный характер очагов включения прямо указывали на неизбежность развития наджелудочковых тахиаритмий.
Несомненно, необходима детализация представленных данных в аспекте прямого анатомического сопоставления результатов электрофизиологического и МР-томографического исследования, поскольку у наших пациентов они топически не совпадали. Однако для корректности такого исследования необходимы соответствующие программные средства сочетанного анализа и сопоставления изображений, которые пока еще только создаются. Кроме того, необходимо сравнение контрастированной МРТ у пациентов с наджелудочковыми тахи- аритмиями ишемического и некоронарогенного генеза.
Однако уже представленные данные свидетельствуют, что МР-томографическое исследование сердца с парамагнитным контрастированием миокарда предсердий является существенным дополнительным методом исследования при наджелудочковых нарушениях ритма и позволяет предполагать их проявление у пациентов с перенесенным ОИМ. Дальнейшее накопление результатов использования контрастированной МРТ при наджелудочковых тахиаритмиях, вероятно, дополнительно усилит и конкретизирует диагностическое значение МРТ сердца у таких пациентов.
Список литературы Контрастированная магнитно-резонансная томография у пациентов с перенесенным инфарктом миокарда и предсердными тахиаритмиями
- Алеев В.Р., Антонченко И.В. Особенности электрофизиологических процессов у пациентов с пароксизмальной и хронической формами фибрилляции предсердий//Вестник аритмологии. -2003. -№ 34. -С. 38-43.
- Антонченко И.В., Татарский Б.А., Попов С.В. Лечение пароксизмальных форм фибрилляции предсердий//Вестник аритмологии. -2009. -№ 53. -С. 3-10.
- Артеменко С.Н., Романов А.Б., Туров А.Н. и соавт. Сравнительная оценка радиочастотной остиальной, антральной изоляции устьев легочных вен и аблации ганглионарных сплетений у пациентов с фибрилляцией предсердий//Вестник аритмологии. -2012. -№ 68. -С. 14-20.
- Баталов Р.Е., Антонченко И.В. Патофизиологические предпосылки катетерного лечения фибрилляции предсердий//Вестник аритмологии. -2010. -№ 60. -С. 70-74.
- Бокерия Л.А., Филатов А.Г., Ковалев А.С. Сравнительный анализ эффективности расширенной радиочастотной аблации зон функционального субстрата при различных формах фибрилляции предсердий//Анналы аритмологии. -2013. -Т. 10, № 2. -С. 111-120.
- Стукалова О.В., Власова Э.Е., Тарасова Л.В. и др. Магнитнорезонансная томография сердца у больных постинфарктным кардиосклерозом перед операцией хирургической реваскуляризации миокарда//Регионарное кровообращение и микроциркуляция. -2013. -Т. 12, № 1. -С. 36-41.
- Стукалова О.В., Синицын В.Е., Терновой С.К. Оценка миокарда у больных ИБС с помощью контрастной МРТ//Медицинская визуализация. -2004. -№ 5. -С. 18-24.
- Терновой С.К., Синицын В.Е. Лучевая диагностика сердечно-сосудистой патологии: новые горизонты//Вестник РАМН. -2003. -№ 12. -С. 65-68.
- Усов В.Ю., Богунецкий А.А. Оценка жизнеспособности ишемически поврежденного миокарда: возможности магнитно-резонансной и эмииссионной томографии//Бюллетень сибирской медицины. -2013. -Т. 12, № 6. -С. 154-166.
- Grothoff M., Piorkowski C., Eitel C. et al. MR imaging -guided electrophysiological ablation studies in humans with passive catheter tracking: initial results//Radiology. -2014. -Vol. 271, No. 3. -P. 695-702.
- Kato R., Lickfett L., Meininger G. et al. Pulmonary vein anatomy in patients undergoing catheter ablation of atrial fibrillation: lessons learned by use of magnetic resonance imaging//Circulation. -2003. -Vol. 107. -P. 2004-2010.
- Lee Y.S., Hyun D.W., Jung B.C. et al. Left atrial volume index as a predictor for occurrence of atrial fibrillation after ablation of typical atrial flutter//J. Cardiol. -2010. -Vol. 56, No. 3. -P. 348-353.
- McGann C.J., Kholmovski E.G., Oakes R.S. et al. New magnetic resonance imaging-based method for defining extent of left atrial wall injury after the ablation of atrial fibrillation//J. Am. Coll. Cardiol. -2008. -Vol. 52. -P. 1263-1271.
- Nordbeck P., Hiller K.H., Fidler F. et al. Feasibility of contrast-enhanced and nonenhanced MRI for intraprocedural and postprocedural lesion visualization in interventional electrophysiology: animal studies and early delineation of isthmus ablation lesions in patients with typical atrial flutter//Circ. Cardiovasc. Imaging. -2011. -Vol. 4, No. 3. -P. 282-294


