Коррекция нарушений гемостаза у пациентов, оперированных в условиях амбулаторной хирургии: взгляд на проблему практикующего врача
Автор: Ванданов Б.К., Шихметов А.Н., Лебедев Н.Н., Задикян А.М., Назаров В.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.14, 2019 года.
Бесплатный доступ
В настоящее время большую актуальность приобрела проблема диагностики и лечения венозных тромбоэмболических осложнений (ВТЭО). В статье анализируются причины возникновения, диагностика и лечение ВТЭО применительно к стационарзамещающим технологиям, приобретающим все большее распространение. В качестве иллюстрации приводятся клинические наблюдения двух пациенток, оперированных в стационаре одного дня , у которых в раннем послеоперационном периоде развились церебральная и субэндокардиальная ишемии, этому способствовало несколько патофизиологических механизмов, среди которых одним из основных явился гиперкоагуляционный синдром. Приведены рекомендации по диагностике гиперкоагуляционного синдрома при помощи теста тромбодинамика, рекомендации по лечению осложнений. Отмечается, что отсутствие пациентов с тяжелой сопутствующей патологией, а также высокотравмирующих операций в амбулаторно-хирургической практике в целом не снижает опасность развития тромбогенных сосудистых осложнений. Начинать профилактику ВТЭО при выявлении нарушений гемостаза, свидетельствующих о выявлении гиперкоагуляции, необходимо до операции, в целях эффективности профилактических мероприятий крайне важно проводить лабораторный мониторинг гемостаза. Выполнение указанных рекомендаций по мнению авторов способно снизить риск возникновения ВТЭО, улучшить результаты хирургического лечения пациентов амбулаторного профиля.
Коагулограмма, гиперкоагуляция, пероральные антикоагулянты, тромбодинамика, амбулаторная хирургия, тромбоз, венозные тромбоэмболические осложнения
Короткий адрес: https://sciup.org/140249331
IDR: 140249331 | DOI: 10.25881/BPNMSC.2020.45.86.007
Violations and correction of hemostasis for the patients operated in the conditions of ambulatory surgery: look to problem of practicing doctor
Presently large actuality was purchased by the problem of diagnostics and treatment of venous thromboembolics complications. In the article reasons of origin, diagnostics and treatment of complications, are analysed as it applies to ambulatory technologies acquiring all greater distribution. As illustration clinical supervisions over of two patients operated in the inpatien department of one day , at that in an early postoperative period the cerebral developed and subendocardial to the ischemia are brought, what was assisted by a few physiopathology mechanisms among that one of basic was a hypercoagulative syndrome. Resulted to recommendation on diagnostics of hypercoagulative syndrome through the test of thrombodynamics, recommendation on treatment of developing. It is marked that absence of patients with heavy concomitant pathology, and also high-injuring operations in ambulatory-surgical practice on the whole does not reduce the danger of development of thrombogenic of vascular complications...
Текст научной статьи Коррекция нарушений гемостаза у пациентов, оперированных в условиях амбулаторной хирургии: взгляд на проблему практикующего врача
Основной проблемой при проведении хирургических вмешательств является опасность развития кровотечения из операционной раны. Прогресс науки и технологий способствует усовершенствованию хирургического инструментария, появлению новых эффективных методов борьбы с кровопотерей, в основном за счет малоинвазивности выполняемых операций. Внедрение в практику альтернативных кровесберегающих технологий (аутодонорство, нормо-, гиперволюмическая гемодилюция, аппаратная реинфузия), а также новых гемостатических лекарственных препаратов позволило значительно снизить количество и тяжесть послеоперационных геморрагических осложнений.
Вместе с тем, растет клоичество артериальных и венозных тромбозов в хирургии и в других областях медицины. Артериальные тромбозы ведут к критической ишемии внутренних органов (инсульты, инфаркты миокарда), а венозные – к образованию тромбов в венах нижних конечностей и тромбоэмболии легочной артерии
(ТЭЛА). ВТЭО у пациентов, перенесших хирургические операции, являются одной из самых актуальных проблем современной хирургии. Почти 25% пациентов, перенесших ТЭЛА, умирают от дыхательной недостаточности.
Известно более 100 факторов тромбогенного риска и состояний, приводящих к сосудистым катастрофам. Одним из таких факторов является хирургическая травма, запускающая в организме пациента ряд патофизиологических реакций, получивших название «хирургический стресс-ответ». Под ним понимают совокупность патофизиологических изменений в организме, вызванных нарушениями метаболизма и иммунными реакциями, индуцированными операционной травмой [1]. Известно, что в совокупности иммунитет, гемостаз и фибринолиз представляют собой единую клеточно-гуморальную защитную систему организма [2]. Таким образом, операционная травма ведет к патофизиологическим изменениям как клеточного и гуморального иммунитета, так и свертывающей и противосвертывающей систем крови.

Ванданов Б.К., Шихметов А.Н., Лебедев Н.Н. и др.
КОРРЕКЦИЯ НАРУШЕНИЙ ГЕМОСТАЗА У ПАЦИЕНТОВ, ОПЕРИРОВАННЫХ В УСЛОВИЯХ АМБУЛАТОРНОЙ ХИРУРГИИ: ВЗГЛЯД НА ПРОБЛЕМУ ПРАКТИКУЮЩЕГО ВРАЧА
К временным факторам тромбообразования также относят длительную иммобилизацию пациента, травму, переломы, повышенное питание, эндокринные заболевания, прием противозачаточных препаратов, гормональную заместительную терапию, наличие антифосфолипидных антител, активные формы рака и др.
Не менее важными причинами развития послеоперационных тромбоэмболических осложнений являются наследственные или генетические формы тромбофилий. С момента введения в 1995 г. Международным обществом по тромбозу и гемостазу (ISTH) понятия «врожденные тромбофилии» под этим термином подразумевают следующие заболевания: мутацию фактора V Лейдена, мутацию протромбина (G20210A), глубокий дефицит антитромбина III, снижение концентрации протеинов C и S, гипергомоцистеинемию. Выше перечисленные приобретенные (временные) и постоянные (наследственные) факторы развития тромбозов представляют опасность при выполнении хирургических операций в стационарных условиях. Так, в научном исследовании Rodgers A. et аl. (2000 г.), посвященном послеоперационным осложнениям, выявлено, что изменения гемостаза наблюдались в 45% случаев и носили фатальный характер [3].
Практически равнозначное влияние хирургической травмы на гемостаз наблюдается у больных, оперированных в условиях амбулаторной хирургии, хотя в научной литературе и интернете недостаточно освещена тема нарушений гемостаза у данной категории пациентов. Для наглядного подтверждения представляем два клинических наблюдения развития церебральной и коронарной ишемии, причины которых заключались в гиперкоагуляционных нарушениях свертывающей системы крови. Дополнительно раскроем методы фармакологической и неспецифицеской периоперационной профилактики ВТЭО, принятые в клинике высоких технологий отраслевого клинико-диагностического центра ПАО «Газпром».
Пациентка А., – 46 лет с длительными кровянистыми выделениями из половых путей в сроки очередной менструации обратилась к врачу-гинекологу, предъявив жалобы на выраженную слабость, головокружение при резкой смене положения тела. С подозрением на гиперплазию эндометрия назначено плановое оперативное лечение. Перед операцией из анализов крови отмечено снижение гемоглобина (HGB) до 117 г/л и повышение D-димеров до 0,75 mg/ml. Данные остальных анализов и дополнительных методов исследования в пределах нормы. Под внутривенной анестезией выполнена гистероскопия, раздельное диагностическое выскабливание слизистой цервикального канала и полости матки. Послеоперационный диагноз: железистая гиперплазия эндометрия, полипы эндометрия, менометроррагия. Ближайший послеоперационный период протекал без особенностей. Гистологическое исследование материала выявило обтурацию просвета сосудов фибриновыми тромбами и фрагменты эндометрия с признаками полипоидной простой гиперплазии.
Спустя несколько часов после выполненной операции пациентка отметила онемение левой половины языка, позже появились жалобы на нечеткость речи, онемение правой половины лица, сглаженность левой носогубной складки. Симптоматика развилась остро. Срочно выполнена магнитно-резонансная томография (МРТ) головного мозга. На полученных изображениях в белом веществе полушарий головного мозга визуализируются несколько мелких, до 3 мм в диаметре, округлых участков с четкими контурами, в том числе один в области зрительного тракта слева; окружающие структуры без признаков отека и объемного воздействия. Отмеченные единичные мелкие очаги в белом веществе полушарий головного мозга, вероятнее всего, имеют сосудистое происхождение.
В лабораторных анализах сохранялась анемия (HGB) до 118 г/л, укорочение АЧТВ, протромбинового времени, повышение D-димеров до 1,15 mg/ml и фибриногена. Была назначена гемодилюционная инфузионная терапия кристаллоидами, Цераксон, Мексидол, Семакс, а также Кардиомагнил 75 мг и Фраксипарин 0,8 мл 2 раза в сутки с переводом на Эликвис в дозе 5 мг 2 раза в сутки. Дальнейшее лечение ноотропами, антиоксидантами, дезагрегантами, антикоагулянтами привело к регрессу неврологического дефицита и нормализации данных коагулограммы.
Пациентка Б., – 45 лет с несостоятельностью мышц тазового дна и недержанием мочи смешанного генеза. Под спинномозговой анестезией выполнена коррекция пролапса гениталий, трансзапирательная пластика уретры. Дополнительные данные из анамнеза – частые геморроидальные кровотечения. Ранний послеоперационный период протекал без особенностей. Жалобы на боли умеренной интенсивности в области операции, гемодинамические показатели стабильные. Спустя 12 часов больная предъявила жалобы на выраженную общую слабость, головокружение, кратковременную потерю сознания, неприятные ощущения и боли за грудиной сжимающего характера. ЭКГ-исследование выявило депрессию сегментов ST во II стандартном, V3-6 грудных отведениях. По данным коагулограммы – укорочение времени свертывания и кровотечения, тромбинового времени, АЧТВ, повышение фибриногена по сравнению с дооперационными показателями. Дополнительно изучены концентрации протеинов S, C и плазминогена, значения которых были ниже нормы, в то время как содержание D-димеров почти в 3 раза превышало референтный показатель.
Немедленно было назначено интенсивное лечение с использованием антикоагулянтов, дезагрегантов, антиоксидантов, инфузионной терапии сбалансированными растворами. Через 1 час было отмечено значительное улучшение общего самочувствия, отсутствие жалоб на неприятные ощущения за грудиной, слабость. На ЭКГ менее выражена депрессия ST, снижение амплитуды зубца
Ванданов Б.К., Шихметов А.Н., Лебедев Н.Н. и др.
КОРРЕКЦИЯ НАРУШЕНИЙ ГЕМОСТАЗА У ПАЦИЕНТОВ, ОПЕРИРОВАННЫХ В УСЛОВИЯХ АМБУЛАТОРНОЙ ХИРУРГИИ: ВЗГЛЯД НА ПРОБЛЕМУ ПРАКТИКУЮЩЕГО ВРАЧА
Р, что свидетельствовало об улучшении кровоснабжения миокарда и отсутствии признаков перегрузки правого предсердия. На вторые сутки, на ЭКГ сегмент ST приблизился к изолинии. Сохранялись изменения показателей коагулограммы в сравнении с дооперационными значениями: было укорочено время свертывания и кровотечения, протромбиновое и тромбиновое время, АЧТВ, повышено содержание фибриногена. Концентрации протеинов С (PC) и протеина S (PS) была ниже нормы, а D-димеров – выше. Содержание плазминогена в крови приблизилось к нормальным значениям (табл. 1). На третьи сутки концентрации фибриногена и D-димеров была выше нормы, а протеина С – ниже. На ЭКГ синусовый ритм, сегмент ST на изолинии, амплитуда зубца Т соответствовала дооперационному значению.
Обсуждение
У обоих пациенток отмечалась выраженная клиника общемозговых симптомов: слабость, головокружение, во втором случае с кратковременной потерей сознания на фоне нормального системного артериального давления. В первом случае общемозговая симптоматика появилась до операции, а во втором – после операции. У обеих женщин наблюдалось снижение уровня гемоглобина, у первой на фоне метроррагии до 118 г/л, а у второй – до 115 г/л на фоне хронических геморроидальных кровотечений и операционной кровопотери до 200 мл. Известно, что повреждение сосудов активирует клеточный и плазменный гемостаз [2]. Любое длительное или повторное кровотечение (в данных случаях длительное маточное кровотечение и рецидивирующее при хроническом геморрое) активирует систему гемостаза и угнетает фибринолитическую, приводя к гиперкоагуляционной фазе диссеминированного внутрисосудистого свертывания крови (ДВС).
Гиперкоагуляционный синдром впервые был выявлен у второй пациентки после операции, а у первой женщины в предоперационном периоде – по концентрации D-димеров (0,75 мг/л). В результате повышенной склонности к тромбообразованию у первой женщины снизился мозговой кровоток с появлением очаговой клинической симптоматики (онемение левой половины языка, нечеткость речи, онемение правой половины лица, сглаженность левой носогубной складки). Во втором случае усиление тромбогенного потенциала крови привело к ишемии миокарда, проявившегося болями за грудиной сжимающего характера, повышением амплитуды и заострением верхушки зубца Р во II, III стандартных и aVF отведениях, депрессией ST во II стандартном, aVF, V3-6 грудных отведениях.
Выявленные биоэлектрические изменения сердца указывали на субэндокардиальную ишемию миокарда распространенного характера по передней стенке левого желудочка с признаками перегрузки правого предсердия.
У второй пациентки концентрация фибриногена повысилась в 1,3 раза, а на вторые и третьи сутки – примерно в 1,6 раза.
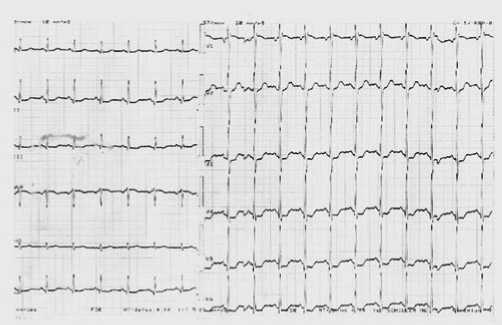
Рис. 1. Электрокардиограмма пациентки Б. после операции.
Табл. 1. Динамика показателей коагулограммы пациентки Б.
|
Показатели |
Референтные значения |
До операции |
1 сут. после операции |
2 сут. после операции |
3 сут. после операции |
|
Протромбиновое время (РТ), с |
13,1–14,1 |
14,1 |
11,5 |
12 |
13,4 |
|
МНО |
1,25 |
1,32 |
1,19 |
1,14 |
|
|
Фибриноген, мг/дл. |
180–350 |
287,6 |
398 |
466 |
466,9 |
|
АЧТВ (АРТТ), с |
32,4–37,5 |
33,3 |
30,4 |
30,3 |
31,3 |
|
Тромбиновое время (ТТ), с |
14–21 |
18,4 |
11,9 |
13,5 |
13,9 |
|
Антитромбин, % |
75–125 |
110,1 |
98,2 |
98,6 |
107,7 |
|
D-димеры, мкг/л. |
63,8–246,8 |
– |
938 |
981 |
772 |
|
Протеин S Ас, % |
60–130 |
– |
45,2 |
47,2 |
49 |
|
Протеин С, % |
70–140 |
– |
52 |
55,9 |
60,6 |
|
Плазминоген, % |
75–150 |
68 |
75 |
82,1 |
|
|
Время свертывания (начало), мин |
0,5–2 |
1 |
0,3 |
0,3 |
0,5 |
|
Время свертывания (конец), мин |
3–5 |
3,3 |
2,8 |
2,7 |
2,8 |
|
Время кровотечения, мин |
2,4 |
2,4 |
0,45 |
0,9 |
1,1 |
По данным литературы повышение концентрации фибриногена наблюдается у большинства больных с церебральной и коронарной ишемией [4]. Содержание D-димеров после операции превышало норму в 3,9 раза в первые сутки, а на вторые и третьи сутки, соответственно, в 4 и в 3,2 раза. Высокая концентрация ПДФ является одним из важных критериев сердечно-сосудистых и цереброваскулярных заболеваний. У больных с венозными тромбозами глубоких вен, тромбоэмболиями легочных артерий и при ДВС – синдроме отмечается резкое повышение содержания D-димеров в плазме крови [5].
Снижение концентрации в плазме крови PC и PS, указывает на угнетение антикоагуляционного звена гемостаза. При дефиците PS резко возрастает риск сердечно-сосудистых катастроф, что связано не только с нарушением активации РС, но и с уменьшением уровня ингибитора внешнего пути образования протромбиназы

Ванданов Б.К., Шихметов А.Н., Лебедев Н.Н. и др.
КОРРЕКЦИЯ НАРУШЕНИЙ ГЕМОСТАЗА У ПАЦИЕНТОВ, ОПЕРИРОВАННЫХ В УСЛОВИЯХ АМБУЛАТОРНОЙ ХИРУРГИИ: ВЗГЛЯД НА ПРОБЛЕМУ ПРАКТИКУЮЩЕГО ВРАЧА
(ТFPI) [6]. Недостаточность протеинов C и S рассматривается как этиологический фактор развития церебральной и коронарной ишемии.
Снижение содержания в крови плазминогена на первые сутки свидетельствует об угнетении фибринолиза. Являясь важной защитной реакцией, фибринолиз предотвращает тромбозы и приводит к реканализации сосудов после остановки кровотечения. Также компоненты фибринолиза регулируют рост и деление клеток, репарацию поврежденных тканей сосудистой стенки, заживление ран, регенерацию мышц [2].
Скрытая коронарная недостаточность, как правило, непосредственно связана с развитием мозговой недостаточности, из-за схожих патофизиологических реакций гемостаза и фибринолиза, а также системной и регионарной гемодинамики [7]. Исследование, проведенное А.В. Фонякиным с соавт. (2005), выявило, что у 16% больных с гемодинамическими нарушениями мозгового кровообращения при холтеровском исследовании выявлены эпизоды без болевой ишемии миокарда [8]. Ухудшение сократимости сердца (ишемия миокарда, аритмия) при субкомпенсированной церебральной гемодинамике увеличивает вероятность развития ишемии мозга [9].
Таким образом, исходя из вышеизложенного, следует, что развитию субэндокардиальной и церебральной ишемии способствовало несколько патофизиологических механизмов. Одним из основных является гиперкоагуляционный синдром, как результат проявления хирургического стресса и длительного рецидивирующего кровотечения. Сосудистая патология и гиперкоагуляция крови значительно ухудшают кровоснабжение тканей и внутренних органов, вызывая их ишемию с последующими функциональными расстройствами. При столь выраженной манифестации клинических проявлений коронарной и церебральной ишемии у обеих женщин необходимо исключить наследственно-генетическую предрасположенность.
Профилактика тромбоэмболических осложнений в амбулаторно-хирургической практике
На первый взгляд, проблема тромбоэмболических осложнений в амбулаторной хирургии может показаться преувеличенной. Вместе с тем, краткий обзор тромбогенных факторов и состояний, представленный в начале данной статьи, а также разбор 2-х клинических наблюдений церебральной и коронарной ишемии указывают на то, что при выполнении стационар-замещающих операций высока вероятность развития тромбогенных сосудистых катастроф.
Какие меры профилактики тромбозов, диагностики и лечения необходимы в амбулаторно-хирургической практике? Для ответа на эти вопросы в Клинике высоких технологий Отраслевого клинико-диагностического центра ПАО «Газпром» принята система мер профилактики. Уменьшение риска гемостазиологических осложнений начинается с дооперационного осмотра пациента, сбора анамнеза; изучением коагулограммы, теста-тромбоди-намики, агрегации тромбоцитов; и достигается своевременной коррекцией имеющихся расстройств гемостаза до и после операции.
Сбор анамнеза. Основная цель – выявление генетических заболеваний свертывающей системы крови. Как правило, пациенты с гемофилией А и В, болезнью Виллебранда знают о своем диагнозе, который выставляется в раннем детстве. Напротив, пациенты с наследственными тромбофилиями могут долгое время не подозревать о наличии болезни. Например, только у 10% больных с мутацией Лейдена тромбозы проявляются в зрелом возрасте невынашиванием беременности, ранними инсультами и инфарктами миокарда [10].
Опрос пациентов включает следующие вопросы: наличие обильных кровотечений, наличие гематом или кровоподтеков, длительные кровотечения после ранее перенесенных операций или экстракции зубов, трансфузия компонентов крови, прием дезагрегантов, антикоагулянтов, а также противозачаточных препаратов и заместительной гормональной терапии. Необходимо уточнить, как протекали беременности у женщин, длительность и интенсивность маточных кровотечений, наличие носовых, геморроидальных и других источников кровотечения. Уточнить, какие имелись наследственные заболевания у близких родственников.
Интерпретация анализов. Скрининговые тесты гемостаза не в полной мере отражают изменения при травме или хирургической операции и больше предназначены для статической оценки показателей системы гемостаза. Прогностический критерий тромбогенного потенциала крови определяется наличием в плазме крови продуктов деградации фибрина (ПДФ). Повышение содержания D-димеров является прямым показанием к расширению перечня гемостазиологических анализов в целях уточнения нарушений гемостаза.
Тест тромбодинамики, являясь глобальным анализом свертывающей системы крови, позволяет на ранних сроках диагностировать гипо- и гиперкоагуляционные изменения, происходящие в исследуемом образце. При данном тесте изучается пространственно-временная динамика свертывания крови, инициированная активатором свертывания, сравнимым с тканевым фактором. С внедрением в клиническую практику теста тромбо-динамики увеличилось количество выявляемых нарушений гемостаза. Так, у лиц с нормальными показателями коагулограммы при проведении теста тромбодинамики отмечалось увеличение скорости роста V, укорочение времени появления спонтанных сгустков Tsp и времени начала образования сгустка Tlang. Данные изменения интерпретируются как гиперкоагуляционные нарушения гемостаза. Объективность изучения коагуляционных изменений крови, выявляемых при тесте тромбодинамики, позволила принять его «на вооружение» в нашей клинике и применять перед операцией, в раннем и отдаленном послеоперационном периоде. Наряду с численными
Ванданов Б.К., Шихметов А.Н., Лебедев Н.Н. и др.
КОРРЕКЦИЯ НАРУШЕНИЙ ГЕМОСТАЗА У ПАЦИЕНТОВ, ОПЕРИРОВАННЫХ В УСЛОВИЯХ АМБУЛАТОРНОЙ ХИРУРГИИ: ВЗГЛЯД НА ПРОБЛЕМУ ПРАКТИКУЮЩЕГО ВРАЧА параметрами в отчете об исследовании отображается последовательность снимков растущего фибринового сгустка, которая наглядно характеризует состояние системы гемостаза пациента.
Своевременная коррекция нарушений гемостаза. Главная идея данной коррекции в достижении баланса антитромботической терапии с минимизацией риска развития операционных кровотечений. Своевременность реализуется незамедлительным началом терапии гиперкоагуляционных изменений, выявленных до операции. Сложно определиться с методом коррекции гемостаза, из-за разнообразия нарушений и сопутствующих факторов подход к каждому пациенту должен быть индивидуальным.
При изменениях скрининговых и глобальных показателей гемостаза, свидетельствующих о гиперкоагуляционном синдроме, нами выбрана следующая тактика профилактики ВТЭО. Если данные нарушения выявлены до операции, то пациенту показан прием профилактических доз пероральных антикоагулянтов (ПОАК). Как показали наши наблюдения, прием профилактических доз таблетированных антикоагулянтов приводил к нормализации показателей гемостаза у пациентов с исходно умеренной гиперкоагуляцией. Определяющим фактором является время, точнее, продолжительность лечения. У больных с выраженной гиперкоагуляцией, формирующей спонтанные сгустки в образцах крови, назначаются лечебные дозы ПОАК. В некоторых случаях целесообразно перенести дату выполнения плановой операции до полной нормализации показателей гемостаза.
Накануне операции прием препаратов отменяется за 12–24 часа до начала операции. Пациентам с нормокоа-гуляцией, но с риском развития ВТЭО по шкале Caprini за 12 часов до операции вводится низкомолекулярный гепарин (НМГ). В случае выбора центральной регионарной анестезии отказаться от приема антикоагулянтов необходимо за 48 часов до операции.
В раннем послеоперационном периоде у пациентов с умеренным риском кровотечения через 12 часов проводится мост-терапия профилактической дозой НМГ, а лечебной дозой – спустя 24 часа. Показанием к назначению НМГ является объем и продолжительность операции, выбор анестезии, длительность послеоперационной иммобилизации. При наличии клиники послеоперационного кровотечения (поступление крови по дренажам, компенсаторная тахикардия, снижение артериального давления, анемия, наличие свободной жидкости в полостях и др.) проведение антикоагулянтной терапии противопоказано.
Выписанные домой пациенты после объемных операций продолжают принимать НМГ в течение 5–7 суток. Больные с малообъемными операциями принимают лечебные дозы НОАК. Доза НОАК и длительность приема зависит от результатов коагулограммы и теста тромбодинамики. Так, при сохраняющейся гиперкоагуляции назначается лечебная доза НОАК, а у больных с нормокоагуляцией – профилактическая доза. Достижение нормокоагуляции по тестам тромбодинамики служит показанием к отмене препаратов в послеоперационном периоде.
К другим механическим способам профилактики тромбоэмболических осложнений относится ранняя активизация пациентов после операции. Ранняя активизация, помимо существенных клинических преимуществ, экономически более эффективна. В целях ускоренной реабилитации важен выбор метода анестезии при объемных
Снимки получены с помощью системы лабораторной диагностики «Регистратор термодинамики Т-2»

Норма

Гипокоагуляция

Гиперкоагуляция
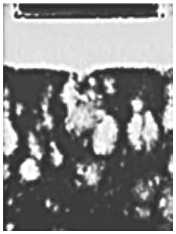
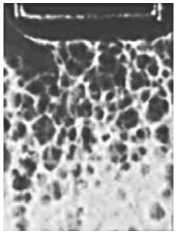
Гиперкоагуляция
Спонтанные сгустки
Скорость роста, V, (мкм/мин)
Размер сгустка, Cs, (мкм)
Время появления спонтанных сгустков, Tsp, (мин)
(20–29)
(800–1200)
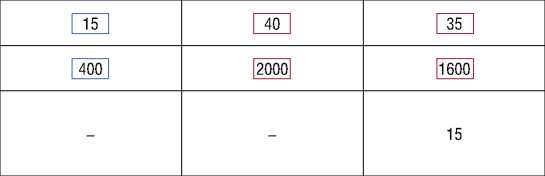
Гиперкоагуляция Спонтанные сгустки
Фибринолиз
Возможен качественный анализ
Возможен качественный анализ
Возможен качественный анализ
Рис. 2. Тест тромбодинамика.
Ванданов Б.К., Шихметов А.Н., Лебедев Н.Н. и др.
КОРРЕКЦИЯ НАРУШЕНИЙ ГЕМОСТАЗА У ПАЦИЕНТОВ, ОПЕРИРОВАННЫХ В УСЛОВИЯХ АМБУЛАТОРНОЙ ХИРУРГИИ: ВЗГЛЯД НА ПРОБЛЕМУ ПРАКТИКУЮЩЕГО ВРАЧА хирургических вмешательствах. Наиболее подходящим методом является сочетание общей анестезии с центральными и периферическими видами обезболивания. Известно, что при проведении эпидуральной анестезии явления гиперкоагуляции менее выражены в сравнении с общей анестезией. Объясняется данный эффект повышением периферического кровотока, снижением концентрации кортизола, катехоламинов, медиаторов боли, провоспалительных цитокинов [11]. Обязательно применение ингаляционных и внутривенных анестетиков с коротким периодом действия, минимальное использование наркотических анальгетиков, что способствует быстрому восстановлению когнитивных функций и ранней реабилитации.
С целью профилактики ВТЭО в периоперационном периоде мы считаем обязательным ношение эластичного компрессионного трикотажа 1 или 2 классов компрессии. Эластичные чулки используются до, во время и после операции, исключение составляют операции на ногах (не надевают во время операции) и облитерация артериальных сосудов нижних конечностей (опасность развития критической ишемии). Обязательно ношение чулок в дневное и ночное время после операции в стационаре кратковременного пребывания и после выписки домой в течение 2–4 недель. Показаниями к ношению компрессионного трикотажа более 4-х недель являются наличие: варикозной болезни, избыточной массы тела, гиподинамии, лабораторно выявляемой гиперкоагуляции. В целях неспецифической профилактики ВТЭО используется перемежающаяся пневмокомпрессия нижних конечностей, гемодилюция, прием нестероидных противовоспалительных средств, занятия с инструктором лечебной физической культуры. Важно помнить о применении интраоперационного согревания пациентов, что уменьшает кровопотерю и потребность в кровезаменителях. Так, снижение температуры тела на 1 °C угнетает функцию тромбоцитов и ферментов свертывающего каскада крови, в результате чего на 16% увеличивается кровопотеря [12]. Вместе с тем гипотермия снижает активность естественных антикоагулянтов и ферментов фибринолиза.
Наличие факторов тромбогенного риска ведет к увеличение частоты возникновения операционных осложнений в хирургической практике. Являясь полностью зависимым от причин возникновения, развитие операционных осложнений вполне предсказуемо и зависит от наличия и количества исходных причин и сопутствующих условий. Прогнозировать угрозу развития ВТЭО позволяет наличие у пациента постоянных (генетических) и временных (объем операции, гемотрансфузия, избыточная масса тела, длительность иммобилизации и т.д.) факторов риска.
Нет сомнений, что риск развития ВТЭО гораздо выше у больных, оперируемых в стационарных условиях, чем у амбулаторно-хирургических пациентов. Однако отсутствие больных с тяжелой сопутствующей патологией и высокотравмирующих операций в амбулаторно- хирургической практике в целом не снижает опасность развития тромбогенных сосудистых осложнений. В целях эффективности профилактических мероприятий крайне важно проводить лабораторный мониторинг гемостаза. Начинать профилактику ВТЭО при выявлении нарушений гемостаза, свидетельствующих об гиперкоагуляции, необходимо до операции. Своевременная коррекция выраженной гиперкоагуляции перед операцией уменьшает проявления операционного стресс-ответа, позволяет уменьшить сроки послеоперационной иммобилизации пациента. Показанием к отмене послеоперационной антикоагулянтной терапии является подтвержденная результатами анализов нормализация показателей свертывающей системы крови.
Таким образом, проведение интраоперационной профилактики ВТЭО, применяемой в Клинике высоких технологий Отраслевого клинико-диагностического центра ПАО «Газпром», является необходимой мерой и носит рекомендательный характер в целях комплексной терапии пациентов амбулаторно-хирургической практики.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Коррекция нарушений гемостаза у пациентов, оперированных в условиях амбулаторной хирургии: взгляд на проблему практикующего врача
- Овечкин А.М., Романова Т.Л. Послеоперационное обезболивание: оптимизация подходов с точки зрения доказательной медицины // Русский медицинский журнал. - 2006. - Т.14. - №12. - С. 865-872.
- Ovechkin AM, Romanova TL. Posleoperatsionnoe obezbolivanie: optimizatsiya podkhodov s tochki zreniya dokazatel'noi meditsiny. RMZh. 2006;14(12):865-872. (In Russ).
- Кузник Б.И. Клеточные и молекулярные механизмы регуляции системы гемостаза в норме и патологии. - Чита: Экспресс-издательство, 2010.
- Kuznik BI. Kletochnye i molekulyarnye mekhanizmy regulyatsii sistemy gemostaza v norme i patologii. Chita: Ekspress-izdatel'stvo; 2010. (In Russ).
- Rodgers A, Walker N, Schug S. Reduction of postoperative mortality and morbidity with epidural or spinal anesthesia: result from overview of randomized trials. BMJ. 2000;321(7275):1493. DOI: 10.1136/bmj.321.7275.1493
- Skurk T, Hauner H. Obesity and impaired fibrinolysis: role of adipose production of plasminogen activator inhibitor-1. Int J Obes Relat Metab Disord. 2004;28(11): 1357-1364. DOI: 10.1038/sj.ijo.0802778
- Key N, Makris M, O'Shaughnessy D, Lillicrap D, editors. Practical hemostasis and thrombosis. 2nd ed. Blackwall Publishing; 2009. 236 p. DOI: 10.1002/9781444306286
- Сostellino FJ, Plopils A. The protein C pathway and pathologic processes. J Thromb Haemost. 2009;7 Suppl 1:140-145.
- DOI: 10.1111/j.1538-7836.2009.03410.x
- Budaj A, Frasinska K, Gore JM, et al. Magnitude of and risk factors for in-hospital and postdischarge stroke in patients with acute coronary syndromes. Circulation. 2005;111(24):3242-3247.
- DOI: 10.1161/CIRCULATIONAHA.104.512806
- Фонякин А.В., Суслина З.А., Гераскина Л.А. Кардиологическая диагностика при ишемическом инсульте. - СПб.: ИНКАРТ, 2005. - 224 c.
- Fonyakin AV, Suslina ZA, Geraskina LA. Kardiologicheskaya diagnostika pri ishemicheskom insul'te. St. Petersburg: INKART; 2005. 224 p. (In Russ).
- Виленский Б.С. Современная тактика борьбы с инсультом. - СПб.: Фолиант, 2005. - 288 с.
- Vilenskii BS. Sovremennaya taktika bor'by s insul'tom. St. Petersburg: Foliant; 2005. 288 p. (In Russ).
- Heit JA. Thrombophilia: clinical and laboratory assessment and management. In: Kithens C, Konkle B, Kessler C, editors. Consultative hemostasis and thrombosis. 2nd ed. Philadelphia: Saunders Elsevier; 2007. P. 213-244.
- Kehlet H, Holte K. Effect of postoperative analgesia on surgical outcome. Br J Anaesth. 2001;87(1):62-72.
- DOI: 10.1093/bja/87.1.62
- Rajagopalan S, Mascha E, Na J, Sessler DI. The effects of mild perioperative hypothermia on blood loss and transfusion requirement. Anesthesiology. 2008;108 (1):71-77.
- DOI: 10.1097/01.anes.0000296719.73450.52


