Коррекция структурных повреждений, связанных с диабетической кардиомиопатией, производным ГАМК
Автор: Смирнов А.В., Тюренков И.Н., Бакулин Д.А., Великородная Ю.И., Паньшин Н.Г., Чернышев А.В., Пустынников В.Э., Болохов Н.С., Похлебин А.А., Самусев Р.П., Замараев В.С., Гуров Д.Ю., Краюшкин А.И., Быхалов Л.С.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Статьи
Статья в выпуске: 1 т.22, 2025 года.
Бесплатный доступ
Сахарный диабет (СД) в настоящее время рассматривают как серьезную эпидемию во всем мире. Он является ведущей причиной сердечно-сосудистых заболеваний и смертности пациентов. Диабетическая кардиомиопатия (ДКМП) в отсутствии ИБС, пороков сердца, артериальной гипертонии и др. является многофакторным заболеванием, приводящим к гипертрофии желудочков, интерстициальным фиброзным изменениям сердца и сердечной недостаточности.
Сердце, сахарный диабет, сукцикард, фиброз, гипертрофия
Короткий адрес: https://sciup.org/142245444
IDR: 142245444 | УДК: 616-091.814 | DOI: 10.19163/2658-4514-2025-22-1-40-46
Correction of structural damage associated with GABA-derived diabetic cardiomyopathy
Diabetes mellitus (DM) is currently considered a serious epidemic worldwide and is the leading cause of cardiovascular disease and mortality in patients with DM. Diabetic cardiomyopathy (DCM) in the absence of coronary heart disease, heart defects, arterial hypertension, etc. is a multifactorial disease leading to ventricular hypertrophy, interstitial fibrotic changes in the heart and heart failure.
Текст научной статьи Коррекция структурных повреждений, связанных с диабетической кардиомиопатией, производным ГАМК
doi:
ORIGINAL ARTICLE doi:
Сахарный диабет (СД) в настоящее время все чаще начинают рассматривать как серьезную мировую эпидемию.
Всемирная организация здравоохранения (ВОЗ) постановила, что к 2040 г. распространенность СД может достичь 10,4 % мирового населения, что составит около 642 млн человек [1].
Риск осложнений сахарного диабета особенно велик у пожилых больных. Среди осложнений СД важная роль отдается нарушениям глюкозного и липидного видов обмена, развивающимся на фоне инсулинорезистентности [2, 3], что способствует инициации и прогрессии повреждения эндотелия и увеличению сосудистой проницаемости. Также оксидативный стресс, нитрозатив-ный стресс и воспаление, являющиеся предикторами развития СД, могут стимулировать развитие диабетической кардиомиопатии (ДКМП) [4, 5].
На более поздних стадиях ДКМП наблюдаются выраженные изменения в структуре и функции сердца.
Одними из ключевых морфологических проявлений являются гипертрофия и фиброзирование левого желудочка (ЛЖ), которые развиваются в ответ на хроническую перегрузку сердца метаболическими факторами и сопровождаются прогрессирующей диастолической и систолической дисфункцией, что приводит к снижению фракции выброса, уменьшению насосной функции сердца и, в конечном итоге, к развитию хронической сердечной недостаточности (ХСН) [6].
Осложнения СД, связанные с сердечной мышцей, сильно повышают риск развития инфаркта миокарда, что требует применения эффективных терапевтических подходов, направленных не только на контроль уровня глюкозы, но и на защиту сердечно-сосудистой системы. Существующие сахароснижающие методы лечения не направлены на снижение смертности от сердечно-сосудистых заболеваний при сахарном диабете, а в некоторых случаях могут даже ухудшать течение сердечной недостаточности [7].
ГАМК-ергическая система является перспективной мишенью для поиска препаратов с комплексной поливалентной активностью, направленных на предупреждение развития осложнений СД. Разработанные комбинированные производные гамма-аминомасляной кислоты (ГАМК), например сукцикард (4-фенилпирацетам в комбинации с янтарной кислотой, 2 : 1), обладающий цитопротек-торными свойствами, что позволяет рассматривать данное вещество в качестве кандидата для лечения сахарного диабета [8].
ЦЕЛЬ РАБОТЫ
Охарактеризовать структурные повреждения в миокарде, развитие фиброза, гипертрофии кардиомиоцитов на модели экспериментального сахарного диабета 2-го типа у стареющих животных с учетом фармакологической коррекции производным ГАМК.
МЕТОДИКА ИССЛЕДОВАНИЯ
Исследование выполнено на 18 беспородных крысах в возрасте 12 месяцев на начало эксперимента, полученных из питомника лабораторных животных (ФГУП питомник лабораторных животных «Рапполово», Ленинградская обл.).
Грызуны содержались в специализированных пластиковых клетках (545 × 395 × 200 мм). В качестве подстила использовались древесные гранулы (пеллеты), которые после введения стрептозотоцина и развития полиурии менялись ежедневно. Животные получали круглосуточный доступ к пище и воде. Световой режим составлял 12/12 часов день-ночь. Дизайн исследования был одобрен этическим комитетом ВолгГМУ, протокол № 2022/116 от 04.03.2022 г.
Эксперимент произведен на белых беспородных крысах, которых в возрасте 12 месяцев подвергали моделированию сахарного диабета в течение 6 месяцев путем введения стрептозо-тоцина [60 мг/кг, Cat No. 14653, Sisco Research Laboratories Pvt. Ltd. (SRL), Индия] через 15 минут после введения никотинамида (230 мг/кг, Sigma-Aldrich, США). Производили контроль уровня глюкозы в крови через 3 суток и через 6 месяцев, при наличии гипергликемии в течение 6 месяцев (от 10 до 18 ммоль/л) включали в исследование [9].
После наблюдения за животными в течение 6 месяцев от моделирования патологии животных разделяли на группы. Первую группу животных ( n = 6) составляли интактные крысы в возрасте 19 месяцев. Вторую группу животных составляли крысы в возрасте 19 месяцев с экспериментальным сахарным диабетом, получавшие 0,9%-й раствор NaCl. Третью группу животных составляли крысы в возрасте 19 месяцев с экспериментальным сахарным диабетом, получавшие в качестве терапии аминалон в дозе 1000 мг/кг.
Четвертую группу животных составляли крысы в возрасте 19 месяцев с экспериментальным сахарным диабетом, получавшие в качестве терапии исследуемое производное ГАМК – сукци-кард (4-фенилпирацетам в сочетании с янтарной кислотой, 2 : 1) в дозе 50 мг/кг.
Соединения вводили на протяжении 4 недель каждый день по одному разу внутрижелудочно.
Эвтаназию проводили декапитацией при нар-котизировании хлоралгидратом в дозе 400 мг/кг, внутрибрюшинно. Образцы тканей сердца фиксировали в растворе забуференного формалина. Изготавливали парафиновые срезы толщиной 4– 5 мкм. Производили их окрашивание гематоксилином и трихромом по Массону.
Фотодокументирование препаратов производили с использованием видео/фотокамеры AxioCam 305 color (Carl Zeiss Microscopy GmbH, Германия), установленной на световом микроскопе AxioImager A2 (Carl Zeiss Microscopy GmbH, Германия) с использованием объективов ×10, ×20, ×40. При морфометрическом исследовании использовали программу Zeiss Zen Pro 2.3 2021 (Carl Zeiss Microscopy GmbH, Германия), определяли диаметр кардиомиоцитов левого желудочка. Фиброз оценивали полуколичественным методом в субэпикардиальной, интрамуральной и эпикардиальной областях миокарда левого желудочка.
Статистическую обработку данных проводили с использованием пакета программы «Statistica 10.0» (USA). При проверки выборки на нормальность проводили тест Колмогорова – Смирнова. Сравнение независимых выборок проводили непараметрическим методом (критерий Краскела – Уоллиса с посттестом Данна). Гипоте- зу о существовании различий между выборками принимали при уровне р < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
При исследовании сердца крыс интактной группы престарческого возраста (19 мес.) выявлено, что средняя масса сердца составила (199 ± 1,53) г, обнаружены явления интерстициального фиброза у части животных в миокарде левого желудочка. Отмечались явления слабовыражен-ного периваскулярного фиброза в субэпикардиальных областях миокарда, что отражает увеличение степени фиброзирования с возрастом. По всей видимости, это основано на увеличении действия хронического воспаления и окислительного стресса на фоне старения (рис. 1 а).
Морфометрическое исследование диаметра кардиомиоцитов левого желудочка у интактных крыс выявило средний диаметр кардиомиоцитов – (14,95 ± 0,22) мкм (рис. 2 б).
При изучении миокарда животных с сахарным диабетом средняя масса сердца составила (207,33 ± 1,98) г, что на 4 % меньше, чем у животных интактной группы. Отмечены наиболее выраженные признаки умеренно выраженного мелкоочагового интерстициального фиброза в интрамуральных отделах миокарда левого желудочка. Кроме того, в единичных случаях обнаружен слабо выраженный фиброз в субэпикардиальных областях. В субэндокардиальных областях у большинства экспериментальных животных были отмечены явления интерстициального фиброза, при чем в единичные случаях – в папиллярных мышцах (рис. 1 б). Диаметр кардиомиоцитов левого желудочка составил (16,40 ± 0,29) мкм, увеличение размеров кардиомиоцитов – 8,9 % (при p < 0,001) (рис. 2 б).
У крыс третьей группы (сахарный диабет, лечение миналоном) средняя масса сердца составила (206,33 ± 1,93) г, что на 0,48 % меньше, чем у животных с экспериментальным СД. В миокарде левого желудочка выявлялась умеренная гипертрофия в сочетании с участками, в которых наблюдались атрофические изменения в кардиомиоцитах (рис. 1 в). Отмечены явления периваскулярного и интерстициального фиброза в интрамуральных областях миокарда. Средний диаметр кардиомиоцитов левого желудочка у животных 3-й группы снижался на 5,43 % ( p > 0,05), по сравнению с группой животных с СД без лечения, и составил (15,52 ± 0,22) мкм (рис. 2 б).
Средняя масса сердца животных с СД, получавших в качестве терапии сукцикард (4-я группа), составила (201 ± 1,63) г, что на 2,89 % меньше, чем у животных 2-й группы с СД. В миокарде левого желудочка отмечено преобладание участков с умеренной гипертрофией, сочетавшихся с участками атрофических изменений (рис. 1 г).
Были выявлены единичные явления периваскулярного и интерстициального фиброза в субэпикардиальных областях миокарда. Кардиомиоциты левого желудочка животных этой группы в диаметре были меньше на 13,12 % (при p < 0,0001) по сравнению со 2-й группой животных с СД [(14,254 ± 0,27) мкм] (рис. 2 б).
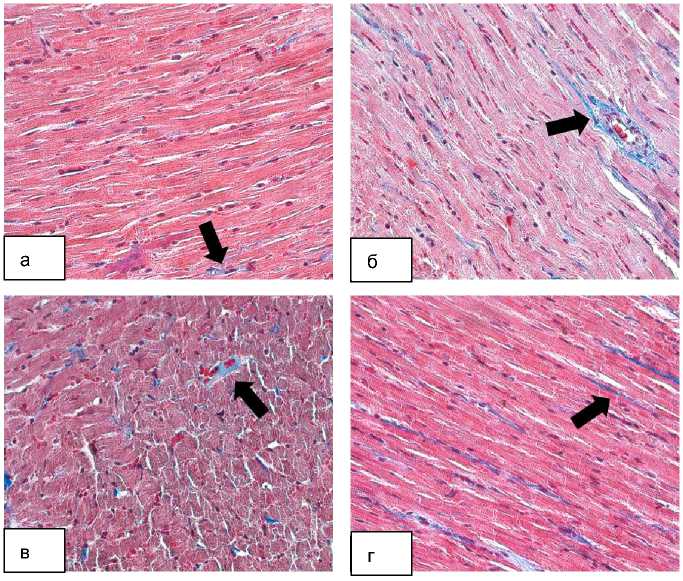
Рис. 1. Структурные изменения миокарда левого желудочка:
а – 1-я группа, миокард крысы в возрасте 19 мес.; б – 2-я группа, миокард крысы в возрасте 19 мес.
с экспериментальным сахарным диабетом; в – 3-я группа, миокард крысы в возрасте 19 мес. с экспериментальным сахарным диабетом, получавшей аминалон; г – 4-я группа, миокард крысы в возрасте 19 мес.
с экспериментальным сахарным диабетом, получавшей сукцикард.
Окраска по Массону. ×400. Черные стрелки – соединительная ткань, участки фиброзирования
б
а
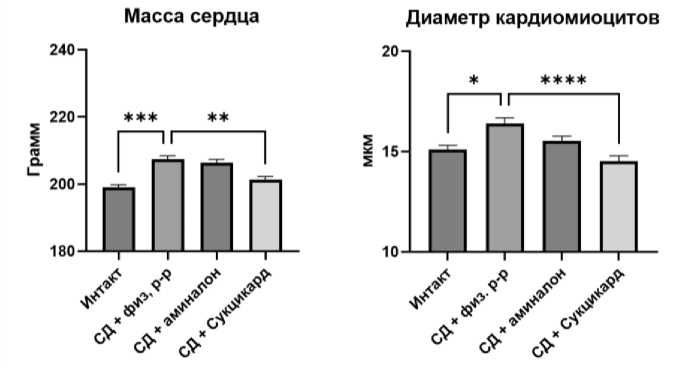
Рис. 2. Результаты измерения массы сердца (а); результаты морфометрии кардиомиоцитов миокарда (б);
* - p < 0,05 * - p < 0,01, *** - p < 0,001, **** - p < 0,0001
Обнаруженные нами данные указывают на значимое повышение диаметра кардиомиоцитов у животных с сахарным диабетом. Это говорит о развившейся гипертрофии миокарда. Так как в кардиомиоцитах хорошо видна поперечная ис-черченность, формирующаяся за счет миофибрилл, можно подтвердить сохранность миофибрилл и отмести отек кардиомиоцитов. Подтверждает все это увеличение средней массы сердца животных с сахарным диабетом.
Было отмечено развитие мелкоочагового интерстициального фиброза в интрамуральных отделах миокарда у животных со стрептозото-цин-никотинамид-индуцированным СД (модель СД 2-го типа). Подобные изменения были обнаружены ранее при стрептозотоцин-индуцируемом СД (модель СД 1-го типа) [10], что свидетельствует о метаболических нарушениях кардиомиоцитов при СД, характерных для ДКМП. На модели СД 2-го типа показано, что сукцикард способствует снижению массы сердца, уровня фиброза в левом желудочке, уменьшению выраженности гипертрофии кардиомиоцитов левого желудочка у крыс, что подтверждается значимым снижением диаметра кардиомиоцитов. Стоит отметить, что в проведенном эксперименте использовались крысы престарческого возраста (19 мес.), у которых уже наблюдалось развитие фиброза, связанного с воз- растными изменениями в сердце, на фоне которых развивались патологические изменения в результате моделирования сахарного диабета, усугубляющие метаболические нарушения в миокарде.
ЗАКЛЮЧЕНИЕ
Результаты исследования демонстрируют, что у крыс престарелого возраста развитие диабетической кардиомиопатии сопровождается значительными морфологическими изменениями в миокарде, включая гипертрофию кардиомиоцитов и фиброз. Возрастные изменения, такие как старческие изменения миокарда, усиливают патологические эффекты сахарного диабета, что подчеркивает важность учета коморбидных состояний при моделировании патологии.
Применение сукцикарда при СД показало выраженное кардиопротективное влияние, выражающееся в уменьшении гипертрофии кардиомиоцитов и снижении степени фиброза, что может быть обусловлено мембрано- и цитопротектив-ным действием производного ГАМК – сукцикарда (4-фенилпирацетам в комбинации с янтарной кислотой, 2 : 1). Это подчеркивает перспективность дальнейших исследований использования сукцикарда в коррекции морфологических нарушений, развивающихся при диабетической кардиомиопатии, особенно в условиях старения.


