Коррекция токсических эффектов этанола у крыс при помощи перорального введения ацетилцистеина
Автор: Морковин Е.И., Осадченко Н.А., Куркин Д.В., Кнышова Л.П., Бакулин Д.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Обзорные статьи
Статья в выпуске: 4 (64), 2019 года.
Бесплатный доступ
В данной работе представлены результаты доклинического исследования эффектов ацетилцистеина в отношении биохимических показателей, характеризующих антиоксидантный статус и функциональную активность гепатоцитов у крыс, перенесших острую интоксикацию этанолом. Введение ацетилцистеина предотвращало развитие признаков окислительного стресса, препятствовало увеличению активности трансаминаз в плазме крови и росту содержания триглицеридов в гомогенатах печени (при оценке через 24 ч после алкогольной интоксикации), что позволяет рассматривать ацетилцистеин как перспективное средство коррекции постинтоксикационно-го состояния, вызванного употреблением высоких доз этанола.
Этанол, постинтоксикационное состояние, похмелье, ацетилцистеин, крысы, доклинические исследования
Короткий адрес: https://sciup.org/142224356
IDR: 142224356 | УДК: 57.084.1
Correction of ethanol toxicity in rats with oral acetylcysteine administration
This article presents the results of a non-clinical study of the effects of acetylcysteine on the biochemical parameters characterizing the antioxidant status and functional activity of hepatocytes in rats after acute ethanol intoxication. Acetylcysteine prevented the induction of oxidative stress. The increase in plasma transaminase activity and in the content of triglycerides in liver homogenates (as assessed 24 hours after alcohol intoxication) were also prevented. The results allow to consider that acetylcysteine is a promising agent, which could be used to correct the ethanol hangover.
Текст научной статьи Коррекция токсических эффектов этанола у крыс при помощи перорального введения ацетилцистеина
В силу увеличивающегося потребления алкогольных напитков проблема проведения эффективной фармакотерапии похмельного синдрома становится одной из приоритетных задач медико-социальных служб. Тяжесть похмельного синдрома определяется концентрацией и скоростью выведения ацетальдегида – продукта биотрансформации этанола, который может сохраняться в течение многих часов после употребления алкоголя. Одним из подходов в терапии похмельного синдрома заключается в попытке скорейшего восстановления метаболической активности гепатоцитов и интенсификации метаболизма и выведения ацетальдегида [9, 10]. Замедление метаболизма ацетальдегида может происходить из-за истощения запасов восстановленного глутатиона, поэтому применение веществ, способных повышать содержание последнего, может активизировать естественные процессы детоксикации и облегчать похмельный синдром. Перспективным может стать применение с данной целью ацетилцистеина, который представляет собой лекарственное средство, являющееся предшественником глутатиона, используемое, в частности, и при других токсических повреждениях печени, сопро- вождающихся развитием оксидативного стресса и снижением метаболизма в гепатоцитах [5].
ЦЕЛЬ РАБОТЫ
Изучить влияние однократного перорального введения ацетилцистеина в отношении биохимических показателей крыс, перенесших острую алкогольную интоксикацию.
МЕТОДИКА ИССЛЕДОВАНИЯ
Работу выполнили на 30 самцах крыс линии Вистар (масса тела 300–450 г), случайным образом разделенных на 3 группы. Животным из 2 групп однократно внутрибрюшинно вводили 20%-й раствор этанола в дозе 3 г/кг, а после восстановления установочного рефлекса [3] однократно внутрижелудочно вводили водный раствор ацетилцистеина в дозе 1 г/кг или физиологический раствор в эквивалентном объеме. Крысам из контрольной группы вводили только физиологический раствор (сначала внутрибрюшинно, а через 3 ч – внутриже-лудочно). Через 24 ч после начала эксперимента [2] животных из всех групп умерщвляли, отбирая образцы крови и ткани печени для последующего анализа. Печень предварительно перфузировали раствором Рингера [1]. Активность аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (АЛТ) в плазме крови животных определяли при помощи соответствующих реагентов (производства ЗАО «Диа-кон-ДС», Россия). Содержание триглицеридов в гомогенатах ткани печени определяли после экстракции гептаном и изопропанолом с последующим фракционированием алкоголятом натрия фотометрически (после инкубации с 2,4-пентандионом при длине волны 410 нм) [4, 6]. Концентрацию малонового диальдегида (МДА) в гомогенатах определяли при помощи реакции с тиобарбитуровой кислотой [8, 12]; концентрацию восстановленного глутатиона – в реакции восстановления 5,5-дитиобис-(2-нитробензойной кислоты) [11]. Активность супероксиддисмутазы (СОД) определяли фотометрическим методом, основанным на оценке степени ингибирования реакции окисления эпинефрина [7, 12]. Все реакции проводили в трипликатах.
Статистическую обработку полученных результатов проводили методами описательной и аналитической статистики. Распределение количественных показателей оценивали, используя тесты Колмогорова – Смирнова и Шапиро – Уилка. При подтверждении гипотезы о нормальном распределении межгрупповые различия оценивали при помощи однофакторного дисперсионного анализа с пост-тестом Ньюмена – Кеулса, а цифровые значения представляли в виде среднего арифметического значения и стандартной ошибки среднего арифметического.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Уровни активности АСТ и АЛТ в плазме крови крыс, которым вводили только физиологический раствор, составляли (131,1 ± 4,78) Ед./л и (27,3 ± 1,49) Ед./л соответственно. У животных, которым вводили этанол и физиологический раствор, данные показатели повысились статистически значимо (p < 0,0001), достигнув (166,9 ± 7,56) Ед./л и (44,9 ± 3,09) Ед./л соответственно, что может отражать гепатотоксиче-ские эффекты высоких доз этанола. У крыс, которым после пробуждения вводили ацетилцистеин, уровни активности АСТ и АЛТ увеличивались несущественно (p > 0,05 при сравнении с показателями, зарегистрированными у животных из группы отрицательного контроля) и составили (143,7 ± 5,00) Ед./л и (33,6 ± 2,08) Ед./л соответственно, что было статистически значимо ниже показателей, отмеченных у крыс, которым после пробуждения вводили физиологический раствор (p < 0,05 и p < 0,01 соответственно).
У крыс, которым вводили этанол и физиологический раствор, активность СОД и содержание глутатиона в гомогенатах печени достигли, соответственно, (39,0 ± 2,65) Ед./мг белка [против (50,9 ± 2,48) Ед./мг белка у животных из группы отрицательного контроля; p < 0,05] и (96,5 ± 3,11) мг/г ткани [против (117,4 ± 2,95) Ед./мг ткани у животных из группы отрицательного контроля; p < 0,0001]. Содержание МДА в гомогенатах печени, напротив, повышалось до (32,2 ± 2,16) нмоль/г ткани [против (25,7 ± 1,49) нмоль/г ткани у животных из группы отрицательного контроля; p < 0,05]. У крыс, которым вводили ацетилцистеин, перечисленные показатели не отличались статистически значимо от зарегистрированных у животных, не получавших этанол (p > 0,05 в каждом из случаев): активность СОД, содержание глутатиона и МДА составили (46,1 ± 2,83) Ед./мг белка, (111,4 ± 3,52) мг/г ткани и (27,0 ± 1,11) нмоль/г ткани соответственно; при этом содержание глутатиона в гомогенатах печени животных из данной группы было статистически значимо выше, чем у крыс из группы положительного контроля (p < 0,05; см. рис.).
Таким образом, однократное введение ацетилцистеина препятствовало развитию у крыс признаков окислительного стресса, вызванного алкогольной интоксикацией.
Наряду с повышением активности трансаминаз в плазме крови признаки токсического поражения печени могут включать ее дистрофические изменения, проявляющиеся образованием жировых капель в гепатоцитах или увеличением содержания триглицеридов в ткани печени [6]. У крыс, которым вводили этанол и физиологический раствор, содержание триглицеридов в гомогенатах печени статистически значимо превышало показатель, зарегистрированный у животных из группы отрицательного контроля [(29,3 ± 0,80) мг/г против (23,9 ± 0,74) мг/г ткани; p < 0,0001]. У животных, которым после пробуждения вводили ацетилцистеин, содержание триглицеридов в гомогенатах печени достигло (24,9 ± 1,09) мг/г ткани, что не отличалось статистически значимо от показателя, полученного у крыс из группы отрицательного контроля (p > 0,05), но было статистически значимо меньше, чем у крыс из группы положительного контроля (p < 0,01; см. рис.). Описанные изменения в активности трансаминаз в плазме крови и содержании триглицеридов в гомогенатах печени позволяют заключить, что ацетилцистеин способен предотвращать развитие токсических повреждений печени, вызванных у крыс однократным внутрибрюшинным введением этанола.
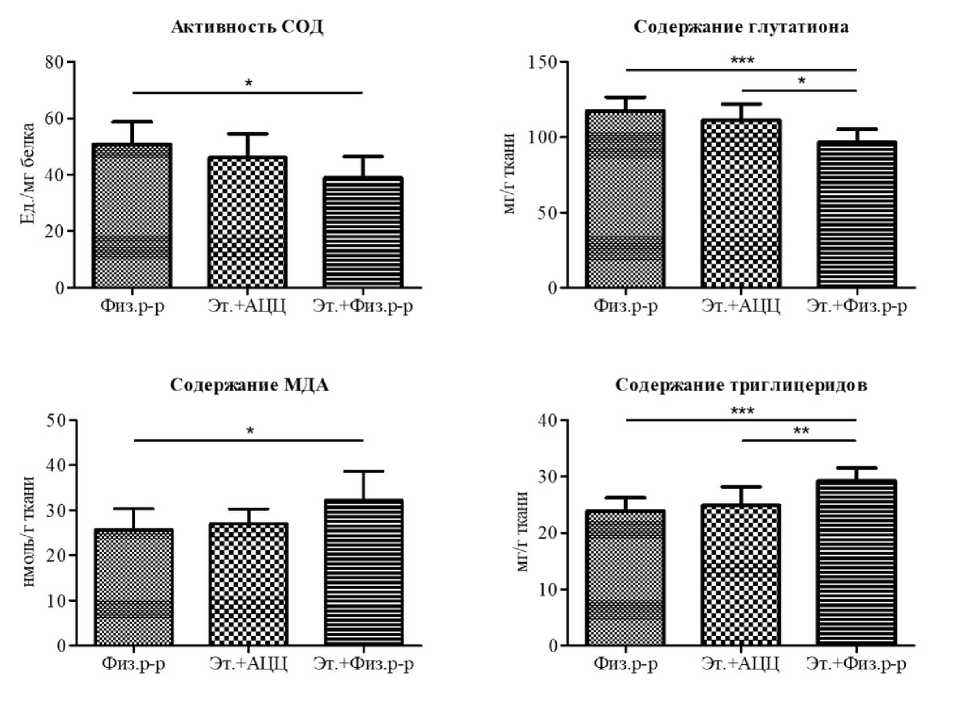
Рис. Влияние однократного перорального введения ацетилцистеина в дозе 1 г/кг на активность супероксиддисмутазы и содержание глутатиона, малонового диальдегида и триглицеридов в гомогенатах печени самцов крыс, перенесших постинтоксикационное состояние, вызванное внутрибрюшинным введением этанола в дозе 3 г/кг
Примечание: Физ. р-р – физиологический раствор; Эт.+АЦЦ – этанол и ацетилцистеин; Эт. + Физ. р-р – этанол и физиологический раствор; данные представлены в виде усредненных индивидуальных значений (n = 3 в каждой из точек), среднего арифметического значения и стандартной ошибки среднего арифметического; СОД – супероксиддисмутаза; МДА – малоновый диальдегид; *, **, *** – p < 0,05, p < 0,01 и p < 0,0001 соответственно (однофакторный дисперсионный анализ с пост-тестом Ньюмена – Кеулса); сравниваемые группы обозначены горизонтальными линиями.
ЗАКЛЮЧЕНИЕ
У крыс, перенесших алкогольную интоксикацию, вызванную однократным внутрибрюшинным введением этанола, ацетилцистеин препятствовал развитию окислительного стресса и предотвращал развитие токсических проявлений печени, что подтверждалось снижением выраженности изменений активности антиоксидантных систем печени и отсутствием существенного увеличения содержания триглицеридов в гепатоцитах. Таким образом, дальнейшая разработка препарата ацетилцистеина для коррекции постинтоксикационного состояния, вызванного употреблением высоких доз этанола, может быть признана перспективной.
СВЕДЕНИЯ О ФИНАНСОВОЙ ПОДДЕРЖКЕ
Данная работа была выполнена при грантовой поддержке Президента Российской Фе- дерации по Соглашению о предоставлении из федерального бюджета грантов в форме субсидий в соответствии с п. 4 ст. 78.1 Бюджетного кодекса Российской Федерации (внутренний номер МК-3454.2019.7) № 075-15-2019-176 от 23.05.2019 г.
Список литературы Коррекция токсических эффектов этанола у крыс при помощи перорального введения ацетилцистеина
- Оптимизация метода выделения микросомальной фракции печени крыс / Е. И. Морковин [и др.] // Волгоградский Научно-Медицинский Журнал. - 2017. - № 1 (53). - C. 42-44.
- Влияние ацетилцистеина на психоневрологические показатели крыс после острой интоксикации этанолом / Е. И. Морковин [и др.] // Вестник Волгоградского государственного медицинского университета. - 2019. - № 3 (71). - C.110-115.
- Морковин, Е. И. Оценка психоневрологического дефицита у грызунов: основные методы / Е. И. Морковин, Д. В. Куркин, И. Н. Тюренков // Журнал высшей нервной деятельности им. И. П. Павлова. - 2018. - № 1 (68). - C. 3-15.
- Biggs, H. G. A manual colorimetric assay of triglycerides in serum / H. G. Biggs, J. M. Erikson, W. R. Moorehead // Clinical Chemistry. - 1975. -№ 3 (21). - C. 437-441.
- Oral and intravenous acetylcysteine for treatment of acetaminophen toxicity: a systematic review and meta-analysis / J. L. Green [и др.] // The Western Journal of Emergency Medicine. - 2013. - № 3 (14). - Р. 218-226.
- Effects of a preparation of combined glutathione-enriched yeast and rice embryo/soybean extracts on ethanol hangover / H.-S. Lee [и др.] // Journal of Medicinal Food. - 2009. - № 6 (12). - C. 13591367.
- Misra, H. P. The role of superoxide anion in the autoxidation of epinephrine and a simple assay for superoxide dismutase / H. P. Misra, I. Fridovich // The Journal of Biological Chemistry. - 1972. - № 10 (247). - C. 3170-3175.
- Ohkawa, H. Assay for lipid peroxides in animal tissues by thiobarbituric acid reaction / H. Ohkawa, N. Ohishi, K. Yagi // Analytical Biochemistry. -1979. - № 2 (95). - C. 351-358.
- The pathology of alcohol hangover / R. Penning [и др.] // Current Drug Abuse Reviews. - 2010. -№ 2 (3). - C. 68-75.
- Ohkawa, H. Alcohol hangover: a critical review of explanatory factors / H. Ohkawa, N. Ohishi, K. Yagi // Human Psychopharmacology. - 2009. - № 4 (24). - C. 259-267.
- Shaik, I. H. Rapid determination of reduced and oxidized glutathione levels using a new thiol-masking reagent and the enzymatic recycling method: Application to the rat liver and bile samples / I. H. Shaik, R. Mehvar // Analytical and bioanalytical chemistry. - 2006. - № 1 (385). - C. 105-113.
- Shanmugam, K. R. Effect of alcohol on blood glucose and antioxidant enzymes in the liver and kidney of diabetic rats / K. R. Shanmugam, K. Mallikarjuna, K. S. Reddy // Indian Journal of Pharmacology. - 2011. - № 3 (43). - C. 330-335.


