Коррозия стали СТ3 в технологических водных растворах нитрата кальция
Автор: Нифталиев С.И., Козадеров О.А., Козадерова О.А., Клоков Г.В.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Фундаментальная и прикладная химия, химическая технология
Статья в выпуске: 1 (55), 2013 года.
Бесплатный доступ
Методом вольтамперометрии изучено коррозионное поведение конструкционной малоуглеродистой нелегированной стали Ст3 в водных растворах нитрата кальция. Выявлено влияние аммонизации раствора и введения добавок моноэтаноламина и бихромата калия на основные параметры коррозионного процесса.
Аммонизированный раствор нитрата кальция, сталь ст3, коррозия, моноэтаноламин, бихромат калия
Короткий адрес: https://sciup.org/14039955
IDR: 14039955 | УДК: 620.193
Corrosion of steel ST3 in technological water solutions of calcium nitrate
Voltammetry method studied corrosion behavior of low carbon alloy structural steel St3 in aqueous solution of calcium nitrate. The effect ammonation solution and additions of monoethanolamine and potassium dichromate on the basic parameters of the corrosion process
Текст научной статьи Коррозия стали СТ3 в технологических водных растворах нитрата кальция
температурный диапазон использования, а также высокая коррозионная активность заметно ограничивают возможности использования концентрированных солевых растворов в качестве охлаждающих жидкостей и теплоносителей.
Распространенным методом защиты от коррозии, особенно в нейтральных или близких к ним средах, где коррозия протекает преимущественно с кислородной деполяризацией, является введение в агрессивную среду специально подобранных соединений – ингибиторов [4,5].
Целью настоящей работы является изучение коррозионной активности модельного раствора нитрата кальция (РНК) и аммонизированного раствора нитрата кальция (АРНК) с неорганическими и органическими добавками в отношении конструкционной малоуглеродистой нелегированной стали Ст3, представленной в системах охлаждения ДВС.
Исследование коррозионной активности водных растворов нитрата кальция (модельного (45 % масс. Ca(NO3)2) и аммонизированного (45 % масс. Ca(NO3)2, 6 % масс. NH4NO3)) проводили при комнатной температуре вольтамперометрическим методом на стали Ст3 в отсутствие добавок и в присутствии бихромата калия и моноэтаноламина (1 % масс.). Использовали трехэлектродную электрохимическую ячейку с хлоридсеребряным электродом сравнения и платиновым вспомогательным электродом. Поляризационные кривые снимали при помощи потенциостата IPC-Compact, изменяя потенциал рабочего стального электрода из катодной в анодную область со скоростью 10 мВ/с. Потенциалы в работе приведены по шкале стандартного водородного электрода, токи отнесены к геометрической площади исследуемого электрода.
Для определения базовых параметров коррозионного процесса (таблица 1) экстраполировали линейные участки анодной и катодной кривых (рисунок 1) до взаимного пересечения в точке с координатами Екорр (потенциал коррозии) и lgiкорр (iкорр – скорость коррозии в токовых единицах) [6]. Значения тафелевых наклонов линейных участков поляризационных кривых приведены в табл. 2.
Таблица 1
Основные параметры коррозионного процесса на стали Ст3 в РНК (числитель) и АРНК (знаменатель)
|
Параметр |
Добавка |
||
|
отсутствует |
K 2 Cr 2 O 7 |
моноэтаноламин |
|
|
рН раствора |
5,6 7,9 |
4,5 7,7 |
11,2 9,7 |
|
Потенциал коррозии Е корр , мВ |
- 546 - 331 |
- 351 - 443 |
- 458 - 376 |
|
Ток коррозии i корр , мкА/см2 |
28 72 |
30 36 |
8 76 |
|
Скорость коррозии K , г/(м2ч) |
0,28 0,72 |
0,30 0,36 |
0,08 0,76 |
|
Проницаемость П , мм/год |
0,31 0,80 |
0,33 0,40 |
0,09 0,84 |
|
Степень защиты Z , % |
— |
0 50 |
71 - 5,5 |
|
Коэффициент торможения Y |
– |
1,0 2,0 |
3,3 0,95 |
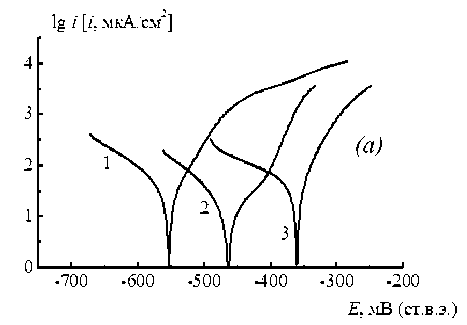
Рис. 1. Поляризационные кривые, полученные на стали Ст3 в модельном (а) и аммонизированном (б) растворах нитрата кальция без ингибитора (1) и с добавкой моноэтаноламина (2) и K 2 Cr 2 O 7 (3)
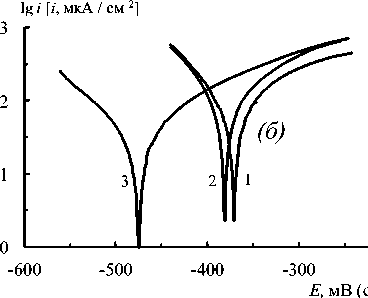
Анализ поляризационных кривых в модельном растворе (рис. 1а) показывает, что бестоковый потенциал коррозии при введении добавок смещается в положительную сторону, а ток анодного процесса при Е = const уменьшается. Эффекты облагораживания коррозионного потенциала и замедления перехода металла в раствор более ярко выражены с добав- кой бихромата калия, чем с моноэтанолами-ном. Влияние на катодный процесс обратное: скорость реакции восстановления на стали при введении ингибиторов в нитратную коррозионную среду не падает, а возрастает. Аммонизация нитратного раствора заметно изменяет электрохимическое поведение системы (рис. 1б). Так, бестоковый потенциал в аммонизированном растворе значительно более положительный, чем в модельном, и при введении добавок, напротив, разблагораживается.
Значения параметров уравнения Тафеля (табл. 2), найденных по линейным участкам E , lg i -кривых на стали в модельном нитратном электролите с разными добавками, свидетельствуют, что коррозия, видимо, протекает с водородной деполяризацией. Действительно, наклон линейного участка катодной полулогарифмической поляризационной кривой составляет (-120 мВ) (исключением является раствор с добавкой моноэтаноламина), что свидетельствует о замедленной стадии разряда
Таблица2
Параметры уравнения Тафеля E = a i + b i •lg i (мВ) для анодного ( aa и Ь а ) и катодного ( ак и Ьк ) парциальных процессов на стали Ст3 в РНК (числитель) и АРНК (знаменатель)
Скорость коррозионного процесса К , найденная из i корр по закону Фарадея, в модельном растворе нитрата кальция ниже, чем в аммонизированном (табл. 1), однако в обоих случаях сталь Ст3 по шкале коррозионной стойкости [7,8] следует отнести к пониженно стойким материалам.
Эффективность добавок в отношении коррозионного процесса оценивали по стандартным параметрам [4]: проницаемости П = 1,11 К ; степени ингибиторной защиты:
Z = K 1 K 2 . юо% _ i корр,1 i корр,2 . 100%
K 1 i корр,1
водорода с переносом одного электрона [4]. Добавление моноэтаноламина, а также аммонизация раствора нитрата кальция снижает кислотность среды (таблица 1), что, вероятно, способствует реализации иного механизма многостадийного катодного процесса, осложненного кислородной деполяризацией.
Аналогичный эффект наблюдается и в анодном поведении стального электрода: если в модельных растворах без ингибитора и с бихроматом калия наклон прямолинейной зависимости потенциала от логарифма анодного тока равен в среднем 40 мВ (табл. 2), что служит признаком электрохимической реакции растворения металла до двухзарядных ионов по двухстадийному механизму с замедленной стадией отщепления второго электрона [4], то введение моноэтаноламина и переход к аммонизированному раствору заметно затрудняют анодный процесс: наклон соответствующего участка Е, lg i- зависимости увеличивается до 60 - 121 мВ (табл. 2).
Y = K 1 _ i корр,1 К “ i , , 2 корр,2
где К 1 ( i корр,1 ) и K 2 ( i ко РР ,2 ) — скорость (плотность тока) саморастворения металла в среде без добавки и с добавкой, соответственно.
Эти параметры, найденные по пересечению линейных участков полулогарифмических поляризационных кривых, отвечающих проте канию парциальных процессов на стали в исследуемых средах, приведены в табл.1.
Введение добавки бихромата калия в модельный раствор заметно снижает скорость анодного растворения стали, однако существенно увеличивает скорость катодной реакции (рис. 1а). Как результат, несмотря на сдвиг коррозионного потенциала в положительную сторону, скорость коррозии практически не изменяется в сравнении с исходным нитратным раствором. В случае моноэтаноламина скорость анодной реакции снижается значительнее, чем катодной, а потому уменьшается и скорость коррозионного процесса в целом. В аммонизированном растворе нитрата кальция моноэтаноламин также снижает скорость анодного растворения стали, однако скорость катодной реакции увеличивается, несмотря на сдвиг коррозионного потенциала в положительную сторону, в результате скорость коррозии практически не изменяется по сравнению с модельным раствором. При применении бихромата калия в качестве ингибитора скорость коррозионного процесса стали Ст3 заметно снижается.
В соответствии со шкалой коррозионной стойкости [7,8] сталь Ст3 в базовом растворе нитрата кальция и с добавкой бихромата калия следует отнести к пониженно стойким материалам; органическая добавка моноэтаноламина к РНК позволяет перевести сталь Ст3 в группу стойких к коррозии материалов. В аммонизированном растворе Ca(NO3)2, как и с добавкой моноэтаноламина, сталь Ст3 можно считать стойким материалом, в то время как введение бихромата калия в АРНК позволяет отнести сталь Ст3 к весьма стойким к коррозии материалам.


