Кристаллизация кальцийсодержащих фаз в алюминиевых электролитах
Автор: Кирик С.Д., Зайцева Ю.Н., Цурган Л.С.
Журнал: Журнал Сибирского федерального университета. Серия: Техника и технологии @technologies-sfu
Статья в выпуске: 2 т.3, 2010 года.
Бесплатный доступ
Выполнены высокотемпературные рентгенографические исследования фаз NaCaAlF6 и Na2Ca3Al2F14. Фиксируемая быстрой закалкой от высоких температур фаза NaCaAlF6 при нагревании до 640оС распадается с образованием Na2Ca3Al2F14. Дальнейший нагрев в вакууме либо на воздухе до 740оС приводит к разложению Na2Ca3Al2F14 на CaF2 и Na3AlF6.. Обратный переход Na2Ca3Al2F14 в NaCaAlF6 не фиксируется. Превращение NaCaAlF6 в Na2Ca3Al2F14 при охлаждении или при нагревании происходит по реакции распада с выделением NaAlF4 в области температур 560-610оС. Термическая обработка образцов электролита демонстрируют прямой и обратный переход тройных фаз. Сформулированы рекомендации по пробоподготовке образцов в целях контроля состава электролита методом РФА.
Производство алюминия, промышленные электролиты, диаграмма состояния системы naf-alf3-caf2, рентгенофазовый анализ
Короткий адрес: https://sciup.org/146114530
IDR: 146114530 | УДК: 669.713.7
Crystallization of calcium-containing phases in aluminum electrolyte
The specific features of calcium-containing phases crystallization have been investigated in case of industrial electrolyte sampling for the purposes of composition control. The influence of cooling rate on the crystallization has been studied. It was found that the phase NaCaAlF6 was stable in the temperature range of 640-740 ºС. Transformation of NaCaAlF6 into Na2Ca3Al2F14 under cooling or hitting goes with isolation of NaAlF4 at 560-610 ºС. High temperature XRD investigation of individual samples of NaCaAlF6 and Na2Ca3Al2F14 has been cared out. Recommendations on an optimal sampling for XRD control procedure were formulated.
Текст научной статьи Кристаллизация кальцийсодержащих фаз в алюминиевых электролитах
Одним из главных элементов технологии производства алюминия является контроль состава электролита [1], который выполняется рентгенофазовым анализом (РФА) закристаллизованных проб. Состав электролита представляет ряд кристаллических фаз: Na3AlF6 (криолит), Na 5 Al 3 F 14 (хиолит), CaF 2 (флюорит) и другие. По калибровочным кривым находят концентрации каждой из присутствующих фаз, которые пересчитывают в концентрации химических компонентов и вычисляют ключевой технологический параметр – криолитовое отношение (КО) – мольное отношение фторида натрия к фториду алюминия [2].
Количественное определение кальцийсодержащих фаз в электролите проблемно. Установлено существование двух тройных фторидов NaCaAlF6, Na2Ca3Al2F14, которые наряду с CaF2 являются кальцийсодержащими фазами, обнаруживаемыми в закристаллизованных образцах электролита [3, 4]. Регистрация фазы NaCaAlF6 методом РФА усложняется в связи с ее слабой окристаллизованностью. При кристаллизации электролита кальций может распределяться между всеми кальцийсодержащими фазами в зависимости от процедуры пробоотбора и состава электролита [5].
В настоящей работе проведено уточнение стадий кристаллизации кальцийсодержащих фаз в образцах промышленного электролита с целью повышения точности измерений технологических характеристик методом РФА. Для этого исследовали: влияние скоростей охлаждения на кристаллизацию кальцийсодержащих фаз в электролитах с разными значениями КО в промышленных образцах и синтезированных в лабораторных условиях; влияние отжига на фазовые переходы кальцийсодержащих фаз в электролитах; выполнены высокотемпературные рентгенографические исследования кальцийсодержащих фаз.
Методики и результаты исследований
Для проведения исследований электролиты массой 10 г плавили в закрытом платиновом тигле в шахтной печи при температурах от 960 до 1000 ºС (в зависимости от величины КО) в течение 20 мин в атмосфере воздуха. Далее образцы охлаждали в массивной металлической изложнице комнатной температуры, в тигле на воздухе или вместе с печью. Охлаждение электролита в печи проводили со скоростью 8 ºС /мин до температур 560, 610 и 710 ºС, выдерживали при этих температурах в течение 30 мин, далее охлаждали на воздухе.
Образцы фаз NaCaAlF 6 , Na 2 Ca 3 Al 2 F 14 были синтезированы в соответствии с рекомендациями [6] из смесей AlF3, CaF2, NaF, взятых в соответствующих стехиометрических соотношениях. Фаза NaCaAlF 6 была получена при 720 ºС, время синтеза – 1 час, а фаза Na 2 Ca 3 Al 2 F 14 – при 560 ºС в течение 30 часов. Во всех случаях проводился контроль потери массы с точностью ± 0,001г.
Съемку рентгенограмм полученных образцов проводили на дифрактометре X’Pert Pro (PANalitical), оборудованном детектором PIXel с графитовым монохроматором, с использованием CuKα-излучения в диапазоне от 10о до 80о с шагом 0,026о по 2 Θ с полным временем сканирования 12 мин. Образец готовился методом прямой набивки в кювете диаметром 27 мм.
Высокотемпературные рентгенографические исследования были проведены на дифрактометре X-Pert Pro (PANalitical) с высокотемпературной камерой NTK1200N «Anton Paar». Образец нагревали со скоростью 50 ºС /мин до установленной температуры и затем проводили съемку в интервале углов 2θ от 5 до 80о. Далее процесс повторялся на следующей температурной ступени.
Области исследованных составов «рабочих электролитов» (выделено цветом) и основные кальцийсодержащие фазы, встречающиеся в охлажденных пробах электролитов, показаны на треугольнике системы NaF-CaF 2 -AlF 3 [4] (рис. 1).
В работах [7,8] установлено, что скорость охлаждения влияет на распределение кальция между фазами NaCaAlF 6 и Na 2 Ca 3 Al 2 F 14 . Быстрое охлаждение дает больше NaCaAlF 6 , но механизм этого влияния не исследован. Эксперименты по охлаждению с разными скоростями (на воздухе, выливанием расплава в изложницу, охлаждение в печи) проведены с образцами, принадлежащими к двум различным областям составов с различным криолитовым отношением. Рентгенографический анализ продуктов показал, что качественного изменения фазового состава при изменении скорости кристаллизации не происходит. Наблюдаются следующие фазы: Na 3 AlF 6 , Na 5 Al 3 F 14 , NaCaAlF 6 , Na 2 Ca 3 Al 2 F 14 и CaF 2 . С увеличением скорости охлаждения линии криолита уширяются примерно на 10 %. Скорость охлаждения оказывает влияние на микроструктуру отдельных фаз образца. Кальций присутствовал в виде трех фаз: NaCaAlF 6 , – 172 –
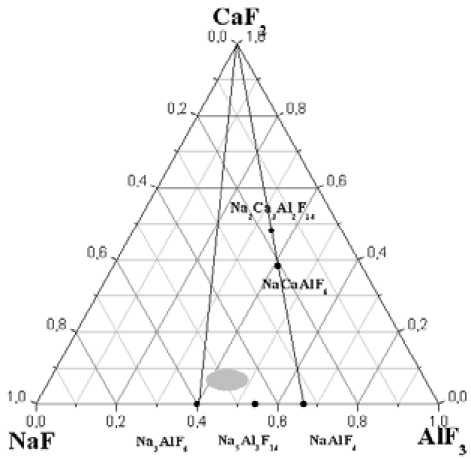
Рис. 1. Треугольник системы NaF-CaF 2 -AlF 3
Na 2 Ca 3 Al 2 F 14 и CaF 2 . Фаза NaCaAlF 6 , доминировала в образцах с КО>2,6, а фаза Na 2 Ca 3 Al 2 F 14 – в образцах с КО<2,3.
Охлаждение расплавленного образца в печи с последующим отжигом при 710, 610 или 560 ºС в результате приводит к изменению фазового состава. После отжига при 710 ºС фиксируется преимущественно NaCaAlF 6 , а после отжига при температурах 610 и 560 ºС – преимущественно Na2Ca3Al2F14. Наиболее вероятным процессом, приводящим к образованию новой фазы, может быть распад при температуре около 610 ºС:
3NaCaAlF 6 → Na 2 Ca 3 Al 2 F 14 + NaAlF 4 . (1)
Для исследований при термических превращениях были синтезированы фазы NaCaAlF6 и Na 2 Ca 3 Al 2 F 14 . В качестве примеси наблюдался CaF 2 , также были обнаружены небольшие количества хиолита и криолита.
Высокотемпературные рентгенографические съемки фаз NaCaAlF 6 и Na 2 Ca 3 Al 2 F 14 проведены путем ступенчатого нагрева в вакууме. Образец фазы NaCaAlF6 нагревали в вакууме до 600 ºС с промежуточными съемками при 100, 300, 400, 500, 550, 570, 600 ºС (рис. 2). До 400 ºС фаза NaCaAlF6 претерпела небольшие структурные изменения при сохранении фазового состава. При 500 ºС начинается процесс распада NaCaAlF 6 с образованием Na 2 Ca 3 Al 2 F 14 по уравнению 1. В условиях вакуума при 500 ºС наблюдалось полное превращение NaCaAlF6 в Na 2 Ca 3 Al 2 F 14 . Последняя фаза затем распалась на Na 3 AlF 6 и CaF 2 .
На рентгенограмме, снятой при 500 ºС, видно, что произошли небольшие структурные изменения фазы NaCaAlF 6 ; появились линии фазы Na 2 Ca 3 Al 2 F 14 (рис. 2). После выдержки в течение часа при 500 ºС исчезли линии фазы NaCaAlF6, увеличилось содержание фаз Na2Ca3Al2F14, CaF 2 и Na 3 AlF 6 .
Нагревание Na2Ca3Al2F14 в высокотемпературной рентгеновской камере показало, что фаза сохраняется примерно до 600 ºС, после чего начинается ее распад. На рентгенограммах за- – 173 –
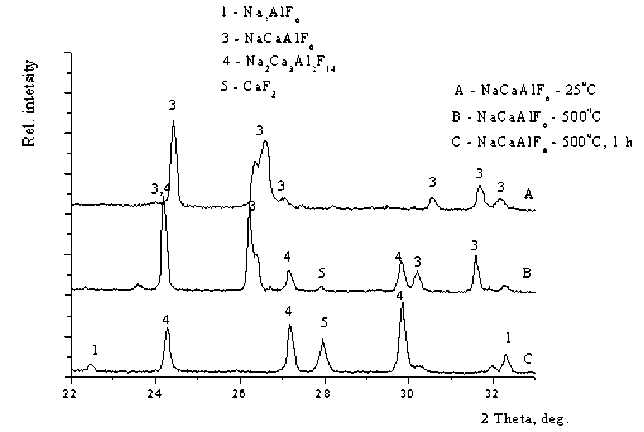
Рис. 2 Рентгенограммы образца NaCaAlF 6 , снятые в высокотемпературной камере при 25 ºС, 500 ºС, при 500 ºС – 1 час.
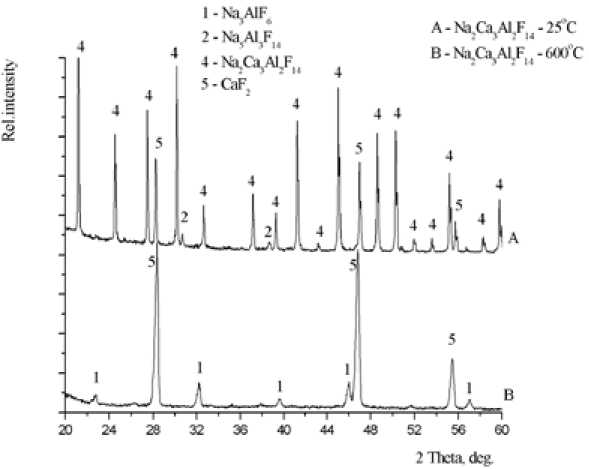
Рис. 3. Рентгенограммы образца Na2Ca3Al2F14, снятые в высокотемпературной камере при 25 ºС, 600 ºС фиксированы только две фазы распада: CaF2 и Na3AlF6 (рис. 3). Наблюдаемый процесс можно описать уравнениями:
Na 2 Ca 3 Al 2 F 14 → 2NaAlF 4 + 3CaF 2 ; (2)
3NaAlF 4 → Na 3 AlF 6 + 2AlF 3 . (3)
На рентгенограмме, снятой при 600 ºС, фаза Na2Ca3Al2F14 исчезла, увеличилось содержание CaF 2 , появились линии Na 3 AlF 6 .
Окончательные продукты превращения принадлежат квазибинарной системе эвтектического типа CaF 2 – Na 3 AlF 6 с эвтектикой при 945 ºС [9]. При охлаждении в данной системе протекает фазовое превращение β-Na3AlF6 → α-Na3AlF6.
Соединение NaAlF 4 на рентгенограммах не наблюдалось, поэтому были проведены исследования паров, образующихся при прокаливании соединения Na2Ca3Al2F14 в платиновой лодочке в токе азота. Конденсат осаждался на водоохлаждаемой поверхности реактора. Исследования тетрафторалюмината натрия приведены в [10-14]. По данным авторов [14], соединение NaAlF 4 образуется по перитектической реакции NaAlF 4 (т) → 1/5 Na 5 Al 3 F 14 (т) + 2/5 AlF 3 (т) при 710 ºС и распадается при 680 ºС. Рентгенографическое исследование собранного конденсата показало наличие соединения NaAlF 4 , что подтверждает сделанные предположения о превращении тройных соединений Na2Ca3Al2F14 и NaCaAlF6 с участием фазы NaAlF4.
Заключение
Проведенные эксперименты позволяют сделать следующие выводы. Образующиеся в системе NaF-AlF3-CaF2 кальциевые криолиты в равновесной диаграмме состояния занимают различные температурные области. Na 2 Ca 3 Al 2 F 14 является низкотемпературной фазой, NaCaAlF 6 – высокотемпературной. Превращение NaCaAlF6 в Na2Ca3Al2F14 происходит по реакции распада с выделением NaAlF 4 . В индивидуальных фазах не происходит обратной реакции превращения Na2Ca3Al2F14 в NaCaAlF6. Вместо этого наблюдается реакция распада фазы Na2Ca3Al2F14 на CaF2 и NaAlF 4 . Фаза NaAlF 4 в условиях съемки в высокотемпературной камере распадается с образованием Na3AlF6. Фаза NaAlF4 обнаружена в парах возгона, что позволяет включить ее материальный баланс с учетом уравнений 1, 2, 3.
Фаза NaCaAlF6 имеет слабую окристаллизованность, что уменьшает точность ее измерения методом РФА. Кристаллизации образца с отсутствием NaCaAlF 6 можно добиться кратковременным прокаливанием в печи при 500-600 ºС уже отобранных проб электролита для перевода кальция из фазы NaCaAlF 6 в Na 2 Ca 3 Al 2 F 14 . Эта процедура позволит определять технологические параметры (КО) электролиза с большей точностью.


