Лапароскопическая коррекция рецидива гастроэзофагеальной рефлюксной болезни и грыжи пищеводного отверстия диафрагмы после дважды провальной фундопликации. Клинический случай
Автор: Гололобов Г.Ю., Ерин С.А., Овчинникова У.Р., Абумуслимов К.К., Хусаинов И.Р., Китиева А.А., Галлямов Э.А.
Журнал: Хирургическая практика @spractice
Рубрика: Хирургия
Статья в выпуске: 4 т.8, 2023 года.
Бесплатный доступ
Цель: выявление основных причин «провалов» предшествующих оперативных вмешательств и способов их профилактики в ходе первичного хирургического лечения грыжи пищеводного отверстия диафрагмы.Материал и методы. С целью решения научной проблемы произведен научных поиск среди источников мировой научной литературы, посвященной проблеме лечения первичных и рецидивных грыж пищеводного отверстия диафрагмы (ГПОД). Кроме того, представлено клиническое наблюдение, в ходе которого было выполнено хирургическое лечение пациента, которому ранее дважды производилась коррекция грыжи и гастроэзофагеальной рефлюксной болезни (ГЭРБ).Результаты. В научной литературе представлены немногочисленные случаи успешной коррекции рецидива ГЭРБ и ГПОД у пациента после двух фундопликаций. Кроме того, предложен термин «провальная фундопликация», который на сегодняшний день не описан отечественной литературе. На взгляд авторов, устранение «неверно» сформированного антирефлюксного механизма, который приводит к запрограммированному рецидиву ГПОД, а также выполнение технически верного антирефлюксного вмешательства позволяет добиться выраженного клинического эффекта у пациентов, которым ранее была выполнена одна и более фундопликаций, при условии адекватной перистальтики пищевода и желудка. В представленном клиническом случае хирургическая тактика основана на принципах устранения последствий предыдущего вмешательства с выполнением повторного вмешательства, направленного на устранение в первую очередь гастроэзофагеального рефлюкса.Заключение. Повторные антирефлюксные оперативные вмешательства представляют значительную трудность для хирургического лечения, что обусловлено несколькими факторами одновременно. Выявление технических ошибок при раннее выполненных антирефлюксных оперативных вмешательствах, устранение их и создание адекватного антирефлюксного механизма способствуют успеху повторного вмешательства. На сегодняшний день необходима стандартизация антирефлюксных вмешательств, поскольку соблюдение технических аспектов первичных оперативных вмешательств является наиболее эффективным способом снижения риска рецидива заболевания и частоты выполнения ревизионных антирефлюксных операций.
Грыжа пищеводного отверстия диафрагмы, гастроэзофагеальная рефлюксная болезнь, лапароскопическая фундопликация, лапароскопическая рефундопликация, провальная фундопликация
Короткий адрес: https://sciup.org/142239983
IDR: 142239983 | УДК: 616.329-089.844:616.26 | DOI: 10.38181/2223-2427-2023-4-1
Laparoscopic treatment of recurrent gastroesophageal reflux disease and hiatal hernia after two failed fundoplications: a clinical case
Aim: identification of the main causes of failures of previous surgical interventions and methods of their prevention during the primary surgical treatment of hernia of the esophageal orifice of the diaphragm.Material and methods. To address the scientific inquiry, an extensive review was conducted across global scientific literature focused on the treatment of primary and recurrent hernias of the esophageal orifice of the diaphragm (GPOD). Additionally, a clinical observation is provided, detailing a surgical intervention performed on a patient who had undergone correction for hernia and gastroesophageal reflux disease (GERD) on two prior occasions.Results. The scientific literature reports limited instances of successfull correction of the recurrence of gastroesophageal reflux disease (GERD) and gastroesophageal orifice diaphragmatic hernias (GPOD) in patients after two fundoplications. The term ‘failed fundoplication’ is introduced, a concept not yet described in domestic literature. Eliminating the incorrectly formed antireflux mechanism, which leads to a programmed recurrence of GPOD, and implementing technically correct antireflux interventions allow for the achievement of a pronounced clinical effect in patients who have undergone one or more fundoplications, provided there is adequate peristalsis of the esophagus and stomach. In the presented clinical case, the surgical procedure is based on the principles of mitigating the consequences of the previous intervention through repeated intervention primarily focused on eliminating gastroesophageal reflux.Conclusion. Repeated antireflux surgical interventions pose a significant challenge in surgical treatment, attributable to multiple factors concurrently. Identifying technical errors during early antireflux surgical interventions, eliminating them, and establishing an adequate antireflux mechanism contribute to the success of repeated interventions. Standardization of antireflux interventions is imperative, as adherence to the technical aspects of primary surgical interventions represents the most effective means to diminish the risk of disease relapse and the frequency of subsequent revision antireflux operations.
Текст научной статьи Лапароскопическая коррекция рецидива гастроэзофагеальной рефлюксной болезни и грыжи пищеводного отверстия диафрагмы после дважды провальной фундопликации. Клинический случай
К этиологическим факторам, обусловливающим развитие патологического рефлюкса, можно отнести нарушение функционирования нижнего пищеводного сфинктера (например, вследствие врожденной слабости нижнего пищеводного сфинктера, системных заболеваний соединительной ткани и др.), однако наиболее частой причиной развития стойких симптомов ГЭРБ является изменение нормальной анатомии зоны пищеводно-желудочного перехода в виде наличия грыжи пищеводного отверстия диафрагмы (ГПОД) [3]. Корреляция между ГЭРБ и наличием ГПОД достоверно подтверждена во многих исследованиях, при этом наличие грыжи наблюдается у 83 % пациентов с ГЭРБ, тогда как распространенность ГЭРБ при наличии ГПОД достигает 68 % [4; 5].
Следует отметить, что наличие ГПОД у пациентов с патологическим рефлюксом является неоспоримым показанием к хирургическому лечению, поскольку основным фактором развития рефлюкса в этом случае является дефект анатомических структур пищеводно-желудочного перехода, который не подлежит коррекции посредством консервативной терапии. При этом лапароскопическая фундопликация остается «золотым стандартом» в современной малоинвазивной антирефлюксной хирургии, обеспечивая эффективность и безопасность методики в 95 % случаев [6]. Однако, несмотря на высокую эффективность и безопасность оперативного вмешательства, в ряде случаев наблюдается развитие реци-8 дивов заболевания.
Рецидив грыжи пищевого отверстия диафрагмы определяется как клинический рецидив ГЭРБ и/или появление новых симптомов (например, болевой синдром, дисфагия, вздутие живота и др.), вне зависимости от рентгенологической картины. Согласно данным мировой литературы, частота рецидива ГПОД после первичного хирургического лечения составляет от 4 до 24 % [7—9]. В ряде случаев развитие клинического и рентгенологического рецидива заболевания обусловлено несоблюдением технических аспектов первичного оперативного вмешательства, тогда здесь применим термин «провальной фундопликации», обусловливающей неизбежное развитие рецидива ГПОД и симптоматики ГЭРБ.
Согласно данным M. Patti с соавт., среди причин провальной фундопликации выделяют следующие [10]: неверное определение показаний к операции; неверное предоперационное обследование пациента; технические ошибки на этапах выполнения антирефлюксного вмешательства.
В большинстве случаев симптомы рецидива ГПОД, как и первичной грыжи, не поддаются консервативной терапии, вызывая необходимость проведения ревизионного вмешательства в объеме восстановления первичной анатомии зоны кардиоэзофагеального перехода и формирования новой фундопликационной манжеты. Следует отметить, что оперативное вмешательство, направленное на формирование физиологичной и адекватно функционирующей фундопликационной манжеты, имеет ряд технических особенностей, соблюдение которых представляется необходимым для достижения успешного результата в случаях работы как с первичными, так и рецидивными ГПОД.
В данной статье представлен вариант коррекции рецидива ГЭРБ и ГПОД у пациента после дважды провальной фундопликации на основании клинического случая с целью выявления основных причин «провалов» предшествующих оперативных вмешательств и способов их профилактики в ходе первичного хирургического лечения.
Описание клинического случая
Пациент К., 39 лет, ИМТ = 29,3 кг/м2, статус ASA II, обратился в ГБУЗ «ГКБ им. С. И. Спасокукоцкого ДЗМ» в августе 2022 г. для планового оперативного лечения. Предъявлял жалобы на изжогу после приема пищи, вздутие живота, боль в эпигастральной области после приема пищи, рвоту съеденной пищей. Из анамнеза известно, что изжога беспокоила с 2000 г., регулярно принимал препараты из группы ингибиторов протонной помпы (ИПП) на протяжении 17 лет, без положительной динамики. В 2017 г. в ходе амбулаторного обследования, по данным рентгенологического исследования, диагностирована ГПОД 1-го типа по классификации SAGES (Society of American Gastrointestinal and Endoscopic Surgeons, 2013) [11]. В том же году пациенту по поводу грыжи была выполнена лапароскопическая фундопликация по Ниссену. В результате первичного оперативного лечения была достигнута клиническая ремиссия, однако спустя 18 месяцев пациент отметил возобновление симптоматики, в связи с чем был обследован амбулаторно. По данным жалоб и инструментальной диагностики был установлен рентгенологический и клинический рецидив ГПОД (рис. 1). В 2019 г. пациенту выполнено оперативное вмешательство в объеме лапароскопической рефундопликации по Ниссену с аллокруропластикой пищеводного отверстия диафрагмы полипропиленовой сеткой. Спустя 1 месяц после ревизионного вмешательства пациент отметил возобновление клинического паттерна заболевания.
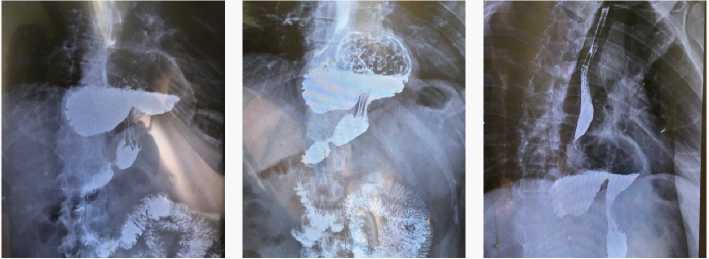
Fig. 1. X-ray of the esophagus and stomach with oral contrast agent after the initial fundoplication, indicating a recurrent hiatal hernia (HH) and a suspected paraesophageal hernia
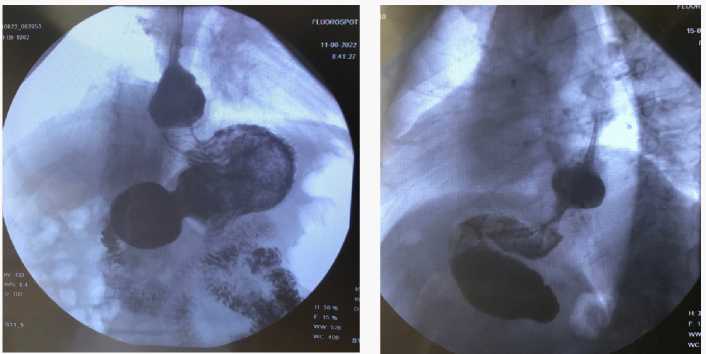
Fig. 2. X-ray of the esophagus and stomach with oral contrast agent after the second fundoplication. Recurrent HH type 2, as per Suppiah’s classification (Slipped Nissen fundoplication)
Оценка предоперационного статуса пациента с помощью опросников продемонстрировала крайне неудовлетворительные результаты: GSRS (англ. Gastrointestinal Symptom Rating Scale)—63 балла, GERD-HRQL (англ. Gastro-Esophageal Reflux Disease Health-Related Quality of Life)—38 баллов. Полученные данные свидетельствовали о крайне низком качестве жизни ввиду стойкой клинической картины основного заболевания.
Пациент подготовлен к ревизионному оперативному вмешательству, направленному на коррекцию дважды неудачно выполненной фундопликации, со следующим предоперационным диагнозом: рецидивная ГПОД 2-го типа по Suppiah, рефлюкс-эзофагит нижней трети пищевода, стадия С (Los Angeles Classification, 2014). Объем запланированного оперативного вмешательства: удаление сетчатого протеза, лапароскопическая рефундопликация.
Техника оперативного вмешательства
При ревизии зоны операционного интереса в условиях выраженного рубцово-спаечного процесса в тканях было определено наличие элементов фундопликационной манжеты и металлических скоб с сетчатым имплантом (рис. 3). После выделения ножек пищеводного отверстия диафрагмы было установлено расширение отверстия до трех диаметров пищевода, также была отмечена миграция ранее установленного сетчатого протеза в заднее средостение.
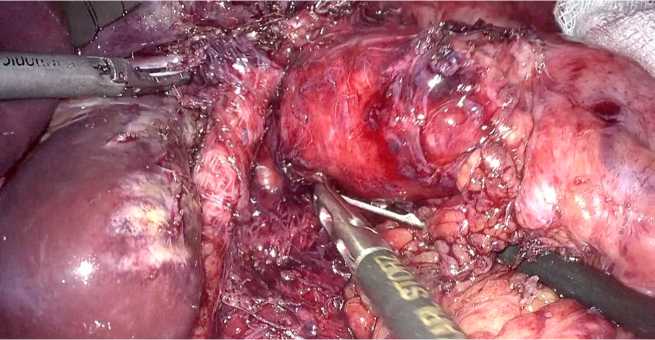
Рис. 3. Интраоперационная картина. Элементы первичной фундопликационной манжеты и инородных фиксирующих материалов
Fig. 3. Intraoperative image. Elements of the primary fundoplication wrap and foreign fixation materials
В ходе работе в зоне кардиоэзофагеального перехода интраоперационная картина свидетельствовала об отсутствии ранее выполненной крурорафии, также выявлен параэзо-фагеальный дефект с наличием грыжевого мешка без наличия параэзофагеальной грыжи, что стало признаком сохраненного в ходе предшествующих вмешательств грыжевого мешка (рис. 4).
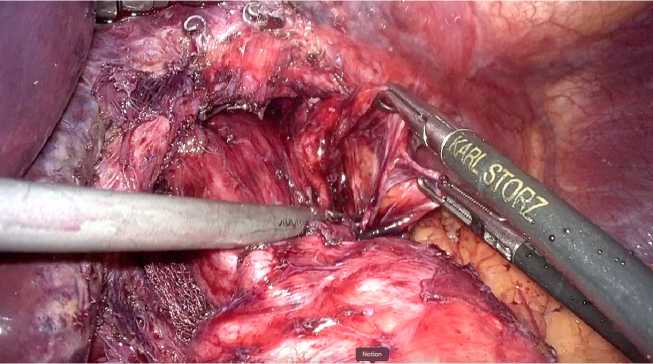
Рис. 4. Интраоперационная картина. Параэзофагеальный дефект с наличием грыжевого мешка без наличия параэзофагеальной грыжи
Fig. 4. Intraoperative image. Paraesophageal defect characterized by the presence of a hernial sac and devoid of a concurrent paraesophageal hernia
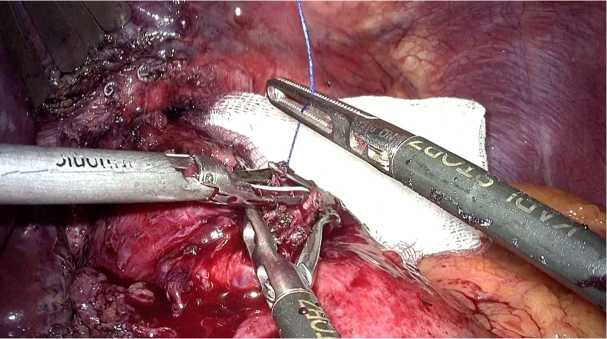
Рис. 5. Интраоперационная картина
Fig. 5. Intraoperative image
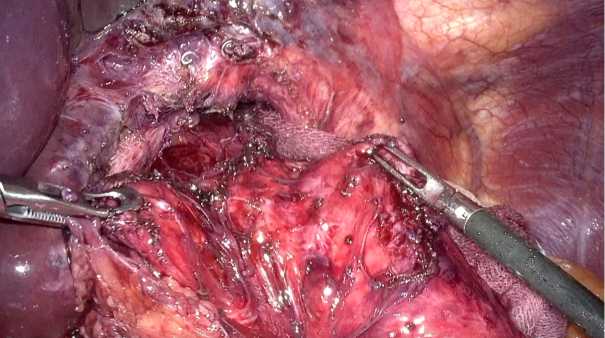
Рис. 6. Интраоперационная картина. Этап демонтажа первичной манжеты
Fig. 6. Intraoperative image. The stage of dismantling the primary wrap
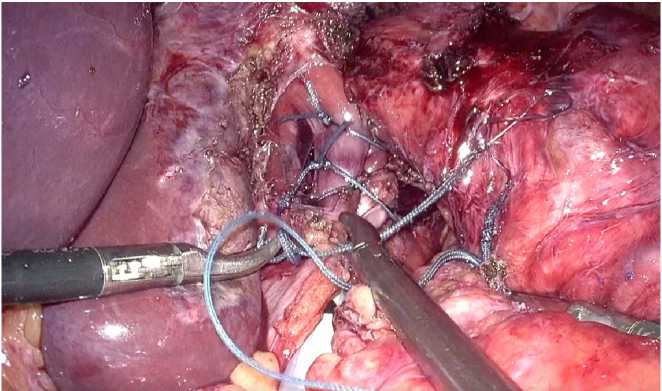
Рис. 7. Интраоперационная картина. Этап задней крурорафии Z-образными швами
Fig. 7. Intraoperative image. A stage of posterior cruroplasty with Z-shaped sutures
На заключительном этапе оперативного вмешательства была сформирована фундо-пликационная манжета по типу «short floppy» Nissen длиной 20 мм (рис. 8). Манжета была фиксирована двумя узловыми швами к передней и задней стенкам пищевода.
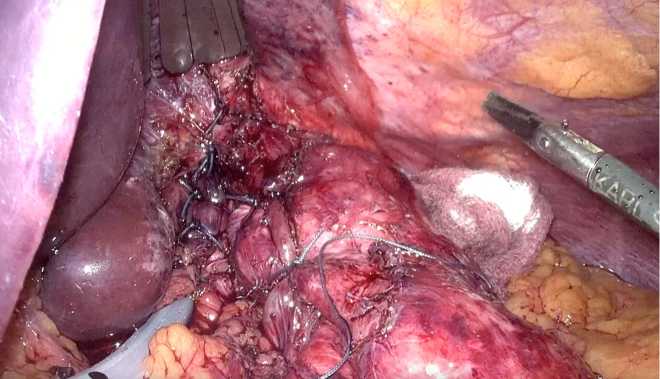
Рис. 8. Интраоперационная картина. Формирование фундопликационной манжеты по типу «short sloppy» Nissen
Fig. 8. Intraoperative picture. Formation of a fundoplication wrap according to the ‘short sloppy’ Nissen type
В левое подпеченочное пространство был установлен страховочный дренаж (6 мм) через доступ в левом подреберье.
Продолжительность операции составила 230 мин. Интраоперационная кровопотеря составила 400 мл. Интраоперационные осложнения отсутствовали. Страховой дренаж удален на 1-е сутки послеоперационного периода. Дренаж из заднего средостенья также 13 удален на 1-е сутки.
В раннем послеоперационном периоде отмечена положительная динамика состояния пациента в виде купирования болевого синдрома и диспепсических явлениии. Контрольное рентгеноскопическое исследование с пероральным контрастированием на 1-е сутки после операции продемонстрировало порционное поступление контраста из пищевода в желудок, данных за задержку и экстравазацию контрастного вещества в области гастроэзофагеального перехода не было, что свидетельствовало об адекватно сформированной функционирующей манжете (рис. 9). По данным контрольного УЗИ брюшной полости, свободной и осумкованной жидкости не определялось.
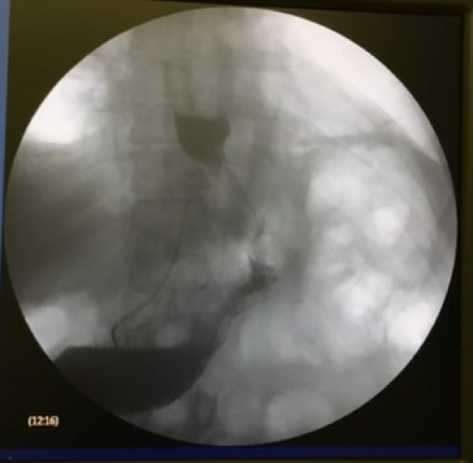
Fig. 9. X-ray examination of the esophagus and stomach with oral contrast agent on the first day after the refundoplication
С учетом гладкого течения послеоперационного периода и отсутствия ранних послеоперационных осложнений'! (согласно унифицированной шкале Clavien-Dindo) пациент выписан на 5-е сутки после операции под амбулаторное наблюдение врачом-хирургом по месту жительства.
Обсуждение
Широкая распространенность ГЭРБ и ГПОД на сегодняшний день обусловливает поливариативность подходов к оперативной технике, что в ряде случаев приводит к несоблюдению технических элементов первичных антирефлюксных вмешательств. Это неизбежно снижает безопасность и эффективность оперативных вмешательств. Согласно данным мировой литературы, частота клинических рецидивов патологического рефлюкса после первичного оперативного лечения составляет от 4 до 24 %, при этом до 9 % случаев требуют проведения ревизионного оперативного вмешательства [12; 13]. В свою очередь, под рецидивом ГПОД следует понимать именно клинический рецидив ГЭРБ и/или появление новых симптомов (например, болевой синдром, дисфагия, вздутие живота и др.), вне зависимости от рентгенологической картины. Группой авторов предложена классификация, наиболее полно отображающая совокупность понятий, связанных с термином «рецидив ГПОД»:
-
• рентгенологический рецидив на фоне клинического благополучия при отсутствии медикаментозного лечения;
-
• клинический рецидив ГЭРБ и/или появление новых симптомов (дисфагия, вздутие и т. д.) на фоне рентгенологического рецидива;
-
• клинический рецидив ГЭРБ и/или появление новых симптомов (дисфагия, вздутие и т. д.) при отсутствии рентгенологического рецидива.
Таким образом, термин «провальная фундопликация» целесообразно определить как выполнение технических ошибок в ходе антирефлюксного вмешательства, которые в совокупности приводят пациента к запрограммированному рецидиву ГПОД.
Г. Ю. Гололобов, С. А. Ерин, У. Р. Овчинникова, К. К. Абумуслимов, И. Р. Хусаинов, А. А. Китиева, Э. А. Галлямов щеводного отверстия диафрагмы U-образной полипропиленовой сеткой, отсутствие предшествующей диссекции и удаления грыжевого мешка, использование неверного шовного материала на этапах формирования манжеты.
Стоит отметить, что классификация S. Horgan (1999) не влияет на тактику ревизионного вмешательства при провальной фундопликации, однако помогает определить причину развития рецидива после первичного хирургического лечения, что, несомненно, важно в рамках стандартизации техники первичных и повторных антирефлюксных вмешательств. Существует ряд исследований, демонстрирующих, что результаты операций по поводу рецидива ГПОД после антирефлюксного вмешательства, как правило, менее удовлетворительны по сравнению с первичной процедурой, особенно после многочисленных неудачных вмешательств. По мнению A. Little и соавт., это обусловлено нарушением моторики пищевода и прогрессирующим разрушением тканей, в том числе связочного аппарата пищевода [17]. В исследовании авторы продемонстрировали, что среди пациентов с меньшим количеством оперативных вмешательств (фундопликация по Ниссену с крурорафией) отмечался более оптимальный клинический результат лечения по сравнению с пациентами, перенесшими многократные антирефлюксные вмешательства (85 и 66 % соответственно). Аналогичные результаты продемонстрировали J. Richter и соавт., заключив, что повторная операция (n ≥ 3) заканчивается успехом лишь в 50 % случаев. К сходным результатам пришли В. В. Анищенко и соавт., продемонстрировав, что из 67 ревизионных оперативных ан-тирефлюксных вмешательств хорошие и отличные результаты были достигнуты в 22,8 % случаев [18].
Поскольку работа с рецидивными случаями ГПОД осуществляется в условиях измененной первоначальной анатомии зоны кардиоэзофагеального перехода и спаечного процесса, основным постулатом повторных антирефлюксных вмешательств является восстановление «первичной анатомии» зоны оперативного интереса в целях соблюдения прецизионности дальнейшей оперативной техники и формирования «физиологичной» манжеты, не суживающей, не ротирующей пищевод и не деформирующей желудок. В качестве еще одного важного аспекта эффективности ревизионных антирефлюксных операций рассматривается отсутствие инородных материалов в зоне пищеводно-желудочного перехода, поскольку на сегодняшний день нет убедительной доказательной базы, подтверждающей отсроченные послеоперационные осложнения при использовании биологических протезов [19; 20].
Важно отметить, что при условии адекватного восстановления первичной анатомии зоны операционного интереса, а также соблюдении всех аспектов выполнения анти-рефлюксного оперативного вмешательства количество предшествующих оперативных вмешательств не является препятствием для успешного исхода ревизионного вмешательства.
Заключение
Повторные антирефлюксные оперативные вмешательства вплоть до настоящего момента представляют значительную трудность для хирургического лечения, что обусловлено несколькими факторами одновременно.
На взгляд авторов, выявление всех технических ошибок при раннее выполненных антирефлюксных оперативных вмешательствах, устранение их и создание адекватного антирефлюксного механизма приведут пациента к выздоровлению. В связи с этим стоит выделять основные технические особенности выполнения фундопликаций, которые будут актуальны как для первичных, так и для повторных операций.
Таким образом, на сегодняшний день крайне необходима стандартизация антиреф-люксных вмешательств, поскольку соблюдение технических аспектов первичных опера- 16 тивных вмешательств является наиболее эффективным способом снижения риска рецидива заболевания и частоты выполнения ревизионных антирефлюксных операций.
Список литературы Лапароскопическая коррекция рецидива гастроэзофагеальной рефлюксной болезни и грыжи пищеводного отверстия диафрагмы после дважды провальной фундопликации. Клинический случай
- Vakil N, van Zanten SV, Kahrilas P, Dent J, Jones R; Global Consensus Group. The Montreal definition and classification of gastroesophageal reflux disease: a global evidence-based consensus. Am J Gastroenterol. 2006 Aug;101(8):1900-20; quiz 1943. https://doi.org/10.1111/j.1572-0241.2006.00630.x
- Hunt R, Armstrong D, Katelaris P, Afihene M, Bane A, Bhatia S, Chen MH, Choi MG, Melo AC, Fock KM, Ford A, Hongo M, Khan A, Lazebnik L, Lindberg G, Lizarzabal M, Myint T, Moraes-Filho JP, Salis G, Lin JT, Vaidya R, Abdo A, LeMair A; Review Team:. World Gastroenterology Organisation Global Guidelines: GERD Global Perspective on Gastroesophageal Reflux Disease. J Clin Gastroenterol. 2017 Jul;51(6):467-478. https://doi.org/10.1097/MCG.0000000000000854
- Schlottmann F, Andolfi C, Herbella FA, Rebecchi F, Allaix ME, Patti MG. GERD: Presence and Size of Hiatal Hernia Influence Clinical Presentation, Esophageal Function, Reflux Profile, and Degree of Mucosal Injury. Am Surg. 2018 Jun 1;84(6):978-982.
- Antoniou SA, Koch OO, Antoniou GA, Asche KU, Kaindlstorfer A, Granderath FA, Pointner R. Similar symptom patterns in gastroesophageal reflux patients with and without hiatal hernia. Dis Esophagus. 2013 Jul;26(5):538-43. https://doi.org/10.1111/j.1442-2050.2012.01368.x
- Ouyang W, Dass C, Zhao H, Kim C, Criner G COPDGene Investigators. Multiplanar MDCT measurement of esophageal hiatus surface area: association with hiatal hernia and GERD. Surg Endosc. 2016 Jun;30(6):2465-72. https://doi.org/10.1007/s00464-015-4499-9
- Balci D, Turkcapar AG. Assessment of quality of life after laparoscopic Nissen fundoplication in patients with gastroesophageal reflux disease. World J Surg. 2007 Jan;31(1):116-21. https://doi.org/10.1007/s00268-005-0658-9
- Katz PO, Dunbar KB, Schnoll-Sussman FH, Greer KB, Yadlapati R, Spechler SJ. ACG Clinical Guideline for the Diagnosis and Management of Gastroesophageal Reflux Disease. Am J Gastroenterol. 2022 Jan 1;117(1):27-56. https://doi.org/10.14309/ajg.0000000000001538
- Maret-Ouda J, Wahlin K, El-Serag HB, Lagergren J. Association Between Laparoscopic Antireflux Surgery and Recurrence of Gastroesophageal Reflux. JAMA. 2017 Sep 12;318(10):939-946. https://doi.org/10.1001/jama.2017.10981
- Campos V, Palacio DS, Glina F, Tustumi F, Bernardo WM, Sousa AV. Laparoscopic treatment of giant hiatal hernia with or without mesh reinforcement: A systematic review and meta-analysis. Int J Surg. 2020 May;77:97-104. https://doi.org/10.1016/j.ijsu.2020.02.036
- Han S, Low DE. Laparoscopic antireflux surgery: are old questions answered? Should it be used conjoined with endoscopic therapy for barrett’s esophagus? Arq Bras Cir Dig. 2022 Jun 24;35:e1664. https://doi.org/10.1590/0102-672020210002e1664
- Kohn GP, Price RR, DeMeester SR, Zehetner J, Muensterer OJ, Awad Z, Mittal SK, Richardson WS, Stefanidis D, Fanelli RD; SAGES Guidelines Committee. Guidelines for the management of hiatal hernia. Surg Endosc. 2013 Dec;27(12):4409-28. https://doi.org/10.1007/s00464-013-3173-3
- Dallemagne B, Arenas Sanchez M, Francart D, Perretta S, Weerts J, Markiewicz S, Jehaes C. Long-term results after laparoscopic reoperation for failed antireflux procedures. Br J Surg. 2011 Nov;98(11):1581-7. https://doi.org/10.1002/bjs.7590
- Frantzides CT, Madan AK, Carlson MA, Zeni TM, Zografakis JG, Moore RM, Meiselman M, Luu M, Ayiomamitis GD. Laparoscopic revision of failed fundoplication and hiatal herniorraphy. J Laparoendosc Adv Surg Tech A. 2009 Apr;19(2):135-9. https://doi.org/10.1089/lap.2008.0245
- Little AG, Ferguson MK, Skinner DB. Reoperation for failed antireflux operations. J Thorac Cardiovasc Surg. 1986 Apr;91(4):511-7.
- Patti MG, Allaix ME, Fisichella PM. Analysis of the Causes of Failed Antireflux Surgery and the Principles of Treatment: A Review. JAMA Surg. 2015 Jun;150(6):585-90. https://doi.org/10.1001/jamasurg.2014.3859
- Horgan S, Pohl D, Bogetti D, Eubanks T, Pellegrini C. Failed antireflux surgery: what have we learned from reoperations? Arch Surg. 1999 Aug;134(8):809-15; discussion 815-7. https://doi.org/10.1001/archsurg.134.8.809
- Little AG, Ferguson MK, Skinner DB. Reoperation for failed antireflux operations. J Thorac Cardiovasc Surg. 1986 Apr;91(4):511-517.
- Анищенко В. В., Разумахина М. С., Платонов П. А., Ковган Ю. М. Анализ отдаленных результатов фундопликации при рефлюксной болезни в сочетании и без грыжи пищеводного отверстия диафрагмы. Science and world. 2014;11(15):129-131.
- Галлямов Э. А., Луцевич О. Э., Кубышкин В. А., Ерин С. А., Агапов М. А., Преснов К. С., Бусырев Ю. Б., Галлямов Э. Э., Гололобов Г. Ю., Зрянин А. М., Старков Г. А., Толстых М. П. Повторные лапароскопические операции при рецидиве гастроэзофагеальной рефлюксной болезни и грыжи пищеводного отверстия диафрагмы. Хирургия. Журнал им. Н. И. Пирогова. 2019;(2):26-31.
- Campos V, Palacio DS, Glina F, Tustumi F, et al. Laparoscopic treatment of giant hiatal hernia with or without mesh reinforcement: A systematic review and meta-analysis. Int J Surg. 2020 May;77:97-104. https://doi.org/10.1016/j.ijsu.2020.02.036


