Лапароскопическая органосохраняющая хирургия в лечении миомы матки
Автор: Андреева Ю.Е., Вторенко В.И., Дымковец В.П., Ванюков А.Е., Торчинов А.М., Цахилова С.Г., Бегизова А.М.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 3 (49), 2016 года.
Бесплатный доступ
Вопрос формирования качественного рубца на матке при лапароскопической миомэктомии сохраняет свою актуальность в настоящее время, особенно для пациенток, планирующих беременность. Ряд технических при емов, описанных в статье, позволяет выполнить лапароскопическую миомэктомию без кровопотери, в условиях хорошей визуализации, с формированием над ежного рубца на матке и профилактикой развитие спаечного процесса. Данная методика позволяет нивелировать ограничения лапароскопического доступа при миомэктомии.
Миома матки, лапароскопическая миомэктомия, окклюзия внутренних подвздошных артерий
Короткий адрес: https://sciup.org/142211257
IDR: 142211257 | УДК: 616-035.1
Laparoscopic-sparing surgery in the treatment of uterine fibroids
The issue of formation of quality of the scar on the uterus after laparoscopic myomectomy remains relevant today, especially for patients who are planning a pregnancy. A number of techniques described in this article allows you to perform laparoscopic myomectomy without bleeding, in good visualization, with the formation of a reliable scar on the uterus and prevent the development of adhesions. This technique allows you to reverse the restrictions laparoscopic myomectomy with.
Текст научной статьи Лапароскопическая органосохраняющая хирургия в лечении миомы матки
Миомэктомия признана основным методом лечения пациенток репродуктивного возраста с миомой матки. В настоящее время противопоказаниями к выполнению органосохраняющей операции на матке являются наличие онкологического процесса репродуктивной системы и гнойновоспалительные процессы в брюшной полости.
По данным Федеральной службы государственной статистики РФ, в нашей стране за год проводится около 130 тыс. гистерэктомий, причем ведущее показание для их выполнения-миома матки [1].
Эндоскопия сегодня широко востребована в гинекологической практике. За три последних десятилетия был накоплен колоссальный мировой опыт использования лапароскопического доступа для осуществления оперативных вмешательств на органах малого таза у женщин, который продемонстрировал техническую возможность проведе- ния операций любой сложности и определил место лапароскопии как основной методики лечения широкого спектра гинекологических заболеваний [2 – 4]. Однако, если для радикальных операций на матке эндоскопический доступ принимается в современной гинекологии безоговорочно, то вопрос о выборе доступа в органосохраняющей хирургии матки до сих пор оста ется дискуссионным [2, 3, 5]. Безусловно для миомэктомии субсерозных узлов выбором доступа является лапароскопия. Гистерорезекция субмукозной миомы по современным представлениям безопасна и высокоэффетивна при размерах узла до 5 см [7 – 10]. Наиболее дискуссионным оста ется вопрос о выборе оперативного доступа при интерстициальном расположении узлов. Многими авторами подчеркиваются несомненные преимущества лапароскопического доступа перед лапоротомным [2, 3]. К ним относятся: минимальная травма передней брюшной стенки, уменьшение послеоперационного болевого синдрома, меньшая вероятность развития спаечного
процесса, более короткие сроки пребывания в стационаре и послеоперационной реабилитации, лучший косметический эффект.
Несомненно, лапароскопический доступ позволил минимизировать операционную травму и улучшить результаты лечения. Однако дискуссионными остаются вопросы функционального состояние рубца на матке после лапароскопической миомэктомии. Ряд авторов подч еркивают, что эндоскопический доступ является предпочтительным при выполнении миомэктомий; однако ключевым моментом является над ежность в восстановлении целостности стенки матки, что имеет важное значение для последующего вынашивания беременности и профилактики акушерских осложнений [2].
Проблема заключается в том, что при лапароскопическом удалении «трудных» узлов хирург сталкивается с определ енными ограничениями [11]. К «трудным» узлам относятся узлы больших размеров (более 6-7 см), с интрамуральным и центрипетальным расположением по задней стенке и в области ребра матки, а также интралигаментар-ные узлы. В таких случаях при выполнении лапароскопической миомэктомии высок риск кровотечения из ложа узла, что может привести к большой кровопотере и конверсии на лапаротомию. В условиях кровотечения плохо визуализируются границы узла и слои стенки матки, высок риск вскрытия полости матки и иссечения участка эндометрия. В такой ситуации хирург чрезмерно активно использует коагуляцию, что приводит к ожогу тканей и, как следствие, к плохому качеству рубца на матке. Затрудненная визуализация мешает полноценному сопоставлению сло ев и над еж-ному ушиванию раны, что также ухудшает качество рубца.
Можно выделить три основные направления на пути оптимизации методов лапароскопической миомэктомии: выбор вида и минимизация воздействия хирургической энергии; усовершенствование техники наложения эндоскопического шва на дефект стенки матки после энуклеации миоматозного узла; использование и совершенствование дополнительных методик, способствующих снижению объема интраоперационной кровопотери [12].
Наряду с модификацией методики ушивания дефекта миометрия после энуклеации узла были предложены превентивные методики, способствующие снижению кровопотери: введение окситоцина во время лапароскопической МЭ, инфильтративное введение адреналина перинодуляр-но. С этой же целью использовался вазопрессин в низких концентрациях, который помимо снижения кровопотери, позволял уменьшить частоту использования электрокоагуляции, способствуя сохранению окружающего миометрия [13]. Тем не менее, использование вазоконстрикторов может повышать вероятность возникновения поздних кровотечений, формирования гематом в области послеоперационных швов. Влияние на другие органы и системы также оста ется нежелательным и опасным при применении данных препаратов. С целью минимизации интраоперационной кровопотери при выполнении МЭ, рядом авторов были предложены дополнительные методики, направленные на уменьшение перфузии матки перед непосредственным удалением узлов без введения вазоконстрикторов. В качестве первого этапа перед лапароскопической МЭ, предлагалось использовать эмболизацию маточных артерий (ЭМА), которая позволяет выполнять хирургический этап на бескровном миометрии [14]. Стоит отметить, что ЭМА рассматривается и как альтернативный метод хирургическому лечению. Между тем, опубликованы данные I.T. Manyonda и соавт., где отмечается сравнимая эффективность лапароскопической МЭ и ЭМА, и если ЭМА сопряжена с меньшим процентом осложнений, то вероятность рецидива ММ значимо выше [15]. Помимо введения эмболов в сосудистое русло, при котором наступает необратимая окклюзия, разработаны методы по созданию временной окклюзии в бассейне маточной артерии непосредственно перед МЭ.
Материалы и методы
В своей работе мы успешно применяем запатентованную авторскую методику лапароскопической миомэктомии с временной окклюзией внутренних подвздошных артерий (патент на изобретение № 2407467; авторы патента Пучков К.В., Андреева Ю.Е., Мельников А.Л., Васин Р.В.)
Техника операции: Операция проводится под интубационным наркозом. Пациентка располагается на спине с раз-вед енными и полусогнутыми в коленных суставах ногами. Необходимо, чтобы нижняя часть ягодиц находилась за пределами операционного стола. Это условие очень важно для создания возможности свободной манипуляцией маткой. В мочевой пузырь устанавливается катетер Фоллея. Обрабатываются оба операционных поля: абдоминальное и влагалищное. Шейка матки фиксируется пулевыми щипцами, выполняется гистерометрия, расширение цервикального канала до № 9 Гегара. Маточный манипулятор вводится в полость матки ввинчиванием и одновременным проталкиванием до возникновения сопротивления. Использование маточного манипулятора очень важно: его система рычагов позволяет перемещать матку в любое удобное положение. Это облегчает выполнение операции и сокращает е е продолжительность, способствует профилактике осложнений. Изготовление манипулятора из материалов, не проводящих электрическую энергию, исключает риск возникновения электрической дуги. После введения манипулятора пулевые щипцы и зеркала из влагалища удаляют.
Выбор троакаров, мест их расположения зависит от физических данных оператора, используемой техники, размеров матки, вероятности спаечного процесса в брюшной полости. Первый троакар (для оптики) устанавливается в параумбиликальной области. Предварительно созда ется
пневмоперитонеум с использованием иглы Вереша. Ещ е 2 10-мм троакара вврдятся в точках Мак Бурнея. При предполагаемом спаечном процессе лучше ввести иглу Вереша в области левого подреберья ( вне зоны сосудов-большая безопасность; самая маленькая вероятность спайкообра-зования в этой области). Необходимо иметь возможность электромеханической морцелляции.
Первым этапом операции является временная окклюзия внутренних подвздошных артерий. Почему мы выполняем окклюзию именно внутренней подвздошной артерии, а не другой, например, маточной? Во-первых, доступ к самой маточной артерии, зачастую, при больших миомах бывает невозможен. Во-вторых, учитывая вариабельность деления внутренней подвздошной артерии и наличие множественных анастомозов между ветвями е е бассейна, выгоднее окклюзировать внутреннюю подвздошную артерию сразу после бифуркации. При этом необходимо понимать, что при этом никогда не происходит полное прекращение кровотока в матке. Кровоток сохраняется за сч ет анастомозирования с бассейном яичниковой артерии и наружной подвздошной артерии, но он теряет свой пульсирующий характер, приближаясь по характеристикам к венозному. Для выполнения этого этапа сначала необходимо определить область бифуркации общей подвздошной артерии, проследить ход внутренней подвздошной артерии и мочеточника. Затем вскрывается брюшина над внутренней подвздошной артерией на протяжении 2–3см и артерия выделяется при помощи диссекции тканей. При выделении артерии необходимо выполнять диссекцию с помощью инструмента, введ енного в троакар на стороне данной артерии. В противном случае, кончиками инструментов можно повредить наружную подвздошную вену, которая всегда интимно прилежит в этой зоне к артерии. Движения инструмента в этой области должны быть очень деликатными, что позволит избежать осложнений. На выделенную артерию накладывается мягкий сосудистый зажим «DeBakey», введ енный в брюшную полость с помощью зажима «Endoclinch». Зажимы накладываются с двух сторон. Следующим этапом выполняется разрез миометрия над узлом миомы с помощью ультразвуковой или монополярной энергии. Узел миомы захватывается двумя мощными 10-мм зажимами и вылущивается из окружающего миометрия. На этом этапе мы вводим внутривенно окситоцин; сокращающаяся матка «выталкивает» узел из окружающих тканей, помогая его выделению. Рана на матке ушивается в несколько рядов, прич ем мышечно-мышечные швы ориентируются вдоль раны, а серозомышечные швы-перпендикулярно ране. Ушивается матка рассасывающейся монофиламентной нитью (Монокрил 1) или самозатягива-ющейся нитью «V-loc». Узлы миомы удаляются из брюшной полости с помощью морцелляции. Матка и придатки укрываются противоспаечными барьерами «Мезогель» или «КолГара». Сосудистые зажимы снимаются.
Для тех случаев, когда интраоперационный доступ к внутренним подвздошным артериям затрудн ен, нами была предложена методика лапароскопической миомэктомии с предварительным ангиохирургическим баллонированием внутренних подвздошных артерий. При этом пациентка предварительно доставляется в ангиохирургическую операционную, где производится установка баллонных катетеров во внутренние подвздошные артерии с двух сторон, баллоны раздуваются и перекрывают кровоток. Пациентка переводится в операционную, где выполняется миомэктомия лапароскопическим доступом, в конце операции баллонные катетеры удаляются, и кровоток восстанавливается, после чего дополнительно контролируется гемостаз.
Результаты
По данной методике в гинекологическом отделении ГКБ №52 с 2014г. по 2016г.прооперировано 10 пациенток. Всем пациенткам выполнялось стандартное предоперационное обследование, включая УЗИ и МРТ малого таза (в 30% случаев). МРТ используется для более точной топографии узлов и при подозрении на узловую форму аденомиоза по данным УЗИ. В стандарт предоперационного обследования входит получение информации о состоянии эндометрия (аспирационная биопсия эндометрия или гистологическое исследование соскобов из полости матки и цервикального канала). Обязательными являются также кольпоскопия и цитологическое исследование эндо- и экзоцервикса.
Количество узлов миомы – от 1 до 5; размер узлов – от 3 до 9 см. Во всех случаях отмечался центрипетальный рост узлов. Кровопотеря до 150 мл. Продолжительность операции 60–90 мин. Продолжительность госпитализации 3–4 дня. Всем пациенткам назначалась антибактериальная терапия в течение 7 дней с интраоперационным введением первой дозы и утеротоническая терапия во время пребывания в стационаре. Болевой синдром купировался назначением НПВС в течение 2–3 суток. В течение первых двух суток после операции отмечалось повышение температуры тела до 38 ° С, далее - субфебрильные цифры до 7-8 суток. До 7-10 дней пациентки отмечали скудные кровянистые выделения из половых путей. После получения результатов гистологического исследования операционного материала всем пациенткам назначался при ем мини-дозированных контрацептивных препаратов на протяжении 4–6 мес. В одном случае применялась методика лапароскопической миомэктомии с предварительным баллонированием внутренних подвздошных артерий.
Заключение
Вышеописанная методика позволяет лапароскопическим доступом выполнять миомэктомию «трудных» узлов без значимой кровопотери, с формированием состоятельного рубца на матке, что необходимо для последующей беременности и родов.
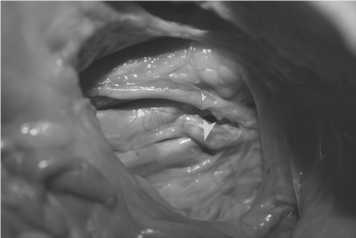
Рис. 1. Препарированные подвздошные сосуды и мочеточник слева (голубой стрелкой выделена внутренняя подвздошная артерия; под ней-наружная подвздошная вена, белой маленькой стрелкой выделен мочеточник)
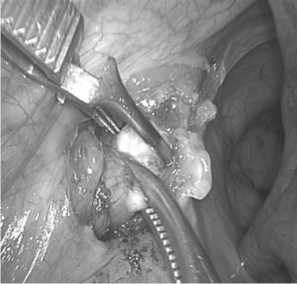
Рис. 2. Наложение сосудистого зажима « DeBakey» на выделенную внутреннюю подвздошную артерию слева
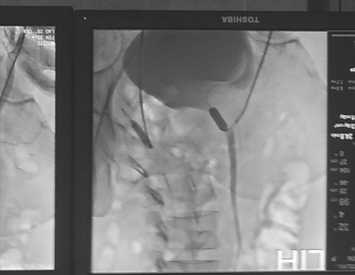
Рис. 3. Балонная окклюзия внутренних подвздошных артерий
Список литературы Лапароскопическая органосохраняющая хирургия в лечении миомы матки
- Подзолкова Н.М., Коренная В.В., Колода Ю.А. Миома матки М. Гэотр-Медиа 2015 150с
- Сухих Г.Т., Адамян Л.В. Новые технологии в диагностике и лечении гинекологических заболеваний, материалы 23 Международного конгресса с курсом эндоскопии, 2010г 304стр.
- Mojgan Mohammadi, Mark Н. Glasser Leiomyomas: Minimally Invasive Approaches to Myomectomy//Prevention and Management of Laparoendoscopic Surgical Complication SLS, Society of Laparoendoscopic Surgeons Aug 10, 2012 1562 Pages
- Сазонова Е.О. Осложнения лапароскопических операций на органах малого таза//автореф.диссер..докт. мед. наук М. 2008г. 235 стр.
- Каппушева Л.М., Бреусенко В.Г., Анисимова С.А. Трансцервикальная миомэктомия//Акушерство и гинекология. 2000. № 2. С. 29-34
- Савельева Г.М., Бреусенко В.Г., Каппушева Л.М. Гистероскопия. М.: ГЭОТАР, 2001
- новикова Е.Г., Пронин С.М. Руководство по гистерорезек-тоскопии в онкогинекологии. Диагностика и хирургия. М.:ООО «Медицинское информационное агентство», 2009. 80с.
- Берлев И.В., Кузнецов С.В., Иванов А.С. Лапароскопическая миомэктомия. Клиническая эффективность и результаты лечения у женщин репродуктивного возраста//Журн. акушерства и женских болезней. 2009. Т. 58.(выпуск 5). С. 110
- Mencaglia L., Cavalcanti de Albuquerque Neto L., Arias Alvarez R.A. Manual of Hysteroscopy-Diagnoctic, Operative and Office Hysteroscopy 2011 Endo:Press Tuttlingen 127p
- Rossetti A., Sizzi O., Soranna L. et al. Long-term results of laparoscopic myomectomy: recurrence rate in comparison with abdominal myomectomy. Human Reprod 2001; 16: 4: 770-774.
- О^ Istre Management of symptomatic fibroids: conservative surgical treatment modalities other than abdominal or laparoscopic myomectomy//Best Practice & Research Clinical Obstetrics and Gynaecology Vol. 22, No. 4, pp. 735-747, 2008
- Савицкий Г.А., ниаури д.А., волков н.н. Минилапаротомия в современной хирургии матки СПб.: Морская карта, 2004г. 256 с.
- Савицкий Г.А., волков н.н. Миомэктомия: современные технологии//Актуальные вопросы физиологии и патологии репродуктивной функции женщин. Спб., 1999. С. 390-394
- Rossetti A., Sizzi O., Soranna L. et al. Long-term results of laparoscopic myomectomy: recurrence rate in comparison with abdominal myomectomy. Human Reprod 2001; 16: 4: 770-774.


