Лапароскопический доступ при позадилонной аденомэктомии в сравнении с традиционным - малый опыт на фоне большого
Автор: Котов С.В., Мамаев И.Э., Юсуфов А.Г., Гуспанов Р.И., Перов Р.А., Беломытцев С.В., Пронкин Е.А., Глинин К.И., Макарченко А.В., Попова М.Б., Шоайдаров М.А., Ахмедов К.К., Сероухов А.Ю.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Андрология
Статья в выпуске: 1, 2018 года.
Бесплатный доступ
Введение. Лапароскопическая модификация аденомэктомии предстательной железы (ПЖ) представляется достойной малоинвазивной альтернативой открытого хирургического лечения доброкачественной гиперплазии предстательной железы (ДГПЖ) больших размеров. Известно, что в большинстве случаев кривая обучения лапароскопической операции более длительна по отношению к ее традиционному аналогу. В работе сопоставлен сравнительно небольшой опыт лапароскопических аденомэктомий с методикой, отработанной на большом материале. Такое сравнение способно продемонстрировать основные преимущества и недостатки нового подхода, а также целесообразность широкого внедрения его в стационарах, где стандартная техника является рутинной. Материалы и методы. В исследование включено 424 пациента с объемом ПЖ более 80мл. 24 пациентам, вошедшим в I группу, выполнена лапароскопическая аденомэктомия. 400 пациентам II группа) выполнена позадилонная аденомэктомия. Произведена сравнительная оценка по следующим параметрам: продолжительность вмешательства, кровопотеря, сроки восстановления мочеиспускания, максимальная скорость потока мочи после операции. Результаты. Не отмечено достоверной разницы между группами пациентов по максимальной скорости мочеиспускания, кровопотере и срокам восстановления мочеиспускания. Средняя продолжительность вмешательства была достоверно выше в группе лапароскопической аденомэктомии. Обсуждение. Лапароскопическая аденомэктомия является эффективной методикой хирургического лечения ДГПЖ больших размеров. К недостаткам можно отнести большее время операции, длительную кривую обучения и материальные расходы. Заключение. По частоте и тяжести осложнений результаты открытой и лапароскопической аденомэктомии сопоставимы. Данный метод может быть применим в рутинной урологической практике у пациентов с большими объемами ПЖ с целью минимизации операционной травмы и сокращения сроков реабилитации.
Доброкачественная гиперплазия предстательной железы, позадилонная аденомэктомия, лапароскопическая аденомэктомия
Короткий адрес: https://sciup.org/142213117
IDR: 142213117
Laparoscopic access in retropubic adenomectomy versus traditional access. Little experience amidst a considerable one
Introduction. Infravesicular obstruction accounted by benign prostatic hyperplasia (BPH) is still among the most common diseases in senior men. Nowadays, transurethral resection is commonly used as a surgical intervention in treating patients with BPH, whose prostate volume is up to 80 cc. Open adenomectomy is a standard for treating patients with large size prostate adenoma. However, the main disadvantages of this method are severe surgical trauma and a high percentage of traumatic complications. Laparoscopic modification of adenomectomy is an adequate minimally invasive alternative to open surgical treatment of BPH. In case of large volumes of the prostate, the choice for adenomectomy is always upon the decision of a surgeon. The aim of our study was to evaluate the results of laparoscopic and open retropubic adenomectomy.
Текст научной статьи Лапароскопический доступ при позадилонной аденомэктомии в сравнении с традиционным - малый опыт на фоне большого
Попова М.Б. – врач-уролог отделения урологии ГКБ им. В.М.Буянова
Шоайдаров М.А. – врач-уролог отделения урологии ГКБ им. В.М.Буянова
Ахмедов К.К. – врач-уролог отделения урологии ГКБ им. В.М.Буянова
Сероухов А.Ю. – врач-уролог Tamale teaching hospital, Ghana
Несмотря на развитие малоинвазивных методов лечения, таких как трансуретральная хирургия с применением биполярной резекции или энуклеации аденомотозных узлов предстательной железы (ПЖ) при помощи гольмиевого лазера, ПлАЭ по-прежнему широко используется и остается предпочтительной при объеме ПЖ более 80-100 см3 [2]. Трансуретральная энуклеация гиперплазированных узлов ПЖ гольмиевым лазером имеет результаты схожие с открытой операцией, од- нако в настоящее время доступность лазерного оборудования в стационарах ограничена из-за его высокой стоимости. Совершенствование технологий и оперативной техники трансуретральной резекции привело к расширению показаний к операциям при больших объемах ПЖ, но вместе с этим – и к увеличению числа «незавершенных» резекций ПЖ и повторных вмешательств.
M.B. Mariano и соавт. выполнили первую лапароскопическую адено-мэктомию (ЛА) в 2002 году [3]. Данная методика воспроизвела этапы открытой ПлАЭ с привнесением преимуществ лапароскопического доступа. Согласно литературным источникам удовлетворительные результаты также получены при проведении операции лапароскопическим доступом с применением робот-ассистированной техники и посредством однопортового доступа [4-7]. Однако лишь в единичных публикациях приводится сравнение лапароскопической адено-мэктомии (ЛА) с традиционной ПлАЭ.
В настоящей статье приведена сравнительная характеристика ПлАЭ и чрез- и внебрюшинной ЛА, выполненных в Университетской клинике РНИМУ им. Н.И. Пирогова на базе урологических отделений ГКБ № 1 им. Н.И. Пирогова и ГКБ им. В.М. Буянова ДЗМ г.Москвы в период с 2014 по 2017 гг.
МАТЕРИАЛЫ И МЕТОДЫ
Использовались стандартные показания к хирургическому лечению ДГПЖ, основывающиеся на данных предоперационного исследования. Последнее включало в себя: анкетирование по шкале IPSS (International Prostatic Symptom Score); оценку качества жизни QoL (Quality of Life); определение уровня простатспецифическо-го антигена (ПСА), проведение стандартных лабораторных исследований крови и мочи, измерение объема ПЖ с помощью ультразвукового исследования; проведение урофлоуметрии; измерение объема остаточной мочи; проведение, по показаниям, уретроци-стоскопии для оценки сопутствующих заболеваний (стриктуры уретры, опухоли, камни и дивертикулы мочевого пузыря).
В первую (I) группу вошли 24 пациента, которым выполнена лапароскопическая аденомэктомия (ЛАЭ). Во вторую (II) группу вошли 400 пациентов, которым выполнена позадилон-ная аденомэктомия. Средние доопера-ционные значения в I и II группах составили: возраст мужчин 64,8 vs 70.5 лет; объем ПЖ 117 vs 120 cм3; Qmax 12.4 vs 8.3 мл/с, IPSS 23 vs 21.6 баллов; QoL 4.5 vs 4.5 баллов. В группе I оперативные вмешательства выполнялись через трансперитонеальный (12 пациентов) и внебрюшинный (12 пациентов) доступы. Техника ПлАЭ давно известна и хорошо описана, в связи с чем остановимся только на деталях лапароскопического варианта операции.
Для статистической обработки все данные о пациентах и результатах лечения внесены в базу данных, созданную на основе электронных таблиц Excel. Статистический анализ полученных результатов проводили с использованием известных статистических методов с применением блока программ Statistica SPPS 13.0 для Windows.
ТЕХНИКА
ЛАПАРОСКОПИЧЕСКОЙ ОПЕРАЦИИ
Пациент под общей анестезией располагается на операционном столе в положении Тренделенбурга под углом до 10 градусов. Устанавливается уретральный катетер Фолея. При вне-брюшинной методике выполняется разрез 2 см по средней линии на 1 см ниже пупка. После вскрытия переднего листка апоневроза и отведения прямой мышцы живота выполняется пальцевая диссекция для доступа к Ретциеву пространству. Брюшина смещается краниально. Затем в направлении лона вводится баллон-диссектор, в который инсуффлиру-ется до 800 мл газа под визуальным контролем. После создания рабочего пространства баллон-диссектор удаляется. Расстановка троакаров соответствует таковой при лапароскопической простатэктомии и схематично представлена ниже (рис. 1).
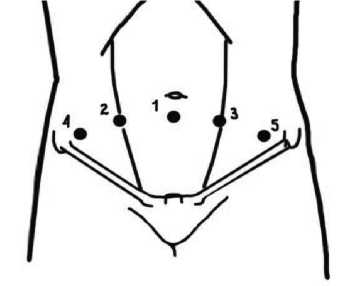
Рис. 1. Расположение троакаров при выполнении лапароскопической аденомэктомии: 1, 2 – троакары 10мм, 3, 4, 5 – троакары 5 мм
Простатическая капсула рассекается по передней поверхности на 5 мм каудальнее шейки мочевого пузыря при помощи монополярной коагуляции поперечным разрезом. Выполняется диссекция аденоматозных узлов по передней и латеральным поверхностям (рис. 2). Вентральная полуокружность уретры на границе с шейкой мочевого пузыря (МП) рассекается поперечно. Выделяется средняя доля ПЖ (при ее наличии). Осуществ-
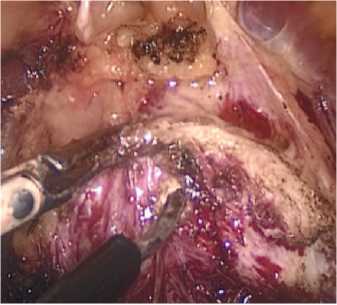
Рис. 2. Поперечный разрез капсулы предстательной железы и выделение передней поверхности аденоматозного узла ляется захват средней доли щипцами и тракция ее кпереди (рис. 3). Формируется дугообразный разрез слизистой в проекции шейки мочевого пузыря под средней долей аденомы между 8 и 4 часами условного циферблата.
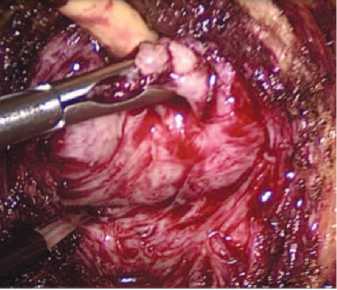
Рис. 3. Тракция средней доли предстательной железы и выделение задней поверхности аденоматозного узла
Разрез углубляется в пределах слоя между аденоматозными узлами и простатической капсулой. Выполняется последовательное выделение долей аденомы по направлению к верхушке железы. Следует дозировано применять коагуляцию на этапе диссекции аденомы в апикальной части с целью предотвращения повреждающего действия на сфинктер уретры. Удаленные аденоматозные узлы погружаются в мешок-экстрактор, который затем извлекается через продолженный разрез в проекции 10 мм порта. Достигается окончательный гемостаз посредством моно-и биполярной коагуляции, проводится ревизия ложа аденомы на предмет резидуальной ткани. В мочевой пузырь устанавливается 3-х ходовый уретральный катетер Фолея Сh 1822, баллон наполняется на 30-40 мл (рис. 4). Разрез капсулы ПЖ по передней поверхности ушивается
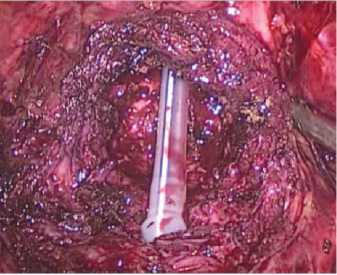
Рис. 4. Установка уретрального катетера непрерывным швом нитью V-loc 2/0 (рис. 5).
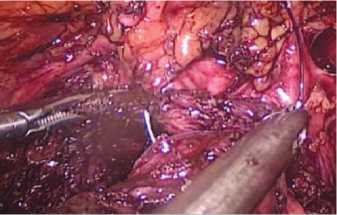
Рис.5. Ушивание капсулы предстательной железы
Мочевой пузырь наполняется 150,0 мл физиологического раствора для оценки герметичности швов. Страховой дренаж устанавливается на место одного из латеральных троакаров.
При трансперитонеальной методике после вскрытия париетальной брюшины и диссекции тканей в Рет-циевом пространстве мочевой пузырь отводится дорзально. Дальнейшие этапы операции аналогичны описанным выше.
РЕЗУЛЬТАТЫ
При сравнении периоперационных параметров между двумя группами пациентов не выявлено значимых различий по возрасту, объему ПЖ, суммой баллов IPSS и показателем QoL. В группе ЛАЭ конверсии к открытой операции не потребовалось ни в одном случае. Отмечено 3 осложнения: у одного пациента развилась динамическая кишечная непроходимость, разрешенная консервативно; в другом случае развился психоз на фоне сосудистой патологии головного мозга; у третьего пациента имела место ТЭЛА мелких ветвей на 4-е сутки послеоперационного периода. Гемотрансфузия не потребовалась ни в одном случае. Летальных исходов не было.
Интраоперационная кровопотеря в I группе составила 350 мл (210-420), во II– 235 мл (0-1500). Сред-
Таблица 1. Периоперационные характеристики пациентов
Параметры ЛАЭ ПлАЭ р
|
Средний возраст пациентов, лет |
70,5 |
64,8 |
> 0,05 |
|
|
Объем предстательной железы до операции, мл |
120 |
117 |
> 0,05 |
|
|
Qmax, мл/с |
До операции Через 3 месяца после операции |
8,3 21,9 |
12,4 22,1 |
> 0,05 |
|
Сроки дренирования мочевого пузыря, дни |
7,4 |
5,2 |
> 0,05 |
|
|
Объем кровопотери, мл |
350 |
235 |
> 0,05 |
|
|
Средняя продолжительность вмешательства, мин |
183 |
101,2 |
> 0,05 |
|
няя продолжительность дренирования мочевого пузыря в I группе была 7,4 дня, в II группе – 5,2 дня. Улучшение послеоперационных значений Qmax было отмечено в обеих группах. Средний показатель Qmax через 3 месяца после операции в группе I равнялся 22,1±5,04 мл/сек, в группе II – 21,9 (7-53,2) мл/сек (табл. 1).
ОБСУЖДЕНИЕ
Согласно данным литературы, сравнительные исследования лапароскопической и открытой аденомэкто-мии показывают преимущества лапароскопии при том, что оба оперативных метода сопоставимы по функциональным результатам [8]. Вместе с тем, имеется незначительное число публикаций по этой проблеме с небольшим числом пациентов. Многие исследования не являются сравнительными и носят описательный характер. В большинстве статей при оценке ЛАЭ констатируется низкий процент кровотечений и гемотрансфузий, короткое время послеоперационной ирригации и дренирования мочевого пузыря, короткий срок пребывания пациентов в стационаре, низкая потребность в анальгезии, непродолжительный период реабилитации, а также возможность выполнить пациентам цистоли-тоэктракцию, герниопластику и ди-вертикулэктомию при наличии показаний.
Применение лапароскопического оборудования позволяет значительно улучшить визуализацию операционного поля в сравнении с открытой хирургией. По мнению F. Porpiglia и соавт., визуализация уретры является одним из самых больших преимуществ лапароскопической техники, поскольку ее идентификация обеспечивает точный срез, благодаря чему минимизируется риск повреждения сфинктера мочевого пузыря и последующего раз-вития недержания мочи у пациента [9-10].
Уменьшение интраоперационной кровопотери при ЛАЭ достигается использование прецизионной техники энуклеации и селективной коагуляцией капсулярных кровеносных сосудов, а также спонтанным тромбообразованием в венах под влиянием СО 2 . Данные факторы способствуют уменьшению продолжительности послеоперационной ирригации мочевого пузыря [9,11].
Осложнения, которые могут возникать при открытой операции (се-ромы, абсцессы), главным образом у пациентов с цистостомическими свищами и инфекцией мочевых путей, не встречаются в лапароскопической хирургии [7,12].
К недостаткам лапароскопического доступа можно отнести большее время операции, длительную кривую обучения и материальные расходы. Время лапароскопической операции всегда больше по сравнению с открытым оперативным вмешательством и зависит от опыта хирурга. Эти выводы нашли подтверждение и в нашем исследовании. Установлено, что средние результаты по объему кровопотери и срокам восстановления самостоятельного мочеиспускания в группе лапароскопической аденомэктомии, на опыте 24 операций несколько уступают таковым в группе открытого вмешательства.
Ограничения нашего исследования заключаются в небольшом числе пациентов, ввиду чего невозможно сделать достоверные выводы. В ситуации, когда различия в объективных результатах использованных методик минимальны, в дальнейшем целесообразно провести сравнительную оценку и по субъективным показателям используя, к примеру, оценку пациентами уровня послеоперационного болевого синдрома. Мы убеждены, что необходимы проспективные исследования с большим числом пациентов, способные определить роль ЛА в клинической практике.
ЗАКЛЮЧЕНИЕ
Резюме:
Введение. Лапароскопическая модификация аденомэктомии предстательной железы (ПЖ) представляется достойной малоинвазивной альтернативой открытого хирургического лечения доброкачественной гиперплазии предстательной железы (ДГПЖ) больших размеров. Известно, что в большинстве случаев кривая обучения лапароскопической операции более длительна по отношению к ее традиционному аналогу. В работе сопоставлен сравнительно небольшой опыт лапароскопических аденомэктомий с методикой, отработанной на большом материале. Такое сравнение способно продемонстрировать основные преимущества и недостатки нового подхода, а также целесообразность широкого внедрения его в стационарах, где стандартная техника является рутинной.
Материалы и методы. В исследование включено 424 пациента с объемом ПЖ более 80мл. 24 пациентам, вошедшим в I группу, выполнена лапароскопическая аденомэктомия. 400 пациентам II группа) выполнена позадилонная аденомэктомия. Произведена сравнительная оценка по следующим параметрам: продолжительность вмешательства, кровопотеря, сроки восстановления мочеиспускания, максимальная скорость потока мочи после операции.
Результаты. Не отмечено достоверной разницы между группами пациентов по максимальной скорости мочеиспускания, кровопотере и срокам восстановления мочеиспускания. Средняя продолжительность вмешательства была достоверно выше в группе лапароскопической аденомэктомии.
Обсуждение. Лапароскопическая аденомэктомия является эффективной методикой хирургического лечения ДГПЖ больших размеров. К недостаткам можно отнести большее время операции, длительную кривую обучения и материальные расходы.
Заключение. По частоте и тяжести осложнений результаты открытой и лапароскопической аденомэктомии сопоставимы. Данный метод может быть применим в рутинной урологической практике у пациентов с большими объемами ПЖ с целью минимизации операционной травмы и сокращения сроков реабилитации.
Список литературы Лапароскопический доступ при позадилонной аденомэктомии в сравнении с традиционным - малый опыт на фоне большого
- Millin TJ. Retropubic prostatectomy: a new extravesical technique: report on 20 cases. Lancet 1945;11:693 DOI: 10.1016/S0022-5347(02)80316-0
- McVary KT, Roehrborn GC, Avins AL, Barry Mj, Bruskewitz RC, Donnell RF, et al. AUA guidelines: management of benign prostatic hyperplasia (BPH) revised. American Urological Association Education and Research Inc.; 2010. Доступно по: http://www.auanet.org/guidelines/benign-pro-static-hyperplasia-(2010-reviewed-and-validity-confirmed-2014). Ссылка активна на 03.03.2018.
- Mariano MB, Graziottin TM, Tefilli MV. Laparoscopic prostatectomy with vascular control for benign prostatic hyperplasia. J Urol 2002;167:2528-9 DOI: 10.1097/00005392-200206000-00046
- R. van Velthoven, Peltier A, Laguna MP, Piechaud T. Laparoscopic extraperitoneal adenomectomy (Millin): pilot study on feasibility. Eur Urol 2004;45:103-9 DOI: 10.1016/s0302-2838(03)00420-2
- Sotelo R, Spaliviero M, Garcia-Segui A, Hasan W, Novoa J, Desai MM, et al. Laparoscopic retropubic simple prostatectomy. J Urol 2005;173:757-60 DOI: 10.1097/01.ju.0000152651.27143.b0
- Rehman J, Khan SA, Sukkarieh T, Chughtai B, Waltzer WC. Extraperitoneal laparoscopic prostatectomy (adenomectomy) for obstructing benign prostatic hyperplasia: transvesical and transcapsular (Millin) techniques. J Endourol 2005;19:491-6 DOI: 10.1089/end.2005.19.491
- Porpiglia F, Fiori C, Cavallone B, Morra I, Bertolo R, Scarpa RM. Extraperitoneoscopic transcap sular adenomectomy: complications and functional results after at least 1 year of followup. J Urol 2011;185:1668-73 DOI: 10.1016/j.juro.2010.12.047
- Porpiglia F, Terrone C, Renard J, Grande S, Musso F, Cossu M, et al. Transcapsular adenomectomy(Millin): a comparative study, extraperitoneal laparoscopy versus open surgery. Eur Urol 2006;49:120-6 DOI: 10.1016/j.eururo.2007.01.012
- A. Garda-Segui, M. Gascon-Mir. Comparative study between laparoscopic extraperitoneal and open adenomectomy. Actas Urol Esp 2012;36(2):110-116 DOI: 10.1016/j.acuroe.2012.04.008
- McCullough TC, Heldwein FL, Soon SJ, Galiano M, Barret E, Cathelineau X, et al. Laparoscopic versus open simple prostatectomy: an evaluation of morbidity. J Endourol 2009;23: 129-33 DOI: 10.1089/end.2008.0401
- Nianzeng X, Yan Y, Zhang J, Wang J, Tian X, Niu Y, et al. Laparoscopic simple prostatectomy with prostatic urethra preserved for benign prostatic hyperplasia. Chin J Androl 2007;9:19-21 DOI: 10.3978/j.issn.2223-4683.2012.02.03
- Сероухов А.Ю., Пронкин Е.А., Глинин К.И., Мамаев И.Э. Лапароскопическая аденомэктомия (предварительные результаты). Вестник урологии 2016;(1):24-31. doi: 10.1234/XXXX-XXXX-2016-1-24-31.


