Лазерная трипсия: контролируемый разлом мочевых камней
Автор: Стрельцова О.С., Почтин Д.П., Антипов О.Л., Еранов Д.И., Гребенкин Е.В.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Экспериментальная урология
Статья в выпуске: 1, 2018 года.
Бесплатный доступ
Введение. Развитие инфекционно-воспалительных процессов в почках является одним из частых осложнений нефроли-тотрипсии в результате мелкой фрагментации камней, диссеминации бактерий из биопленок инфицированных камней по полостной системе почки. Поиск новых методик дробления камней, предполагающих контролируемую крупнооскольчатую их фрагментацию, позволит не только минимизировать возможное инфицирование мочевой системы, но и предотвратить потерю мелких фрагментов камня, как источник резидуального камнеобразования. Цель - поиск режима лазерной литотрипсии, который обеспечит эффективную фрагментацию почечных конкрементов, исключая их неконтролируемый мелкооскольчатый разлом. Материалы и методы. В серии экспериментов использован лазер на кристалле Ho:YAG с накачкой излучением тулиевого волоконного лазера. Ho:YAG лазер генерировал на длине волны 2097 нм импульсы (длительностью 20-40 нс) с частой повторения, варьируемой от 5 до 40 кГц, при средней мощности до 35 Вт (энергия в импульсах варьировала в пределах 0,5-3,0 мДж), а также лазер на керамике ТтТшОз с накачкой излучением эрбиевого волоконного лазера с рамановским сдвигом длины волны (на 1670 нм). Этот лазер на керамике генерировал в импульсно-периодическом режиме (импульсы длительностью 30-40 нс с частотой повторения, варьируемой в пределах 14-25 кГц) излучение на длине волны 1967 нм (средняя мощность излучения изменялась от 100 мВт до 10 Вт). Оба лазера созданы в ИПФ РАН (Н. Новгород). Измерялось время перфорации камня насквозь (до прохождения лазерного излучения через камень) и контроль полученного канала камня визуально и при микроскопии в проходящем свете. Изучен эффект лазерного дробления 25 камней ех vivo. Результаты. Серией экспериментов выявлено, что оптимальным режимом генерации лазера (на длине волны 2097 нс) для выполнения режима контролируемого разлома камня является частота повторения импульсов 200 - 1000 Гц длительностью 20-30 нс и энергией импульса 45 - 55 мДж. То есть режим лазерной генерации со сравнительно малой импульсной энергией (единицы - десятки мДж), но высокой частотой повторения импульсов (сотни герц - десятки килогерц) позволяет обеспечить деструк цию конкрементов на фрагменты с достаточным для извлечения его через кожух - амплац размером. Время перфорации камня насквозь составило от 2 до 300 секунд и зависело от его плотности, размера по длине и химического состава. Выводы. Вариантом профилактики инфекционно-воспалительного процесса в почке после нефролитотрипсии может стать контролируемая деструкция без разбрасывания содержимого конкрементов по полостной системе почки, что возможно обеспечить подбором режимов лазерного воздействия при контактной литотрипсии.
Литотрипсия, мочекаменная болезнь, лазеры
Короткий адрес: https://sciup.org/142213141
IDR: 142213141
Laser-mediated tripsy: a controlled disintegration of urinary stones
Introduction. The development of infectious/inflammatory processes in kidneys in among the most common complications of nephrolithotripsy due to fragmentation of urinary stones into small particles and dissemination of bacteria from infected stone-derived biofilms into the kidney cavity system. The search for new methods of stone fragmentation implying controlled large comminuted fragmentation will allow not only to minimize possible contamination of the urinary system but also to prevent the loss of small particles of the disintegrated stone, which account for residual lithiasis. Aim. The search for a mode of laser lithotripsy, which will ensure effective fragmentation of kidney concrements excluding their uncontrolled disintegration into small particles. Materials and methods. In a series of experiments we used the Ho:YAG laser with thulium fiber laser pumping. The pulses generated by the Ho:YAG laser had the wavelength of 2097 nm whose duration was 20-40 ns and frequency varied from 5 to 40 kHz; the mean value of power was 35 W (pulse energy varied from 0.5 to 3.0 mJ). We also used the Tm:Lu2O3 ceramic laser with an erbium-pumped laser with the Raman shift at 1670 nm. This ceramic laser was emitting at 1967 nm in a pulsed-periodic regime (the duration and frequency of pulses were 30-40 ns and 14-25 kHz, respectively); mean power values varied from 100 mW to 10 W. Both lasers were created in the Institute of Applied Physics, Russian Academy of Sciences (Nizhny Novgorod). The duration of transverse stone perforation (before the passage of a pulse through the stone) was recorded; the newly formed tunnel was analyzed both visually and using light microscopy. The effect of laser fragmentation on 25 stones ex vivo was studied. Results. In a series of experiments, we have determined that the optimal mode of laser generation at 2097 nm for controlled lithotripsy implies the frequency of pulses from 200 to 1000 Hz and their energy of 45-55 mJ. This means that the mode of laser generation with a relatively low pulse energy (tens of mJ) but high frequency of pulses (hundreds of Hz - tens of kHz) ensures the destruction of concrements into fragments which can be accessed through Amplatz sheath. The duration of transverse perforation was from 2 to 300 seconds and depended on the density, length and chemical composition of the stone. Conclusion. Controlled destruction not followed by dissemination of the stone-derived particles through the kidney cavity could be a solution for the prevention of infectious/inflammatory processes after nephrolithotripsy, which could be achieved by adjusting the mode of laser-mediated contact lithotripsy.
Текст научной статьи Лазерная трипсия: контролируемый разлом мочевых камней
экспериментальная и клиническая урология № 1 2 0 18 энергии импульса от 0,17 до 2,3 мДж получен в 8 случаях из 9 (табл. 1). Микроструктурная плотность этих камней составила от 161 ед. HU до 1566 ед. HU.
Режим работы при длине волны 1967 нм, частоте повторения 15 кГц, энергии импульса 0,4-0,6 мДж оказался не эффективным в 4 случаях из 7. Микроструктурная плотность камней составила от 401ед. HU до 1933 ед. HU.
Визуальный контроль полученного перфоративного канала показал, что трещины на конкрементах отсутствовали. В проходящем свете под микроскопом были выявлены неровности контура каналов, разломы отсутствовали (рис. 2).
ОБСУЖДЕНИЕ
Проблема развития осложнений при эндоскопическом лечении мочекаменной болезни на фоне возросшей антибиотикорезистентности становится все более актуальной. Ведущим способом удаления конкрементов из чашечно-лоханочной системы почки является перкутанная нефролитола-паксия. При этом стандартный размер нефростомического хода– 24-30 Ch. В последние годы наблюдается тенденция к уменьшению доступа до
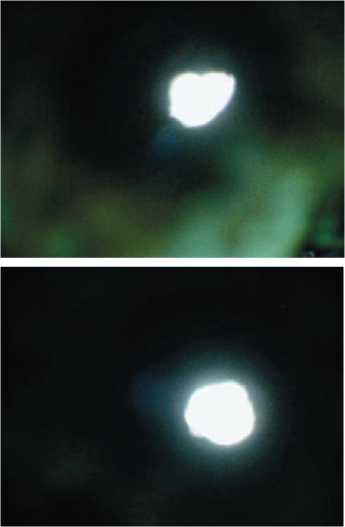
Рис. 2. Исследование каналов камней микроскопией в проходящем свете (об. х10, ок. х10)

14-18 Ch (miniperc). Однако преимущества кожухов меньшего размера при стандартной чрескожной пункционной нефролитотрипсии не доказаны. Известно, что инструменты меньшего калибра несут риск повышения внутрипочечного давления, удлиняется время выполнения операции [13].
Как отмечалось выше, в настоящее время для литотрипсии традиционно используется излучение Ho:YAG лазеров с ламповой накачкой и энергией в пачках импульсов свободной генерации 0,5-2 Дж, следующих с низкой частотой повторения 5-15 Гц [14,15]. Механизм разрушения конкремента при использовании гольмиевого лазера с импульсно-периодической ламповой накачкой, генерирующего длину волны 2140 нм, состоит в вапоризации камня. Жидкость испаряется во время лазерного импульса с большой энергией, а за счет увеличения и схлопывания пузырьков образуется ударная волна. Дальнейшая передача энергии происходит с паром через образовавшиеся полости.
Сравнительно недавно начали применяться тулиевые волоконные лазеры с длиной волны излучения ~1940 нм с пиковой мощностью до 500 Вт в импульсах длительностью в сотни микросекунд [16]. По данным исследования авторов, камни мочевой системы на этой длине волны имеют большее поглощение, чем на длине волны 2120 нм из-за близкого локального максимума поглощения воды. Причем высокая энергия в импульсах также приводит к полному разрушению камня и образованию мелких осколков в чашечно-лоханочной системе почки.
В проведенных нами экспериментах использованы режимы воздействия на камни мочевой системы при длине волны 2097 и 1967 нм. Результаты показали, что оптимальным режимом генерации лазера (на длине волны 2097 нс) для выполнения режима контролируемого разлома камня является частота повторения импульсов 200-1000 Гц длительностью 20-30 нс и энергией импульса 45-55 мДж. То есть режим лазерной генерации со сравнительно малой импульсной энергией (единицы – десятки мДж), но высокой частотой повторения импульсов (сотни герц – десятки килогерц) позволяет обеспечить деструкцию конкрементов на фрагменты с определенным/доста-точным для извлечения его через кожух – амплац размером.
Полученные результаты показали, что с точки зрения скорости дробления камней лазер на кристалле Ho:YAG с волоконно-лазерной накачкой (генерирующий на длине волны 2097 нм) значительно превосходит лазер на керамике Tm:Lu2O3 (на длине волны 1967 нм). Однако представляется, что это превосходство связано в основном с большей импульсной энергией лазера на кристалле Ho:YAG (достигающей десятков мДж) по сравнению с импульсной энергией в 0,40,6 мДж лазера на керамике. С другой стороны, длина волны генерации лазера на керамике Tm:Lu2O3 – 1967 нм обеспечивает больший коэффициент поглощения водой, чем излучение Ho:YAG лазера на длине волны 2097 нм. Поэтому при достижении аналогичной импульсной энергии (в десятки мДж) на длине волны 1967 нм следует ожидать более эффективного воздействия на камни, чем излучением на длине волны 2097 нм. Фактором, влияющим на результаты проведенных нами экспериментов, является их выполнение в атмосферном воздухе, хотя камни доставались из раствора и были сырыми к моменту лазерного воздействия. Лазерное дробление камней в жидкой среде (воде или моче) может несколько изменить скорость их разрушения, что требует дальнейшего проведения экспериментальной работы.
ВЫВОДЫ
Резюме:
Введение. Развитие инфекционно-воспалительных процессов в почках является одним из частых осложнений нефроли-тотрипсии в результате мелкой фрагментации камней, дис-семинации бактерий из биопленок инфицированных камней по полостной системе почки. Поиск новых методик дробления камней, предполагающих контролируемую крупнооскольчатую их фрагментацию, позволит не только минимизировать возможное инфицирование мочевой системы, но и предотвратить потерю мелких фрагментов камня, как источник резидуального камнеобразования.
Цель – поиск режима лазерной литотрипсии, который обеспечит эффективную фрагментацию почечных конкрементов, исключая их неконтролируемый мелкооскольчатый разлом.
Материалы и методы. В серии экспериментов использован лазер на кристалле Ho:YAG с накачкой излучением тулиевого волоконного лазера. Ho:YAG лазер генерировал на длине волны 2097 нм импульсы (длительностью 20-40 нс) с частой повторения, варьируемой от 5 до 40 кГц, при средней мощности до 35 Вт (энергия в импульсах варьировала в пределах 0,53,0 мДж), а также лазер на керамике Tm:Lu 2 O 3 с накачкой излучением эрбиевого волоконного лазера с рамановским сдвигом длины волны (на 1670 нм). Этот лазер на керамике генерировал в импульсно-периодическом режиме (импульсы длительностью 30-40 нс с частотой повторения, варьируемой в пределах 14-25 кГц) излучение на длине волны 1967 нм (средняя мощность излучения изменялась от 100 мВт до 10 Вт). Оба лазера созданы в ИПФ РАН (Н. Новгород). Измерялось время перфорации камня насквозь (до прохождения лазерного излучения через камень) и контроль полученного канала камня визуально и при микроскопии в проходящем свете. Изучен эффект лазерного дробления 25 камней еx vivo.
Результаты. Серией экспериментов выявлено, что оптимальным режимом генерации лазера (на длине волны 2097 нс) для выполнения режима контролируемого разлома камня является частота повторения импульсов 200 – 1000 Гц длительностью 20-30 нс и энергией импульса 45 – 55 мДж. То есть режим лазерной генерации со сравнительно малой импульсной энергией (единицы – десятки мДж), но высокой частотой повторения импульсов (сотни герц – десятки килогерц) позволяет обеспечить деструк-
Summary:Laser-mediated tripsy: a controlled disintegration of urinary stones
O.S. Streltsova, D.P. Pochtin, O.L. Antipov, I.D. Eranov, E.V. Grebenkin
Introduction. The development of infectious/inflammatory processes in kidneys in among the most common complications of nephrolithotripsy due to fragmentation of urinary stones into small particles and dissemination of bacteria from infected stone-derived biofilms into the kidney cavity system. The search for new methods of stone fragmentation implying controlled large comminuted fragmentation will allow not only to minimize possible contamination of the urinary system but also to prevent the loss of small particles of the disintegrated stone, which account for residual lithiasis.
Aim. The search for a mode of laser lithotripsy, which will ensure effective fragmentation of kidney concrements excluding their uncontrolled disintegration into small particles.
Materials and methods. In a series of experiments we used the Ho:YAG laser with thulium fiber laser pumping. The pulses generated by the Ho:YAG laser had the wavelength of 2097 nm whose duration was 20-40 ns and frequency varied from 5 to 40 kHz; the mean value of power was 35 W (pulse energy varied from 0.5 to 3.0 mJ). We also used the Tm:Lu2O3 ceramic laser with an erbium-pumped laser with the Raman shift at 1670 nm. This ceramic laser was emitting at 1967 nm in a pulsed–periodic regime (the duration and frequency of pulses were 30-40 ns and 14-25 kHz, respectively); mean power values varied from 100 mW to 10 W. Both lasers were created in the Institute of Applied Physics, Russian Academy of Sciences (Nizhny Novgorod). The duration of transverse stone perforation (before the passage of a pulse through the stone) was recorded; the newly formed tunnel was analyzed both visually and using light microscopy. The effect of laser fragmentation on 25 stones ex vivo was studied.
Results. In a series of experiments, we have determined that the optimal mode of laser generation at 2097 nm for controlled lithotripsy implies the frequency of pulses from 200 to 1000 Hz and their energy of 45-55 mJ. This means that the mode of laser generation with a relatively low pulse energy (tens of mJ) but high frequency of pulses (hundreds of Hz – tens of kHz) ensures the экспериментальная и клиническая урология № 1 2 0 18 цию конкрементов на фрагменты с достаточным для извлечения его через кожух – амплац размером. Время перфорации камня насквозь составило от 2 до 300 секунд и зависело от его плотности, размера по длине и химического состава.
Выводы. Вариантом профилактики инфекционно-воспалительного процесса в почке после нефролитотрипсии может стать контролируемая деструкция без разбрасывания содержимого конкрементов по полостной системе почки, что возможно обеспечить подбором режимов лазерного воздействия при контактной литотрипсии.
destruction of concrements into fragments which can be accessed through Amplatz sheath. The duration of transverse perforation was from 2 to 300 seconds and depended on the density, length and chemical composition of the stone.
Conclusion. Controlled destruction not followed by dissemination of the stone-derived particles through the kidney cavity could be a solution for the prevention of infectious/inflammatory processes after nephrolithotripsy, which could be achieved by adjusting the mode of laser-mediated contact lithotripsy.
Список литературы Лазерная трипсия: контролируемый разлом мочевых камней
- Мартов А.Г. Мочекаменная болезнь. Прошлое и настоящее. Урология сегодня. URL: http://urotoday.ru/system/files/urologia-1-2010-to-web.pdf;2010;(1): 1,3с.
- Диденко Л.В., Перепанова Т.С., Толордава Э.Р. и др. К вопросу об инфекционном генезе камней почек (электронно-микроскопическое исследование). Урология 2012;(3):4-7.
- Чухловин А.Б., Эмануэль Ю.В. Роль локальных инфекций в генезе мочекаменной болезни. Нефрология 2011;15(3):11-16.
- Палагин И.С., Сухорукова М.В., Дехнич А.В., Эйдельштейн М.В., Шевелев А.Н., Гринев А.В., и др. Современное состояние антибиотикорезистентности возбудителей внебольничных инфекций мочевых путей в России: результаты исследования «ДАРМИС» (2010-2011). Клиническая микробиология и антимикробная химиотерапия 2012;14(4):280-302.
- Margel D, Ehrlich Y, Brown N, Lask D, Livne P M, Lifshitz DA. Clincal implication of routine stone culture in percutaneous nephrolithotomy-a prospective study. Urology 2006;67(1):26-9. doi: 10.1016/j.Urology.2005.08.008
- Гольмиевый лазер в медицине. . М.: "Триада-Х", 2003. -240 с.
- Pierre S, Preminger GM. Holmium laser for stone management. World J Urol 2007;25(3): 235-9 DOI: 10.1007/s00345-007-0162-y
- Koras OI, Bozkurt IH, Yonguc T, Degirmenci T, Arslan B, Gunlusoy B, et al. Risk fac-tors for postoperative infectious complications following percutaneous nephrolithotomy: a pro-spective clinical study. Urolithiasis 2015;43(1):55-60 DOI: 10.1007/s00240-014-0730-8
- Yang T, Liu S, Hu J, Wang L, Jiang H. The Evaluation of Risk Factors for Postoperative Infectious Complications after Percutaneous Nephrolithotomy. Biomed Res Int 2017;2017:4832051 DOI: 10.1155/2017/4832051
- Раджабов У.А., Перепанова Т.С. Метафилактика инфекционных камней почек после перкутанной нефролитотрипсии. Экспериментальная и клиническая урология 2015;(2):80-83
- Antipov OL, Eranov ID, Kositsyin RI. 36 W Q-switched Ho:YAG laserat 2097 nm pumped by Tm fiber laser: evaluation of different Ho3+doping concentrations. Laser Phys Lett 2017;14(1), 015002.
- Antipov O, Novikov A, Larin S, Obronov I. Highly efficient 2 pmCWandQ-switchedTm3+:Lu2O3 ceramics lasers in-band pumped by a Raman-shifted erbium fiber laserat 1670 nm. Optics Letters 2016;41(10):2298-2301
- Tepeler A, Akman T, Silay MS, Akcay M, Ersoz C, Kalkan S, et al. lComparison of intrarenal pelvic pressure during micro-percutaneous nephrolithotomy and conventional percutaneous nephrolithotomy Urolithiasis 2014;42(3): 275-279 DOI: 10.1007/s00240-014-0646-3
- Zilberman DE, Lipkin ME, Ferrandino MN, Simmons WN, Mancini JG, Raymundo ME, et al. The digital flexible ureteroscope: in vitro assessment of optical characteristics. J Endourol 2011;25(3):519-22 DOI: 10.1089/end.2010.0206
- Van Cleynenbreugel B, Kiliç Ö, Akand M. Retrograde intrarenal surgery for renal stones -Part 1. Turk J Urol 2017;43(2):112-121 DOI: 10.5152/tud.2017.03708
- Глыбочко П.В., Альтшфроулер Г.Б., Винаров А.З., Еникеев Д.В., Дымов А.М., Сорокин Н.И., Замятина В.А., Коваленко А.А. Оценка возможностей тулиевого лазера (Tm) в литотрипсии in vitro. Материалы V Российского Конгресса по Эндоурологии и Новым Технологиям. Ростов на Дону, 8-10 сент. 2016. URL: http://uroweb. ru/article/otsenka_vozmogno stey_tulievogo_lazera_tm _v_litotripsii_in_vitro


