Лечебная тактика при синдроме Маллори-Вейсса
Автор: Фомин П.Д., Белый В.Я., Никишаев В.И., Задорожний А.М.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.7, 2012 года.
Бесплатный доступ
Работа основана на результатах лечения 2127 пациентов с синдромом Маллори-Вейсса за период с 1979 по 2009 год. Разработана эндоскопическая классификация локализации разрывов слизистой по отношению к пищеводно-желудочному соединению в соответствии с сосудистыми зонами данной области. Доказана необходимость проведения миниинвазивных эндохирургичних вмешательств на разрывах слизистой при эндоскопических стигматах F IIA, F 11В с целью снижения частоты рецидивов кровотечения. На основе проведенных исследований определен оптимальный объем лечебно-диагностической тактики при синдроме Маллори-Вейсса, применение которой улучшило результаты лечения.
Синдром маллори-вейсса, пищеводно-желудочное соединение, миниинвазивные эндохирургические вмешательства, рецидив кровотечения
Короткий адрес: https://sciup.org/140188098
IDR: 140188098 | УДК: 616.34-005.1-08-035
Treatment strategy of the Mallory-Weiss syndrome
The work is based on the results of treatment of 2127 patients with Mallory-Weiss syndrome from 1979 to 2009. Endoscopic classification of mucous breaks localization against to the esophagogastric junction in accordance with vascular areas of this region was developed. The necessity of miniinvasive endosurgery interventions on the mucous membrane ruptures with endoscopic stigmats F IIA, F IIB to reduce bleeding recurrences. Based on our research identified the optimal amount of diagnostic and treatment tactics at Mallory-Weiss syndrome, using of which has improved the results of treatment.
Текст научной статьи Лечебная тактика при синдроме Маллори-Вейсса
Несмотря на высокую частоту синдрома Маллори-Вейсса (СМВ) в структуре причин желудочно-кишечных кровотечений (от 6,5% [1] до 16, 8% [3, 6]), одного мнения относительно причин его возникновения, лечебной тактики до сих пор не выбрано. В опубликованных работах приводятся противоречивые взгляды относительно объема лечебной тактики при СМВ, эффективности различных методов миниинвазивных эндохирургических вмешательств (МЭВ), показаний к хирургическому лечению.
Хотя за последние годы можно отметить существенное уменьшение количества оперативных вмешательств при СМВ, и все же, несмотря на возможности эндоскопических методов в достижении гемостаза и профилактики рецидивов кровотечения (РК), больных с данным заболеванием продолжают оперировать с хирургической активностью от 6,9% [2, 5] до 15,4% [4], с высокой послеоперационной летальностью (от 3,8% [4] до 24,3% [5]) и РК в послеоперационном периоде (11,8% [2] – 13,6% [5]).
Цель исследования – улучшить результаты лечения больных с СМВ за счет усовершенствования лечебнодиагностической тактики.
Материалы и методы
Проведен анализ результатов лечения 2127 больных с СМВ за период с 1979 по 2009 г. Все больные были разделены на три группы. Сформированные клинические группы соответствовали этапам внедрения и возможностям эндоскопических малоинвазивных технологий в диагностике и лечении больных с желудочно-кишечными кровотечениями, в том числе и с СМВ.
В первой группе находились больные, при лечении которых эндоскопические методы использовались как основной диагностический метод (с 1979 по 1982 г. – 476 больных). После установления диагноза все они получали стандартную консервативную местную и общую терапию и, в случае ее безуспешности (продолжающееся кровотечение или его рецидив), подвергались операции – гастротомии с прошиванием разрывов слизистой. В случаях сочетания СМВ с язвенной болезнью двенадцатиперстной кишки дополнительно выполняли ваготомию с дренирующей желудок операцией и вмешательством на язве.
Во второй группе (с 1982 по 2003 г. – 1236 человек) были больные, у которых эндоскопическое исследование было дополнено различными методами МЭВ, как для остановки кровотечения, так и для профилактики его рецидива. Важным, на наш взгляд, было то обстоятельство, что различные методы применялись практически при всех вариантах разрывов слизистой, по мере их освоения и внедрения. Это послужило основой для всестороннего объективного анализа проблемных вопросов, оценки эффективности различных методов МЭВ к их применению в каждом конкретном случае.
В третьей (основной) клинической группе (с 2004 по 2009 г. – 415 человек), на основе детального анализа результатов лечения больных первых двух групп, была реализована дифференцированная лечебно-диагностическая тактика. С целью изучения состояния слизистой дна, кардиального, верхней трети тела и антрального отделов желудка, гистологических форм гастритов и инфицирования Helicobacter pylori было проведено патоги-стологическое исследование у 70 больных с СМВ. В группу контроля были включены 60 амбулаторных пациентов, которым эндоскопию выполняли по поводу диспепсии.
Через 10–14 дней этим же пациентам с СМВ повторяли исследование для оценки заживления разрывов и состояния слизистой с повторным забором материала для морфологического исследования.
Эндоскопию выполняли эндоскопами «ЛОМО», «AСМI», «Olympus», Fujinon с использованием системы Fujinon EPX-4400. Для остановки продолжающегося кровотечения, а так же для профилактики его рецидивов нами использовались аппликационные методы, эндоскопическая инъекционная терапия, термические методы (охлаждающая терапия, электрохирургические методы: электрокоагуляция тканей вокруг стигматы, монополярная электрокоагуляция с одновременной подачей 10% раствора NaCl через канал коагуляционного зонда без прижатия электрода к тканям, механическая тампонада кровоточащего сосуда электродом с проведением электрокоагуляции, биполярная электрокоагуляция, радиочастотная коагуляция, аргоноплазменная коагуляция, электрокоагуляция в сочетании с инъекционной терапией), а также клипирование.
Удельный вес больных с СМВ среди всех находившихся под нашим наблюдением больных с желудочнокишечными кровотечениями колебался от 3,4 (1987 г.) до 11,6% (2009 г.). Большинство пациентов (84,3%) относились к трудоспособному возрасту – от 20 до 65 лет, значительно преобладали мужчины (84,7%).
Причинами, приведшими к развитию СМВ, в основном была рвота, вызванная употреблением алкоголя (67,8%), перееданием (3,5%), употреблением недоброкачественных пищевых продуктов (1%). У 27,7% больных СМВ развился на фоне сопутствующих заболеваний. У 10,7% больных причинами возникновения внезапного повышения внутрижелудочного давления, что и повлекло развитие СМВ, были икота (54,2%), длительный беспрерывный кашель (23,2%), гипертонический криз (16,4%), физическая нагрузка (6,2%).
Результаты и их обсуждение
В I группе под нашим наблюдением находилось 476 больных. У 306 (64,3%) из них кровотечение на момент госпитализации остановилось, у 170 (35,7%) при эндоскопии выявлено продолжающееся кровотечение. Все больные получали однотипную консервативную терапию: парентеральное введение гемостатических препаратов, инфузионно-трансфузионную терапию, местное применение антацидов, средств, снижающих портальное давление. У 135 (79,4%) с продолжающимся кровотечением его удалось остановить. У 35 (20,6%) гемостатическая терапия эффекта не дала. У 14 (8,2%) возник РК. Эти 49 (10,3%) больных были оперированы. Во всех случаях выполнена гастротомия с прошиванием разрывов слизистой в кардиальном отделе желудка узловыми швами. Использовали нерассасывающийся шовный материал. В послеоперационном периоде развились осложнения: нагноение раны – у 12 (24,5%), левосторонний поддиафрагмальный абсцесс – у 1 (2%). РК возник у 1 (2%) больного.
У двух больных (с разрывами на передней стенке желудка) операции выполнены при эндоскопической ассистенции. С помощью эндоскопа были четко указаны места разрывов. Кровотечение было остановлено с помощью одиночных узловых швов с прошиванием всех слоев стенки желудка без вскрытия просвета. Перитонизация вторым рядом серозно-мышечных швов. С помощью эндоскопа была также проконтролирована надежность гемостаза. Эти больные выздоровели без осложнений.
Умерло 6 (12,2%) больных. Причины смерти: острая печеночная недостаточность – у 3, острый инфаркт миокарда – у 1, послеоперационная пневмония – у 2 больных.
У всех умерших больных были проведены гистологические исследования стенок пищевода и желудка в зоне разрывов. Выявлены однотипные изменения: атрофические изменения слизистой оболочки, очаги некрозов в подслизистом слое, паралитическое расширение сосудов микроциркуляторного русла и их очаговое полнокровие в межжелезистых стромальных слоях, геморрагическая инфильтрация, размозжение мышечных пучков собственной пластинки слизистой оболочки, серозное пропитывание (имбибиция) поверхностных слоев подслизистого слоя, периваскулярная инфильтрация, фиброз мышечного слоя. Полученные данные свидетельствуют об определенной предрасположенности измененных стенок пищевода и желудка к разрыву.
Анализ результатов лечения больных в первой клинической группе убедительно показал: консервативная терапия недостаточно эффективна, диагностическая эндоскопия обязательно должна быть дополнена МЭВ, обеспечивающими остановку продолжающегося кровотечения и профилактику его рецидивов, открытые операции при СМВ сопровождаются значительным числом послеоперационных осложнений и высокой летальностью.
Во второй группе преобладали больные с остановившимся кровотечением – 1009 (81,6%) пациентов: с эндоскопическими стигматами кровотечения F IIC и F III было 597 (48,3%), F IIА и F IIВ – 412 (33,3%) больных. С продолжающимся кровотечением (F IA, F IB) было госпитализировано 227 (18,4%) больных.
Основной целью анализа результатов лечения больных во второй клинической группе была оценка эффективности различных методов МЭВ, выполненных с целью остановки продолжающегося кровотечения и профилактики его рецидивов. Была установлена полная неэффективность аппликационной и охлаждающей терапии при продолжающемся кровотечении (ни в одном случае не удалось достичь эндоскопического гемостаза). Высокоэффективными при остановке кровотечения оказались клипирование, электрохирургические методы, эндоскопическая инъекционная терапия. Непосредственные результаты были примерно одинаковыми. Более важной для оценки примененных методик была частота РК: после клипирования их не было, после электрохирургического воздействия они возникли у 8,6% (при этом частота РК

достоверно не отличалась между различными методами гемостаза), а после инъекционной терапии – у 42,9% больных. Было отмечено, что в большинстве случаев РК появились после повторной рвоты или икоты.
При определении эффективности применяемых различных методов МЭВ, использованных для профилактики возникновения РК, у больных с самостоятельно остановившимся кровотечением установлена их одинаково высокая эффективность. Определенными преимуществами обладал метод неконтактного воздействия – аргоноплазменная коагуляция. Во время ее проведения мы не наблюдали возобновления кровотечения. Общее число больных с РК в группе было 64 (5,2%).
Во второй клинической группе был прооперирован 1 (0,08%) больной по поводу кровоточащей язвы луковицы двенадцатиперстной кишки с выявленным до операции СМВ. После вмешательства на язве было обнаружено просачивание крови из разрыва в области пищеводно-желудочного соединения. Выполнена высокая гастротомия с ушиванием разрыва кетгутом. Больной выздоровел. Умерло 7 (0,56%) больных, у которых СМВ развился на фоне тяжелой соматической патологии.
С целью определения частоты локализации разрывов слизистой при СМВ в третьей (основной) группе нами было разработано эндоскопическое распределение области пищеводно-желудочного соединения на отдельные зоны.
Локализация разрывов была нами классифицирована следующим образом:
-
LI – на уровне розетки нижнего пищеводного сфинктера (не доходя до пищеводно-желудочного соединения);
-
LII – в области пищеводно-желудочного соединения:
LIIа – от розетки нижнего пищеводного сфинктера до пищеводно-желудочного соединения;
LIIb – на уровне пищеводно-желудочного соединения с частичным переходом на пищевод и кардиальный отдел желудка;
LIIc – дистальнее пищеводно-желудочного соединения с переходом на кардиальный отдел желудка;
LIIІ – в кардиальном отделе желудка с переходом на верхнюю треть тела желудка;
LIV – в верхней трети тела желудка.
Согласно данных эндоскопического определения зоны пищеводно-желудочного соединения, наибольшее количество разрывов наблюдалось дистальнее пищеводно-желудочного соединения с переходом на кардиальный отдел желудка (LIIc) – 200 (37,5%) у 171 больного. Несколько меньше на уровне пищеводно-желудочного соединения с частичным переходом на пищевод и кардиальный отдел желудка (LIIb) – 146 (27,3%) у 122 больных и в кардиальном отделе с переходом на верхнюю треть тела желудка (LIIІ) – 111 (20,8%) у 53 больных. Наименьшее количество разрывов слизистой было в верхней трети тела желудка (LIV) – 4 (0,7%) у 2 больных.
Кроме того, нами были оценены эндоскопические стигматы кровотечения в зависимости от места локализации разрывов (таб. 1).
Проведенный анализ показал прямую сильную корреляционную связь (r = 0,89) между эндоскопическими стигматами кровотечения и локализацией разрывов: продолжающееся кровотечение и эндоскопические стигматы недавнего кровотечения с высоким риском возникновения РК (F IIА, F IIВ) наблюдались при расположении разрывов дистальнее пищеводно-желудочного соединения (LIV, LIII, LIIc), а эндоскопические стигматы недавнего кровотечения с низким риском возникновения РК (F IIС) и разрывы под фибрином (F III) встречались проксимальнее – ближе к розетке нижнего пищеводного сфинктера (LI, LIIa).
Объяснение полученных данных было найдено нами после сопоставления локализации разрывов слизистой с сосудистыми зонами в области пищеводно-желудочного соединения, что схематично представлено на рисунке 1.
При расположении разрывов в более мощной желудочной сосудистой зоне кровотечение носило упорный и выраженный характер с высоким риском возникновения
Эндоскопические стигматы кровотечения в зависимости от локализации разрывов
|
Локализация разрывов |
Эндоскопические стигматы кровотечения (%) |
Всего (%) |
||||||
|
F IA |
F IB |
F IIA |
F IIB |
F IIC |
F III |
|||
|
LI |
– |
– |
– |
– |
4 (1) |
5 (1,2) |
9 (2,2) |
|
|
LII |
LIIа |
– |
– |
– |
6 (1,5) |
8 (1,9) |
44 (10,6) |
58 (14) |
|
LIIb |
– |
9 (2,2) |
17 (4,1) |
21 (5) |
16 (3,9) |
59 (14,2) |
122 (29,4) |
|
|
LIIc |
– |
25 (6) |
42 (10,1) |
49 (11,8) |
24 (5,8) |
31 (7,5) |
171 (41,2) |
|
|
L IIІ |
6 (1,4) |
39 (9,4) |
6 (1,4) |
2 (0,5) |
– |
– |
53 (12,7) |
|
|
L IV |
2 (0,5) |
– |
– |
– |
– |
– |
2 (0,5) |
|
|
Всего (%) |
8 (1,9) |
73 (17,6) |
65 (15,6) |
78 (18,8) |
52 (12,6) |
139 (33,5) |
415 (100) |
|
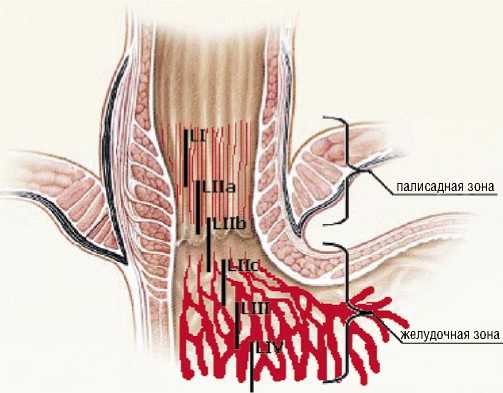
палисадная зона желудочная зона
Рис. 1. Сопоставление локализации разрывов с сосудистыми зонами

РК. При локализации разрывов в палисадной зоне картина была обратной.
При патогистологическом изучении слизистой нижней части кардии и прилегающих к нему отделов желудка у больных с СМВ и пациентов с диспепсией, у которых наблюдалось интенсивное срыгивание воздуха при обследовании с пролабированием слизистой верхней трети тела желудка в пищевод (11,7% пациентов), были выявлены аналогичные изменения. Эти изменения были обратимы. Частота выявления различных форм гастритов (при контрольном обследовании) и частота обсемененности слизистой желудка Helicobacter pylori у больных с СМВ и пациентов, обследованных по поводу диспепсии, достоверно не отличались.
В третьей клинической группе лечебная тактика была реализована на основании выводов из анализа материалов первой и второй групп.
У больных с продолжающимся кровотечением, а также с высокой угрозой его возникновения (224 (54%) пациента) были использованы положительно зарекомендовавшие себя методы МЭВ: электрокоагуляция – у 66, биполярная электрокоагуляция – у 34, радиочастотная коагуляция – у 30, эндоскопическая инъекционная терапия с последующей электрокоагуляцией – у 30, аргоноплазменная коагуляция – у 29, электрокоагуляция с последующей инъекционной терапией – у 34 больных. Всем больным с остановившимся кровотечением (F IIА, F IIВ) проведены МЭВ разрывов с целью профилактики РК.
Эндоскопические вмешательства проводили по усовершенствованной методике с учетом роли срыгивания воздуха (во время и после исследования) в возобновлении кровотечения. После проведения полного эндоскопического осмотра и проведения МЭВ на других источниках кровотечения эвакуировали воздух из желудка и вмешательство на разрывах выполняли при минимальной инсуффляции воздуха с обязательной полной его эвакуацией после завершения вмешательства. У больных в состоянии алкогольного опьянения, с неадекватным поведением, в состоянии возбуждения использовали тотальную интравенозную анестезию.
У 11 больных (2,6%) возникли РК, причем у 8 (72,7%) больных в кардиальном отделе желудка с переходом на верхнюю треть тела желудка (LІІІ). В верхней трети тела желудка (LIV) – у 2 (18,2%). На уровне пищеводно-желудочного соединения с переходом на кардиальный отдел желудка (LIIc) – у 1 (9,1%). При локализации разрывов в других зонах пищеводно-желудочного соединения (LI, LIIа, LIIb) РК не было.
Во всех случаях рецидивов при эндоскопии было выявлено продолжающееся кровотечение (F IB). Причина – повторная рвота и икота. Всем больным была проведена повторная эндоскопическая остановка кровотечения под седацией с пролонгированной тотальной интравенозной анестезией в течении 6–24 ч. в условиях отделения интенсивной терапии. РК отмечено не было. Открытых оперативных вмешательств в третьей группе не проводили. Умерших не было.
Улучшение результатов заключается в уменьшении РК в 1,8 раза (P < 0,05), уменьшении продолжительности лечения в 1,5 раза (P < 0,05) и исключении необходимости открытых оперативных вмешательств.
Выводы
-
1. Тяжесть и интенсивность кровотечения зависят от локализации разрывов, что объясняется их положением относительно сосудистых зон. Наиболее тяжелые случаи наблюдаются у больных с разрывами в проекции сосудов желудочной зоны.
-
2. СМВ развивается у больных при наличии предрасполагающих и производящих факторов. К первым относятся морфологические изменения стенки органов (атрофия слизистой), ко вторым – рвота, икота, кашель (т.е. резкое повышение внутрибрюшного давления).
-
3. Морфологические изменения слизистой в области пищеводно-желудочного соединения и их обратимый характер говорят о травматической природе повреждения при СМВ. Частота выявления различных форм гастритов и частота обсемененности слизистой желудка Helicobacter pylori у больных с СМВ и пациентов, обследуемых по поводу диспепсии, достоверно не отличалась.
-
4. Методом выбора для остановки кровотечения и профилактики рецидива являются МЭВ. Наиболее надежные из них – электрохирургические вмешательства, клипирование.
-
5. Важнейшим методом профилактики возникновения кровотечения во время эндоскопического обследования и профилактики возникновения рецидива в отдаленном периоде является подавление икоты и рвоты.
-
6. Открытые операции должны быть исключены из перечня лечебных мероприятий при СМВ.
Список литературы Лечебная тактика при синдроме Маллори-Вейсса
- Братусь В.Д. Новые тенденции в лечении больных с острыми желудочно-кишечными кровотечениями//Укр. журн. малоiнвазив. та ендоскоп. хiрургiї. -2001. Vol. 5, № 1. -С. 5-6.
- Грома В.Г. Хiрургiчна тактика i лiкування хворих з синдромом Меллорi-Вейсса: автореф. дис.... канд. мед. наук/Днiпропетровська державна медична академiя. Д., 2003. -19 с
- Кондратенко П.Г. Организационные вопросы оказания специализированной помощи больным с острыми кровотечениями в просвет пищеварительного канала/П.Г. Кондратенко, М.В. Соколов, Н.Л. Смирнов//Укр. журн. малошвазив. та ендоскоп. хiрургil. -2007. Vol. 11, № 1. -С. 24-25.
- Дужий I.Д. Особливостi синдрому Меллорi-Вейсса у жiнок/I.Д. Дужий, В.П. Шевченко, О.I. Борисенко та iн.//Укр. журн. малоiнвазив. та ендоскоп. хiрургiї. -2007. Vol. 11, № 2. -С. 30-31.
- Трофiмов М.В. Принципи визначення та формування лiкувальної тактики у хворих на синдром Меллорi-Вейсса: автореф. дис.... канд. мед. наук/Днiпропетровська державна медична академiя. Д., 2007. -20 с.
- Хаджиев О.Ч. Лечебная тактика при острых желудочно-кишечных кровотечениях/О.Ч. Хаджиев, А.К. Бабалич, Н.И. Каракурсаков и др.//Укр. журн. малоiнвазив. та ендоскоп. хiрургiї. -2007. Vol. 11, № 2. -С. 35-36.


