Лечение больных с абдоминальным сепсисом в реанимационном отделении многопрофильного стационара
Автор: Васильев И.Т., Мумладзе Р.Б., Якушин В.И., Евдакимов Е.А., Власенко А.В., Жуховицкий В.Г., Шестопалов А.Е., Логинов С.П., Митрохин А.А., Эминов М.З., Багателия З.А., Лебедев С.С.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 3 (37), 2014 года.
Бесплатный доступ
В работе обобщен опыт лечения 232 больных с абдоминальным сепсисом (АС), находившихся на лечении в реанимационном отделении ГКБ им. С.П. Боткина с 2008 по 2012 годы. Причинами, приведшими к развитию сепсиса, явились острые хирургические заболевания и травматические повреждения органов брюшной полости и забрюшинного пространства. В работе представлен комплексный подход в лечении этого тяжелого осложнения. Но основным методом лечения, безусловно, является хирургический. Выделены две типовые разновидности хирургического вмешательства: удаление очагов инфекции и дренирование гнойных очагов. Изучен микробный пейзаж АС, что позволило дифференцированно подходить к выбору антибактериальной терапии. Важное место в лечении АС занимает интенсивная терапия, включающая рациональную индивидуальную инфузионную терапию, оптимизацию транспорта кислорода и гемодинамики, респираторную и нутритивную поддержку. Одним из решающих факторов в развитии патогенеза сепсиса является эндогенная интоксикация (ЭИ). Для определения уровня эндотоксикоза использованы ряд интегральных показателей, включающих предложенный авторами индекс эндогенной интоксикации. В качестве важного метода борьбы с ЭИ, наряду с другими, широко используется один из экстракорпоральных методов детоксикации - гемофильтрация (CVVH). Изучение клинических эффектов гемофильтрации позволило прийти к заключению, что оптимальным сроком проведения CVVH является полупродленный режим (12-18 часов). Существенным направлением в лечении АС является устранение функциональных нарушений кишечника (ФНК), которые могут проявляться в виде пареза и функциональной кишечной непроходимости и являются одним из источников ЭИ. Дренирование паретически измененной кишки с последующим ее опорожнением не всегда бывает достаточным для восстановления ее физиологических функций. Поэтому в клинике применяется внутрикишечная терапия, включающая использование энтеросорбентов и озонированного 0,9% раствора хлорида натрия глюкозо-электролитных смесей. С целью восстановления функции кишечника используется метод гипербарической оксигенации, к которому имеются и ряд других показаний после хирургической коррекции абдоминальной инфекции.
Перитонит, абдоминальный сепсис, лечение
Короткий адрес: https://sciup.org/142211156
IDR: 142211156 | УДК: 616.94-07
Текст научной статьи Лечение больных с абдоминальным сепсисом в реанимационном отделении многопрофильного стационара
К началу XXI столетия сепсис по прежнему остается одной из самых актуальных проблем современной медицины [4, 5, 8]. Согласно современным представлениям абдоминальный сепсис является системной воспалительной реакцией организма в ответ на развитие инфекционного процесса в органах, локализующихся в брюшной полости и забрюшинного пространства [1, 10, 11, 15].
В настоящее время накопилось достаточное количество рекомендаций по лечению абдоминального сепсиса [2, 3, 7, 14, 16]. Вместе с тем, в силу улучшения диагностики [6, 12], неуклонного повсеместного роста заболеваемости и стабильно высокой летальности [9, 13, 17], проблема лечения этой категории больных остается далеко от своего разрешения.
Неоднородность клинических ситуаций, при которых развивается абдоминальный сепсис, часто требует нестандартных клинических, в том числе и хирургических решений, отличающихся от типовых вариантов действий, направленных на устранение источника сепсиса.
Хирургическое вмешательство является центральным звеном лечебной программы вне зависимости от причины возникновения абдоминального сепсиса (перитонеальный, панкреатогенный, холангиогенный и др.).
Мы обладаем опытом хирургического лечения 232 больных абдоминальным сепсисом, находившихся на лечении в реанимационном отделении хирургической клиники ГКБ им. С.П. Боткина с 2008 по 2012 год.
Хирургическое лечение
Причинами, обусловившими развитие абдоминального сепсиса, явился острый деструктивный панкреатит у 72 больных, перфоративная язва желудка и 12-перстной кишки – у 44, острый аппендицит – у 35, неопухолевые перфорации ободочной кишки – у 19, злокачественные новообразования брюшной полости и забрюшинного пространства – у 11, острый холецистит – у 10, перфорация тонкой кишки – у 8, острая кишечная непроходимость – у 7 больных. В остальных 26 наблюдениях причиной абдоминального сепсиса были абсцессы брюшной полости, воспалительные гинекологические заболевания, нарушение мезентериального кровообращения, травматические повреждения органов брюшной полости и др.
Накопленный опыт позволяет нам выделить две типовые разновидности хирургического вмешательства:
-
а) удаление очагов инфекции;
-
б) дренирование гнойных полостей, что достигается либо путем открытого вмешательства, либо с применением малоинвазивных технологий, широко применяемых в нашей клинике.
Оперативное вмешательство по поводу распространенного перитонита всегда выполняется под многокомпонентной общей анестезией с искусственной вентиляцией легких и предусматривает выполнение следующих основных задач:
-
— устранение источника перитонита;
-
— интраоперационную санацию, рациональное дренирование брюшной полости и забрюшинного пространства;
-
— интубацию кишечника, находящегося в состоянии пареза.
Оптимальным доступом при распространенном перитоните является срединная лапаротомия, обеспечивающая возможность полноценной ревизии и санации всех отделов брюшной полости.
После вскрытия брюшной полости забрюшинного пространства по возможности удаляется патологическое содержимое (гной, кровь, желчь, каловые массы и т.д.). Наиболее полноценно и менее травматично эти действия выполняются с помощью электрического отсоса со специальным наконечником, что предотвращает присасывание петель кишечника и большого сальника.
Следующий этап – последовательная ревизия органов брюшной полости и при необходимости забрюшинного пространства с целью выявления источника перитонита. Устранение источника перитонита наиболее ответственный этап вмешательства, и производится, учитывая функциональные возможности больного. При невозможности радикального удаления источника перитонита пораженный орган выводится внебрюшинно или отграничивается марлевыми тампонами от свободной брюшной полости. Однако использование тампонов с дренирующей целью не всегда бывает эффективно.
Особое внимание при распространенном перитоните уделяется определению показаний к резекции полых органов и адекватному выбору объема резекции. Наложение швов и анастомозов полых органов в условиях перитонита всегда сопровождается повышенным риском несостоятельности швов анастамоза. С этой целью применяют варианты отсроченного анастомозирования. При этом выполняется обструктивная резекция с обязательной зондовой декомпрессией проксимального участка кишки, обеспечивающей возможность адекватной аспирации кишечного содержимого и, следовательно, декомпрессии кишечника.
У ряда больных концы пересеченной кишки выводятся рядом на брюшную стенку через отдельный разрез в виде полных свищей. Такая тактика не может быть рекомендована в качестве наиболее рациональной при расположении зоны резекции вблизи связки Трейца. В этом случае риск несостоятельности анастомоза конкурирует с риском искусственного создания высокого тонкокишечного свища с его опасными функциональными последствиями, особенно для тяжелого больного. Поэтому вопрос чаще решается в пользу анастомоза.
При крайне тяжелом состоянии больного проксимальные и дистальные концы резецированной кишки не выводятся на переднюю брюшную стенку виде кишечных свищей, а временно, до стабилизации состояния больного, ушиваются наглухо.
Сроки выполнения реконструктивного этапа устанавливают при последующих ревизиях брюшной полости, и определяющими критериями при этом являются: разрешение перитонита, восстановление жизнеспособности кишечника, а также стабилизация состояния больного.
Вопрос о формировании первичного анастомоза после резекции правой половины ободочной кишки в условиях распространенного перитонита решается индивидуально в зависимости от выраженности воспаления брюшины и сроков его развития. Резекция левой половины ободочной кишки при перитоните должна завершатся формированием одноствольной колостомы и ушиванием периферического конца кишки по типу операции Гартмана.
При распространенном перитоните оптимальным методом интраоперационной санации брюшной полости является многократное промывание её подогретыми до температуры тела сбалансированными кристаллоидными солевыми растворами щадящим способом до чистых промывных вод. Фибринозные наложения удаляются пинцетом или влажным тупфером без повреждения висцеральной брюшины. Плотно фиксированные к висцеральной брюшине сгустки фибрина удалять не следует. После промывания брюшной полости раствор удаляется электроотсосом. Объем санирующих растворов должен составлять не менее 8–12 литров.
В клинике для санации брюшной полости широко используется озонированный 0,9% раствор хлорида натрия, который обладает выраженным антибактериальным действием в отношении аэробной и, что особенно важно, анаэробной микрофлоры.
После санации брюшной полости определяются показания к дренированию тонкой кишки. Оно показано при выраженных признаках паралитической непроходимости кишечника. Декомпрессия тонкой кишки осуществляется чаще путем назогастроэнтерального введения зонда.
Противопоказаниями к выполнению назоинтестинальной интубации являются: технические трудности установки зонда, обусловленные анатомическими особенностями (сужение или искривление носовых ходов, деформация пило-роантрального отдела желудка и 12-перстной кишки, зоны связки Трейца), крайняя тяжесть состояния больного. Возможные варианты проведения зонда – назоинтестинальная интубация и трансанальная интубация, дренирование через гастро-, энтеро- или аппендикостому. Оптимальным следует считать неинвазивные методы декомпрессии кишечника. Как правило, используем одно- или двухпросветные зонды, обеспечивающие активную аспирацию кишечного содержимого. Они также могут быть использованы и для энтерального введения питательных сред, лекарственных препаратов в послеоперационном периоде.
Дренирование тонкой кишки продолжается в течение 3–4 суток, и зонд удаляется после восстановления двигательной активности кишечника. В том случае, если опера- ция была сопряжена с рассечением спаек, с целью каркасной функции зонд оставляется в течение 7–8 суток. У больных пожилого возраста с выраженной сердечно-легочной недостаточностью предпочтение следует отдавать ретроградным методам дренирования через подвздошную кишку путем энтеростомии, аппендико- или цекостому.
Необходимость дренирования брюшной полости является аксиомой в лечении распространенного перитонита. Количество и качество дренажей определяется характером и распространенностью перитонита. Дренажи устанавливаются по стандартной методике к зоне источника перитонита и во все отлогие места брюшной полости. Дренажи используют для пассивной или активной эвакуации экссудата или санации брюшной полости в межоперативном периоде. В случае гнойно-некротического поражения забрюшинного пространства или панкреатогенном перитоните высоко эф-фектовно использование дренажей Пенроза.
Варианты завершения первичной операции при распространенном перитоните определены выбором дальнейшей тактики хирургического лечения. При необходимости проведения в дальнейшем повторных вмешательств с целью санации брюшной полости производится только ушивание кожи и подкожной клетчатки. Осложнения в виде образовавшихся гнойников брюшной полости, как правило, удается разрешить путем пункции и дренирования под ультразвуковым контролем.
Показаниями к выбору санационных релапаротомий являются:
-
— разлитой фибринозно-гнойный или каловый перитонит;
-
— признаки анаэробного инфицирования брюшной полости;
-
— невозможность одномоментной ликвидации или надежной локализации источника перитонита;
-
— множественные межкишечные гнойники;
-
— крайняя тяжесть состояния больного, исключающая возможность выполнения операции одномоментно в полном объеме.
Интервал между оперативными вмешательствами после первой операции обычно составляет 24–48 часов.
Основными критериями завершения санационных релапаротомий являются:
-
1) прозрачный серозный экссудат;
-
2) наличие перистальтики тонкой кишки;
-
3) отсутствие гнойно-фибринозных наложений на висцеральной и париетальной брюшине.
-
4) отсутствие распространенного гнойного и некротического поражения операционной раны или передней брюшной стенки.
При наличии клинической картины продолженного вялотекущего перитонита после плановых хирургических вмешательств производится так называемая релапаротомия «по показаниям».
Выбор метода лечения острого деструктивного панкреатита определяется тяжестью, формой и фазой течения заболевания, а также наличием системных и местных осложнений.
Основным видом лечения острого панкреатита в фазе токсемии является комплексная интенсивная консервативная терапия.
Хирургические вмешательства в эту фазу ограничиваются малоинвазивными вмешательствами: видеолапароскопией, чрескожной пункцией или дренированием острых жидкостных скоплений брюшной полости и забрюшинного пространства, декомпрессией билиарного тракта под контролем УЗИ. Открытые хирургические вмешательства (лапаротомия или люмботомия) в фазу токсемия при тяжелом панкреатите противопоказаны!
Лечение острого панкреатита в этот период асептического воспаления должно оставаться консервативным. При показаниях к хирургическому лечению преимущество отдается чрескожным вмешательствам. Открытые вмешательства должны производиться не ранее 2-х недель от начала заболевания и только по строгим показаниям.
При развитии гнойных осложнений показано срочное хирургическое вмешательство. В этот период основную роль играют открытые дренирующие и санирующие вмешательства. Основным методом санации гнойно-некротических очагов является некрсеквестрэктомия, которая может быть как одномоментной, так и многоэтапной. Малоинвазивные вмешательства должны использоваться по ограниченным показаниям.
Открытые вмешательства, в том числе повторные, являются операцией выбора в случаях значительной распространенности гнойно-некротического процесса или при отграниченном процессе, когда применение чрескожных дренирующих вмешательств не дает возможности достичь адекватной санации парапанкреатической и забрюшинной клетчатки (наличие в полости гнойника крупных некротических масс). Оптимальным доступом является вне-брюшинный, в виде люмботомии с продлением разреза на брюшную стенку по направлению к прямой мышце живота, что позволяет при необходимости, дополнить этот доступ лапаротомией. Объем операции – некрсеквестрэктомия. Способ завершения операции зависит от адекватности нек-рсеквестрэктомии. При полном удалении некротических тканей – это «закрытое» дренирование двухпросветными дренажами по числу отрогов полости через контрапертуры на брюшной стенке. При неполном удалении некротических тканей – это «открытое» дренирование двухпросветными дренажами по числу отрогов полости в сочетании с тампонированием полости через операционную рану и оставлением доступа для последующих программных ревизий и некрэктомий через оментобурсостому или люмбостому. И в том, и в другом случае проводится послеоперационное аспирационно-промывное лечение зоны операции.
Контроль за эффективностью дренирования должен проводиться с помощью фистулографии, УЗИ и КТ каждые 7–10 дней. Неэффективность дренирования или появление новых гнойных очагов является показанием к повторной операции с дополнительной некрэктомией и дренированием.
Абсолютным показанием к чрескожному дренированию под контролем УЗИ являются ограниченные гнойные жидкостные образования (жидкостные скопления, панкреатический абсцесс, инфицированная псевдокиста).
При наличии большого массива некротических тканей, а также признаках распространенной забрюшинной флегмоны чрескожные дренирующие вмешательства под УЗ-наведением могут быть использованы только как временная этапная санация гнойника с целью стабилизации состояния больного и достижения оптимальных сроков проведения радикального хирургического вмешательства – открытой санирующей и дренирующей операции (предпочтительно из внебрюшишого доступа).
При развитии аррозивного кровотечения в очаге гнойной деструкции и наличии в стационаре ангиографического оборудования показана топическая диагностика источника кровотечения (на высоте кровотечения) и остановка его путем эндоваскулярного вмешательства. При хирургической остановке кровотечения следует произвести ревизию зоны кровотечения, удалить секвестры, прошить место кровотечения (временный гемостаз) и выполнить перевязку сосудов на протяжении, вне гнойного очага (окончательный гемостаз). Накладывать швы на стенку сосуда в зоне дефекта в гнойной ране не следует. В ряде случаев и при невозможности произвести перевязку сосудов вне гнойного очага показана дистальная резекция поджелудочной железы и спленэктомия.
Лечение гнойного холангита является комплексным и включает назначение инфузионной терапии, направленной на уменьшение проявлений интоксикации и полиорганной недостаточности, и введения антибиотиков широкого спектра действия.
Антибактериальная терапия должна сочетаться со своевременной оперативной или эндоскопической билиарной декомпрессией и коррекцией проходимости желчных протоков. В настоящее время предпочтение отдается малоинвазивным методам декомпрессии.
Выбор метода билиарной декомпрессии зависит от причины непроходимости желчных протоков и уровня обструкции. Эндоскопическая папиллосфинктеротомия (ЭПСТ) в сочетании с литоэкстракцией и санацией желчных протоков в настоящее время являются методом выбора в лечении холедохолитиаза и рубцовых стриктур дистальных отделов билиарного тракта. Однако не всегда удается посредством эндоскопических чреспапиллярных вмешательств устранить холедохолитиаз. Основными причинами неэффективности эндоскопических вмешательств на боль- шом дуоденальном сосочке (БДС) являются: недоступность БДС вследствие ранее перенесенных операций на желудке; расположение БДС в полости крупных дивертикулов; наличие фиксированных камней, размер которых превышает диаметр нижележащих отделов желчных протоков; сочетание холедохолитиаза со стенозом терминального отдела холедоха.
При неэффективности эндоскопических вмешательств билиарная декомпрессия выполняется антеградным способом путем чрескожной чреспеченочной холангиостомии под ультразвуковым и рентгентелевизионным контролем. При невозможности наложения холангиостомии из-за анатомического взаиморасположения трубчатых структур печени, что часто сопряжено с техническими трудностями и осложнениями, выполняется чрескожная чреспеченочная холецистостомия под контролем ультразвука.
При опухолевом поражении проксимальных отделов билиарноо тракта более эффективно чрескожное чреспеченочное дренирование желчных протоков.
В комплексном лечении холангита целесообразно применять методы внутрипротокового воздействия, основанные на введении в желчные протоки различных лекарственных сред, или воздействия на печень, желчь и слизистую оболочку желчных протоков методом эфферентной терапии и физиолечения (холесорбция, озонотерапия, лазерное и УВЧ-облучение и др.).
При формировании крупных одиночных холангиоген-ных абсцессов тактика лечения заключается во вскрытии и дренировании гнойника. Предпочтение следует отдавать малоинвазивным чрескожным способам дренирования, выполняемым под контролем УЗИ или КТ.
Множественные мелкие холангиогенные абсцессы недоступны для хирургического лечения, поскольку вскрытие или дренирование всех гнойников оказывается технически невозможным и патогенетически необоснованным. Ведущую роль в лечении множественных холангиогенных абсцессов печени играет рациональная антибактериальная терапия, направленная на отграничение гнойных очагов в сочетании с дренирующими вмешательствами для устранения препятствия желчеоттоку. Наибольшей концентрации антибиотиков в непосредственной близости гнойного очага можно добиться при использовании методов регионарной антибактериальной терапии путем внутриартериального и лимфотропного введения препаратов.
Малоинвазивные вмешательства
Развитие малоинвазивных дренирующих технологий повсеместно привело к снижению объема «открытых» оперативных пособий, выполняемых по поводу отграниченных гнойников органов брюшной полости. Современная ультразвуковая аппаратура позволяет четко локализовать гнойный очаг, определить траекторию безопасного под- хода и выполнить его санацию в кротчайшие сроки от момента диагностики. Практика показывает, что при наличии квалифицированного специалиста по ультразвуковой диагностике и определенного опыта в клинике безопасную траекторию для пункции и последующего дренирования отграниченного гнойника брюшной полости можно выполнить практически всегда.
На сегодняшний день мы располагаем опытом 3 тыс. дренирующих операций. За анализируемый период с 2008 по 2012 годы произведено 158 чрескожных дренирований 138 пациентам. Локализация гнойников было следующей: абсцесс подпеченочного пространства – 44 (28,7%); абсцесс левого поддиафрагмального пространства – 34 (22,0%); абсцесс правого поддиафрагмального пространства – 22 (14,4%); межкишечные абсцессы – 19 (12,4%). Служба интервенционных дренирующих технологий в ГКБ им. С.П. Боткина функционирует с 1997 года.
Дренирование выполняем в специально оборудованной операционной, оснащенной стандартным рентгенологическим оборудованием с С-дугой и ультразвуковым аппаратом. Используем методику стилет-катетер. Применяем дренажи с функционирующим концом по типу «свиной хвост» фирмы «МИТ (Россия) и «Balton» (Польша). В ряде случаев при больших по объему гнойниках брюшной полости целесообразно установка двух дренажей, в верхнюю и нижнюю его части, с целью более адекватного дренирования и создания промывной системы. В наших наблюдениях два дренажа было установлено 15 больным. Технический успех достигнут в 100% случаев (при отсутствии безопасной траектории дренирование не выполняли). Интраоперационно в обязательном порядке выполняли забор материала для бактериологического исследования и определения чувствительности микрофлоры к антибиотикам.
В послеоперационном периоде гнойную полость ежедневно промывали растворами антисептиков или озонированным раствором хлорида натрия. В случае установки двух дренажей осуществляли проточное промывание полости. В обязательном порядке выполняли фистулографию полости на 3–4 сутки от момента дренирования. Динамику уменьшения полости абсцесса контролировали по динамическому ультразвуковому исследованию. После окончания закрытия полости дренаж удаляли.
Интраоперационных осложнений не было. В послеоперационном периоде отмечены осложнения в виде перитонита – 2 больных, дуоденального свища – 1, неполного наружного желчного свища – 5, панкреатического свища – 3, тонкокишечного свища – 3, толстокишечного свища – 2 больных. Следует отметить, что указанные осложнения скорее связаны с источником формирования абсцесса, чем с техническими аспектами дренирования. Летальных исходов, непосредственно связанных с дренированием, не было.
Таким образом, чрескожное дренирование абсцессов брюшной полости под ультразвуковым наведением является малотравматичным, высокоэффективным, практически не имеющим противопоказаний оперативным вмешательством, позволяющим в кратчайшие сроки выполнить санацию гнойного очага.
Больным с острым панкреатитом и панкреонекро-зом с острыми жидкостными скоплениями сальниковой сумки и забрюшинного пространства произведено 136 пункционно-дренирующих операций. В клинике проводится двухэтапный метод хирургического лечения больных с тяжелым панкреонекрозом. Первым этапом на фоне выраженного интоксикационного синдрома производится дренирование жидкостных скоплений сальниковой сумки и жидкостных скоплений парапанкреатической клетчатки под УЗ-наведением с установкой дренажей и формированием промывных систем - 110 (80,8%) операций. У части пациентов данная методика является окончательной, позволяющей вылечить пациента без открытого оперативного вмешательства - 48 1(35,3%) пациентов. Следует отметить, что 21 (15,4%) пациентов из этой группы дренирование сальниковой сумки и жидкостных скоплений забрюшинного пространства мы проводили под УЗ-наведением транс-гастрально, за не имением других мест доступа к зоне интереса. Операции проведены без каких либо осложнений. Вторым этапом при наличии показаний в «холодном периоде» производится лапаротомия с удалением секвестров, санацией забрюшинного пространства и брюшной полости, дренированием и формирование оментобурсостомы и соответствующим ведением пациентов в послеоперационном периоде. Данная двухэтапная методика лечения таких тяжёлых больных позволяет снизить число осложнений и летальных исходов, и рекомендуется к применению в клинической практике. 26 (19,12%) пациентам в экстренном порядке произведено дренирование нагноившихся ложных кист поджелудочной железы.
Антибактериальная терапия
Антибактериальная терапия является одним из важных компонентов лечения сепсиса. Антибиотики при сепсисе должны назначаться неотложно до получения результатов бактериологических исследований. В последние годы были получены убедительные данные, что ранняя эмпирическая антибактериальная терапия сепсиса приводит к снижению летальности и частоты осложнений. Чрезвычайно важным является назначения по возможности адекватной стартовой антибактериальной терапии. Она должна базироваться на основе спектра предполагаемых возбудителей в зависимости от локализации первичного очага.
При эмпирическом подходе целесообразно назначать антибиотики широкого спектра активности, учитывая обширный перечень потенциальных возбудителей с различной чувствительностью и устойчивостью. После получе- ния результатов бактериологических исследований режим антибактериальной терапии должен быть скорректирован с учетом выделенных микроорганизмов и их антибиотико-чувствительности.
Нами исследованы 65 проб экссудата из брюшной полости и 93 проб крови у 57 пациентов с абдоминальным сепсисом. Исследования проводились в классической аранжировке с использованием конвенциального выбора питательных сред (bio Merilux, Франция). Посредством бактериологического анализатора «Wolk Way 40S» («Dade Bering», США) осушествляли идентификацию выделенных культур и оценку их чувствительности к антимикробным средствам.
Из экссудата брюшной полости было выделено 87 культур микроорганизмов. В том числе 51,7% (45) в монокультуре, и 48,3% (42) в ассоциациях: состоящих из 2-х (88,1% – 37 больных) из 3-х (11,9% – 5 больных) микроорганизмов. В составе ассоциации чаще всего определялись Klebsiella pneumoniae с грампозитивной микрофлорой ( Enterococcus faecium, Staphylococcus aureus ) или грамнегативная флора ( Escherichia coli, Acinetobacter lwoffii ). Существенную роль в ассоциациях играли грибы рода Candida .
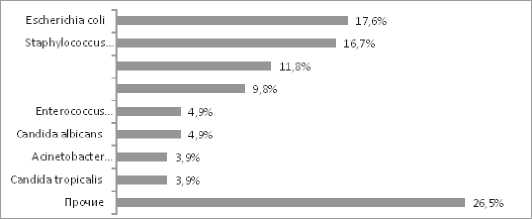
Рис. 1. Спектр ведущей микрофлоры, изолированной из отделяемого брюшной полости у пациентов с абдоминальным сепсисом
В спектре выделенных культур (рис. 1) из отделяемого брюшной полости доминировали представители семейства Enterobacteriaceae (33,3%) от изолированных микроорганизмов, среди них наиболее часто встречались Klebsiella pneumoniae (11,1%) и Е. coli (17,6%) Среди грамнегативных неферментирующих бактерий (ГОНФБ) доминировала Acinetobacter lwoffii (3,9%), Pseudomonas aeruginosa (3,8%). Грампозитивная микрофлора была представлена в первую очередь родом Staphylococcus – 25,3%, в этой группе доминировали Staphylococcus aureus (16,7%), коагулазонегативные стафилококки встречались реже – Staphylococcus epidermidis (9,8%). Представители рода Enterococcus изолировались в 4,9% случаях, при этом основное число принадлежит Enterococcus faecium , стрептококки встречались в эксудате брюшной полости в 4,6% случаях. Заметное положение в структуре абдоминальной инфекции занимали дрожжеподобные грибы рода Candida, среди которых доминировали Candida albicans (4,9%).
Среди представителей семейства Enterobacteriaceae не было выделено резистентных штаммов к карбопенемам, цефалоспоринам III–IV поколений, 70% штаммов были чувствительны к пенициллинам, а 45% штаммов – резистентны к фторхинолонам. 21,4% штаммов Staphylococcus aureus определялись как метицилленрезистентные (MRSA). И 22,2% штаммов стафилококков были резистентны к инги-биторзащищенным пенициллинам. Более половины (66,7%) выделенных штаммов S. aureus характеризовались как резистентные к фторхинолонам. Другие представители грам-позитивной микрофлоры (в частности род Enterococcus ) характеризовались резистентностью к аминогликозидам, тетрациклинам, фторхинолонам I–II поколений и 50% штаммов – к фторхинолонам III поколений и карбопенене-мам. При этом не было выделено ни одного штамма энтерококка, резистентного к ванкомицину. Все выделенные штаммы рода Streptococcus были чувствительны к пенициллинам, и всем β-лактамным препаратам. Грамнегативные неферментирующие бактерии (ГОНФБ) были чувствительны к аминогликозидам и резистентны к цефалоспоринам II поколения. 83,3% штаммов ГОНФБ были резистентны к цефалоспоринам III поколения и 20% штаммов – к IV поколению. Среди этой группы микроорганизмов 83,3% штаммов резистентны к фторхинолонам и 50% штаммов – к карбопенемам.
Большая часть представителей дрожжеподобных грибов рода Candida, изолированных из хирургических отделений, были резистентны в отношении флюконазола (54,5%), нистатина (66,7%). При этом все изолированные дрожжеподобные грибы были чувствительны к амфотерицину-В. Среди изолированных микроорганизмов из брюшной полости 4,6% (4) определялись как полирезистентные. Все полирези-стентные микроорганизмы были представлены штаммами Klebsiella pneumoniae .
Из проб крови выделено 96 культур. Из них 95,8% (92) в монокультуре, и 4,2% (4) в ассоциациях из 2-х микроорганизмов.
В спектре выделенных культур (рис. 2) из крови пациентов доминировали представители рода Staphylococcus
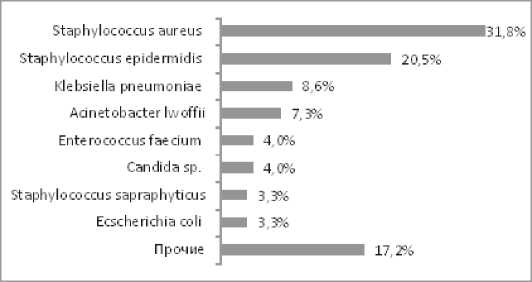
Рис. №2. Спектр ведущей микрофлоры, изолированной из крови у пациентов с абдоминальным сепсисом
(57,5%). Наиболее часто встречались S. aureus (30%), S. epidermidis (23.3%). Среди ГОНФБ (11,7%) доминировали (83%) Acinetobacter lwoffii . Заметное положение в структуре абдоминального сепсиса занимали дрожжеподобные грибы рода Candida (10,8%) среди которых доминировали С. hillermanii – 33,3%.
Представители семейства Enterobacteriaceae из крови при абдоминальном сепсисе выделялись в 10% случаях. В этой группе микроорганизмов доминировали штаммы Klebsiella pneumoniae (8,6%). Из крови выделялись представитель грампозитивной микрофлоры – Enterococcus faecium (5%), Streptococcus pyogenes (1,7%) и в 0,8% случаях анаэробные бактерии ( Eubacterium lentum ).
45% S. aureus, выделенных из крови, определялись как метицилленрезистентные, и 60% штаммов – резистентные к ингибиторзащищенным пенициллинам, 20% – к фторхино-лонам II поколения и 50% – к фторхинолонам III поколения, 30% были резистентны к линезолиду. Коагулазонегативные стафилококки ( S. epidermidis ) в 40% случаях определялись как метицилленрезистентные (MRSE) и 35% штаммов S. epidermidis были резистентны к ингибиторзащищенным пенициллинам.
Представители ГОНФБ – Acinetobacter Iwoffii в 85% случаях были резистентны к цефалоспоринам III поколения, 52% резистентны к ингибиторзащищенным пенициллинам и 38% – к карбопенемам.
Большая часть (66,7%) представителей семейства Enterobacteriaceae были резистентны к фторхинолонам, и все штаммы энтеробактерий были резистентны к аминогликозидам. Не было выделено штаммов семейства Enterobacteriaceae резистентных к карбопенемам.
Большая часть (75%) представителей дрожжеподобных грибов рода Candida, изолированных из крови, были резистентны в отношении нистатина и вориконазола. При этом большинство дрожжеподобных грибов (54%) были чувствительны к амфотерицину, флуконазолу, клотримазолу, кетоконазолу и интраконазолу.
Данные микробиологических исследований играют решающую роль для рациональной терапии абдоминальной инфекции в хирургии. Микробиологическая диагностика позволяет идентифицировать резистентные бактерии и своевременно оптимизировать назначение антибиотиков.
Однако данные о частоте каждого возбудителя при той или иной локализации первичного очага достаточно неоднородны, что связано и с особенностями стационара. Тем не менее, в ряде случаев в этиологии абдоминального сепсиса можно выделить в спектре ведущей микрофлоры наиболее часто встречающихся патогенов: среди представителей семейства Enterobacteriaceae – Escherichia coli, Klebsiella pneumoniae , среди ГОНФБ – Acinetobacter Iwoffii и Pseudomonas aeruginosa, среди грампозитивной микрофлоры – Staphylococcus aureus и Enterococcus faecium .
Заметную роль в этиологии сепсиса играют и дрожжеподобные грибы рода Candida .
Принципиальным условием лечения сепсиса является эрадикация возбудителей. Одним из критериев выбора антибактериальной терапии служит оценка чувствительности микрофлоры к антимикробным препаратам in vitro .
Но не всегда есть параллель между микрофлорой из раны и из крови при абдоминальном сепсисе. Обязательным компонентом лечебной программы абдоминального сепсиса является своевременная и адекватная антибактериальная терапия.
Принципиально важной особенностью абдоминального сепсиса является эндогенное инфицирование очагов асептического воспаления брюшной полости из желудочнокишечного тракта. Данные микробиологических исследований играют решающую роль для рациональной терапии абдоминальной инфекции в хирургии. Микробиологическая диагностика позволяет идентифицировать резистентные бактерии и своевременно оптимизировать назначение антибиотиков. При интраабдоминальных абсцессах различной локализации помимо аэробной и факультативно анаэробной микрофлоры учавствуют и анаэробные микроорганизмы (бактероиды, фузобактерии, пептококки, клостридии). Это следует учитывать при исследовании отделяемого брюшной полости и назначении антибактериальной терапии.
Следует отметить, что в микробиологической структуре интраабдоминальных инфекционных осложнений, развивающихся в послеоперационном периоде или во время пребывания больного в стационаре, особое значение приобретают госпитальные штаммы возбудителей: среди которых наиболее часто встречаются S. aureus, S. epidermidis, Enterococcus spp., Acinetobacter spp., Pseudomonas aeruginosa, Klebsiella pneumonia . Эти микроорганизмы отличаются высокой и поливалентной резистентностью к антибиотикам, что крайне затрудняет эффективное лечение больных. Огромную проблему в этом отношении представляют гра-мотрицательные микроорганизмы, например Acinetobacter spp. и Klebsiella pneumonia , устойчивые ко многим антибактериальным препаратам. Эффективны против этих возбудителей лишь карбапенемы.
Результаты микробиологического исследования являются основой целенаправленного режима антибактериальной терапии. Корректность и достоверность этих исследований зависят от соблюдения правил забора биологического материала. В пейзаже абдоминального сепсиса доминируют грамнегативные бактерии, в реанимационных отделениях помимо бактериальной микрофлоры ведущую роль играют представители дрожжеподобных грибов. Приобретённая резистентность к антимикробным средствам (в том числе, применяющихся в клинической практике) среди микроорганизмов, а также наличие полирезистентной микрофлоры, ассоциированной с абдоминальной инфекцией, распространена достаточно широко, что диктует необходимость постоянного её мониторинга.
Список литературы Лечение больных с абдоминальным сепсисом в реанимационном отделении многопрофильного стационара
- Гельфанд Б.Р., Бурневич С.З. и др. Абдоминальный сепсис: современный взгляд на нестареющую проблему//Вестник интенсивной терапии. 1996. №4. С. 29-35.
- Мороз В.В., Лукач В.Н. и др. Сепсис. Клинико-патофизиологические аспекты интенсивной терапии. Петрозаводск, 2004.
- Костюченко А.Л., Бельских А.Н., Тулупов А.Н. Интенсивная терапия послеоперационной раневой инфекции и сепсиса. Санкт-Петербург, 2000.
- Руднов В.А. Сепсис: Современный взгляд на проблему//Клиническая антимикробная химиотерапия. 2000. Т. 2, №2. С. 2-7.
- Савельев В.С. Сепсис в хирургии: состояние проблемы и перспективы/В кн.: «50 лекций по хирургии». Под редакцией В.С. Савельева. М., 2003. С. 317-320.
- Светухин А.М. и др. Клинико-морфологические аспекты диагностики сепсиса//Новые технологии в диагностике и лечении хирургической инфекции на основе доказательной медицины. М., 2003. С. 93-95.
- Сепсис. Классификация, клинико-диагностическая концепция, лечение./Под редакцией Савельева В.С., Гельфанда Б.Р. М., 2011.
- Сепсис в начале XXI века. Классификация, клинико-диагностическая концепция, лечение. Патолого-анатомическая диагностика. Практическое руководство. М.: НИССХ им. Бакулева А.Н. РАМН, 2004.
- Angus D.S. et al. Epidemiology et sever sepsis in the undated states: analysis of incidence, on come and associated costs care//Crit. Care Med. 2001. Vol. 29. P. 1303-1310.
- Bone R.S. Toward a theory regarding the pathogenesis of the systemic inflammatory response syndrome: what we do and do not know about cytokine regulation//Crit. Care Med. 1996. Vol. 24. P. 163-170.
- Bouchud P.Y., Calondra T. Pathogenesis of sepsis: new concepts and implications for future treatment//BMJ. 2003. Vol. 326. P. 262266.
- Carvalko P.R.A., Frotta E.A. Advances in sepsis diagnosis and treatment//S. Pediatria. 2003. Vol. 79 (Supl. 2). P. 195-204.
- Delinger R.P. et al. Surviving Sepsis Campaign: International guidelines for management of severe sepsis shock//Crit. Care Med. 2008. Vol. 36. P. 296-327.
- JourangP. Patel and al. New treatment strategies for severe sepsis and septic shock//Curr. Opin. Crit. Care. 2003. Vol. 9. P. 390-396.
- Hotchkiss R.S., Kare I.E. The pathogenesis and treatment of sepsis//N. Eng. J. Med. 2003. Vol. 348. P. 138-150.
- Jimes M.F., Marshall J.C. Sours control in the management of sepsis «surviving Sepsis Campaign guidelines for management severe sepsis and septic shock»//Intensive Care Med. 2001. Vol. 27. P. 49-62.
- Vincent J.L., Sakr Y. et al. Sepsis in European Intensive Care Units: Results of the SOAP Study//Crit. Care Med. 2006. Vol. 34, №2. P. 344-353.


