Лечение нейрогенной дисфункции мочевого пузыря и вторичного энуреза у детей и подростков
Автор: Морозов В.И., Байбиков Р.С., Закиров А.К., Юльметов Г.А.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Детская урология
Статья в выпуске: 4, 2018 года.
Бесплатный доступ
Введение: Под нейрогенной дисфункцией мочевого пузыря (НДМП) следует понимать разнообразные формы нарушения его резервуарной и эвакуаторной функции, развивающиеся вследствие поражения нервной системы на ее различных уровнях - от коры головного мозга до интрамурального аппарата, до сих пор нет единого мнения об этиологии данного заболевания. Цель исследования: обобщить результаты обследования и лечения 133 детей с нейрогенной дисфункцией мочевого пузыря (НДМП) в возрасте от 3 до 14 лет. Материалы и методы: Авторами предложен двухэтапный алгоритм обследования детей с НДМП: уронефрологический и неврологический этапы диагностики. Рассматривается необходимость топической диагностики поражения нервной системы у больных с нейрогенной дисфункцией мочевого пузыря. Приводятся данные корреляции функционального состояния мочевого пузыря в зависимости от уровня поражения центральной нервной системы. Описаны методики базисной терапии очагов перинатальных поражений нервной системы как причины нейрогенных дисфункции мочевого пузыря у детей, а также методы симптоматической фармако- и физиотерапии, направленных на нормализацию функционального состояния мочевого пузыря и уродинамики мочевых путей в целом...
Дети, нейрогенный мочевой пузырь, энурез
Короткий адрес: https://sciup.org/142216899
IDR: 142216899
Treatment of neurogenic bladder dysfunction and secondary enuresis in children and adolescents
Treatment of neurogenic bladder dysfunction and secondary enuresis in children and adolescents V.I. Morozov, R.S. Baybikov, A.K. Zakirov, G.A. Yulmetov Introduction: The article presents the results of examination and treatment of 133 children with neurogenic bladder dysfunction aged 3 to 14 years. Materials and methods: A two-stage algorithm of examination with this pathology is proposed: uronephrological and neurological stages of diagnosis. The necessity of topical diagnosis of nervous system damage in patients with neurogenic bladder dysfunction is considered. The data of correlation of the functional state of the bladder depending on the level of Central nervous system damage are presented. The methods of basic therapy perinatal injuries foci of the nervous system as the root cause of neurogenic bladder dysfunction in children, as well as methods of symptomatic pharmacotherapy and physiotherapy aimed at normalizing the functional state of the bladder and urodynamic are described...
Текст научной статьи Лечение нейрогенной дисфункции мочевого пузыря и вторичного энуреза у детей и подростков
од нейрогенной дисфункцией мочевого пузыря (НДМП) следует понимать разнообразные формы нарушения его резервуарной и эвакуаторной функции, развивающиеся вследствие поражения нервной системы на ее различных уровнях – от коры головного мозга до интрамурального аппарата [1,3,5,8,9,16,17,19]. Несмотря на пограничный характер данной патологии исследования НДМП ведутся, чаще всего, в рамках одной специальности [4,6,7,18]. До настоящего времени нет единого мнения в отношении этиологии данного заболевания. Большинство авторов занимающихся изучением НДМП, отмечают ведущую роль нарушений нервной системы в развитии заболевания [13,14,20], но акцент в лечении делается все же на стабилизацию функционального состояния мочевого пузыря различными методами симптоматической терапии [2,15,21]. При этом явно недооцениваются перспективы лечения самого очага поражения нервной системы как первопричины заболевания [10]. На наш взгляд, топическая диагностика поражений нервной системы и целенаправленное терапевтическое воз- действие на указанные структуры в сочетании с симптоматической терапией функциональных расстройств мочевого пузыря могут существенно улучшить результаты лечения НДМП, которые до настоящего времени остаются пока еще малоутешительными. Несмотря на достигнутые определенные успехи в этом направлении общая эффективность проводимого лечения у больных НДМП остается пока еще невысокой: 44,4% – у пациентов с поражением конуса и эпиконуса спинного мозга и 50,0-70,5% – у детей с высокими уровнями поражения центральной нервной системы (цервикальный и церебральный) [1,7]. Таким образом, остаются нерешенными вопросы качества жизни детей с нейрогенной дисфункцией мочевого пузыря и вторичным энурезом, а также вопросы рецидивирующей инфекции мочевыводящих путей при клинических формах НДМП, сопровождающихся нарушениями уродинамики [11,12,21]. Все это обуславливает актуальность обсуждения проблемы НДМП и требует дальнейших усилий научных работников и практических врачей различных специальностей в изучении этой патологии детского возраста.
МАТЕРИАЛЫ И МЕТОДЫ
Под нашим наблюдением находились 133 ребенка с НДМП в возрасте от 3 до 14 лет, из них мальчиков было 63, девочек – 70. Распределение пациентов по возрасту было следующим: от 3 до 7 лет – 39 детей, от 8 до 11 лет– 55, от 12 до 14 лет – 39 детей. У 52% пациентов наряду с НДМП определялся вторичный энурез. Всем детям проводилось комплексное урологическое (включая уродинами-ческое) и неврологическое обследование, включающее в себя ЭМГ, РЭГ, ЭхоЭГ, ЭЭГ (электроэнцефалограмма). По результатам неврологического обследования пациенты были распределены на группы по уровню поражения нервной системы – церебральный, цервикальный, поясничнокрестцовый, сочетанный и отдельная группа объединила пациентов с невротическими состояниями (табл. 1).
Таблица 1. Распределение пациентов в зависимости от уровня поражения нервной системы
|
Уровень поражения |
Количество больных |
|
|
абс. |
% |
|
|
Церебральный |
22 |
16,5 |
|
Цервикальный |
59 |
44,4 |
|
Пояснично-крестцовый |
31 |
23,3 |
|
Сочетанный |
18 |
13,5 |
|
Невротические состояния |
3 |
2,3 |
|
Всего |
133 |
100,0 |
Функциональное состояние мочевого пузыря и уретры по данным уродинамических исследований в зависимости от уровня поражения нервной системы представлено в таблице 2. Всем пациентам, распределенным по перечисленным выше группам, были выполнены ретроградная цистометрия и профилометрия уретры, в зависимости от результатов пациенты были распределены на тех, у кого были выявлены нормо-, гипер- и гипорефлексия, а также нормальный, повышенный и сниженный тонус, соответственно.
Лечение пациентов проводили с учетом функционального состояния мочевого пузыря и уровня (или очага) поражения нервной системы. Основное (фоновое) неврологическое лечение назначалось при участии невропатолога. При церебральных поражениях больным назначались препараты, улучшающие метаболизм нервной ткани и восстанавливающие в ней обменные процессы: витамины группы В, АТФ, ко-карбоксилаза, ноотропил (пирацетам, аминалон, энцефабол, церебро-лизин), глутаминовая кислота как препарат, улучшающий кислородный обмен, повышающий устойчивость нервной ткани к гипоксии, стимулирующий ее регенерацию. При наличии симптомов гиперактивности в качестве седативных препаратов назначали настойку валерианы или пустырника, глицин или тенотен детский.
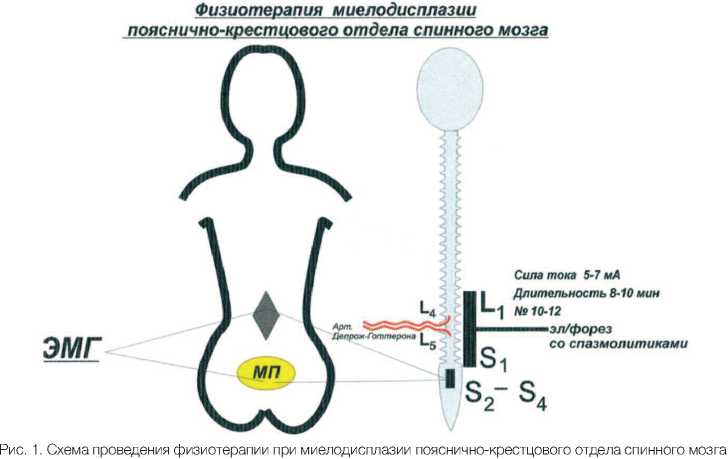
Проводились также различные физиотерапевтические процедуры и, прежде всего, электрофорез со спазмолитиками на различные отделы позвоночника и спинного мозга (рис. 1). У больных с клиникой родовой травмы шейного отдела позвоночника и позвоночных артерий электроды накладывались поперечно на верхне-шейный отдел позвоночника: один электрод на рукоятку грудины, другой – на шейнозатылочную область. В качестве спазмолитика использовали 1% раствор эуфиллина или 1% раствор никотиновой кислоты. Сила тока не превышала 5-7 мА, а длительность процедуры – не более 8-10 мин. Курс лечения состоял из 10-12 процедур. При поражении терминальных отделов спинного мозга электрофорез со спазмолитиками проводили с двух полей по продольной методике на область L1-Lv-S1, т. е. у места вхождения в спинно-мозговой канал артерии Депрож-Готте-рона (L1v-Lv). При поражении зоны поясничного утолщения электроды накладывали на уровне Dlx-Ll позвонков – зона кровоснабжения артерии Адамкевича, которая на уровне Dxl-Dx11 позвонков входит в спинномозговой канал.
После курса электрофореза со спазмолитиками на те же области назначали индуктотермию или па-рафин-озокеритовые аппликации – метод глубокого теплового воздействия на нервную ткань спинного мозга. Таким образом, после улучшения гемодинамики в пораженных сегментах спинного мозга методом электрофореза со спазмолитиками, глубокого прогревания индуктотер-мией или парафином заметно улучшались обменные процессы в нерв-
Таблица 2. Данные уродинамических исследований у больных с НДМП при различных уровнях поражения нервной системы
|
Данные уродинамических исследований |
||||||
|
Уровень поражения |
Ретроградная цистометрия |
Профилометрия уретры |
||||
|
нервной системы |
Нормо-рефлексия |
Гиперрефлексия |
Гипорефлексия |
Нормальный тонус |
Повышенный тонус |
Сниженный тонус |
|
Церебральный (n=22) |
5 (22,7%) |
17(77,3%) |
– |
5 (22,7%) |
17(77,3%) |
– |
|
Цервикальный (n=59) |
13(22%) |
46 (78%) |
– |
33 (56%) |
26 (44%) |
– |
|
Пояснично- крестцовый (n=31) |
3 (9,7%) |
– |
28 (90,3%) |
17(54,8%) |
– |
14(45,2%) |
|
Сочетанный (n=18) |
3 (16,7%) |
10(55,5%) |
5(27,8) |
3 (16,7%) |
10 (55,5) |
5(27,8%) |
|
Невротические состояния (n=3) |
1 (33,3%) |
2 (66,7%) |
– |
1 (33,3%) |
2(66,7%) |
– |
ной ткани. Одновременный прием ноотропных препаратов на фоне проводимой физиотерапии, на наш взгляд, постепенно приводит к регенерации пораженных участков спинного мозга (или их «созреванию» при миелодисплазии) и восстановлению функций иннервируемых ими органов.
При наличии спастических явлений в нижних конечностях, гипертонусе мышц тазовой диафрагмы назначали расслабляющий массаж мышц промежности и нижних конечностей, а при вялых парезах
этих мышц – тонизирующий массаж. При истинном сфинктерном недержании мочи (и кала) назначали лечебную гимнастику на укрепление мышц промежности по Кегелю. При проявлениях микцион-ной недостаточности (нарушение накопления и выведения мочи) – упражнения на укрепление мышц передней брюшной стенки с целью повышения абдоминального давления. Дифференцированно назначали препараты, нормализующие деятельность вегетативной нервной системы – при парасимпатикотонии назначали холинолитические препараты, а при дистонии вегетативной нервной системы – вегетотропные препараты. В лечении больных с незаторможенным мочевым пузырем (при парасимпатикотонии) использовали спазмекс по 2,5 мг 2 раза в сутки с 6-летнего возраста, продолжительность терапии составила 1 месяц.
Одновременно с фоновым (неврологическим) лечением проводили лечение, направленное на стабилизацию функции мочевого пузыря, профилактику и ликвидацию различных осложнений, возникших в результате как неврологических, так и урологических нарушений. При этом использовали консервативные и хирургические методы лечения. Характер симптоматической терапии зависел прежде всего от функционального состояния мочевого пузыря. Больным с гиперрефлексией детрузора назначали тепловые процедуры (парафин-озокеритовые аппликации) на надлобковую область, КВЧ-терапию или лазеротерапию на биологически активные точки (меридиан мочевого пузыря – V 2, V 14, V 19) и проекцию мочевого пузыря. Низкоинтенсивное лазерное облучение (гелий-неоновый лазер) дает хороший лечебный эффект и при непосредственном воздействии на мочевой пузырь (вну-трипузырное лазерное облучение). Применялся гелий-неоновый лазер с диаметром светового пятна 6-7 мс, плотностью мощности 1 МВт/см2, экспозиция составила 3,4,5,7,10,5,4,3 мин (возрастание и убывание), длительность курса лечения 10 дней. При таком воздействии лазера на мочевой пузырь восстанавливался регионарный кровоток, устранялась гипоксия детрузора, которая играет значительную роль в формировании гиперрефлексии мочевого пузыря [3].
Из фармакологических препаратов при гиперрефлексии мочевого пузыря пациентам назначали пика-милон (0,075-1,3 мг/кг) 3 раза в день в течение 30 дней, спазмекс по 2,5 мг 2 раза в день в течение 4 недель. Преимущество последнего препарата (в сравнении с дриптаном, дет-рузитолом и др.) в том, что он не проникает через гематоэнцефалический барьер и может назначаться уже с 6-летнего возраста (очень важно у детей с перинатальными поражениями головного мозга), что отражено в инструкции к препарату. Кроме того, спазмекс оказался весьма эффективным и при синдроме вторичного энуреза на фоне гиперрефлексии детрузора. Также пациентам ректально назначались свечи с красавкой (беладонной) курсом до 10 дней.
Больным с гипорефлексией детрузора и скрытой миелодисплазией пояснично- крестцового отдела спинного мозга проводилась электростимуляция мочевого пузыря. Для восстановления нормального мочеиспускания применяли высокую трансректалъную электростимуляцию мочевою пузыря. При этом активный электрод вводили на глубину 5-8 см в зависимости от возраста пациента, частота тока составляла 120 Гц, длительность импульса – 3 мс, продолжительность сеанса электролечения – 18-20 мин. Курс электролечения составил 10-12 дней. Из фармакологических препаратов этой группе больных назначали витамин В12 внутримышечно в сочетании с фолиевой кислотой per os в течение 10 дней, про-зерин в инъекциях или порошках в возрастной дозировке до 20-30 дней.
Больным с детрузорно-сфинктерной диссинергией и гипертонусом мышц урогенитальной диафрагмы назначали миорелаксанты: сир-далуд или мидокалм per os. Данные препараты подавляют полисинапти-ческие спинно-мозговые рефлексы и понижают повышенный тонус поперечно-полосатых мышц промежности. Расслабление поперечнополосатой мускулатуры тазового дна позволяло снизить повышенное уретральное сопротивление. Эффективность лечения контролировали с помощью ультразвукового исследования (УЗИ) мочевого пузыря до и после мочеиспускания, а также урофлоуметрии (УФМ) (фармакопроба с миорелаксантами) (рис 2, 3).
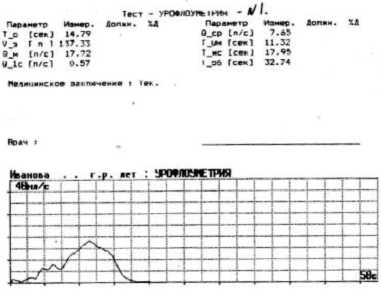
Рис. 2. Урофлоуметрия исходная у пациентов с детрузорно-сфинктерной диссинергией и гипертонусом мышц урогенитальной диафрагмы
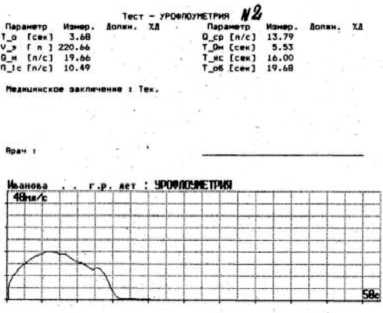
Рис. 3. Урофлоуметрия на фоне курсового приема мидокалма (через 30 мин после внутримышечного введения разовой дозы препарата: уменьшилось время задержки акта мочеиспускания и увеличилась максимальная и средняя скорость потока мочи)
При гипо- и арефлекторном мочевом пузыре у детей с грубой миелодисплазией терминальных сегментов спинного мозга применяли различные методы лечения, в том числе и только паллиативные, к ко- экспериментальная и клиническая урология № 4 2 0 1 8 торым относились принудительный ритм мочеиспускания и периодическая катетеризация мочевого пузыря. Принудительный ритм мочеиспускания с вовлечением мышц брюшного пресса (брюшной тип мочеиспускания) назначали во всех случаях при компенсированной микционной недостаточности.
Эффективность паллиативного лечения контролировали с помощью УЗИ мочевого пузыря до и после мочеиспускания. Если после натуживания и микции (иногда в 23 приема) остаточная моча не определялась или определялась в небольшом количестве (до 10-15% от исходного объема), то этот метод лечения считался приемлемым для данного пациента. Большую помощь в лечении подобных пациентов оказывали детские психологи, которые во время сеансов психотерапии давали пациентам «установку» на принудительный ритм мочеиспускания. В случаях неэффективности при больших объемах остаточной мочи (до 20-25% и более) проводили периодическую катетеризацию мочевого пузыря – у 6 (19,4%) детей из 31 с перинатальной патологией пояснично-крестцового отдела спинного мозга. Режим катетеризации назначали индивидуально (от 5 до 6 раз в течение дня). Таким образом, устранение Ее хронической задержки мочи, а следовательно, и ишемии детрузора позволяло предупредить развитие различных осложнений (пузырномочеточниковый рефлюкс, уретеро-гидронефроз, хронический пиелонефрит), которые в итоге приводят к развитию хронической почечной недостаточности (ХПН).
Показанием к хирургическому лечению НДМП, на наш взгляд, являются: резистентность к консервативной терапии и угроза быстрого развития ХПН. Предпочтение отдавалось малоинвазивным хирургическим вмешательствам. При гиперрефлекторной форме НДМП (10 детей) применяли методику гидродилатации мочевого пузыря «на утомляемость» (5-6 дилатаций на курс лечения), что приводило к увеличению объемов мочевого пузыря, первого и второго позывов при ци-стометрии на 30-35%. После введения в практику лечения НДМП фармакологических препаратов, снижающих тонус детрузор (дриптан, спазмекс), необходимость в подобных хирургических манипуляциях отпала. У больных с гипорефлектор-ной формой НДМП оперативные методы лечения применялись значительно чаще. При этом учитывались преобладающие клинические синдромы заболевания (хроническая задержка мочи, недержание мочи, сочетание этих симптомов), стадии микционной недостаточности и угроза развития ХПН. При выраженных нарушениях уродинамики верхних и нижних мочевых путей, чаще всего у детей оперированных по поводу спинномозговой грыжи, угрозе или уже развившейся ХПН больным накладывали цисто-кутанеостому (8 детей). В процессе длительной консервативной терапии периодически проводили контрольное обследование мочевыводящей системы (УЗИ 1 раз в 3 месяца, цистометрия 1 раз в 6 месяцев) в целях определения динамики заболевания. После восстановления рефлекторной деятельности мочевого пузыря (3 ребенка за время наблюдения в течение 3 лет) проводили иссечение и «закрытие» цисто-кутанестомы с последующим принудительным ритмом акта мочеиспускания. Одному больному с ис-
Таблица 3. Оперативные методы лечения и инвазивные вмешательства у детей с НДМП
|
Уровень поражения ЦНС |
Вид оперативного вмешательства |
Катетеризация мочевого пузыря |
Итого |
|
|
Цисто-кутанео-стомия |
Дилатация уретры |
|||
|
Церебральный (n=22) |
1 (4,5%) |
2 (9,1%) |
– |
3(13,6%) |
|
Цервикальный (n=59) |
3 (5,1%) |
– |
– |
3 (5,1%) |
|
Пояснично- крестцовый (n=31) |
8 (25,8%) |
4(12,9%) |
6 (19,4%) |
18(58,1%) |
|
Сочетанный (n=18) |
– |
1 (5,6%) |
– |
1 (5,6%) |
|
Невротические состояния (n=3) |
– |
1 (33,3%) |
– |
1 (33,3%) |
|
Всего (n =133) |
12 (9,0%) |
8 (6,0%) |
6 (4,5%) |
26 (19,5%) |
тинным (сфинктерным) недержанием мочи проведена операция пластики шейки мочевого пузыря по В.М. Державину с хорошими функциональными результатами.
При детрузорно-сфинктерной диссинергии и гипертонусе урогенитальной диафрагмы наряду с консервативной терапией у 7 больных проводили поднаркозную дилатацию мембранозной части уретры механическим уретродилататором (рис. 4).

При сопутствующих запорах выполняли пальцевую дилатацию анального сфинктера по Рекамье. У всех 7 больных после дилатации уретры на фоне проводимой консервативной терапии исчез повышенный тонус мышц тазового дна, о чем свидетельствовало снижение уретрального давления до нормальных цифр по данным профиломет-рии уретры и УФМ.
Виды оперативных вмешательств и манипуляций у больных с НДМП при различных уровнях поражения ЦНС представлены в таблице 3.
Таким образом, описанные выше комбинированные методы лечения различных клинических форм НДМП у детей позволили существенно улучшить результаты лечения (табл. 4).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Результаты лечения всех больных оценивались при катамнестиче-ском обследовании не ранее одного года после завершения этапного лечения. При этом учитывались жалобы больного, клиническая симптоматика, данные лабораторных исследований, УФМ, УЗИ почек и мочевого пузыря до и после мочеис-
Таблица 4. Результаты лечения 133 больных с НДМП через 1 год
|
Уровень |
Результат лечения |
||
|
поражения ЦНС |
Без динамики |
Улучшение |
Излечение |
|
Церебральный (n=22) |
– |
19(86,41%) |
3 (13,6%) |
|
Цервикальный (n=59) |
– |
45 (76,3%) |
14 (23,7%) |
|
Пояснично- крестцовый (n=31) |
– |
30 (96,8%) |
1 (3,2%) |
|
Сочетанный (n=18) |
– |
15 (83,3%) |
3 (16,7%) |
|
Невротические состояния (n=3) |
– |
2 (66,7%) |
1 (33,3%) |
|
Всего (n =133) |
– |
111 (83,5%) |
22 (16,5%) |
Таблица 5. Результаты лечения 133 больных с НДМП после завершения этапного лечения через 3 года
|
Уровень |
Результат лечения |
||
|
поражения ЦНС |
Без динамики |
Улучшение |
Излечение |
|
Церебральный (n=22) |
– |
14 (63,6%) |
8 (36,4%) |
|
Цервикальный (n=59) |
– |
29 (49,2%) |
30 (50,8%) |
|
Пояснично- крестцовый (n=31) |
– |
25 (80,6%) |
6 (19,4%) |
|
Сочетанный (n=18) |
– |
12 (66,7%) |
6 (33,3%) |
|
Невротические состояния (n=3) |
– |
1 (33,3%) |
2 (66,7%) |
|
Всего (n =133) |
– |
81 (60,9%) |
52 (39,1%) |
пускания. Инвазивные методы контрольной диагностики (микционная цистоуретрография, цистоуретро-скопия с калибровкой уретры) назначали строго по показаниям. Результаты лечения, полученные через 1 год в каждой из 5 клинических групп больных, отражены в таблице 4.
Последующее этапное лечение, проводимое курсами через 3 мес., позволило значительно улучшить вышеизложенные показатели. Результаты лечения через 3 года реабилитации больных отражены в таблице 5.
Наилучшие результаты лечения получены в группе больных с «высо- ким» уровнем поражения ЦНС и, прежде всего, у больных с последствиями родовой травмы шейного отдела позвоночника. Менее оптимистическими оказались результаты лечения больных энурезом и миелодисплазией пояснично-крестцового отдела спинного мозга.
ЗАКЛЮЧЕНИЕ
-
1. Лечение НДМП у детей и подростков должно проводиться индивидуально у каждого больного с учетом уровня и характера поражения нервной системы, а также функционального состояния мочевого пузыря и мышц урогенитальной диафрагмы.
-
2. При лечении НДМП у детей и подростков основной или базисной должна быть терапия первичного очага поражения нервной системы.
-
3. При антенатальных, диспла-стических поражениях нервной системы прогноз заболевания в плане полного выздоровления при проведении консервативной терапии, чаще всего, сомнительный, в связи с чем у этой группы пациентов целесообразно применять и оперативные (предпочтительнее малоинвазивные) методы лечения при наличии медицинских показаний к ним. Основой успешной реабилитации детей с НДМП должен быть принцип этапного лечения и преемственности этих больных при «передаче» их во взрослую сеть с постоянной и длительной диспансеризацией с участием врачей-специалистов смежных специальностей (уролога, нефролога, невропатолога).
Резюме:
Введение: Под нейрогенной дисфункцией мочевого пузыря (НДМП) следует понимать разнообразные формы нарушения его резервуарной и эвакуаторной функции, развивающиеся вследствие поражения нервной системы на ее различных уровнях – от коры головного мозга до интрамурального аппарата, до сих пор нет единого мнения об этиологии данного заболевания.
Цель исследования: обобщить результаты обследования и лечения 133 детей с нейрогенной дисфункцией мочевого пузыря (НДМП) в возрасте от 3 до 14 лет.
Список литературы Лечение нейрогенной дисфункции мочевого пузыря и вторичного энуреза у детей и подростков
- Билялов М.Г. Роль вегетативной нервной системы в генезе нейрогенной дисфункции мочевого пузыря по типу незаторможенности у детей и ее коррекция: автореф. дис. канд. мед. наук/М.Г. Билялов. Казань, 1998; 20.
- Бондаренко С.Г., Абрамов Г.Г. Этаноловая блокада при резистентной форме нестабильного мочевого пузыря у детей. Детская хирургия. 2004 (1):31-33.
- Вишневский Е.Л. Важнейшие итоги и перспективы исследований в урологии детского возраста. Е.Л. Вишневский, В.Г. Гельд//Российский вестник перинатологии и педиатрии. 2002(6); 44-48.
- Вишневский Е.Л. Диагностика и лечение нейрогенных дисфункций мочевого пузыря у детей. Педиатрия. 1997; 3: 42-44.
- Вишневский Е.Л. Клиническая оценка расстройств мочеиспускания. Е.Л. Вишневский, О.Б. Лоран, А.Е. Вишневский. М., 2001:95.
- Державин В.М., Вишневский Е.Л., Гусарова Т.Н. Диагностика и лечение нейрогенного мочевого пузыря у детей: Методическое пособие. Москва. 1993.
- Игнатьев Р.О. Эффективность малоинвазивных хирургических методов лечения расстройств эвакуаторной функции толстой кишки у детей с миелодисплазией: автореф. дис.. канд. мед. наук. Р.О. Игнатьев. М., 2003:20.
- Кириллов В.И. Нейрогенные дисфункции мочевого пузыря у детей. Кириллов В.И., Киреева Н.Г//РМЖ. 1998(9):7.
- Кольбе О.Б., Сазонов О.Н., Моисеев А.Б. и др. Сочетанные нарушения функции мочевого пузыря и толстой кишки у детей. Педиатрия. 2003; 6: 91-94.
- Морозов В.И., Ахунзянов А.А., Билялов М.Г., Байбиков Р.С. Неврологические аспекты диагностики нейрогенной дисфункции мочевого пузыря у детей. Детская хирургия, 2000(2):18-22.
- Морозов В.И., Рашитов Л.Ф. Энурез и нейрогенные дисфункции мочевого пузыря у детей: Метод. пособие. Казань. 2011: 59 c.
- Морозов В.И., Рашитов Л.Ф., Морозов Д.В. Нейрогенные дисфункции висцеральных органов у детей (хирургические и педиатрические аспекты). Казань. 2008: 152 c.
- Мохорт В.А., Гресь А.А. Лечение сочетанных неврогенных дисфункция мочевого пузыря и прямой кишки. Хирургия. 1985; 9: 57-61.
- Нестеренко О.В. Дифференцированный алгоритм лечения детей с первичным ночным энурезом. Нестеренко О.В., Горемыкин В.И., Елизарова С.Ю., Сидорович О.В. Современные проблемы науки и образования. 2013(2).
- Нестеренко О.В., Горемыкин В.И., Мещерякова Е,Е, Елизарова С.Ю., Сидорович О.В. Нарушения уродинамики у детей с вторичным хроническим пиелонефритом. Научное обозрение. Медицинские науки. 2014(2):82-82.
- Рудакова Э.А. Дисфункции мочевого пузыря у детей раннего возраста: автореф. дис. докт. мед. наук/Э.А. Рудакова. М., 1995:28.
- Салов П.П. Нейрогенные дисфункции тазовых органов. П.П. Салов. Новокузнецк, 2002:592.
- Albright L., Pollcck E., Adelson P.D. Principles and Practice of Pediatric Neurosurgery. New York. 1999: 291-320.
- Function of Hollow Viscera in Children with Constipation and Voiding Difficulties. C. Lucanto, S.B. Bauer, P.E. Hyman, A.F. Flores. Dig Dis Sci 2000;45,(7):1274-1280.
- Sturm M., Cheng Y. The Management of the Pediatric Neurogenic Bladder. 2016. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4992015/
- Vega, PJ.M. High-pressure bladder: an underlying factor mediating renal damage in the absence of reflux?/PJ.M. Vega, L.A. Pascual. BJU Jnt. 2001;(86);6:581-584.


