Лечение последствий переломов диафиза плечевой кости с использованием различных методов стимуляции костеобразования в условиях стабильной фиксации отломков
Автор: Барабаш Анатолий Петрович, Гражданов Константин Александрович, Барабаш Юрий Анатольевич, Балаян Вардан Дживанширович
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 2, 2012 года.
Бесплатный доступ
Представлены результаты хирургического лечения 39 пациентов с последствиями переломов диафиза плечевой кости. Приводится описание и оценка клинической эффективности разработанных новых методов стимуляции костеобразования в условиях стабильной фиксации отломков при реабилитации больных с несросшимися переломи и ложными суставами плечевой кости.
Плечевая кость, последствия переломов, стимуляция костеобразования, ложный сустав, несросшийся перелом
Короткий адрес: https://sciup.org/142121555
IDR: 142121555
Treatment of the consequences of humeral shaft fractues using different techniques of osteogenesis stimulation under stable fixation of fragments
The results of surgical treatment of 39 patients with consequences of humeral shaft fractures are presented in the work. The description and evaluation of the clinical effectiveness of the new developed techniques of osteogenesis stimulation under stable fixation of fragments are demonstrated during rehabilitation of patients with humeral non-united fractures and pseudoarthroses.
Текст научной статьи Лечение последствий переломов диафиза плечевой кости с использованием различных методов стимуляции костеобразования в условиях стабильной фиксации отломков
Переломы диафиза плеча – широко распространенный вид травмы скелета. Общее количество переломов плечевой кости среди всех переломов длинных трубчатых костей достигает 13,5 %, при этом на долю переломов диафиза приходится от 14,4 до 72 % и наблюдаются они преимущественно у лиц трудоспособного возраста от 20 до 50 лет [1].
Приоритет в реабилитации пациентов с данным видом травм в настоящее время отдается хирургическим методам лечения. Несмотря на значительные успехи современной оперативной травматологии, достигнутые за последнее время в лечении диафизарных переломов плечевой кости, хирурги в своей практической деятельности нередко встречаются с осложнениями переломов: замедленной консолидацией и ложными суставами.
Лечение больных с несросшимися переломами и ложными суставами длинных костей представляет наибольшие трудности в современной травматологии. Удельный вес больных с ложными суставами и дефектами среди других повреждений опорно-двигательного аппарата составляет от 15,7 до 57,6 % [2]. Замедленное сращение и ложные суставы пле- чевой кости встречаются в 12,5 % случаев ложных суставов другой локализации [2]. Преимущественно ложные суставы плечевой кости встречаются в средней (52,3 %) и нижней трети (31,6 %) диафиза плечевой кости. Ведущими факторами в патогенезе замедленной консолидации являются ухудшение кровоснабжения и стойкие гемоциркуляторные нарушения в поврежденном сегменте.
Многообразие методик оперативного лечения ложных суставов и дефектов диафиза плечевой кости до настоящего времени не решило проблему повышения регенераторной способности костных структур [3]. Поэтому разработку и использование эффективных, щадящих методов регуляции репаративной остеорегенерации, особенно на начальных этапах ее нарушения, следует признать оправданными и перспективными.
Целью исследования явилась оценка апробированных в клинике предложенных нами новых методов стимуляции костеобразования при хирургическом лечении несросшихся переломов и ложных суставов плечевой кости.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Объектом исследования явились 39 пациентов с несросшимися переломами, ложными суставами и дефектами диафизарной части плечевой кости, которым проведено оперативное лечение в отделе- нии острой травмы и реконструктивной хирургии СарНИИТО за период с 2005 по 2010 год включительно. Среди пациентов большинство составили женщины – 21 (54,8 %) в возрасте от 28 до 65 лет и
18 (46,2 %) мужчин в возрасте от 23 до 57 лет.
Большинству пациентов (33 – 84,6 %) с последствиями переломов диафиза плечевой кости, которым ранее выполняли хирургические вмешательства по поводу острых переломов плечевой кости, для фиксации отломков применяли в 21 случае накостные пластины, в 5 случаях – аппараты внешней фиксации и у 7 пациентов – интрамедуллярные стержни. В 6 (15,4 %) клинических наблюдениях до поступления в нашу клинику оперативные вмешательства не проводились.
У 27 пациентов наличие ложных суставов плечевой кости сопровождалось облитерацией костномозгового канала и дефектом костной ткани на протяжении от 0,5 до 60 мм. В 12 наблюдениях выявлены несросшиеся или замедленно срастающиеся переломы диафиза плечевой кости.
Все больные были прооперированны с вмешательством в зоне патологии.
При оперативном лечении несросшихся переломов выполнялась ревизия места перелома с экономной резекцией отломков, удаление металлической конструкции при ее наличии и восстановление проходимости костномозгового канала на всем протяжении. Для фиксации перелома наиболее часто использовались интрамедуллярные стержни с блокированием (9 пациентов) или спице-стержневой аппарат (3 пациента), а для стимуляции костеобразования – продольная остеотомия концов отломков. Перед продольной остеотомией производилась отслойка надкостницы выше и ниже зоны несрос-шегося перелома длиной не более 3 см, затем проводилось продольное рассечение концов отломков через патологическую зону в двух взаимно перпендикулярных плоскостях, таким образом создавался дополнительный очаг костеобразования (патент РФ № 2181267, приор. от 18.03.99 г.). Отслойка надкостницы выше и ниже зоны ложного сустава или несращение длиной не более 3 см усиливали васкуляризацию, вызывали формирование новых периостально-медуллярных сосудистых связей и улучшали трофику сегмента конечности в целом. Выполнение продольного рассечения кости через патологическую зону после отслойки надкостницы и обоих отломков в двух взаимно перпендикулярных плоскостях позволяли создать четыре васкуля-зированных несвободных трансплантата на каждом отломке, что приводило к увеличению регионарного кровотока в 3,6 раза [4].
Тактика оперативного лечения при наличии ложного сустава плечевой кости определяется наличием и величиной дефекта костных структур. Для замещения дефекта использовалась как аутокость, губчатые трансплантаты, забиравшиеся из гребня подвздошной кости, так и кортикальные или губчатые аллотрансплантаты.
При использовании аутокости применялась новая технология костной пластики: после поднадкостничного выделения зоны ложного сустава дефективный участок кортикального слоя обоих отломков обрабатывали до кровоточащей кости. На обработанный участок кортикального слоя отломков накладывали губчатый аутотрансплантат и выполняли в нем сквозные отверстия, проходящие через трансплантат и кость. Фиксировали трансплантат к своему ложу лигатурами, проведенными вокруг кости. Отломки фиксировали в чрескост-ном аппарате или интрамедуллярным стержнем с блокированием (патент РФ № 2383309, приор. от 24.09.2008 г.). Обработка дефективного или измененного участка кортикального слоя обоих отломков до кровоточащей кости позволяла восстановить кровоснабжение кортикального слоя кости. Наложение на обработанный участок кортикального слоя губчатого трансплантата и выполнение в нем отверстий, достигающих костномозговой полости, восстанавливало сообщение костномозговой полости с надкостницей, стимулируя образование множественных периостально-медуллярных анастомозов, улучшающих питание трансплантата как стороны надкостницы, так и костномозгового канала. Имплантированный в краевой дефект трансплантат васкуляризуется и является в зоне ложного сустава своеобразным донором солей, белков и минералов. Подшивание трансплантата к кортикальному слою кости способствовало дополнительной фиксации отломков и плотному прижатию трансплантата к сформированному ложу.
Четырем больным с ложными суставами в форме дефекта плечевой кости на протяжении от 40 до 60 мм выполнено замещение губчатыми аутотрансплантатами с формированием продольного канала для интамедуллярного стержня.
Для сохранения величины отломков при их склерозе прибегали к искусственной реконструкции Гаверсовой системы в концах отломков (заявка на выдачу патента РФ № 2010121613, приор. от 27.05.2010 г.). Со стороны торцевой поверхности отломков по всему периметру их кортикального слоя на протяжении участка поврежденной кости с увеличенной площадью формировали сеть сквозных косых каналов, веерообразно расходящихся от зоны ложного сустава в сторону периоста и соединяющихся с костномозговым каналом, для восстановления утраченной вследствие склероза сосудистой сети, что, в свою очередь, приводило к нормализации минерального обмена и сращению кости.
Как один из методов стимуляции костной регенерации использовалась трансплантация костного мозга в зону патологии (патент РФ № 2375006, приор. от 25.07.2008 г.). После ревизии и обработки зоны ложного сустава или несросшегося перелома диафиза плечевой кости перед введением интрамедуллярного стержня в обоих отломках на расстоянии 5-30 мм от их концов выполняли сквозные поперечные каналы под углом 45° к грани стержня. После введения в костномозговую полость стержня Fixion из-за увеличивающегося давления происходило выдавливание (трансплантация) костномозгового содержимого в зону повреждения. Миграция содержимого костномозгового канала в зону патологии профилактирует сосудистый блок и позволяет избежать жировой эмболии.
Диагностика и контроль заживления костной раны были клинико-рентгенологическими. Исходы оценивали по системе СОИ-1 [6].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Результаты лечения прослежены у всех пациентов в сроки от 6 месяцев до 5 лет. Добиться консолидации удалось у всех пациентов с несрос-шимися переломами диафиза плечевой кости (12 пациентов) в сроки от 4 до 8 месяцев. Исходы лечения по системе СОИ – 1 составили 74-92 % от анатомо-функциональной нормы.
У больных с ложными суставами (27 пациентов) удалось добиться сращения в 24 случаях в сроки от 6 месяцев до 1 года. Оценка результатов лечения по системе СОИ-1 укладывалась в диапазон 68-90 % от анатомо-функциональной нормы. У трёх пациентов предприняты повторные оперативные вмешательства после интрамедуллярного остеосинтеза. Для компрессии в зоне ложного сустава накладывался аппарат внешней фиксации до момента появления рентгенологических признаков сращения в зоне патологии.
Для иллюстрации исходов оперативного лечения пациентов с последствиями травм диафиза плечевой кости приводятся клинические примеры хирургической реабилитации 2-х больных, ранее оперированных в других стационарах и поступивших к нам в различные сроки после первичного остеосинтеза.
Клинический пример № 1. Больная С., 28 лет. Диагноз: ложный сустав левой плечевой кости на уровне средней и нижней третей диафиза с краевым дефектом костной ткани. Состояние после накостного остеосинтеза. Поступила в СарНИИ-ТО через 4 месяцев после первичной операции с жалобами на боли в области нижней трети плеча, ограничение функции левой верхней конечности, на фоне болевого синдрома сформировалась контрактура в локтевом суставе (сгибание/разгибание 110-120°/0/50-60°; пронация/супинация 80°/0/80°) (рис. 1).
После обследования больной предпринято оперативное вмешательство - удаление металлической конструкции, ревизия ложного сустава, при ревизии патологической зоны у пациентки отмечено закрытие костномозгового канала в обоих отломках, значительный краевой дефект диафиза площадью 4×2 см (на рисунке 1 обозначен стрелкой) по наружной поверхности в зоне прилегания пластины к кости. Учитывая вышеизложенное, после восстановления проходимости костномозговой полости для стимуляции процессов регенерации костной ткани выполнена продольная остеотомия отломков, для фиксации ложного сустава использован интрамедуллярный стержень с блокированием, краевой костный дефект заполнен губчатым аутотрансплантатом из крыла подвздошной кости. Послеоперационный период протекал без осложнений. Дополнительная фиксации в косыночной повязке в течение двух недель, затем лечебная физкультура для суставов левой верхней конечности.
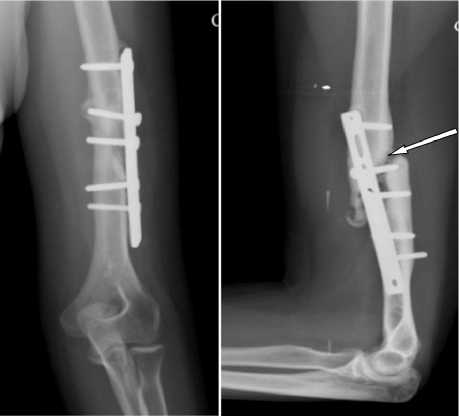
Рис. 1. Рентгенограммы плечевой кости больной С. в прямой и боковой проекциях через 4 месяца после остеосинтеза пластиной
На рисунке 2 представлена контрольная рентгенография плечевой кости через 4 месяца после повторного остеосинтеза. Сращение в зоне ложного сустава удовлетворительное, костный аутотрансплантат, введенный в зону краевого дефекта, на стадии перестройки (обозначен стрелкой). Жалоб больная на момент контрольного осмотра не предъявляла, движения в суставах оперированной конечности в полном объеме. Оценка результата лечения по системе СОИ-1 – 92 % от анатомо-функциональной нормы (рис. 2).
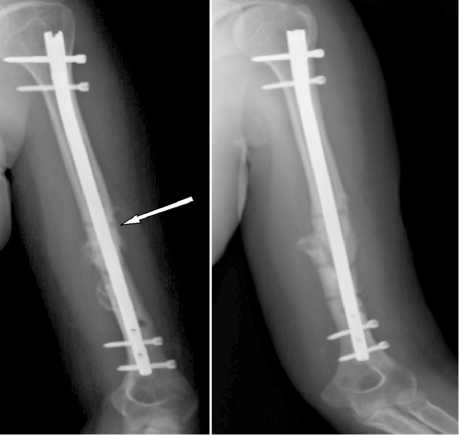
Рис. 2. Рентгенограммы плечевой кости больной С. через 4 месяца после реконструктивно-пластической операции фиксации отломков блокирующимся интрамедуллярным стержнем
Клинический пример № 2. Больная К., 40 лет. Диагноз: ложный сустав правой плечевой кости на уровне средней трети диафиза. Состояние после накостного остеосинтеза перелома плечевой кости. Поступила в СарНИИТО через 6 месяцев после первичной операции с жалобами на боли в правом плече, деформацию сегмента, нарушение функции правой верхней конечности. Проведенное рентгенологическое обследование, данные компьютерной томографии сегмента подтвердили наличие склероза в области концов отломков на протяжении 30 мм, что также было обнаружено и при ревизии ложного сустава (рис. 3).
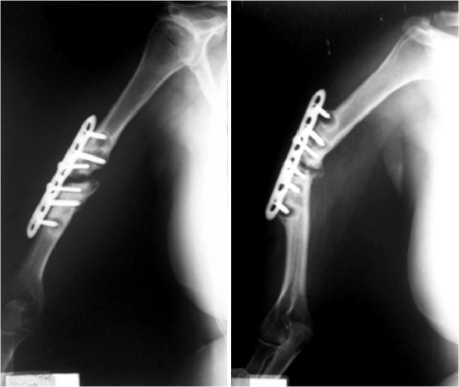
Рис. 3. Рентгенограммы правой плечевой кости больной
К. через 6 месяцев после остеосинтеза пластиной
Больной выполнена операция – удаление металлической конструкции, ревизия ложного сустава. Наличие склероза концов отломков предопределило дальнейший алгоритм оперативного вмешательства: было выполнено продольное и поперечное засверли-вание концов обоих отломков (искусственное восстановление Гаверсовой системы), интрамедуллярный остеосинтез стержнем системы «Fixion», трансплантация костного мозга в зону патологии.
При контрольном осмотре через четыре месяца было отмечено замедленное сращение, но это и не удивительно – для реваскуляризации склеротически измененных концов отломков необходимо время. Че- рез четыре месяца после операции пациентка приступила к работе медсестрой в детском санатории г. Ессентуки.
На рисунке 4 представлена контрольная рентгенография плечевой кости через 8 месяцев после повторного остеосинтеза. Отмечено сращение ложного сустава. При клиническом осмотре жалоб больная на момент контрольного осмотра не предъявляла, сохранялось умеренное ограничение движений в плечевом и локтевом суставе. Оценка результата лечения по системе СОИ-1 – 88 % от анатомо-функциональной нормы. Если бы в этом случае была выполнена резекция концов отломков в пределах 6-7 см, то сращение бы наступило в сроки 4-5 месяцев. В последующем необходимо бы было выполнять удлинение плечевого сегмента, что потребовало бы минимум полгода (рис 4).
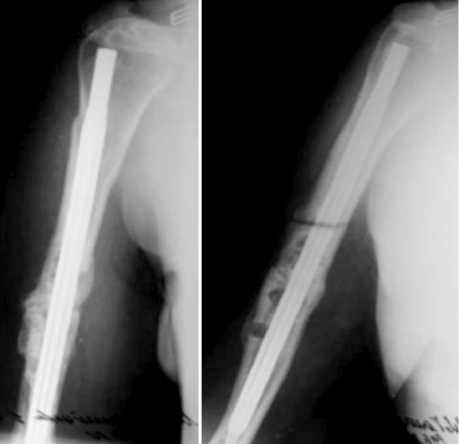
Рис. 4. Рентгенограммы правой плечевой кости больной К. через 8 месяцев после реконструктивной операции и фиксации отломков интрамедуллярным стержнем системы «Fixion IM»
ЗАКЛЮЧЕНИЕ
Проведенный анализ исходов лечения показал, что использование дополнительной стимуляции регенерации костной ткани является необходимым и обязательным элементом оперативного вмешательства при хирургическом лечении последствий переломов диафиза плечевой кости. Выполнение продольной остеотомии концов отломков по разработанной технологии в сочетании с прочной фиксацией отломков является эффективным способом стимуляции процессов остеорепарации. Для максимального эффекта от выполняемой костной пластики при замещении дефектов диафиза плечевой кости необходима дополнительная обработка костного трансплантата с целью его интеграции с реципиент-ной зоной. Продольное и поперечное засверливание концов отломков благоприятно сказывается на заживлении костной раны и должно использоваться как один из элементов хирургической реабилитации больных с несросшимися переломами и ложными суставами диафизарной части плечевой кости. Этот прием позволяет избежать обширных резекций кон- цов отломков, максимально сохранить величину сегмента конечности, кроме этого, создание дополнительного очага костеобразования в зоне патологии приводит к активизации репаративного процесса. Устойчивая фиксация отломков позволяет не только избежать дополнительной иммобилизации, но и в ранние сроки начать реабилитационные мероприятия, направленные на восстановление функции суставов поврежденной конечности.
Исходы лечения 39 пациентов с несросшимися переломами и ложными суставами, в том числе с дефектом костной ткани, составили от 68 до 92 %. Нижний предел реабилитации (68 % от анатомофункциональной нормы) был зафиксирован у 2-х пациентов за счет ограничения функции в суставах поврежденного сегмента, так как пациенты поступали к нам через продолжительные сроки после начала лечения в других стационарах. У большинства пациентов восстановление анатомо-функциональных показателей по системе СОИ-1 было 89±5 %.


