Локальные инграоперационные и ранние послеоперационные осложнения эндопротезирования тазобедренного сустава
Автор: Волокитина Елена Александровна, Зайцева Ольга Павловна, Колотыгин Денис Анатольевич, Вишняков А.А.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 3, 2009 года.
Бесплатный доступ
Приведены данные по наиболее часто встречающимся локальным интра- и послеоперационным осложнениям эндопротезирования тазобедренного сустава. Из 1096 случаев имплантаций эндопротезов тазобедренного сустава локальные осложнения легкой и средней степени тяжести получены в 3,9 % (некроз краев раны - 0,9 %, гематома послеоперационной раны -1,0 %, лигатурный свищ - 0,2 %, переломы большого вертела - 0,7 %, переломы диафиза бедра в верхней трети - 0,2 %, вывих головки протеза - 0,4 %, нейропатия седалищного нерва по малоберцовому типу - 0,3 %, нейропатия бедренного нерва - 0,3 %), локальные тяжелые - в 2,8 % (тотальная асептическая нестабильность эндопротеза - 2,1 %, тотальная инфицированная нестабильность - 0,7 %). Проанализированы причины возникновения локальных интраоперационных осложнений и осложнений ближайшего послеоперационного периода, приведены меры их профилактики и оптимальные методики лечения.
Эндопротез, тазобедренный сустав, ошибки и осложнения эндопротезирования, вывих головки протеза, околопротезный перелом, гематома, нейропатия
Короткий адрес: https://sciup.org/142121235
IDR: 142121235 | УДК: 616.728.2-007.248-089.844:
Local intraoperative and early postoperative complications after endoprostheses of the hip
The data on the most common local intra- and postoperative complications after endoprosthetics of the hip are reported. Among 1096 cases of the hip endoprostheses implantations the local complications of slight and medium severity developed in 3,9 % of the cases (wound edge necrosis - 0,9 %, postoperative wound hematoma - 1,0 %, ligature fistula -0,2 %, fractures of the greater trochanter - 0,7 %, femoral diaphyseal fractures of the upper third - 0,2 %, prosthesis head dislocation - 0,4 %, sciatic nerve neuropathy of fibular type - 0,3 %, femoral nerve neuropathy - 0,3 %), and those of high severity were observed in 2,8 % of the cases (endoprosthesis total aseptic instability - 2,1 %, total infected instability - 0,7 %). The causes of local intraoperative and early postoperative complications have been analyzed, the measures for their prevention and optimal treatment techniques have been reported.
Текст научной статьи Локальные инграоперационные и ранние послеоперационные осложнения эндопротезирования тазобедренного сустава
Наиболее эффективным хирургическим методом лечения тяжелой патологии тазобедренных суставов на сегодняшний день является эндопротезирование, которое позволяет в короткие сроки достигнуть высокого реабилитационного эффекта и существенно повысить качество жизни больных. Однако накопленный за последние годы коллективный клинический опыт применения операций по имплантации искусственных суставов позволил судить не только о преимуществах, но и недостатках этого вида лечения, осложнения которого отличаются особой тяжестью [1, 3, 9]. Если проблема качества эндопротезов практически решена за счет широкого внедрения на российский рынок импортных изделий, отличающихся высокой технологией изготовления, то риск внутри- и по- слеоперационных осложнений самого метода остается высоким – от 4,8 до 10 % [2, 5, 6]). Несмотря на законодательно определенные и рекомендованные для внедрения стандарты лечения больных с патологией тазобедренного сустава методом эндопротезирования (Приказ Министерства здравоохранения и Социального развития России № 516 от 11.08.05 об утверждении стандарта медицинской помощи больным кок-сартрозом), процедуры предупреждающих действий ошибок и осложнений разработаны не в полной мере, последовательность их проведения по лечебным этапам не определена. Целью данной работы явилась разработка мер профилактики локальных интраоперационных и ранних послеоперационных осложнений эндопротезирования тазобедренного сустава.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Данная работа выполнялась на базе ортопедического отделения № 7 ФГУ РНЦ «ВТО» им. акад. Г.А. Илизарова и травматологического отделения «Окружной больницы «Травматологический центр» г. Сургута. Исследование базируется на анализе ближайших (до 1 года) и отдаленных (от 1 года до 7 лет) результатов лечения 956 больных (1096 имплантаций) с тяжелой патологией тазобедренного сустава приобретенного и врожденного генеза, пролеченных методом эндопротезирования в период с 2001 по 2007 год включительно, из них мужчин – 434, женщин – 522. Возраст первично прооперированных пациентов колебался от 15 до 85 лет (в среднем 51,3±12,9 года). Преобладающее большинство (723 – 75,6 %) составили лица наиболее трудоспособного возраста – от 21 до 60 лет, на момент поступления в клинику 657 (68,7 %) из них были нетрудоспособными инвалидами.
Использовались статистический, клинический, рентгенологический, ультразвуковой, физиологический (электромиография) методы исследования. Результаты исследований обработаны общепринятыми статистическими методами.
Основным показанием для первичного эндопротезирования тазобедренного сустава явился двусторонний обменно-дистрофический коксар-троз (26,8 %), односторонний посттравматический коксартроз (26,2 %) и односторонний диспласти-ческий коксартроз (20,5 %). У 782 (81,7 %) пациентов, обратившихся для лечения методом эндопротезирования, была диагностирована III стадия, у 174 (18,3 %) пациентов – IV стадия остеоартроза (ОА). Всего 956 больным было выполнено 1096 первичных имплантаций тазобедренных суставов. Эндопротезирование одного тазобедренного сустава было выполнено 796 (72,6 %) больным. Эндопротезирование обоих тазобедренных суставов выполнено 150 (27,4 %) больным, причем у 38 (3,5 %) больных эндопротезирование правого и левого тазобедренных суставов было выполнено в один операционный день.
Известные системы изучения результативности метода эндопротезирования (шкала W.H. Harris (1969) [10], анкета «ВОЗ КЖ-100» [8]) рассчитаны на оценку функции тазобедренного сустава в отдаленные сроки, когда последствия случившихся интра- и послеоперационных локальных осложнений уже купированы, а информация о допущенных ошибках становится не актуальной и теряется. Поэтому для выявления всех осложнений лечебно-диагностического процесса нами была применена собственная система оценок результатов лечения (хорошо, удовлетворительно, неудовлетворительно), основанная на тщательном анализе течения ближайшего послеоперационного периода.
Оценка «хорошо» подразумевала отсутствие интра- и послеоперационных осложнений, восстановление безболезненной функции сустава в первый месяц, нормализацию походки на 6-й месяц после имплантации. Оценка «удовлетворительно» допускала наличие внутри- и послеоперационных осложнений легкой и средней степени тяжести, не повлекших за собой реимплантацию или удаление эндопротеза, функция сустава восстанавливалась через 3-6 месяцев, походка нормализовалась или оставалась легкая хромота спустя 6-9 месяцев после операции. «Неудовлетворительно» оценивались все случаи с тяжелыми общими (ТЭЛА, острая сердечно-сосудистая недостаточность и т.д.) и тяжелыми локальными (асептическая или инфицированная нестабильность протеза) осложнениями, повлекшими за собой летальный исход или повторное оперативное вмешательство по замене эндопротеза.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Ближайшие результаты первичных имплантаций тазобедренного сустава распределились следующим образом: хорошо - 1017 (92,7 %), удов- летворительно - 46 (4,3 %), неудовлетворительно - 33 (3,0 %). Группа с осложнениями составила 79 клинических случаев. Наиболее часто ослож- нения встречались у больных от 41 до 70 лет - 63 пациента (79,7 %). Локальные осложнения преобладали у пациентов в возрасте от 41 до 50 лет, чаще проявлялась нестабильность компонентов эндопротеза, что мы объясняем активным физическим образом жизни.
По тяжести проявления локальные осложнения, относящиеся непосредственно к зоне имплантата (вывих, околопротезный перелом, гематома, нейропатия бедренного или седалищного нервов, изнашивание, нестабильность компонентов протеза), мы разделили на обратимые (легкие, средние) и необратимые (тяжелые); по ин-фицированности – на асептические и септические (поверхностное и глубокое инфицирование); по времени проявления – на интраоперационные, ранние и поздние послеоперационные [4, 7]).
Среди локальных осложнений легкой и средней степени тяжести были отмечены следующие: послеоперационный некроз краев раны – 10 (0,9 %), гематома, требующая ревизии раны – 11 (1,0 %), вывих головки протеза – 4 (0,4 %), интраоперационный перелом большого вертела – 8 (0,7 %), перелом диафиза бедра в верхней трети – 2 (0,2 %), и лигатурный свищ – 2 (0,2 %). Нейропатия седалищного нерва по малоберцовому типу развилась в 3 случаях (0,3 %), нейропатия бедренного нерва – у 3 больных (0,3 %). Клинические проявления всех локальных осложнений легкой и средней степени тяжести были купированы в ближайшем послеоперационном периоде.
К необратимым (тяжелым) локальным осложнениям относили нестабильность протеза, как асептическую – 23 (2,1 %), так и инфицированную – 8 (0,7 %), развившуюся в сроки до 5 лет. Случаи нестабильности эндопротезов, за исключением рецидивирующих вывихов головки протеза (4), в данной работе мы не анализировали, уделяя основное внимание локальным интраоперационным и ранним послеоперационным осложнениям.
Некроз краев раны. Некроз краев раны в послеоперационном периоде был отмечен в 10 случаях и был обусловлен продолжительностью операции свыше двух часов; провоцирующими факторами явились рубцовые изменения мягких тканей в проекции разреза вследствие ранее выполненных операций, чрезмерно развитый подкожно жировой слой и сахарным диабет как сопутствующее заболевание. Для лечения такого осложнения назначали инфузионную терапию с ангиопротекторами (Актовегин 10,0 мл (160 мг) на 200 мл физиологического раствора внутривенно № 5, Трентал 100 мг на 200 мл физиологического раствора внутривенно № 5). На перевязках при наличии признаков подкожной гематомы края раны расширяли зондом, эвакуировали гемморагическое содержимое из подкожно-жирового слоя, на область послеоперационного шва накладывали гель Актовегина –
20 %. При отсутствии эффекта от консервативной терапии участок некроза иссекали под местной инфильтрационной анестезией 0,5 % раствором новокаина, в пределах здоровых тканей. На кожу накладывали узловые адаптированные петлеобразные швы по Данати. Для снижения вероятности возникновения некроза кожи доступ к суставу выполняли вне имеющихся старых рубцов или же их иссекали. Во время длительной операции периодически ослабляли натяжение мягких тканей и перемещали тазовый («Большой Хоман») и бедренный защитники («Кобра») на другие участки кожного покрова.
Гематома послеоперационной раны . Гематома послеоперационной раны как одно из осложнений ближайшего послеоперационного периода наблюдалась в шести случаях 11 (1,0 %) вследствие недостаточного гемостаза во время ушивания раны и неадекватного ее дренирования. Локализовались гематомы, как правило, в пустотных пространствах, которые образуются при иссечении утолщенной дегенеративной капсулы, остеофитов и патологических рубцовых тканей вокруг сустава - это область вокруг шейки эндопротеза, подфасциальное надмышечное пространство и надфасциальное пространство. Симптомами гематомы являются общее повышение температуры до 37,2-38º, озноб в вечернее и ночное время, а также локальные боли, отек и гиперемия кожного покрова в области послеоперационного шва. В отдельных случаях через швы из раны отделялась сукровичная жидкость.
Для дифференциальной диагностики локального и общего воспалительного процесса использовали ультразвуковой метод. Исследование проводили в В-режиме на ультразвуковом аппарате «SONOLINE» SI-450 фирмы «SIЕMENS» (Германия) линейным датчиком с частотой 7,5 Мгц; изучали состояние околосуставных тканей, капсулы, мышц бедра. На вторые – третьи сутки после имплантации гематома в области послеоперационной раны рассматривается нами как нормальное явление. В этот период гематома идентифицировалась как гомогенное эхонегативное очаговое образование, располагающееся вокруг шейки бедренного компонента протеза, под- или надфасциально (рис. 1). В этот период рана активно дренировалась двумя дренажными трубками: под шейкой протеза и под ушитой широкой фасцией бедра над мышцами. Третья трубка устанавливалась в случаях выраженного подкожно-жирового слоя и дренировала надфасциальное пространство. При адекватном дренировании гематома с каждым днем уменьшалась в объеме, до полного рассасывания. На четвертые-шестые сутки после операции в гематоме начинали определяться кровяные сгустки, которые визуализировались в виде эхопозитивных включений. На 7-8-е сутки начинался обратный процесс - лизис сгустков крови, и содержимое гематомы вновь становилось эхонегативным.

Обнаружение гомогенного эхонегативного очагового образования вокруг шейки протеза или в подфасциальном пространстве на 9-10-е сутки после операции, в совокупности с локальными и общими клиническими признаками, свидетельствовало о необходимости эвакуации гематомы аспирационным или хирургическим путем. После уточнения ее размеров и локализации под контролем УЗИ зондом расширяли края раны и эвакуировали содержимое, накладывали асептическую повязку и продлевали курс антибактериальной терапии до 10 дней. При выраженном болевом синдроме, отечности бедра в верхней трети, гиперемии кожного покрова и пастозности мягких тканей в области послеоперационного шва выполняли ревизию раны в условиях операционной. Снимали швы, разводили края раны, устанавливали специальный защитник за тазовую кость для лучшей визуализации раны, тщательно ее промывали физиологическим раствором и антисептиками, удаляя все сгустки и некротические ткани. После тщательного гемостаза рану повторно дренировали и ушивали. Больному рекомендовали соблюдать постельный режим в течение 5-7 дней. Содержимое гематомы в обязательном порядке исследовали микробиологически. При наличии роста микроорганизмов меняли антибиотик в зависимости от определенной чувствительности, проводили повторный курс антибиотикотерапии.
Нейропатии. В нашем исследовании неврологические осложнения возникли в шести случаях (0,5 %): нейропатия бедренного нерва – 3 случая, нейропатия седалищного нерва по малоберцовому типу - 3 случая. Причинами таких осложнений явилась сама операционная травма, вызывающая локальный отек мягких тканей и сдавливание (компрессию) отечными тканями нервных стволов (особенно у больных с невыраженным подкожножировым и мышечным слоем). Кроме того, технология эндопротезирования тазобедренного сустава предусматривает такой обязательный элемент, как тракция бедра при пробном и окончательном вправлении головки протеза во впадину, которая может при чрезмерных усилиях вызвать ишемию нервного ствола.
В случаях, когда неврологические нарушения возникали непосредственно после завершения оперативного вмешательства, осложнение расценивали как острая тракционная нейропатия. Когда неврологическая симптоматика проявлялась в течение первых двух-трех суток после завершения операции, осложнение расценивали как отсроченная нейропатия, обусловленная компрессией и ишемией нерва в результате отека и гематомы в области мягких тканей. При появлении первых признаков нейропатии назначали анальгетические, спазмолитические, антигипоксантные, антиоксидантные медикаментозные средства; применялись также мембранопротектеры, антиагреганты и биостимуляторы. Схема комплексного лечения, разработанная в РНЦ «ВТО», представлена следующими препаратами: Трамадол 1 мл (100 мг) до 3 раз в день № 3, затем Трамадол по 1 таблетке 2 раза в день № 4; Актовегин 10,0 мл (160 мг) × 200 мл физиологического раствора внутривенно № 5, затем по 1 таблетке (200 мг) 2 раза в день № 20; Мидокалм 1 мл (100 мг) 1 раз в сутки внутривенно № 5, затем по 1 таблетке (150 мг) 2 раза в день до купирования спастических явлений; Мильгамма 2 мл 1 раз в день № 5, затем по 1 таблетке (100 мг) 1 раз в день № 30, или Нейромультивит по 1 таблетке 3 раза в день № 30. С десятых суток от начала медикаментозной терапии назначали Нейромидин 1 мл (15 мг) 2 раза в день внутримышечно № 14, затем по 1 таблетке (20 мг) 2 раза в день № 30. Наряду с медикаментозной терапией больной получал массаж нижних конечностей и сеансы ГБО. С десятых суток назначали электростимуляцию мышц бедра и голени аппаратом «Миоритм-040» (режим стимуляции, кольцевой способ подключения); период миграции тока постепенно увеличивали с 4 до 16 секунд, а продолжительность процедуры – с 10 до 25 минут; силу тока - до выраженного сокращения мышц. Данный лечебный комплекс проводили один раз в три месяца до полного купирования неврологической симптоматики.
Профилактика неврологических осложнений во время оперативного вмешательства заключается в сокращении времени операции, щадящей хирургической технике с минимальным травмированием околопротезных тканей. В начале тракции за бедро хирург должен определить, какие потребуются усилия для вправления, если усилия значительные, то не следует усиливать тракцию, а необходимо поменять пробную головку на головку с меньшей величиной «offset» или мобилизовать проксимальный отдел бедра. В случаях, когда после замены головки бедро все-таки не вправляется, необходимо еще раз проанализировать данные предоперационного проектирования имплантации и, возможно, решить вопрос о замене рашпиля ножки протеза на меньший размер.
Переломы бедренной кости. В нашем исследовании переломы пластинки большого вертела бедренной кости (8) произошли на этапе пробного вправления на рашпиле или уже на установленном бедренном компоненте протеза; винтообразный перелом верхней трети диафиза (2) случился в момент «press-fit» имплантации бесцементного бедренного компонента. Во всех случаях был выполнен остеосинтез серкляжной проволокой (рис. 2). Меры профилактики такого локального осложнения заключаются в мобилизации проксимального отдела бедра перед выведением его в рану (иссечение остатков дегенеративно измененной капсулы вокруг спила бедренной кости, поперечное рассечение напряженного нижнего листка широкой фасции бедра), в ослаблении медиальных отделов спила бедренной кости электропилой или тонки долотом по оси диафиза при появлении усилий во время введения рашпиля или бедренного компонента.
а б в
Рис. 2. Рентгенограммы правого тазобедренного сустава больной Г., 57 лет, DS: правосторонний коксартроз III стадии: а – до операции, прямая проекция; б, в – после операции (прямая и боковая проекции); выполнена имплантация бесцементного протеза SLPS ЗАО «Алтимед», остеосинтез проволокой перелома большого вертела
Вывихи головки протеза. Вывихи бедра после операции эндопротезирования встретились в 4 случаях, что составило 0,36 % от общего количества вмешательств. У 3 пациентов вывихи произошли в ближайшем послеоперационном периоде, одна пациентка поступила с застарелым вывихом головки протеза из другого лечебного учреждения.
В результате анализа рентгенограмм и статуса пациентов выявлено, что причинами рецидивирующих вывихов бедра явилось неверное определение величины «offset» (2), рубцовые изменения в мышцах и мягких тканях, окружающих сустав (1), ошибки при ориентации тазового и бедренного компонентов протеза (недостаточное погружение и избыточная вертикализа-ция, анте- или ретроверсия чашки протеза, из- быточная антеверсия бедренного компонента) (1). Во всех случаях провоцирующим фактором возникновения вывиха явилось несоблюдение пациентом двигательного режима в ближайшем послеоперационном периоде.
После увеличения offset’а заменой головки (S на L, XL) у трех пациентов натяжение ягодичных мышц было восстановлено и рецидивов вывихов больше не было. В случае вывиха в результате сниженных функциональных возможностей ягодичных мышц (1) достаточно было после закрытого вправления вывиха фиксировать конечность в кокситной гипсовой повязке на 2 месяца, и релюксации больше не повторялись. У пациентки с застарелым вывихом потребовалась переустановка тазового и бедренного компонентов протеза.
Технология имплантации протеза тазобедренного сустава предусматривает установку чашки с горизонтальным наклоном 40-50º и антеверзией 10-15º; ножки - в положении антеверзии 10-15º по отношению к межмыщелковой линии. Изменение анатомии тазовой и бедренной кости в результате переломов, дисплазии и предшествующих хирургических вмешательств (корригирующие, опорные остеотомии), дефекты кости, выраженный остеопороз и положение больного на боку при недостаточном опыте хирурга являются факторами, существенно повышающими риск неправильной пространственной ориентации компонентов протеза.
С целью предупреждения неправильной установки бедренного компонента, нами разработан следующий технический прием. При обработке бедренного канала рашпилями, помимо ориентации на мыщелки бедренной кости, перед пробой на вправление можно сделать специальные метки на костной ткани спила бедра с помощью электроножа, определяющие ротационное положение рашпиля. После пробного вправления, в случаях сохраняющегося ротационного вывиха или подвывиха головки протеза из впадины рашпиль, а затем и ножка протеза, устанавливаются относительно нанесенных ранее меток с увеличением угла внутренней ротации бедренного компонента в канале. Применение такого приема позволяло достигать оптимального биомеханического соотношения углов установки чашки и ножки протеза, при которых исключался ротационный вывих или подвывих головки из впадины.
При затруднениях в ориентации протеза следует дополнительно рентгенологически проконтролировать положение рашпиля, фрезы или пробного компонента при подготовке имплантационного ложа и во время пробного вправления.
В качестве примера вывиха головки протеза в ближайшем послеоперационном периоде в результате сочетания двух провоцирующих факторов (анатомо-функциональная неполноценность ягодичных мышц и мышц бедра в результате рубцового изменения тканей и несоблюдение двига- тельного режима) приводим следующее клиническое наблюдение.
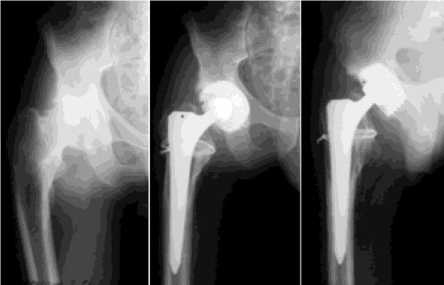
Клинический пример. Больная Б., 23 лет, поступила в клинику с диагнозом: левосторонний вторичный коксартроз III ст. Состояние после межвертельной опорной остеотомии левого бедра с вальгизацией проксимального отдела. Укорочение левой нижней конечности - 3 см (рис. 3, а). В клинике выполнено эндопротезирование левого тазобедренного сустава бесцементным протезом фирмы «Ceraver» с парой трения керамика-керамика, моделирование большого вертела с фиксацией пластинки вертела двумя шурупами. Положение компонентов протеза на контрольных рентгенограммах после операции биомеханически правильное. Послеоперационный период протекал без особенностей, проводились занятия лечебной физкультурой, направленные на восстановление тонуса мышц и обучение правильной походке. На 14-е сутки после присажи-вания пациентки в низкое кресло произошел вывих головки протеза (рис. 3, б).
В условиях операционной под внутривенной анестезией выполненно закрытое вправление головки протеза во впадину. Учитывая дегенеративные изменения мышц и рубцы в результате выполненных ранее хирургических вмешательств, конечность после вправления вывиха фиксирована в положении отведения 1100 и внутренней ротации 100 в кокситной гипсовой повязке на 2 месяца; через 3 недели фиксации освобожден коленный сустав. На контрольной рентгенограмме положение компонентов правильное, стабильное (рис. 3, в). Повторных вывихов в течение последующих 3 лет не наблюдали.
Профилактикой вывихов головки эндопротеза из впадины в раннем послеоперационном периоде (при условии биомеханически правильной установки компонентов протеза) является строгое соблюдение рекомендаций, ограничивающих низкое приседание, приведение и наружную ротацию бедра, и регулярные занятия ЛФК для улучшения тонуса мышц нижних конечностей.

а б в
Рис. 3. Рентгенограммы левого тазобедренного сустава в прямой проекции больной Б., 23 лет: а – до операции эндопротезирования; б – после операции эндопротезирования бесцементным протезом «Ce-raver» с вывихом головки протеза; в – после закрытого вправления вывиха
Лигатурный свищ. Лигатурный свищ был отмечен в двух случаях. Возникновение данного осложнения мы связываем с использованием шовного материала «Кетгут», вызывающего локальное раздражение в области раны с последующей воспалительной реакцией. После замены шовного материала на «Викрил» лигатурных свищей не было.
ЗАКЛЮЧЕНИЕ
Для профилактики локальных осложнений важное значение на этапе обследования имеет выявление анатомических особенностей в зоне имплантации, не позволяющих установить стандартный протез тазобедренного сустава: искривленный или очень узкий костномозговой канал, плоская вертлужная впадина, тонкие тазовые кости, рубцовое изменение мышц в области тазобедренного сустава в результате ранее перенесенных операций. С помощью дополнительного КТ- или МРТ-исследования следует уточнить структуру кости и мягких тканей, окружающих пораженное сочленение, не пропустить очаги хронической инфекции и деструкции. Особое внимание необходимо уделять предоперационному проектированию имплантации по скиаграммам, с помощью которого устанавливаются такие биомеханические параметры, как оптимальная величина «offset», уровень формирования имплантационного ложа для тазового компонента, размеры протеза и вид его фиксации, а также варианты выполнения костной аутопластики дефектов краев, моделирующей резекции пластинки большого вертела и корригирующих остеотомий. Хирургическая техника эндопротезирования должна быть тщательно отработана, а технология вмешательства в обязательном порядке должна включать все меры и способы профилактики возможных интраоперационных осложнений. Повышению результативности операции эндопротезирования в значительной мере способствует строгое соблюдение больными рекомендуемого двигательного режима, а от врачей требуется особое внимание к общему и локальному статусу больного в раннем послеоперационном периоде.


