Магнитно-резонансная томография сердца с парамагнитным контрастным усилением в оценке механизмов формирования наджелудочковых аритмий у пациентов с резистентной артериальной гипертонией
Автор: Мочула Ольга Витальевна, Попов Сергей Валентинович, Фальковская Алла Юрьевна, Мордовин Виктор Федорович, Шелковникова Татьяна Александровна, Зюбанова Ирина Владимировна, Лукьяненок Павел Иванович, Усов Владимир Юрьевич
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4 т.31, 2016 года.
Бесплатный доступ
Данная статья посвящена магнитно-резонансной оценке состояния левого предсердия (ЛП) у пациентов с резистентной артериальной гипертонией (РАГ) и гипертрофией левого желудочка (ГЛЖ) в динамике их лечения с помощью транскатетерной ренальной денервации. Для этого оценивалась динамика состояния ЛП в ходе лечения, анализировались взаимосвязи между показателями массы миокарда левого желудочка (ММ ЛЖ) и степенью дилатации левого предсердия (ЛП). В обследовании, которое проходило на базе НИИ кардиологии (Томск), приняли участие 40 пациентов. Всем пациентам трижды проводилось магнитно-резонансное (МР) исследование: исходно, через 6 и 12 мес. после лечения. Было выявлено следующее: объем ЛП статистически значимо снижался (p
Транскатетерная ренальная денервация, резистентная гипертония, магнитно-резонансная томография сердца, наджелудочковые нарушения ритма, объем левого предсердия
Короткий адрес: https://sciup.org/14920146
IDR: 14920146 | УДК: 616.125.2-122
Cardiac mri with paramagnetic contrast enhancement in assessment of supraventricular arrhythmias formation in patients with resistant hypertension
Present article is devoted to MRI assessment of the status of the left atrium (LA) in patients with resistant hypertension (RH) and left ventricular (LV) hypertrophy in the dynamics of treatment with transcatheter renal denervation (TRD). To achieve this the dynamics of the state of the LA during treatment was assessed; the relationship between the LV mass and the degree of dilation of the LA was analyzed. We studied 40 patients (mean age 56.6±8.4 years) with RH and LV hypertrophy who underwent TRD treatment. All patients received MRI study before TRD and after 6 and 12 months after the treatment. Based on MRI data, we quantified LA volume and LV mass. LA volume statistically significantly decreased 12 months after treatment (from initial 57.95 (47.28; 65.16) cm3 to 54 (44.58; 64.73) cm3 (p
Текст научной статьи Магнитно-резонансная томография сердца с парамагнитным контрастным усилением в оценке механизмов формирования наджелудочковых аритмий у пациентов с резистентной артериальной гипертонией
Введение причин, приводящих к формированию мозговых инсуль тов и инфаркта миокарда. Нарушения ритма, в большин-АГ, несмотря на очевидные успехи в борьбе с этим стве своем наджелудочкового генеза, играют в патогене-заболеванием, продолжает оставаться одной из главных зе осложнений АГ весьма важную роль [3]. В частности, ремоделирование сердца, которое происходит в результате прогрессирования АГ, с одной стороны, выступает в качестве компенсаторной реакции, которая дает сердцу возможность работать в условиях повышенного давления, а с другой, является одним из этапов прогрессирования изменений сердца к формированию дисфункции левого желудочка (ЛЖ) и развитию сердечной недостаточности [10]. Ремоделирование сердца у больных АГ отождествляют, прежде всего, с ГЛЖ. ГЛЖ может не только выявляться у лиц, уже имеющих повышенное артериальное давление, но и предшествовать развитию АГ [5].
Практически неизбежно и одновременно с изменениями массы миокарда и биомеханики ЛЖ развиваются и предсердные биомеханические и электрофизиологические нарушения [1, 3]. Их важнейшей клинической манифестацией является формирование пароксизмальных наджелудочковых тахиаритмий (ПНЖТ), а впоследствии и мерцательной аритмии.
Магнитно-резонансная томография (МРТ) в последние годы зарекомендовала себя как надежный метод всесторонней функциональной и морфологической диагностики состояния сердца, в первую очередь, миокарда желудочков. У пациентов с ишемическими поражениями она позволяет эффективно прогнозировать состояния, при возраст составлял 56,6±8,4 лет (p>0,05). Из их общего числа было 52,5% мужчин (n=21), средний возраст – 55,8±8,5 лет (p>0,05), и 47,5% женщин (n=19), средний возраст – 57,4±8,5 лет (p>0,05). У всех пациентов, по данным ультразвукового и электрокардиографического исследования, были отмечены признаки ГЛЖ.
Исследование пациентов проводилось на МР-томог-рафе фирмы Toshiba Vantage Titan, с индукцией магнитного поля 1,5 Т, с синхронизацией по ЭКГ, при этом общая продолжительность составляла в среднем 35–50 мин. Для охвата зоны интереса была использована поверхностная 16-канальная катушка с высоким соотношением сигнал/шум с большим полем обзора (до 500х500 мм). Локалайзер центрировался на область верхушечного толчка. Длительность задержки дыхания составляла от 4–6 до 12–17 с в зависимости от импульсной последовательности (ИП). Были выполнены следующие протоколы исследования сердца в ЭКГ-синхронизации:
– Исходно: позиционирующие ИП в аксиальной, сагиттальной, двухкамерной проекции по короткой оси и четырехкамерной проекции по длинной оси сердца; ИП GRE-SSFP (ИП с устойчивым состоянием свободной прецессии, изображения с “темной кровью”) в Т1- которых наджелудочковые нарушения ритма сердца наиболее вероятны [2]. Однако оценка состояния предсердий у пациентов с РАГ пока не проводилась. Поэтому мы попытались оценить состояние предсердий, в первую очередь, ЛП, у пациентов с РАГ и ГЛЖ в динамике лечения методом транскатетерной ренальной денервации. В частности, для этого количественно оценивалась динамика состояния ЛП в ходе лечения АГ методом транскатетерной ренальной денервации, анализировались взаимосвязи между показателями ГЛЖ и степенью дилатации ЛП.
Материал и методы
В период с 2014–2016 гг. на базе отделения рентгеновских и томографических методов диагностики НИИ кардиологии (Томск) было обследовано 40 пациентов. Основным критерием включения пациентов в исследование было показание к проведению денервации почечных артерий.
В исследование были включены пациенты с РАГ, которым в связи с неэффективностью медикаментозной терапии была проведена транскатетерная двусторонняя ренальная денервация почечных артерий. Всего было обследовано 40 пациентов, при этом средний
б
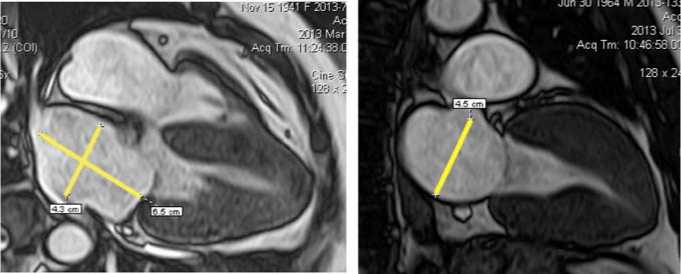
Рис. 1. Определение объема ЛП. Кино-режим (импульсная последовательность SSFP). Изображения сердца в четырехкамерной (а) и двухкамерной (б) проекциях по длинной оси в фазу систолы ЛЖ
а б
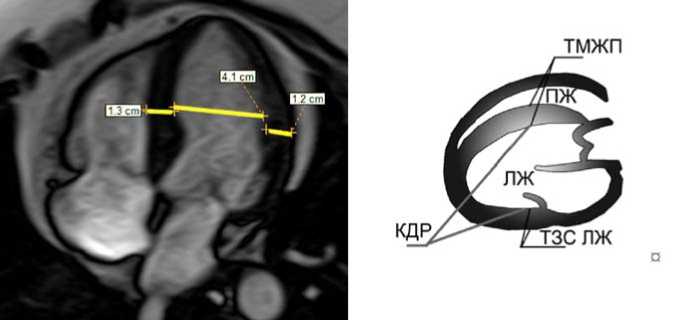
Рис. 2. Определение ММ ЛЖ. Кино-режим (импульсная последовательность SSFP). Изображения сердца в двухкамерной (а) проекции по длинной оси в фазу диастолы ЛЖ. Схематическое представление измеряемых параметров (б)
и Т2-взвешенности; кино-режим, изображения с “яркой кровью” в двухкамерной проекции по короткой оси и четырехкамерной проекции по длинной оси сердца.
– После введения парамагнетика-контраста: для оценки раннего контрастирования исследовался первый пассаж контрастного препарата (1–3 мин после введения препарата) с использованием сверхбыстрых градиентных последовательностей (GRE) с инверсией и Т1-взвешенностью или быстрый кино-режим.
Для анализа полученных изображений был использован программный пакет eFilm Workstation.
Для сбора данных волюметрических показателей миокарда использовался кино-режим в проекциях по короткой и вертикальной длинной оси сердца.
Определялись следующие параметры.
Определение объема левого предсердия (ОЛП, см3). Для расчета ОЛП была использована модель эллипсоида, которая предполагает, что ЛП может быть представлено в виде вытянутого эллипса с объемом, который рассчитывается по следующей формуле:
4n L ( Di/ Y D2/ ) /3 (/2)( /2 )( /2 ),
где L – длина длинной оси, D1 и D2 – ортогональные поперечные размеры ЛП [4].
Объем ЛП определялся на изображениях, полученных с помощью ИП SSFP в двухкамерной и четырехкамерной проекциях по длинной оси в фазу систолы ЛЖ (рис. 1). Также данная последовательность была использована для расчета ММЛЖ. Параметры сканирования представлены в таблице 1.
Определение ММ ЛЖ . Для определения ММ ЛЖ применялась формула R.B. Devereux и N. Reichek (рис. 2): ММ ЛЖ=1,04х([КДР+ТЗС ЛЖ+ТМЖП]3–[КДР]3)–13,6 [9].
Для определения геометрии ЛЖ необходимыми данными являются: толщина межжелудочковой перегородки (ТМЖП), толщина задней стенки (ТЗС) ЛЖ и конечно-диастолический размер (КДР) ЛЖ. Эти параметры могут быть непосредственно измерены при МРТ в кинорежиме в конце диастолы.
Протокол исследования был одобрен этическим комитетом НИИ кардиологии. Исследование проводилось с соблюдением международных принципов Хельсинской декларации и всех этических стандартов по защите людей и животных в процессе выполнения научной работы. У всех пациентов, включенных в исследование, было получено информированное согласие.
Таблица 1
Параметры сканирования сердца для получения киноизображений сердца (ИП SSFP)
|
Параметры |
Значения |
|
TR, мс |
3,7 |
|
TE, мс |
1,9 |
|
FA, градусы |
72 |
|
Толщина среза, мм |
8 |
|
Матрица, пиксел х пиксел |
128x240 |
Статистический анализ данных выполнялся с помощью пакета прикладных программ STATISTICА 8.0 (StatSoft). Для проверки закона распределения был использован критерий согласия Шапиро–Уилка W – объем выборки равен 40 , т.к. выборки не подчинялись нормальному закону распределения, данные представлены в виде: Ме(Q1; Q3), где Ме – медиана, Q1 – 1-й квартиль (25%), Q3 – 3-й квартиль (75%) . Для определения значимости различий в выборках применялся парный критерий Вилкок-сона для зависимых выборок Т. Для корреляционного анализа применялся коэффициент Спирмена (т.к. величины не подчинялись нормальному закону распределения). Различия в сравниваемых группах считались статистически значимыми при уровне статистической значимости 95% (р<0,05).
Результаты и обсуждение
Мы оценивали то, как влияет ОЛП на развитие пароксизмальных наджелудочковых нарушений ритма у данных пациентов (рис. 3). Из всей группы пациентов с АГ и сформировавшейся на ее фоне ГЛЖ при отсутствии у всех пациентов митральной регургитации более первой степени у одного была диагностирована частая пароксизмальная мерцательная аритмия, спонтанно не купировавшаяся, а требовавшая в большинстве случаев медикаментозной терапии либо электроимпульсного лечения. У 6 пациентов имели место частые эпизоды ПНЖТ.
Анализ ОЛП у данных пациентов показал, что у всех, кроме одного пациента с частыми ПНЖТ, он существенно выше 70 см3 (от 74 до 89 см3). У одного пациента с меньшим ОЛП (58 см3) отмечалось наличие множественных очагов повреждения стенки, визуализирующихся как предсердные включения парамагнитного контраста мелкоочагового характера. Как было показано ранее [6, 7], это является дополнительным независимым фактором, провоцирующим формирование пароксизмальных наджелудочковых нарушений ритма, в частности, за счет формирования множественных очагов re-entry. Среди пациентов, у которых пароксизмальных аритмий зафиксировано не было, показатели ОЛП были существенно меньше.
При проведении транскатетерной ренальной денервации почечных артерий у пациентов с частыми ПНЖТ или мерцательной тахиаритмией во всех случаях в послеоперационном периоде отмечалось умеренное снижение ОЛП, причем у 2 из 6 ПНЖТ практически прекратились. В связи с малостью размеров выборки эти показатели недостаточны для достоверного утверждения о соответствующем антиаритмогенном эффекте радиочастотной аблации (РЧА) на ОЛП, однако тенденция к послеоперационному снижению вероятности развития ПНЖТ у таких пациентов очевидна.
Таким образом, величина ОЛП оказывается наиболее существенной в аспекте прогноза пароксизмальных наджелудочковых нарушений ритма у пациентов с АГ, подобным образом для случаев с ишемической болезнью сердца и перенесенным инфарктом миокарда [2].
При этом дискриминантное значение ОЛП, разделяющего пациентов с низким и высоким риском ПНЖТ при
а
б
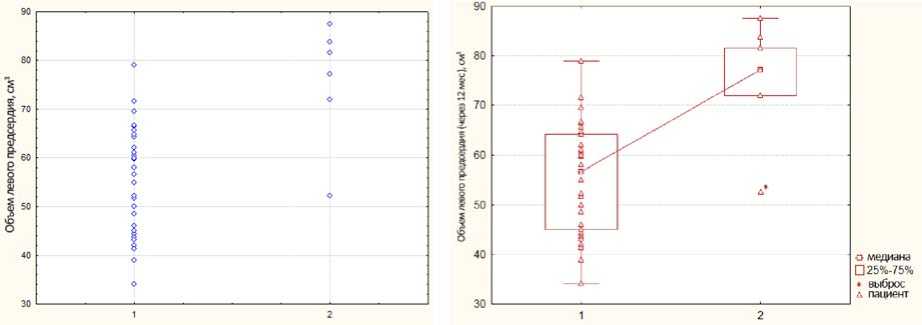
Рис. 3. Показатели ОЛП в группах пациентов с АГ и синусовым ритмом (1) и наличием частых ПНЖТ (2). Данные представлены как медиана с межквартильным размахом (а), и как распределение индивидуальных значений (б). Можно видеть, что, несмотря на различия в количестве пациентов в этих группах, пациенты группы 2 в большинстве находятся по показателю ОЛП выше величины 70–75 см3, тогда как в группе с синусовым ритмом (1) величина ОЛПу всех пациентов кроме двух ниже этой величины
б
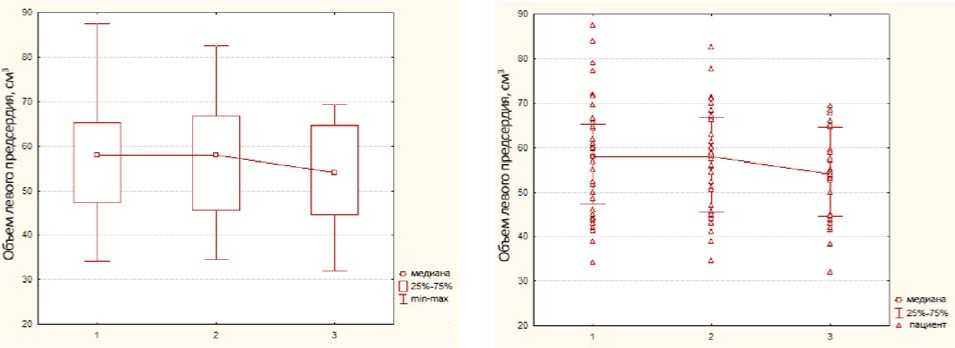
Рис. 4. Динамика ОЛП. Данные представлены как медиана с межквартильным размахом (а), и как распределение индивидуальных значений (б): исходно (1), через 6 (2) и 12 (3) мес. после лечения
АГ, было практически тем же, что и при перенесенном остром инфаркте миокарда (ОИМ) – 70–74 см3 [7].
Ни в одном из случаев мы не наблюдали, чтобы процедура РЧА оказывала дополнительное повреждающее воздействие на предсердия, в частности, на состояние стенки, с формированием дополнительных зон фиброза и самое главное – увеличением их размеров и объема. Это является дополнительным аргументом в пользу основного антиаритмического эффекта в дополнение к гипотензивному.
В настоящем исследовании мы не оценивали дополнительно, как влияет состояние симпатической иннервации на состояние предсердий, в частности уровень адреналина и норадреналина в крови у этих пациентов. Однако, учитывая доказанное в различных группах больных с АГ снижение норадреналина в плазме [8], рационально полагать, что у наших пациентов картина носит сходный характер.
По данным МР-исследования сердца обследуемых пациентов с РАГ и ГЛЖ в динамике их лечения ОЛП незначительно увеличился относительно исходного уровня 57,95 (47,28; 65,16) см3 до 58 (45,6; 66,9) см3 через 6 мес. после лечения и снизился до 54 (44,58; 64,73) см3 через 12 мес. после лечения (рис. 4).
ОЛП статистически значимо снижался (p<0,05) относительно исходного значения 57,95 (47,28; 65,16) и спустя 12 мес. после лечения 54 (44,58; 64,73), а изменения показателя через 6 мес. после лечения не были статистически значимы 58 (45,6; 66,9) см3 (p>0,05).
Через 6 мес. после лечения у 40% пациентов мы наблюдали снижение ОЛП, у 35% пациентов наблюдалось увеличение объема, а у 25% изменений не было.
Через 12 мес. после лечения уже у 57,5% пациентов наблюдалось снижение ОЛП, у 27,5% пациентов отмечалось увеличение объема, а у 15% изменений не было. Причем из числа тех 10 пациентов, у которых не было
Таблица 2
Изменение ОЛП у пациентов через 6 и 12 мес. после лечения (n=40)
Таблица 3
Изменение массы миокарда у пациентов через 6 и 12 мес. после лечения (n=40)
Сроки Уменьшение Увеличение Без изменений
Через 6 мес. после лечения 16 14 10
Через 12 мес. после лечения 23 11 6
Сроки Уменьшение Увеличение Без изменений
Через 6 мес. после лечения 26 13 1
Через 12 мес. после лечения 32 8 0
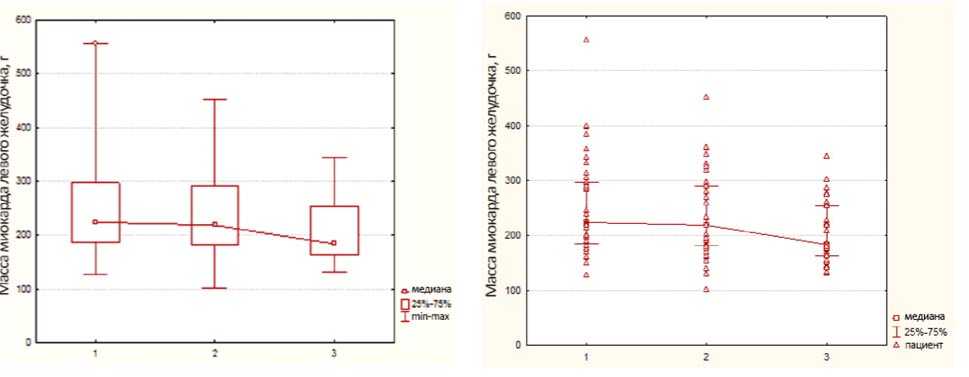
а
б
Рис. 5. Динамика ММ ЛЖ. Данные представлены как медиана с межквартильным размахом (а), и как распределение индивидуальных значений (б): исходно (1), через 6 (2) и 12 мес. (3) после лечения
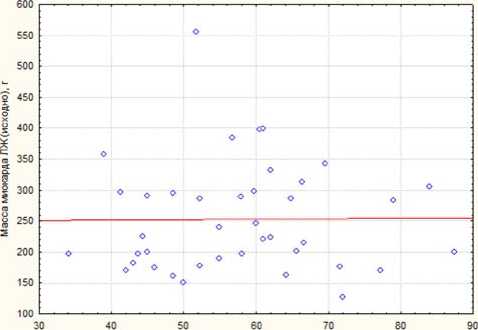
Объем левого предсердия (исходно), см*
Рис. 6. График, отражающий взаимосвязь между показателями: ММ ЛЖ и ОЛП до лечения (коэффициент Спирмена=0,065, р=0,69)
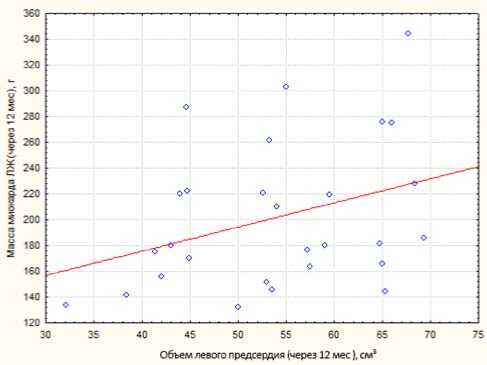
Рис. 7. График, отражающий взаимосвязь между показателями: ММ ЛЖ и ОЛП после лечения, через 12 мес. (коэффициент Спирмена=0,37, р<0,05)
изменений ОЛП через 6 мес. после лечения, уже через 12 мес.: у 6 пациентов уровень объема остался на прежнем значении от исходного; у 3 пациентов произошло уменьшение объема, а у 1 пациента объем увеличился (табл. 2).
Данные МР-измерений показали, что ММ ЛЖ также имела тенденцию к снижению после лечения, а именно, ММ ЛЖ статистически значимо снижалась относитель- но исходных измерений 224,15 (185,79; 296,87) г, рисунок 5:
– через 6 мес. после лечения ММ ЛЖ статистически значимо снизилась до 218,84 (181,98; 290,44) г, p=0,002;
– через 12 мес. после лечения ММ ЛЖ статистически значимо снизилась до 183,67 (163,76;254,5) г, p<0,001.
Через 6 мес. после лечения мы определили, что у 65% пациентов наблюдалось снижение ММ ЛЖ, у 32,5% – увеличение, у 2,5% – изменений не наблюдалось.
Через 12 мес. после лечения уже у 80% пациентов наблюдалось снижение ММ ЛЖ, у 20% пациентов наблюдалось ее увеличение. У пациента, у которого через 6 мес. после лечения не отмечалось изменения динамики ММ ЛЖ, через 12 мес. она увеличилась (табл. 3).
Для нас было важно определить, имеется ли взаимосвязь между ОЛП и ММ ЛЖ, поскольку увеличение камер сердца, в частности ЛП, может свидетельствовать об увеличении венозного возврата к сердцу, в результате чего увеличивается преднагрузка на ЛЖ и, как следствие, развитие его гипертрофии.
Корреляционный анализ данных показал (критерий Спирмена), что между ОЛП и ММ ЛЖ исходно, до выполнения процедуры транскатетерной ренальной денервации, не было выявлено взаимосвязи: коэффициент Спир-мена=0,065, р=0,69 (рис. 6).
При корреляционном анализе данных показателей спустя 12 мес. после лечения определялась слабая взаимосвязь, при этом коэффициент Спирмена был равен 0,37, р<0,05, это говорит в пользу того, что данный показатель является независимым (рис. 7).
Выводы
Таким образом, есть все основания считать, что транскатетерная ренальная денервация у пациентов с АГ обладает статистически значимым антиаритмогенным эффектом, в первую очередь, за счет уменьшения механического напряжения и уменьшения объемных показателей предсердий у таких пациентов в результате транскатетерной ренальной денервации. Представляется, что основным практическим следствием этого факта является то, что при наличии у пациента с РАГ частых наджелудочковых нарушений ритма процедура транскатетерной ренальной денервации оказывается показанной в первую очередь.
Список литературы Магнитно-резонансная томография сердца с парамагнитным контрастным усилением в оценке механизмов формирования наджелудочковых аритмий у пациентов с резистентной артериальной гипертонией
- Искендеров Б.Г., Лохина Т.В., Шибаева Т.М. и др. Динамика электрофизиологических показателей сердца у больных артериальной гипертонией в зависимости от суточного профиля артериального давления; геометрии левого желудочка и метаболических нарушений//Тер. архив. -2006. -Т. 78, № 9. -С. 12-17.
- Шомахов Р.А., Голухова Е.З. Возможности магнитно-резонансной томографии с контрастным усилением у пациентов с нарушениями ритма сердца: взгляд кардиолога//Креативная кардиология. -2014. -№ 4. -С. 75-83.
- Потешкина Н.Г., Джанашия П.Х. Структурно-функциональное ремоделирование миокарда и прогнозирование аритмий у больных артериальной гипертонией//Артериал. гипертен. -2005. -Т. 11, № 4. -С. 249-251.
- Рекомендации по количественной оценке структуры и функции сердца//Рос. кардиол. журн. -2012. -№ 3 (95), приложение 1. -С. 1-28.
- Туев А.В., Ховаева Я.Б. Особенности структурно-функциональных показателей сердца у лиц с разным уровнем артериального давления//Рос. кардиол. журн. -2002. -№ 5. -С. 38-41.
- Усов В.Ю., Бабокин В.Е., Мочула О.В. и др. Контрастированная магнитно-резонансная томография у пациентов с перенесенным инфарктом миокарда и предсердными тахиаритмиями//Рос. кардиол. журн. -2014. -№ 12(116). -С. 38-43.
- Усов В.Ю., Бабокин В.Е., Мочула О.В. и др. Магнитно-резонансная томография сердца с контрастным усилением в прогнозировании риска предсердных тахиаритмий у пациентов с перенесенным инфарктом миокарда//Рос. электронный журнал лучевой диагностики. -2014. -Т. 4, № 4. -С. 16-21.
- Пекарский С.Е., Баев А.Е., Мордовин В.Ф. и др. Эндоваскулярная денервация сегментарных ветвей почечной артерии для лечения резистентной АГ -рандомизированное контролируемое исследование эффективности и безопасности в сравнении с существующим методом симпатической денервации почек//Тезисы XII Всероссийского конгресса "Артериальная гипертония 2016: Итоги и перспективы". -М.: ИнтерМедсервис, 2016. -С. 62-63.
- Devereux R.B., Reichek N. Echocardiographic determination of left ventricular mass in man: anatomic validation of the method//Circulation. -1977. -Vol. 55. -P. 613-618.
- Levy D., Garrison R.J., Savage D.D. et al. Prognostic implications of echocardiographically determined left ventricular mass in the Framingham Heart Study//N. Engl. J. Med. -1990. -Vol. 322 (22). -P. 1561-1566.


