Маркеры аэрогенной комбинированной экспозиции металлоксидными соединениями и трансформированного протеомного профиля плазмы крови у детей
Автор: Землянова Марина Александровна, Зайцева Нина Владимировна, Кольдибекова Юлия Вячеславовна, Пескова Екатерина Владимировна, Булатова Наталья Ивановна, Степанков Марк Сергеевич
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Медико-биологические аспекты оценки воздействия факторов риска
Статья в выпуске: 1 (41), 2023 года.
Бесплатный доступ
Изучение изменений гомеостатического равновесия организма, в первую очередь на клеточно-молекулярном уровне, является актуальным направлением фундаментально-прикладных научных исследований для задач прогнозирования негативных эффектов со стороны здоровья человека в условиях воздействия химических факторов риска. У детей обоснованы прогностически значимые маркеры трансформированного протеомного профиля плазмы крови, доказанно связанные с аэрогенной комбинированной экспозицией металлоксидными соединениями (на примере оксидов меди и никеля). Предложен инновационно-методический подход на основе протеомного профилирования плазмы крови, включающий: идентификацию тождественных белков и генов, кодирующих их экспрессию; количественную оценку параметров показателей в системе «тождественный белок - концентрация химического вещества в крови»; прогнозирование негативных эффектов по критериям молекулярно-клеточной дестабилизации гомеостаза в условиях хронической аэрогенной экспозиции химических веществ. Реализация предложенного алгоритма выполнена на примере сопоставления измененных белков и пептидов, полученных в протеомном профиле плазмы крови детей, подверженных реальной аэрогенной комбинированной экспозиции оксидами никеля и меди, и мелких грызунов при экспериментальной комбинированной и изолированной экспозиции изучаемых веществ, эквивалентной реальному уровню. Установлено, что длительная аэрогенная комбинированная экспозиция одновременно оксидами меди и никеля обусловливает в крови экспонированных детей повышенные до 2,4 раза относительно показателей у неэкспонированных детей и референтных значений концентрации меди и никеля, обоснованные в качестве маркеров экспозиции. Результаты натурных исследований верифицированы повышенным содержанием аналогичных веществ в крови при экспериментальном моделировании эквивалентной комбинированной экспозиции на биологической модели. На основе протеомного профилирования плазмы крови в экспериментальных и натурных исследованиях обоснован тождественный протеомный маркер - APOBEC1 комплементарный фактор (ген А1CF), доказанно связанный с маркерами экспозиции (одновременно никелем и медью в крови). Снижение экспрессии данного белка в условиях сохраняющейся аэрогенной комбинированной экспозиции оксидами никеля и меди позволяет прогнозировать развитие негативного эффекта в виде модификации липопротеинов низкой плотности с дальнейшей индукцией атеросклеротических изменений сосудов, что является одним из факторов риска сердечно-сосудистых заболеваний.
Протеомные маркеры, маркеры экспозиции, детское население, биологическая модель, экспрессия гена а1cf, прогнозирование негативных эффектов
Короткий адрес: https://sciup.org/142237419
IDR: 142237419 | УДК: 57.044, | DOI: 10.21668/health.risk/2023.1.13
Markers of combined aerogenic exposure to metal oxides and transformed plasma proteomic profiles in children
Changes in homeostatic balance of the body, primarily at the cellular-molecular level, are a relevant research object in fundamental and applied studies. They can be eligible indicators for predicting negative effects under exposure to chemical risk factors. The aim of this study was to substantiate markers of a transformed plasma proteomic profile in children. These markers should have prognostic value and an evidence-based association with combined aerogenic exposure to metal oxides (copper and nickel oxides used as an example). We propose an innovative methodical approach based on plasma proteomic profiling that includes the following: identification of identical proteins and genes encoding their expression; quantification of indicators within the ‘identical protein - a chemical concentration in blood’ system; prediction of negative effects as per indicators of homeostasis destabilization at the cellular-molecular level under chronic aerogenic exposure to chemicals. The proposed algorithm was tested by comparing changed proteins and peptides identified in plasma proteomic profiles of children exposed simultaneously to nickel and copper oxides in ambient air in actual conditions and small rodents under experimental combined and isolated exposure to the analyzed chemicals in levels equal to real ones. Long-term aerogenic exposure simultaneously to copper and nickel oxides was established to create elevated nickel and copper levels in blood of exposed children substantiated as markers of exposure. They were up to 2.4 times higher against the same indicators in unexposed children and reference levels as well. The results of field observations were verified by elevated levels of the same chemicals in blood under experimental modeling of an equivalent combined exposure performed on biological models. APOBEC1 complement factor (the А1CF gene) was substantiated as an identical proteomic marker based on plasma proteomic profiling in experimental and field investigations. It has an evidence-based association with markers of exposure (nickel and copper simultaneously identified in blood). Lower expression of this protein under persistent combined aerogenic exposure to nickel and copper oxides makes it possible to predict such a negative effect as modification of low density lipoproteins with further induction of atherosclerotic changes in vessels, the latter being a risk factor of cardiovascular diseases.
Текст научной статьи Маркеры аэрогенной комбинированной экспозиции металлоксидными соединениями и трансформированного протеомного профиля плазмы крови у детей
Землянова Марина Александровна – доктор медицинских наук, главный научный сотрудник, заведующий отделом биохимических и цитогенетических методов диагностики; доцент кафедры микробиологии и иммунологии (e-mail: ; тел.: 8 (342) 236-39-30; ORCID: .
Зайцева Нина Владимировна – академик РАН, доктор медицинских наук, профессор, научный руководитель (e-mail: ; тел.: 8 (342) 237-25-34; ORCID: .
Кольдибекова Юлия Вячеславовна – кандидат биологических наук, старший научный сотрудник, заведующий лабораторией метаболизма и фармакокинетики отдела биохимических и цитогенетических методов диагностики (e-mail: ; тел: 8 (342) 237-18-15; ORCID: .
Пескова Екатерина Владимировна - младший научный сотрудник лаборатории биохимической и наносенсор-ной диагностики отдела биохимических и цитогенетических методов диагностики (e-mail: ; тел: 8 (342) 237-18-15; ORCID: .
Булатова Наталья Ивановна – научный сотрудник лаборатории биохимической и наносенсорной диагностики (e-mail: ; тел: 8 (342) 236-80-18; ORCID: .
Степанков Марк Сергеевич – младший научный сотрудник лаборатории биохимической и наносенсорной диагностики (e-mail: ; тел: 8 (342) 237-18-15; ORCID: .
Высокоактуальным направлением фундаментальных и прикладных научных исследований является изучение изменений гомеостатического равновесия организма, формирующихся на самых ранних этапах их развития, в первую очередь на клеточномолекулярном уровне [1]. Применение технологии протеомного анализа позволяет расширить теоретические представления о клеточно-молекулярных механизмах развития негативных эффектов, тем самым повысить предиктивный потенциал диагностики ряда заболеваний неинфекционного генеза. Поиск информативных молекулярных маркеров является одним из приоритетных направлений фундаментальных научных исследований в Российской Федерации1. Новые знания в области модификации этиопатогенеза заболеваний, связанных с воздействием риск-индуцированных факторов, являются научной основой установления условий, причин, механизмов возникновения, предупреждения и снижения риска и вреда здоровью человека [2].
Процесс модификации механизма развития негативных эффектов может быть связан с взаимодействием химических факторов риска с генами, модулирующими экспрессию определенных белков, которые обеспечивают функциональную активность молекулярно-биологических процессов [3]. На фоне сохраняющегося модифицирующего действия химических факторов происходит молекулярноклеточная трансформация гомеостаза, обусловливающая формирование негативных эффектов, тем самым повышая риск развития заболевания2. Анализ генов, кодирующих белки, на которые оказывают влияние химические факторы, даёт представление о биологических функциях и молекулярных сетях, изменяющихся в ответ на химическое воздействие. Изучение таких генно-химических взаимодействий является мощным информационным ресурсом для получения и развития знаний об этиологии и моле- кулярных механизмах, лежащих в основе модификации процессов, ассоциированных с воздействием химических факторов риска [4, 5].
Поскольку белки играют ключевую роль в обеспечении жизнедеятельности клеток и организма в целом, качественные и количественные изменения белкового состава, регистрируемые в текущий момент исследования, могут быть потенциально информативными для самого раннего выявления негативных эффектов, обусловливающих дальнейшее формирование существенных функциональных расстройств критических органов и систем.
Таким образом, в настоящее время наиболее перспективна тематика научных исследований, касающихся поиска протеомных маркеров и их комбинаций – потенциальных молекулярных мишеней, отражающих состояние и функциональные характеристики этиопатогенетически мотивированных механизмов в ответ на воздействие химических факторов риска. Выявление при этом генно-химических взаимодействий между экспрессией белкового маркера и фактором экспозиции позволяет прогнозировать негативные исходы со стороны здоровья, что явилось основанием для определения цели настоящего исследования. Данная работа является продолжением цикла исследований, выполненных в ФБУН «ФНЦ медико-профилактических технологий управления рисками здоровью населения», посвященных применению «омиксных технологий» для обоснования информативных молекулярно-клеточных маркеров негативных эффектов [6, 7].
Цель исследования – выявление у детей прогностически значимых маркеров трансформированного профиля плазмы крови, доказанно связанных с аэрогенной комбинированной экспозицией металлоксидных соединений (на примере оксидов меди и никеля).
Материалы и методы. Выявление и обоснование молекулярных белковых маркеров, изменение которых ассоциировано с аэрогенной экспозицией оксидов меди и никеля, выполнено с применением предложенного инновационно-методического подхода, включающего следующие этапы:
– подтверждение факта аэрогенной экспозиции на основе определения параметров показателей в системе «концентрация вещества в атмосферном воздухе – концентрация вещества в биосреде»;
– сравнительный анализ статистически различающихся по интенсивности белковых пятен на основе протеомного профилирования плазмы крови и идентификации выделенных белков;
– выявление белков и пептидов, тождественных в результате экспериментальных и натурных исследований при комбинированном воздействии химических веществ;
– количественная оценка параметров причинно-следственных связей между тождественными белками и пептидами и концентрацией химических веществ в биосреде;
– прогнозирование негативных эффектов на основе построения и анализа биоинформационной молекулярной матрицы тождественных белков с выявлением их функций, биологических процессов и экспрессии в тканях.
Реализация предложенного алгоритма выполнена на примере сопоставления измененных белков и пептидов, полученных в протеомном профиле плазмы крови детей, подверженных реальной аэрогенной комбинированной экспозицией оксидами никеля и меди, и мелких грызунов (биологическая модель) при экспериментальной комбинированной и изолированной экспозиции, эквивалентной реальному уровню изучаемых веществ.
Экспериментальные исследования проведены на самках крыс линии Wistar. Особи в количестве 24 были разделены на четыре группы по шесть крыс в каждой: опытная группа № 1 – животные, подверженные изолированному действию стандартного образца никеля в дозе 0,38 мг/кг; опытная группа № 2 – животные, подверженные изолированному действию меди в дозе 1,23 мг/кг; опытная группа № 3 – животные, подверженные комбинированному действию смеси никеля и меди в дозах, указанных выше; группа контроля № 4 – контрольные живот- ные, содержавшиеся в аналогичных условиях, но не подверженные воздействию изучаемых химических веществ. Дозы химических веществ, вводимые экспериментальным животным, эквивалентны установленной реальной аэрогенной экспозиции при хроническом воздействии с учетом массы тела животных и видовых особенностей. Отбор крови у крыс осуществляли через 24 ч после воздействия из подъязычной вены в объеме 3 см3.
Экспериментальные исследования выполнены с соблюдением требований Европейской конвенции по защите позвоночных животных, используемых в экспериментальных или иных научных целях (ETS № 123)3, и комитета по этике ФБУН «ФНЦ медикопрофилактических технологий управления рисками здоровью населения».
Протеомное профилирование плазмы крови выполнено 45 детям в возрасте 4–7 лет, в том числе 25 подвергающихся длительной аэрогенной комбинированной экспозиции оксидами никеля (на уровне 0,0034 мг/(кг ⋅ день)) и меди (на уровне 0,0016 мг/ (кг ⋅ день)) – группа наблюдения, и не подвергающихся воздействию изучаемых химических веществ – группа сравнения (20 человек). Критерием формирования выборок детей группы наблюдения является повышенное ( ≥ 1,2 Rfl ) содержание меди и никеля в крови, детей группы сравнения - содержание изучаемых химических веществ соответствует минимальным или референтным значениям в крови (никель Rfl = 0,01 мг/дм3, медь Rfl = 0,9 мг/дм3)4.
Обследование детей проведено в соответствии с этическими принципами Хельсинкской декларации (64th WMA General Assembly, 20135) при обязательном наличии добровольно информированного согласия законного представителя и соблюдении требований комитета по этике ФБУН «ФНЦ медикопрофилактических технологий управления рисками здоровью населения» (протокол № 1 от 04.02.2021).
Анализ крови на содержание меди и никеля выполнен в соответствии с МУК 4.1.3230-146 на масс-спектрометре Agilent 7500cx (Agilent Technologies, США).
Исследование протеомного профиля плазмы крови включал отбор образцов, двумерный электрофорез в полиакриламидном геле7, анализ двумерной электрофореграммы, выделение значимых белковых пятен по их интенсивности, масс-спектрометрический анализ на хроматографе UltiMate 3000 (Германия) и тандемном масс-спектрометре ABSciex 4000 QTRAP с источником ионизации Nanospray 3 (Канада). Идентификацию белков проводили по базе данных UniProt8 с выборкой по таксону Homo Sapience и Rattus norvegicus. Определение гена, кодирующего идентифицированный белок, выполнено с помощью базы данных HUGO Gene Nomenclature Committee database (HGNC)9 и The Rat Genome Database (RGD)10. Описание биологических функций белков выполнено с помощью ресурса The Gene Ontology11, сбор информации о филогенетике и функциональной геномике – PhyloGenes12, получение данные об экспрессии белков в тканях организма – Tissue expression database13 и The Human Protein Atlas14. Информацию и анализ о возможных этиопатогенетических механизмах развития прогнозируемых негативных эффектов, ассоциированных с воздействием химических факторов, осуществляли на исследовательских платформах Comparative Toxicogeno-mics15 и DisGeNET16.
Оценку полученных значений показателей у экспонированных детей выполняли относительно неэкспонированных; у экспериментальных животных опытных групп - относительно показателей в группе контроля. Описательная статистика количественных переменных представлена в виде среднего значения ( M ), ошибки среднего ( m ). Статистическую значимость различий переменных между группами определяли по критерию Манна – Уитни ( U ≤ U кр ) при заданном уровне значимости p ≤ 0,05. Статистическую обработку данных осуществляли с помощью пакета программ Statistica 10.
Обоснование молекулярных маркеров негативных эффектов выполнено на основании полученных моделей зависимостей «химические вещества в крови – статистически значимая интенсивность белкового пятна», описываемых уравнением множественной линейной регрессии по формуле:
-
У, = b Oj+^L b ij x i ,
где y j – зависимая переменная (показатель интенсивности j -го белкового пятна, int);
x i – независимая переменная, i -й влияющий фактор (концентрация вещества в крови, мг/дм3);
b0 j , bi j – коэффициенты модели.
Достоверность и адекватность моделей оценивали с помощью дисперсионного анализа с использованием F -критерия Фишера, коэффициента детерминации ( R2 ), t -критерия Стьюдента при статистической значимости p ≤ 0,05.
Результаты и их обсуждение. Сравнительный анализ содержания меди и никеля в крови экспериментальных животных позволил установить достоверные статистические различия концентраций изучаемых веществ. При изолированной экспозиции никелем его концентрация в крови составила 0,014 ± 0,002 мг/дм3, при комбинированной смесью веществ – 0,008 ± 0,001 мг/дм3, что выше в 2,9 и в 1,7 раза соответственно относительно контрольных значений ( р = 0,001–0,012). Уровень меди в крови при изолированной экспозиции составил 2,323 ± 0,060 мг/дм3, при комбинированном смесью веществ – 2,006 ± 0,047 мг/дм3, что превысило в 1,5 и в 1,3 раза соответственно содержание вещества в контрольной группе ( р = 0,0001–0,002). Содержание меди и никеля в крови при изолированной экспозиции соответственно в 1,2 и в 1,8 раза выше, чем при комбинированной ( р = 0,002–0,022).
Реальная аэрогенная комбинированная экспозиция одновременно оксидами меди и никеля обусловливает в крови экспонированных детей повышенные в 1,2–2,4 раза концентрации изучаемых веществ относительно неэкспонированных ( р = 0,032–0,033) и повышенные в 1,2–1,3 раза уровни относительно референтных значений. На основании установленной и параметризированной связи концентрации меди и никеля в крови с концентрацией данных металлов в атмосферном воздухе (медь a 0 = 0,515, a 1 = 752,32; никель a 0 = 0,005, a 1 = 145,36, р = 0,05) медь и никель в крови обоснованы в качестве маркеров аэрогенной экспозиции.
Сравнительная оценка результатов денситометрии протеомного профиля плазмы крови крыс с изолированным воздействием меди и никеля позволила выявить восемь белков, аналогичных белкам, выделенным при комбинированном воздействии смеси указанных веществ (табл.1).
Таблица 1
Статистически значимые белки, доказано связанные с факторами экспериментальной комбинированной экспозиции
|
№ п/п |
Статистически значимые белки |
Достоверность модели зависимости «вещество – интенсивность значимого белкового пятна при комбинированном воздействии» ( р ≤ 0,05) |
||
|
Изолированная экспозиция |
Комбинированная экспозиция |
|||
|
медь |
никель |
медь + никель |
||
|
1 |
Компонент белка теломеразы 1 |
- |
Компонент белка теломеразы 1 |
0,002 |
|
2 |
Цитоскелетный кератин II типа 75 |
- |
Цитоскелетный кератин II типа 75 |
0,0001 |
|
3 |
Пероксисомальная , 2 , 4-диеноил-КоА-редуктаза |
- |
Пероксисомальная , 2 , 4-диеноил-КоА-редуктаза |
0,002 |
|
4 |
Адвиллин |
- |
Адвиллин |
0,019 |
|
5 |
Цитозольная альдегиддегидрогеназа 1 |
- |
Цитозольная альдегиддегидрогеназа 1 |
0,008 |
|
6 |
- |
Фактор удлинения 1-γ |
Фактор удлинения 1-γ |
0,001 |
|
7 |
- |
Белок-носитель стирола 2 |
Белок-носитель стирола 2 |
0,002 |
|
8 |
- |
Миозин-6 |
Миозин-6 |
0,002 |
|
9 |
- |
Кальций-связываю-щий белок 7 |
Кальций-связывающий белок 7 |
0,002 |
|
10 |
- |
Белок переноса везикул SEC22В |
Белок переноса везикул SEC22В |
0,001 |
|
Статистически значимые белки, выявленные одновременно в эксперименте при изолированной и комбинированной экспозиции |
||||
|
11 |
Гемоглобин субъединица β-2 |
0,001 |
||
|
12 |
Гликогенсинтаза, мышечная |
0,001 |
||
|
13 |
CAP - GLY домен содержащий линкерный белок 4 |
0,002 |
||
|
14 |
Белок переноса везикул SEC22A |
0,001 |
||
|
15 |
Белок SDA1 гомолог |
0,003 |
||
|
16 |
Активатор транскрипции BRG1 |
0,001 |
||
|
17 |
Каппа-цепь C области Ig, аллель |
0,001 |
||
|
18 |
APOBEC1 комплементарный фактор |
0,006 |
||
На основе денситометрического исследования и сопоставления белков в протеомном профиле плазмы крови экспонированных и неэкспонированных детей идентифицировано 20 достоверно различающихся пятен по их интенсивности и доказано связанных с повышенным содержанием меди и никеля в крови (табл. 2).
Сравнительный биоинформационный анализ филогенетики выявленных белков и кодирующих их экспрессию генов при экспериментальной и реальной комбинированной экспозиции позволил установить один тождественный белок - фактор комплементации APOBEC1 и ортологичный кодирующий его ген у человека - A1CF. Спектр пептида тождественного белка представлен на рисунке.
APOBEC1 комплементарный фактор представляет собой существенный компонент ферментного комплекса, редактирующего мРНК аполипопротеина В (ApoB), необходимого для сборки липопротеинов низкой плотности (ЛПНП) из липидов. У грызунов (Rattus norvegicus) комплементарный фактор APOBEC1 широко распространен в тканях печени [8], почек [9], кишечника [10], щитовидной железы и нервной системы [11]. У человека данный фактор экспрессируется исключительно в эпителиальных клетках желудочно-кишечного тракта, в тонком кишечнике [12, 13]. Результаты ряда экспериментальных исследований показали, что сверхэкспрессия APOBEC-1 в печени эффективно снижает уровни ApoB, регулируя метаболизм холестерина [14]. Низкая экспрессия гена A1CF у человека является одной из причин, по которой высокое потребление жиров является потенциально опасным для здоровья. В процессе всасывания экзогенных липидов уровень ApoB увеличивается, вызывая повышенный синтез липопротеина низкой плотности [15], что может привести к атеросклеротическим изменениям сосудов [14, 16].
Выявлена и оценена многофакторная зависимость ( R2 = 0,19; b 0 = 3581,2; b 1 = -384,5; b 2 = -11137,7; р = 0,017) снижения интенсивности белка APOBEC-1 комплементарного фактора в плазме крови при повышенном содержании одновременно никеля и меди в крови, являющихся маркерами экспозиции. Полученная зависимость согласуется с результатами научных исследований по генно-химическим взаимодействиям данного белка и изучаемых химических веществ. Показано, что экспозиция меди и никеля
Таблица 2
Параметры многофакторной модели зависимости изменения интенсивности белкового пятна в плазме крови от содержания одновременно никеля и меди в крови обследованных детей
|
№ п/п |
Наименование белка в пятне |
Направление изменения интенсивности белкового пятна |
Параметры модели «маркер экспозиции (никель и меди в крови) – протеомный маркер (интенсивность белкового пятна)» |
Достоверность различий ( р ≤ 0,05) |
|||
|
b 0 |
медь ( b 1 ) |
никель ( b 2) |
коэффициент детерминации ( R 2) |
||||
|
1 |
Обменник натрий/водорода 2 |
Снижение |
5291,9 |
-1458 |
-54723 |
0,24 |
0,013 |
|
2 |
Протеин 33, содержащий спиральную катушку |
Снижение |
5245,2 |
-1202,9 |
-63777,4 |
0,21 |
0,025 |
|
3 |
Миотубулярин |
Снижение |
1803 |
-1065,8 |
-39425,8 |
0,23 |
0,016 |
|
4 |
Фактор коагуляции V |
Снижение |
439,2 |
-270,6 |
-7449,8 |
0,19 |
0,032 |
|
5 |
Орнитин декарбоксилазный антизим 2 |
Снижение |
1112,9 |
-616,7 |
-28418,7 |
0,25 |
0,011 |
|
6 |
RING пальцевый протеин неопрятный гомолог |
Снижение |
2656,4 |
-821,9 |
-39891,8 |
0,19 |
0,031 |
|
7 |
Витронектин |
Снижение |
3092,7 |
-1860,8 |
-40674,4 |
0,16 |
0,059 |
|
8 |
Центросомный белок 290 кДа |
Снижение |
2242,6 |
-830,3 |
-49443,7 |
0,30 |
0,003 |
|
9 |
Цинковый белковый протеин 221 |
Снижение |
2989,8 |
-1496,5 |
-49250,8 |
0,24 |
0,013 |
|
10 |
Аполипопротеин A-I |
Снижение |
936,8 |
-660,6 |
1007,4 |
0,19 |
0,032 |
|
11 |
ADAM-подобный, decysin 1 |
Снижение |
3739,1 |
-1020,1 |
-62371,9 |
0,25 |
0,010 |
|
12 |
Ядерный белок MDM1 |
Повышение |
1596,3 |
935,8 |
38990 |
0,17 |
0,048 |
|
13 |
Фактор комплементации APOBEC1 |
Снижение |
3581,2 |
-384,5 |
-11137,7 |
0,13 |
0,017 |
|
14 |
DNAJ гомолог подсемейства C участник 3 |
Повышение |
2231,2 |
1747,2 |
63004,9 |
0,24 |
0,013 |
|
15 |
WD повторный белок 64 |
Повышение |
1014,9 |
768,6 |
44043,7 |
0,22 |
0,019 |
|
16 |
Зависимая от напряжения субъединица кальциевых каналов L-типа бета-4 |
Снижение |
1391,3 |
-861,5 |
-22471,4 |
0,25 |
0,010 |
|
17 |
Богатые лейцином повторы и домены, подобные иммуноглобулинам, белок 3 |
Снижение |
2531,7 |
-1032,3 |
-40311,9 |
0,19 |
0,033 |
|
18 |
Протеин-глутамин-гамма-глутамилтрансфераза E |
Повышение |
394,6 |
-35,5 |
32116,8 |
0,19 |
0,032 |
|
19 |
Пироглутамилпептидаза 1-подобный белок |
Повышение |
1657,4 |
666,3 |
39792,4 |
0,17 |
0,048 |
|
20 |
Тяжелая цепь клатрина 2 |
Снижение |
2605,8 |
-1031,1 |
-95362,5 |
0,36 |
0,001 |
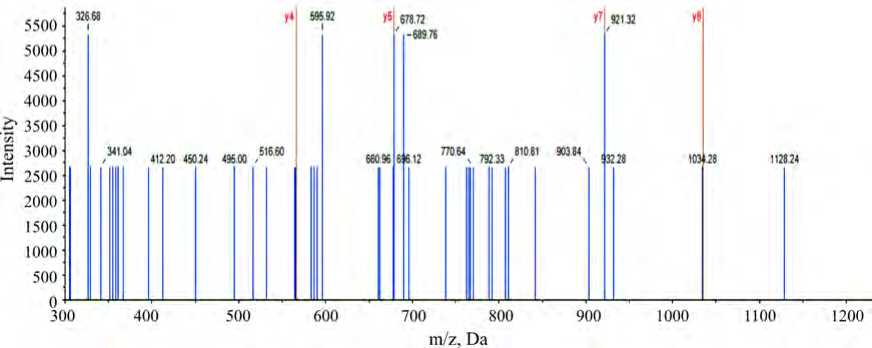
Рис. Спектр пептида SGPGLSGTQK (Комплементарный фактор APOBEC-1) (база данных SwissProt) плазмы крови ребенка приводит к снижению экспрессии гена A1CF. Это свидетельствует об их модифицирующем влиянии на молекулярные функции и биологические процессы данного белка [17]. Результаты экспериментальных исследований показали, что экспозиция никелем обусловливает повышение уровней триглицеридов и ЛПНП в сыворотке крови, что может негативно сказаться на обмене липидов в целом [18]. Аэрогенная экспозиция меди может привести к увеличению выработки активных форм кислорода и окислительному стрессу. Следствием чего является окислительная модификация ЛПНП, индуцирующая локальный иммунный ответ в стенке кровеносного сосуда с дальнейшим развитием атеросклеротических изменений – одного из факторов риска возникновения сердечно-сосудистых заболеваний [19–21].
Выводы. В результате выполненных исследований установлено, что длительная аэрогенная комбинированная экспозиция одновременно оксидами меди и никеля обусловливает в крови экспонированных детей повышенные (относительно показателей у неэкспонированных и референтных уровней) в 1,2–2,4 раза концентрации никеля и меди, обоснованные в качестве маркеров экспозиции. Результаты натурных исследований верифицированы повышенным в 1,7–2,9 раза содержанием аналогичных веществ в крови (относительно контроля) при экспериментальном моделировании эквивалентной комбинированной экспозиции на биологической модели (мелкие грызуны). Обоснован протеомный маркер APOBEC1 комплементарный фактор (ген А1CF), тождественный при экспериментальной и натурной экспозиции, доказанно связанный с маркерами экспозиции (одновременно с содержанием никеля и меди в крови). Снижение экспрессии данного белка в условиях сохраняющейся аэрогенной экспозиции оксидами никеля и меди позволяет прогнозировать развитие негативного эффекта в виде модификации липопротеинов низкой плотности с дальнейшей индукцией атеросклеротических изменений сосудов, что является одним из факторов риска сердечнососудистых заболеваний.
Финансирование. Исследование не имело спонсорской поддержки.
Список литературы Маркеры аэрогенной комбинированной экспозиции металлоксидными соединениями и трансформированного протеомного профиля плазмы крови у детей
- Омиксные технологии: роль и значение для развития персонализированной медицины / М.А. Пальцев, А.С. Чемезов, Н.С. Линькова, А.О. Дробинцева, В.О. Полякова, Н.Н. Белушкина, И.М. Кветной // Молекулярная медицина. - 2019. - № 4. - С. 3-8. DOI: 10.29296/24999490-2019-04-01
- Концепция факторов риска для здоровья населения / П.Ф. Кику, Д.С. Жигаев, Н.С. Шитер, К.М. Сабирова, М.А. Мезенцева // Бюллетень физиологии и патологии дыхания. - 2016. - № 62. - С. 101-109. DOI: 10.12737/23260
- Поиск белковых биомаркеров при атеросклерозе с помощью протеомных технологий как перспективное направление науки / Р.А. Жетишева, М.А. Ковалева, И.А. Каменихина, Л.И. Ковалев, В.Г. Наумов // Атеросклероз и дис-липидемии. - 2020. - Т. 39, № 2. - С. 12-19. DOI: 10.34687/2219-8202.JAD.2020.02.0002
- Comparative Toxicogenomics Database (CTD): update 2021 / A.P. Davis, C.J. Grondin, R.J. Johnson, D. Sciaky, J. Wiegers, T.C. Wiegers, C.J. Mattingly // Nucleic Acids Research. - 2021. - Vol. 49, № D1. - P. D1138-D1143. DOI: 10.1093/nar/gkaa891
- Chemical-Induced Phenotypes at CTD Help Inform the Predisease State and Construct Adverse Outcome Pathways / A.P. Davis, T.C. Wiegers, J. Wiegers, R.J. Johnson, D. Sciaky, C.J. Grondin, C.J. Mattingly // Toxicological sciences: an official journal of the Society of Toxicology. - 2018. - Vol. 165, № 1. - P. 145-156. DOI: 10.1093/toxsci/kfy131
- Зайцева Н.В., Землянова М.А., Долгих О.В. Геномные, транскриптомные и протеомные технологии как современный инструмент диагностики нарушений здоровья, ассоциированных с воздействием факторов окружающей среды // Гигиена и санитария. - 2020. - Т. 99, № 1. - С. 6-12. DOI: 10.33029/0016-9900-2020-99-1-6-12
- Долгих О.В., Дианова Д.Г., Казакова О.А. Ванадий в среде обитания как фактор риска негативной модификации клеточной гибели: научный обзор // Анализ риска здоровью. - 2020. - № 4. - С. 156-169. DOI: 10.21668/health.risk/2020.4.18
- Cunningham R.P., Porat-Shliom N. Liver Zonation - Revisiting Old Questions With New Technologies // Frontiers in physiology. - 2021. - № 12. - P. 732929. DOI: 10.3389/fphys.2021.732929
- Peroxisome-Deficiency and HIF-2a Signaling Are Negative Regulators of Ketohexokinase Expression / T. Eberhart, M.J. Schonenberger, K.M. Walter, K.N. Charles, P.L. Faust, W.J. Kovacs // Frontiers in cell and developmental biology. - 2020. -№ 8 (566). DOI: 10.3389/fcell.2020.00566
- Peroxidized Linoleic Acid, 13-HPODE, Alters Gene Expression Profile in Intestinal Epithelial Cells / N. Faizo, C.A. Narasimhulu, A. Forsman, S. Yooseph, S. Parthasarathy // Foods (Basel, Switzerland). - 2021. - Vol. 10, № 2. - P. 314. DOI: 10.3390/foods10020314
- Mysterious inhibitory cell regulator investigated and found likely to be secretogranin II related / J.E. Hart, I.J. Clarke, G.P. Risbridger, B. Ferneyhough, M. Vega-Hernández // Peer J. - 2017. - № 5. - P. e3833. DOI: 10.7717/peerj.3833
- Chen X.S. Insights into the Structures and Multimeric Status of APOBEC Proteins Involved in Viral Restriction and Other Cellular Functions // Viruses. - 2021. - Vol. 13, № 3. - P. 497. DOI: 10.3390/v13030497
- Transcriptome-wide sequencing reveals numerous APOBEC1 mRNA-editing targets in transcript 3' UTRs / B.R. Rosenberg, C.E. Hamilton, M.M. Mwangi, S. Dewell, F.N. Papavasiliou // Nat. Struct. Mol. Biol. - 2011. - Vol. 18, № 2. - P. 230-236. DOI: 10.1038/nsmb.1975
- Hypermutation induced by APOBEC-1 overexpression can be eliminated / Z. Chen, T.L. Eggerman, A.V. Bocharov, I.N. Baranova, T.G. Vishnyakova, G. Csako, A.P. Patterson // RNA (New York, N.Y.). - 2010. - Vol. 16, № 5. - P. 1040-1052. DOI: 10.1261/rna.1863010
- Lo C.C., Coschigano K.T. ApoB48 as an Efficient Regulator of Intestinal Lipid Transport // Front. Physiol. - 2020. -Vol. 11. - P. 796. DOI: 10.3389/fphys.2020.00796
- The RNA-Binding Protein A1CF Regulates Hepatic Fructose and Glycerol Metabolism via Alternative RNA Splicing / K.C. Nikolaou, H. Vatandaslar, C. Meyer, M.W. Schmid, T. Tuschl, M. Stoffel // Cell reports. - 2019. - Т. 2, № 29. - P. 283-300.e8. DOI: 10.1016/j.celrep.2019.08.100
- Song M.O., Li J., Freedman J.H. Physiological and toxicological transcriptome changes in HepG2 cells exposed to copper // Physiological genomics. - 2009. - Vol. 38, № 3. - P. 386-401. DOI: 10.1152/physiolgenomics.00083.2009
- Экспериментальная оценка токсичности наночастиц оксида никеля двух размеров в субхроническом эксперименте / М.П. Сутункова, Б.А. Кацнельсон, Л.И. Привалова, С.Н. Соловьева, В.Б. Гурвич, И.А. Минигалиева, С.В. Кли-нова, Т.В. Бушуева [и др.] // ЗНиСО. - 2018. - Т. 309, № 12. - C. 30-35.
- Investigation on the Association of Copper and Copper-to-Zinc-Ratio in Hair with Acute Coronary Syndrome Occurrence and Its Risk Factors / E.A. Dziedzic, A. Tuzimek, J.S. Gqsior, J. Paleczny, A. Junka, M. Kwasny, M. Dqbrowski, P. Jankowski // Nutrients. - 2022. - Vol. 14, № 19. - P. 4107. DOI: 10.3390/nu14194107
- Marín-García J. Molecular Determinants of Atherosclerosis // Post-Genomic Cardiology. - 2014. - Р. 183-215. DOI: 10.1016/b978-0-12-404599-6.00006-8
- Сухоруков В.Н., Карагодин В.П., Орехов А.Н. Атерогенные модификации липопротеинов низкой плотности // Биомедицинская химия. - 2016. - Т. 62, № 4. - С. 391-402. DOI: 10.18097/PBMC20166204391


