Машинная перфузия печени с умеренным макростеатозом: эффективность двойной гипотермической оксигенированной перфузии (D-HOPE)
Автор: Новрузбеков М.С., Балкаров А.Г., Яремин Б.И., Казымов Б.И., Свищева П.О., Павлова О.Н., Ханова С.М., Хубутия М.Ш.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Донорство и трансплантация органов и тканей
Статья в выпуске: 6 т.15, 2025 года.
Бесплатный доступ
Цель исследования. Оценка эффективности машинной перфузии в режиме гипотермической оксигенированной перфузии (HOPE) в снижении ишемически-реперфузионного повреждения (ИРП) донорской печени человека с умеренным макростеатозом путём анализа маркеров окислительного стресса, антиоксидантной защиты, воспалительного ответа, морфологических изменений и клинических исходов трансплантации. Материалы и методы. Проспективное пилотное исследование с включением 7 донорских печеней человека с макростеатозом 30–50%, верифицированным при экстренном гистологическом исследовании (окраска Oil Red O на замороженных срезах). Органы последовательно распределялись в контрольную группу — стандартное холодовое хранение при 4°C в растворе HTK (n=3) — и группу HOPE — гипотермическая оксигенированная перфузия при 10 °C в течение 4 часов с использованием системы Aferetica PerLife с непрерывным мониторингом портального сопротивления (целевой диапазон 0,15–0,25 мм рт.ст./(мл/мин/г)), клиренса лактата и рН перфузата (n=4). Портальный поток поддерживался в диапазоне 0,25–0,35 мл/мин/г, парциальное давление кислорода — 60–80 кПа. Оценивались маркеры окислительного стресса (малоновый диальдегид, МДА), активность антиоксидантных ферментов (супероксиддисмутаза, каталаза, глутатионпероксидаза), концентрация интерлейкина-6 (IL-6) в перфузате, морфологические признаки повреждения гепатоцитов (вакуолизация цитоплазмы, кариопикноз) при оценке в 10 полях зрения при ×400 двумя независимыми патологоанатомами вслепую, клинические исходы трансплантации на протяжении 6 месяцев наблюдения. Статистический анализ: однохвостовой тест Манна–Уитни (априорно направленная гипотеза), корреляционный анализ Спирмена, уровень значимости p<0,05. Данные представлены как M±SEM. Результаты. В группе HOPE зафиксировано статистически значимое снижение уровня МДА к моменту реперфузии (T3): 3,9±0,7 против 5,8±1,2 нмоль/мг белка в контрольной группе (p=0,029, снижение на 33%). Активность антиоксидантных ферментов в группе HOPE значимо превышала контроль: супероксиддисмутаза 18,7±2,8 против 12,3±2,1 Ед/мг белка (p=0,029); каталаза 203±34 против 145±28 Ед/мг белка (p=0,029); глутатионпероксидаза 13,2±2,1 против 8,9±1,6 Ед/мг белка (p=0,029). Концентрация IL-6 в перфузате к концу перфузии составила 52±14 пг/мл. Частота вакуолизации цитоплазмы гепатоцитов через 2 часа после реперфузии (T4): 38±9% в группе HOPE против 65±11% в контроле (p=0,029); кариопикноз: 11±3% против 18±4%. Портальное сопротивление в группе HOPE снизилось на 39% за 4 часа перфузии (p=0,063 от исходного). Клиренс лактата составил 50%. Корреляционный анализ выявил связь между МДА (Т3) и пиковым АЛТ (ρ=0,79, p=0,036), между МДА (Т3) и билирубином на 7-е сутки (ρ=0,71, p=0,074), между вакуолизацией (Т4) и длительностью пребывания в ОРИТ (ρ=0,83, p=0,021). Пиковые значения АЛТ: 820±190 Ед/л (HOPE) против 1180±340 Ед/л (контроль), снижение на 31%. Уровень общего билирубина на 7-е сутки: 41±11 против 62±16 мкмоль/л. Длительность пребывания в ОРИТ: 2,8±0,9 против 4,3±1,4 суток. За 6 месяцев наблюдения в контрольной группе зафиксированы тромбоз печёночной артерии (n=1, 33%) и билиарная стриктура (n=1, 33%); в группе HOPE сосудистых и билиарных осложнений не отмечено. Все реципиенты живы. Заключение. Гипотермическая оксигенированная перфузия обеспечивает значимую по биохимическим, антиоксидантным и морфологическим критериям защиту донорских печеней с умеренным макростеатозом от ИРП. Установлена прогностическая ценность МДА и морфологических маркеров для клинических исходов. Полученные предварительные данные обосновывают проведение многоцентровых рандомизированных исследований для валидации метода с последующей разработкой персонализированных протоколов перфузии.
Трансплантация печени, макростеатоз macrosteatosis, гипотермическая оксигенированная перфузия, двойная перфузия, ишемически-реперфузионное повреждение, консервация органов, окислительный стресс, антиоксидантная защита, маргинальные доноры, холодовая ишемия, липидная пероксидация
Короткий адрес: https://sciup.org/143185467
IDR: 143185467 | УДК: 616.36-089.843+616.36-003.826+615.036.8+616-092:612.015.11 | DOI: 10.20340/vmi-rvz.2025.6.TX.5
Machine Perfusion of Livers with Moderate Macrosteatosis: Efficacy of HOPE with Controlled Rewarming (D-HOPE)
Aim. To evaluate the efficacy of dual hypothermic oxygenated machine perfusion (D-HOPE) in reducing ischemia-reperfusion injury (IRI) in human donor livers with moderate macrosteatosis by analysing markers of oxidative stress, antioxidant defence, inflammatory response, morphological changes, and post-transplant clinical outcomes. Materials and Methods. A prospective pilot study enrolling 7 human donor livers with macrosteatosis of 30–50%, verified by urgent intraoperative histological examination (Oil Red O staining of frozen sections). Organs were sequentially allocated to a control group — static cold storage at 4°C in HTK solution (n=3) — or to the D-HOPE group — dual hypothermic oxygenated perfusion at 10 °C for 4 hours using the Aferetica PerLife system with continuous monitoring of portal resistance (target range 0.15–0.25 mmHg/(ml/min/g)), lactate clearance, and perfusate pH (n=4). Portal flow was maintained at 0.25–0.35 ml/min/g; oxygen partial pressure at 60–80 kPa. Assessed parameters included markers of oxidative stress (malondialdehyde, MDA), antioxidant enzyme activity (superoxide dismutase, catalase, glutathione peroxidase), interleukin-6 (IL-6) concentration in the perfusate, morphological signs of hepatocyte injury (cytoplasmic vacuolisation, karyopyknosis) scored in 10 high-power fields (×400) by two independent blinded pathologists, and clinical outcomes over a 6-month follow-up period. Statistical analysis: one-tailed Mann–Whitney test (a priori directional hypothesis), Spearman correlation analysis; significance threshold p<0.05. Data are presented as M±SEM. Results. The D-HOPE group demonstrated a statistically significant reduction in MDA at the time of reperfusion (T3): 3.9±0.7 vs. 5.8±1.2 nmol/mg protein in the control group (p=0.029; reduction of 33%). Antioxidant enzyme activity in the D-HOPE group significantly exceeded control values: superoxide dismutase 18.7±2.8 vs. 12.3±2.1 U/mg protein (p=0.029); catalase 203±34 vs. 145±28 U/mg protein (p=0.029); glutathione peroxidase 13.2±2.1 vs. 8.9±1.6 U/mg protein (p=0.029). Perfusate IL-6 concentration at the end of perfusion was 52±14 pg/ml. Hepatocyte cytoplasmic vacuolisation at 2 hours post-reperfusion (T4): 38±9% in D-HOPE vs. 65±11% in controls (p=0.029); karyopyknosis: 11±3% vs. 18±4%. Portal resistance in the D-HOPE group declined by 39% over the 4-hour perfusion period (p=0.063 from baseline). Lactate clearance was 50%. Correlation analysis revealed associations between MDA (T3) and peak ALT (ρ=0.79, p=0.036), between MDA (T3) and serum bilirubin on post-operative day 7 (ρ=0.71, p=0.074), and between vacuolisation (T4) and ICU length of stay (ρ=0.83, p=0.021). Peak ALT values: 820±190 U/L (D-HOPE) vs. 1,180±340 U/L (control), representing a 31% reduction. Total bilirubin on post-operative day 7: 41±11 vs. 62±16 μmol/L. ICU length of stay: 2.8±0.9 vs. 4.3±1.4 days. During the 6-month follow-up, the control group recorded hepatic artery thrombosis (n=1, 33%) and biliary stricture (n=1, 33%); no vascular or biliary complications were observed in the D-HOPE group. All recipients are alive. Conclusion. Dual hypothermic oxygenated perfusion provides statistically significant protection of moderately macrosteatotic donor livers from IRI, as assessed by biochemical, antioxidant, and morphological criteria. MDA and morphological markers demonstrated predictive value for post-transplant clinical outcomes. These preliminary data support the conduct of multicentre randomised trials to validate the technique and subsequently develop personalised perfusion protocols.
Текст научной статьи Машинная перфузия печени с умеренным макростеатозом: эффективность двойной гипотермической оксигенированной перфузии (D-HOPE)
Трансплантация печени остаётся единственным радикальным методом лечения терминальных заболеваний печени. Острый дефицит донорских органов является ключевой проблемой современной трансплантологии: согласно данным международных регистров, на один доступный донорский орган приходится в среднем 3–4 реципиента, находящихся в листе ожидания, а ежегодная смертность среди ожидающих трансплантации составляет 15–20% [1, 2]. Эта диспропорция побуждает трансплантационные центры последовательно расширять критерии приемлемости донорских органов.
Среди органов с расширенными критериями донора (ОРД) особое место занимают печени с макростеатозом. Умеренный макростеатоз — поражение 30–50% гепатоцитов крупнокапельными жировыми включениями — встречается у 20–30% потенциальных доноров [3, 4], что представляет существенный резерв для увеличения донорского пула. Однако стеатозные печени характеризуются повышенной уязвимостью к ишемически-реперфузионному повреждению (ИРП): нарушение микроциркуляции вследствие сдавления синусоидов увеличенными гепатоцитами, митохондриальная дисфункция и высокое содержание полиненасыщенных жирных кислот — субстрата для перекисного окисления — при- водят к увеличению частоты первичной дисфункции трансплантата до 40–50%, ишемических холангиопа-тий до 30–35% и повышению риска ранней потери трансплантата [5–7].
Патофизиология ИРП в стеатозной печени включает каскад взаимоотягощающих процессов. Накопление липидов в гепатоцитах приводит к компрессии синусоидов и редукции перфузии на 40–60%, что усугубляет гипоксию. Митохондриальная дисфункция, характерная для стеатоза, проявляется снижением активности комплексов I и III дыхательной цепи и истощением пула АТФ уже на этапе холодовой ишемии [5, 6]. При реперфузии массивное поступление кислорода в условиях дефицита антиоксидантов запускает генерацию активных форм кислорода (АФК), преимущественно через ксантиноксидазный путь. Перекисное окисление полиненасыщенных жирных кислот генерирует токсические альдегиды (малоновый диальдегид, 4-гидроксиноненаль), повреждающие клеточные мембраны и усиливающие митохондриальную дисфункцию. Активация pattern recognition receptors (TLR4, TLR9) молекулярными паттернами повреждения — damage-associated molecular patterns (HMGB1, митохондриальная ДНК, окисленные липопротеины) — индуцирует воспалительный каскад через NF- κ B, приводя к экспрессии провоспалительных цитокинов (TNF- α , IL-1 β , IL-6) и хемокинов (CXCL1, CCL2) [6, 7]. Интерлейкин-6, обладающий как про-, так и противовоспалительными свойствами в зависимости от контекста, служит биомаркером степени активации эндотелия и куп-феровских клеток [17].
Традиционная статическая консервация при 4 °C в растворе HTK (гистидин-триптофан-кетоглутарат) или UW (раствор Висконсинского университета) демонстрирует ограниченную эффективность для сте-атозных органов. Гипотермия замедляет метаболизм, но полностью не предотвращает истощение АТФ, прогрессирующий клеточный отёк вследствие нарушения работы ионных насосов и накопление токсических метаболитов. Машинная перфузия, обеспечивающая непрерывную доставку кислорода и питательных веществ, а также удаление токсических метаболитов, рассматривается как перспективная альтернатива [8]. Среди её вариантов наибольшее клиническое признание получила гипотермическая оксигенированная перфузия (HOPE, Hypothermic Oxygenated Perfusion), при которой орган перфузируется оксигенированным раствором при 8–12 °C [9].
Крупные клинические исследования убедительно продемонстрировали преимущества HOPE при трансплантации ОРД. Исследование Dutkowski et al. (2015, n=221) показало снижение частоты ишемических холангиопатий с 30% до 6% [10]. Работы van Rijn и соавт. (2017) и Patrono и соавт. (2019) подтвердили снижение частоты первичной дисфункции и улучшение ранней функции трансплантата [11, 12]. Метаанализ Schlegel и соавт. (2019, n>1000) зафиксировал стабильные положительные результаты применения HOPE [13]. Вместе с тем большинство упомянутых исследований были сфокусированы на печенях пожилых доноров или органах с длительной холодовой ишемией; систематические данные об эффективности HOPE специально для стеатозных печеней в литературе отсутствуют.
Настоящее пилотное исследование представляет первый российский опыт систематизированного применения HOPE для донорских печеней с умеренным макростеатозом с комплексной оценкой биохимических, антиоксидантных, морфологических и клинических параметров.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Оценить эффективность пилотного применения гипотермической оксигенированной перфузии (HOPE) в снижении ишемически-реперфузионного повреждения донорских печеней человека с умеренным макростеатозом (30–50%) путём комплексного анализа маркеров окислительного стресса, активности антиоксидантных ферментов, воспалительного ответа, морфологических изменений гепатоцитов и клинических исходов трансплантации.
ЗАДАЧИ ИССЛЕДОВАНИЯ
-
1. Разработать и верифицировать протокол машинной перфузии донорской печени с макростеатозом 30–50% в режиме HOPE с определением параметров температурного режима (10 °C), скорости портального потока (0,25–0,35 мл/мин/г), парциального давления кислорода (60–80 кПа) и длительности перфузии (4 часа).
-
2. Оценить динамику продуктов липидной пероксидации (малоновый диальдегид) и активность антиоксидантных ферментов (супероксиддисмутаза, каталаза, глутатионпероксидаза) в ткани печени в ключевых временных точках: до перфузии (T0), непосредственно перед трансплантацией (T3) и через 2 часа после реперфузии (T4).
-
3. Охарактеризовать воспалительный ответ органа в процессе перфузии по концентрации IL-6 в перфузате, оценить динамические параметры качества перфузии (портальное сопротивление, клиренс лактата, рН) и провести сравнительный анализ морфологических изменений при стандартном холодовом хранении и HOPE.
-
4. Оценить корреляцию биохимических и морфологических маркеров повреждения с клиническими исходами трансплантации в 6-месячный период наблюдения.
МАТЕРИАЛЫ И МЕТОДЫ
Дизайн исследования и включение органов
Проспективное пилотное исследование проводилось на базе центра трансплантации печени НИИ скорой помощи им. Н.В. Склифосовского. Часть лабораторных анализов выполнена на мощностях Медицинского университета «Реавиз» (Самара). В исследование включались донорские печени человека (n=7) от доноров со смертью мозга, у которых при экстренном гистологическом исследовании биопта-та, взятого непосредственно после изъятия органа, выявлялся макростеатоз в диапазоне 30–50%.
Критерии исключения: макростеатоз <30% или >50%; микровезикулярный стеатоз; время холодовой ишемии >12 часов; наличие признаков выраженного воспаления печени при интраоперационной ревизии; тромбоз воротной или печёночной вены.
Органы последовательно, в порядке поступления, распределялись в одну из двух групп согласно заранее утверждённому протоколу: контрольную (n=3) и группу HOPE (n=4). Рандомизация в классическом смысле не проводилась ввиду пилотного характера исследования и малого числа наблюдений; данное ограничение отражено в соответствующем разделе.
Гистологическая верификация стеатоза
Экстренное гистологическое исследование выполнялось на замороженных срезах с окраской Oil Red O. Процент гепатоцитов с крупнокапельными жировыми включениями оценивался двумя независимыми патологоанатомами, не осведомлёнными о принадлежности образцов к группам. Для количественного анализа подсчитывалось 500 клеток в 5 случайно выбранных полях зрения при увеличении ×200. Межэкспертная согласованность оценивалась по коэффициенту внутриклассовой корреляции (ICC) и составила 0,89 (95% ДИ 0,81–0,94), что свидетельствует о высокой воспроизводимости метода.
Ишемическое прекондиционирование
Всем донорам выполнялся манёвр Прингла (пережатие печёночно-двенадцатиперстной связки) продолжительностью 10 минут с последующей 10-минутной реперфузией непосредственно перед холодовой перфузией и изъятием органа. Процедура входила в стандартный протокол кондиционирования органов учреждения. Следует учитывать, что ишемическое прекондиционирование само по себе является протективным вмешательством с доказанным эффектом активации эндогенных защитных механизмов через индукцию HSP70, HO-1 и аденозиновых рецепторов [14]; поскольку оно проводилось в обеих группах в равной мере, его влияние на межгрупповые различия минимально, однако при интерпретации абсолютных значений маркеров ИРП данный фактор необходимо принимать во внимание.
Экспериментальный протокол
Протокол консервации и перфузии
После изъятия и начальной консервации раствором HTK органы транспортировались в операционную в условиях холодовой ишемии при 4 °C. По прибытии выполнялась биопсия для экстренной гистологии и подтверждения степени стеатоза, после чего осуществлялся дополнительный забор ткани печени для определения исходного уровня изучаемых параметров (T0).
Органы контрольной группы сохранялись при 4 °C в растворе HTK вплоть до момента трансплантации. Органы группы HOPE подключались к системе Aferetica PerLife (Aferetica, Италия). Перфузионный раствор на основе Belzer Machine Perfusion Solution (MPS, Bridge to Life, США) насыщался кислородом до парциального давления 60–80 кПа; целевая температура составляла 10°C, продолжительность перфузии — 4 часа (рис. 1).
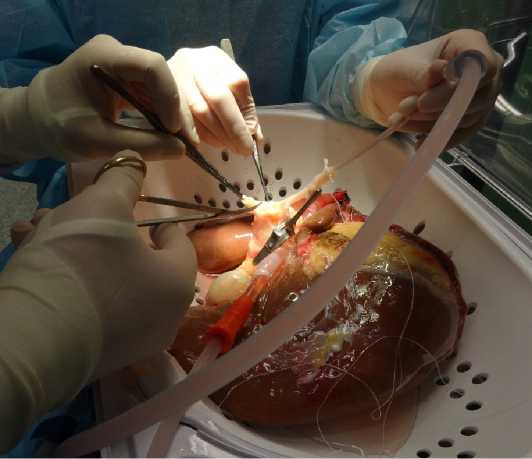
Рисунок 1. Back-table трансплантата печени в процессе выполнения biHOPE
Figure 1. Back-table of the liver transplant during biHOPE
Применялся протокол двойной (артериопор-тальной) гипотермической оксигенированной перфузии (D-HOPE, Dual-HOPE). Параметры перфузии:
-
• артериальный контур: давление 70 мм рт. ст., скорость потока 300 мл/мин;
-
• портальный контур: давление 12 мм рт. ст., скорость потока 0,25–0,35 мл/мин/г массы органа;
-
• непрерывный мониторинг артериального и портального давления, pH, лактата и глюкозы в перфузате.
Выбор диапазона pO₂ 60–80 кПа обусловлен техническими особенностями применявшейся афере-тической системы и необходимостью поддержания умеренной оксигенации без риска гипероксическо- кованных протоколов HOPE (40–60 кПа) [10], но го повреждения; данный диапазон несколько пре- находится в пределах физиологически безопасных вышает параметры, используемые в части опубли- значений.
Временные точки забора материала
|
Точка |
Описание |
Материал |
|
T0 |
Исходный уровень — сразу после изъятия и верификации степени стеатоза |
Биоптат печени |
|
T3 |
По завершении 4-часовой перфузии (D-HOPE) или перед трансплантацией после холодового хранения (контроль) |
Биоптат печени; перфузат (D-HOPE) |
|
T4 |
Интраоперационно, через 2 часа после реперфузии in vivo |
Биоптат печени |
Биоптаты немедленно замораживались в жидком азоте (для биохимии) или фиксировались в 10% нейтральном формалине (для гистологии). Образцы перфузата забирались каждые 60 минут, центрифугировались при 3000 g × 10 мин и хранились при -80 °C до анализа.
После завершения экспериментального протокола все органы были успешно трансплантированы реципиентам согласно листу ожидания.
Оценка окислительного стресса
Концентрация малонового диальдегида (МДА) определялась спектрофотометрическим методом с тиобарбитуровой кислотой (TBA). Ткань печени (50 мг) гомогенизировалась в холодном фосфатном буфере (pH 7,4) с ингибитором протеаз (Complete Mini, Roche); после центрифугирования при 10 000 g ×15 мин супернатант инкубировался с 0,67% TBA при 95 °C × 60 мин. Комплекс МДА-TBA экстрагировался н-бутанолом и измерялся при 532 нм (коэффициент молярной экстинкции 1,56×10⁵ М⁻¹см⁻¹). Концентрация выражалась в нмоль/мг белка; содержание белка определялось по методу Лоури.
Оценка антиоксидантной системы
Активность супероксиддисмутазы (СОД) определялась спектрофотометрически при 550 нм по степени ингибирования восстановления нитросинего тет-разолия (NBT) в системе ксантин/ксантиноксидаза. Активность каталазы оценивалась по скорости разложения перекиси водорода при 240 нм. Активность глутатионпероксидазы измерялась по окислению NADPH при 340 нм в присутствии глутатионредукта-зы. Все измерения проводились при 25 °C. Активность выражалась в Ед/мг белка, где одна единица соответствует количеству фермента, катализирующему превращение 1 мкмоль субстрата в минуту.
Оценка воспалительного ответа
Концентрация IL-6 в перфузате определялась методом иммуноферментного анализа с использованием коммерческого набора Human IL-6 Quantikine ELISA Kit (R&D Systems, США) в соответствии с инструкцией производителя. Анализ проводился в дубликатах; оптическая плотность измерялась при 450 нм с референс-длиной волны 540 нм на микро-планшетном ридере (BioTek ELx800). Минимальная определяемая концентрация составила 0,70 пг/мл;
внутри- и межсерийная вариабельность не превышала 5,2% и 7,8% соответственно. IL-6 измерялся только в перфузате группы HOPE ввиду отсутствия перфузата в контрольной группе; прямое межгрупповое сравнение данного параметра невозможно.
Гистологический анализ
Световая микроскопия
Парафиновые срезы толщиной 4 мкм окрашивались гематоксилином и эозином. Оценка проводилась двумя независимыми патологоанатомами вслепую в 10 случайно выбранных полях зрения при ×400. Регистрировались: процент гепатоцитов с вакуолизацией цитоплазмы (клеточный отёк); процент клеток с кариопикнозом (необратимое ядерное повреждение); наличие очаговых некрозов; степень синусоидальной дилатации. Разногласия между оценщиками разрешались консенсусом при повторном совместном просмотре препаратов. Межэкспертная согласованность по коэффициенту ICC составила 0,87 (95% ДИ 0,78–0,92).
Полутонкие срезы
Для предварительной оценки и выбора репрезентативных участков изготавливались полутонкие срезы толщиной 0,5–1 мкм на ультрамикротоме. Срезы окрашивались 1% раствором толуидинового синего на 1% растворе тетрабората натрия в течение 30–60 секунд при 60°C, после чего промывались дистиллированной водой и высушивались. Окраска толуидиновым синим позволяла оценить общую морфологию ткани, выявить зоны повреждения и определить оптимальные участки для ультратонких срезов. Просмотр осуществлялся на световом микроскопе при увеличении ×400–1000.
Электронная микроскопия
Образцы ткани печени размером 1×1×1 мм фиксировались в 2,5% глутаральдегиде на 0,1 М какодилатном буфере (pH 7,4) в течение 2 часов при 4 °C. После трёхкратной отмывки буфером проводилась постфиксация в 1% тетраоксиде осмия (OsO₄) в течение 1 часа. Образцы обезвоживались в серии этанола возрастающей концентрации (50%, 70%, 96%, 100%) и пропиленоксиде, после чего заливались в эпоксидную смолу (Epon-812).
Ультратонкие срезы толщиной 70–90 нм изготавливались на ультрамикротоме, контрастировались уранилацетатом и цитратом свинца по Рейнольдсу. Исследование проводилось на трансмиссионном электронном микроскопе HITACHI HT7800 (Hitachi High-Tech Corporation, Япония) при ускоряющем напряжении 80 кВ. Цифровые изображения получали с помощью встроенной CCD-камеры.
Оценивались следующие ультраструктурные параметры: состояние митохондрий (набухание, деструкция крист, электронная плотность матрикса), целостность мембран эндоплазматического ретикулума, состояние ядерной оболочки и распределение хроматина, сохранность межклеточных контактов (десмосомы, плотные контакты), наличие аутофагосом и признаков апоптоза, состояние синусоидального эндотелия и пространств Диссе. Полуко-личественная оценка ультраструктурных повреждений проводилась по 4-балльной шкале (0 — норма, 1 — минимальные изменения, 2 — умеренные изменения, 3 — выраженные изменения) в не менее чем 20 клетках на образец.
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ
Послеоперационный мониторинг включал: АЛТ, АСТ, общий билирубин, МНО в динамике (1, 3, 7, 14, 30-е сутки); ультразвуковую допплерографию печёночной артерии и воротной вены в раннем послеоперационном периоде (ежедневно в течение первой недели); регистрацию сосудистых и билиарных осложнений, длительности пребывания в ОРИТ и выживаемости реципиентов в течение 6 месяцев.
Статистический анализ
Статистический анализ выполнен в программной среде R версии 4.3.0. Нормальность распределения проверялась критерием Шапиро–Уилка (интерпретируемым с осторожностью при n<10). При отклонении от нормального распределения применялся критерий Манна–Уитни для сравнения двух независимых групп. Учитывая априорно направленный характер гипотезы (ожидаемое снижение маркеров ИРП в группе HOPE по сравнению с контролем), применялся однохвостовой вариант теста. При n=3 и n=4 минимально достижимое однохвостовое p-значение точного критерия перестановок составляет 1/C(7,3) = 0,029. Динамика параметров перфузии внутри группы HOPE оценивалась парным критерием Вилкоксона (однохвостовой; при n=4 парах минимально достижимое p = 0,063). Корреляционный анализ выполнялся по методу Спирмена; для пары ρ=0,71 (n=7) получено p=0,074, что расценивается как тенденция без достижения уровня значимости. Уровень значимости: p<0,05. Все данные представлены как M±SEM (среднее ± стандартная ошибка среднего). Поправка на множественные сравнения не применялась ввиду пилотного и разведочного характера исследования; результаты следует трактовать как предварительные, требующие подтверждения на большей выборке.
РЕЗУЛЬТАТЫ
Характеристики донорских органов
В исследование включены 7 донорских печеней. Характеристики органов по группам представлены в таблице 1.
|
Таблица 1. Характеристики донорских органов Table 1. Characteristics of donor organs |
|||
|
Параметр |
Контроль (n=3) |
HOPE (n=4) |
p |
|
Степень макростеатоза, % |
38±6 |
41±5 |
0,64 |
|
Время холодовой ишемии, ч |
6,2±1,1 |
5,8±0,9 |
0,71 |
|
Масса органа, г |
1580±140 |
1620±120 |
0,79 |
Примечание: все органы соответствовали критериям ОРД согласно классификации Eurotransplant. Межгрупповые различия по основным характеристикам статистически незначимы.
Все органы соответствовали критериям ОРД. Степень макростеатоза, верифицированная окраской Oil Red O, находилась в диапазоне 30–50% во всех наблюдениях; межгрупповые различия по этому критическому параметру отсутствовали, что обеспечивало сопоставимость групп по исходной степени повреждения.
Параметры перфузии и динамические показатели качества (группа HOPE)
На протяжении всего 4-часового периода перфузии заданные параметры поддерживались в целевых диапазонах: портальный поток 0,25–0,35 мл/мин/г, pO₂ перфузата 60–80 кПа, температура 10±0,5°C. Значимых технических отклонений не зафиксировано.
Динамика параметров, отражающих качество перфузии и метаболическую активность органов, представлена в таблице 2.
Портальное сопротивление снизилось на 39% за период перфузии (p=0,063), что свидетельствует о восстановлении микроциркуляции и редукции синусоидального отёка. Клиренс лактата составил 50% от исходного уровня, отражая сохранность метаболической функции печени в условиях гипотермической перфузии. Стабилизация рН в физиологическом диапазоне (7,39±0,02 к 4-му часу) указывает на метаболическую компенсацию органа. Потребление глюкозы (снижение на 27% за 4 часа) подтверждает наличие базового энергетического метаболизма, поддерживаемого умеренной оксигенацией.
Таблица 2. Динамика параметров перфузии (группа HOPE, n=4, M±SEM)
Table 2. Dynamics of perfusion parameters (HOPE group, n=4, M±SEM)
|
Параметр |
0 ч |
1 ч |
2 ч |
3 ч |
4 ч |
p* |
|
Портальное сопротивление, мм рт.ст./(мл/мин/г) |
0,31±0,04 |
0,28±0,03 |
0,24±0,03 |
0,21±0,02 |
0,19±0,02 |
0,063 |
|
Лактат, ммоль/л |
8,2±1,1 |
6,9±0,9 |
5,8±0,8 |
4,9±0,7 |
4,1±0,6 |
0,063 |
|
рН |
7,18±0,05 |
7,26±0,04 |
7,32±0,03 |
7,37±0,02 |
7,39±0,02 |
0,063 |
|
Глюкоза, ммоль/л |
11,2±0,8 |
10,1±0,7 |
9,3±0,6 |
8,7±0,5 |
8,2±0,5 |
0,063 |
Примечание: *p — для сравнения значений в точках 0 ч и 4 ч (парный однохвостовой критерий Вилкоксона; при n=4 минимально достижимое p = 0,063).
Маркеры окислительного стресса
Уровень МДА прогрессивно увеличивался в обеих группах от точки T0 к точке T3 вследствие накопления продуктов липидной пероксидации в ходе холодовой ишемии. Однако степень этого нарастания существенно различалась между группами.
Таблица 3. Динамика МДА в ткани печени (M±SEM, нмоль/мг белка)
Table 3. Dynamics of MDA in liver tissue (M±SEM, nmol/mg protein)
|
Группа |
T0 (исходно) |
T3 (перед трансплант ацией) |
Δ от T0, % |
p (T0 vs T3) |
|
Контроль (n=3) |
2,1±0,4 |
5,8±1,2 |
+176% |
0,125 |
|
HOPE (n=4) |
2,3±0,3 |
3,9±0,7 |
+70% |
0,063 |
|
p (межгрупповое) |
0,68 |
0,029 |
— |
— |
В контрольной группе концентрация МДА в точке T3 составила 5,8±1,2 нмоль/мг белка, что почти в 3 раза превышает исходный уровень. В группе HOPE аналогичный показатель был значимо ниже: 3,9±0,7 нмоль/мг белка (p=0,029 по критерию Манна– Уитни), что соответствует снижению на 33% относительно контроля. Данные свидетельствуют о существенном подавлении процессов липидной пероксидации при применении HOPE.
Активность антиоксидантных ферментов
Оценка активности ключевых ферментов антиоксидантной защиты в точке T3 (непосредственно перед трансплантацией) выявила статистически значимые межгрупповые различия.
Таблица 4. Активность антиоксидантных ферментов в точке T3 (M±SEM)
Table 4. Antioxidant enzyme activity at point T3 (M±SEM)
|
Фермент |
Контроль (n=3) |
HOPE (n=4) |
Δ, % |
p |
|
Супероксиддисмутаза, Ед/мг белка |
12,3±2,1 |
18,7±2,8 |
+52% |
0,029 |
|
Каталаза, Ед/мг белка |
145±28 |
203±34 |
+40% |
0,029 |
|
Глутатионпероксидаза , Ед/мг белка |
8,9±1,6 |
13,2±2,1 |
+48% |
0,029 |
Активность всех трёх основных антиоксидантных ферментов была значимо выше в группе HOPE по сравнению с контролем. Это указывает на активацию эндогенной антиоксидантной защиты в процессе гипотермической оксигенированной перфузии, что может рассматриваться как адаптивный ответ на умеренный окислительный стресс — своего рода «прекондиционирование перфузией».
Воспалительный ответ
Концентрация IL-6 в перфузате группы HOPE к концу 4-часовой перфузии концентрация IL-6 в перфузате достигла значения (T3) значения 52±14 пг/мл. Данный уровень свидетельствует об умеренной воспалительной активации, характерной для успешной перфузии. Полученные значения не превышают порогового уровня 100 пг/мл, ассоциированного с тяжёлым органным повреждением [15], и сопоставимы с данными международных протоколов HOPE [10, 12].
Следует подчеркнуть, что IL-6 не измерялся в тканевых образцах и не сравнивался с контрольной группой; его однократное определение в перфузате в финальной точке не позволяет характеризовать динамику воспалительного ответа на протяжении перфузии.
Морфологические признаки повреждения
Гистологический анализ биоптатов, взятых через 2 часа после реперфузии in vivo (T4), выявил значимые межгрупповые различия по маркерам клеточного повреждения.
Таблица 5. Морфологические маркеры повреждения гепатоцитов в точке T4 (M±SEM)
Table 5. Morphological markers of hepatocyte damage at point T4 (M±SEM)
|
Показатель |
Контроль (n=3) |
HOPE (n=4) |
Δ, % |
p |
|
Вакуолизация цитоплазмы, % клеток |
65±11 |
38±9 |
-42% |
0,029 |
|
Кариопикноз, % клеток |
18±4 |
11±3 |
-39% |
0,11 |
|
Очаговые некрозы, баллы (0–3) |
2,1±0,4 |
1,3±0,3 |
-38% |
0,09 |
Вакуолизация цитоплазмы гепатоцитов (клеточный отёк) зарегистрирована в 65±11% клеток контрольной группы против 38±9% в группе HOPE (p=0,029), что соответствует снижению на 42%. Ка-риопикноз — морфологический маркер необратимого повреждения — выявлен в 18±4% гепатоцитов в контроле и 11±3% в группе HOPE (тенденция к снижению на 39%, статистическая значимость не достигнута).
В контрольной группе морфологические изменения были более выражены в перипортальных зонах (зона 1 по Rappaport) — области наиболее интенсивного метаболизма и наибольшей уязвимости при ИРП. В группе HOPE зональная гетерогенность по- вреждения была менее выражена, что может отражать более равномерное распределение кислорода и субстратов по печёночной дольке при машинной перфузии по сравнению со статическим хранением.
А
Б
В
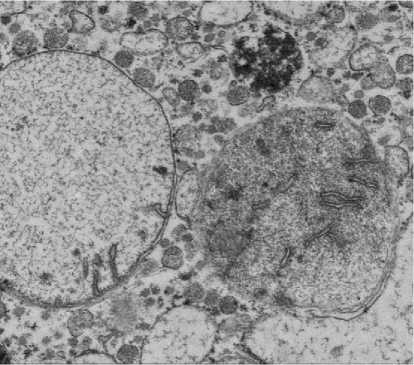
Г
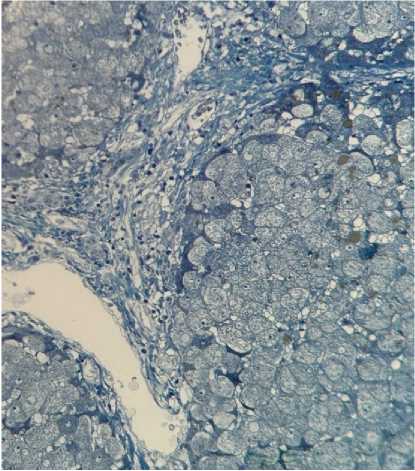
Д
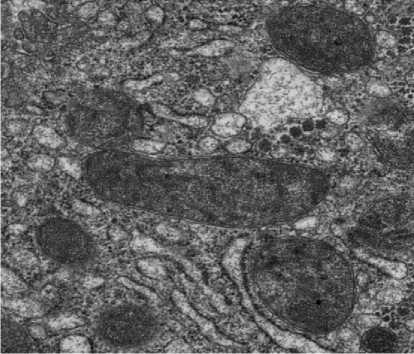
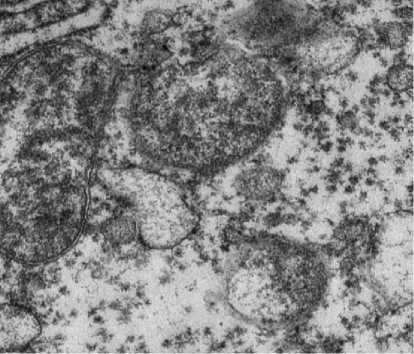
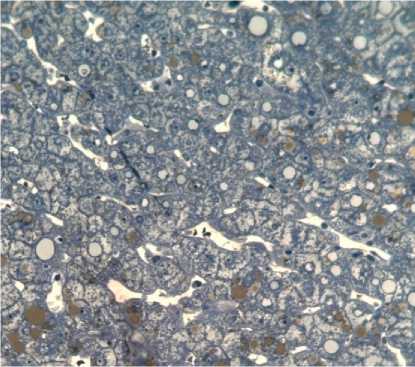
Рисунок 2. Гистологические признаки ишемически-реперфузионного повреждения трансплантатов печени в группах сравнения. А. Группа HOPE, ТЭМ — митохондрии с сохранной двухконтурной мембраной, дифференцируемыми кристами, точка Т4. Б. Митохондрии с нарушением целостности мембраны, разрушением крист. Группа холодового статического хранения. ТЭМ, точка Т4. В. Группа HOPE, точка Т2. Вакуолизация цитоплазмы гепатоцитов, кариопикноз ядер. Окраска толуидиновым синим, ×400. Г. Митохондрии неправильной формы с деформированными и разрушенными кристами. Группа холодового статического хранения. ТЭМ, точка Т2. Д. Некроз гепатоцитов в 1 зоне ацинуса. Окраска толуидиновым синим, ×400. Группа холодового статического хранения. Точка Т2 Figure 2. Histological features of ischemia-reperfusion injury in liver grafts across comparison groups. A. HOPE group, TEM — mitochondria with intact double-membrane, differentiable cristae, time point T4. Б. Mitochondria with disrupted membrane integrity and cristae destruction. Cold static storage group. TEM, time point T4. В. HOPE group, time point T2. Vacuolization of hepatocyte cytoplasm, karyopyknosis of nuclei. Toluidine blue staining, ×400. Г. Irregularly shaped mitochondria with deformed and destroyed cristae. Cold static storage group. TEM, time point T2. Д. Hepatocyte necrosis in acinar zone 1. Toluidine blue staining, ×400. Cold static storage group. Time point T2
Клинические исходы трансплантации
Результаты клинического наблюдения за реципиентами на протяжении 6 месяцев представлены в таблице 6.
Таблица 6. Клинические исходы трансплантации (M±SEM)
Table 6. Clinical outcomes of transplantation (M±SEM)
|
Показатель |
Контроль (n=3) |
HOPE (n=4) |
Δ, % |
p |
|
Пиковый АЛТ, Ед/л |
1180±340 |
820±190 |
-31% |
нз* |
|
Пиковый АСТ, Ед/л |
1520±410 |
1090±260 |
-28% |
нз* |
|
Общий билирубин на 7-е сутки, мкмоль/л |
62±16 |
41±11 |
-34% |
нз* |
|
Длительность ОРИТ, сутки |
4,3±1,4 |
2,8±0,9 |
-35% |
нз* |
|
Тромбоз печёночной артерии, n (%) |
1 (33%) |
0 (0%) |
— |
нз* |
|
Билиарная стриктура, n (%) |
1 (33%) |
0 (0%) |
— |
нз* |
|
Выживаемость реципиентов, 6 мес |
3/3 (100%) |
4/4 (100%) |
— |
— |
Примечание: *нз — различия не достигают статистической значимости при данном размере выборки; результаты носят предварительный характер.
Все клинические показатели демонстрируют устойчивую тенденцию в пользу группы HOPE: снижение пиковых значений АЛТ на 31%, АСТ на 28%, уровня билирубина на 7-е сутки на 34%, длительности пребывания в ОРИТ на 35%. Однако при n=3 и n=4 ни один из этих показателей не достигает статистической значимости.
Пиковые значения АЛТ в обеих группах оставались ниже порогового уровня 2000 Ед/л, ассоциированного с высоким риском первичной дисфункции трансплантата [16]. В контрольной группе за период наблюдения зафиксированы два осложнения: тромбоз печёночной артерии (n=1, потребовал экстренной ретрансплантации на 12-е сутки) и стриктура общего печёночного протока (n=1, успешно разрешена эндоскопическим стентированием). В группе HOPE сосудистых и билиарных осложнений не отмечено. Все реципиенты живы на момент завершения 6-месячного наблюдения.
Корреляционный анализ
Выполнен корреляционный анализ Спирмена между биохимическими/морфологическими маркерами и клиническими исходами для всей выборки (n=7).
Таблица 7. Корреляционный анализ (метод Спирмена, n=7)
Table 7. Correlation analysis (Spearman's method, n=7)
|
Пара параметров |
ρ |
p |
|
МДА (Т3) vs пиковый АЛТ |
0,79 |
0,036 |
|
МДА (Т3) vs общий билирубин (7 день) |
0,71 |
0,074 |
|
Вакуолизация (Т4) vs длительность ОРИТ |
0,83 |
0,021 |
|
IL-6 перфузата (HOPE) vs пиковый АЛТ |
-0,18 |
0,82* |
|
Активность СОД (Т3) vs пиковый АЛТ |
-0,68 |
0,09 |
Примечание: *Анализ проведён только для группы HOPE (n=4).
Уровень МДА в момент трансплантации (Т3) демонстрирует умеренную положительную корреляцию с маркерами печёночного повреждения в раннем послеоперационном периоде: пиковым АЛТ ( ρ =0,79, p=0,036) и уровнем билирубина на 7-е сутки ( ρ =0,71, p=0,074). Это подтверждает прогностическую ценность МДА как предиктора тяжести ИРП. Частота вакуолизации гепатоцитов через 2 часа после реперфузии (Т4) также коррелирует с длительностью пребывания в ОРИТ ( ρ =0,83, p=0,021), что указывает на связь между степенью морфологического повреждения и клиническим течением.
Отсутствие корреляции между IL-6 в перфузате и пиковым АЛТ ( ρ =-0,18, p=0,82) может отражать адаптивный, а не повреждающий характер воспалительного ответа при HOPE. Данное наблюдение требует дальнейшего изучения с расширением панели цитокинов (TNF- α , IL-10, TGF- β ).
ОБСУЖДЕНИЕ
Окислительный стресс как центральный механизм ИРП при стеатозе
Статистически значимое снижение уровня МДА в группе HOPE (3,9±0,7 против 5,8±1,2 нмоль/мг белка, p=0,029, снижение на 33%) свидетельствует о существенном подавлении липидной пероксидации – ключевого звена патогенеза ИРП в стеатозных печенях. Печени с макростеатозом содержат повышенное количество полиненасыщенных жирных кислот, служащих субстратом для перекисного окисления [5], что обусловливает их особую уязвимость к окислительному стрессу по сравнению с нестеатозными органами.
Механизм антиоксидантного действия HOPE включает несколько взаимодополняющих факторов. Гипотермия (10°C) редуцирует скорость образования активных форм кислорода пропорционально снижению метаболической активности — приблизительно в 3–4 раза по сравнению с нормотермией. Постоянная оксигенация при умеренном парциальном давлении (60–80 кПа) предупреждает критическую гипоксию — триггер массивной генерации свободных радикалов при последующей реоксигенации. Непрерывный поток перфузата обеспечивает выведение токсических продуктов пероксидации (МДА, 4-гидроксиноненаль) из ткани органа, предотвращая их дальнейшее повреждающее действие на мембраны и белки [9, 10].
Важно учитывать, что все доноры в обеих группах получали ишемическое прекондиционирование (манёвр Прингла 10+10 мин), которое само по себе активирует эндогенные антиоксидантные механизмы через индукцию белков теплового шока (HSP70), гемоксигеназы-1 (HO-1) и активацию аденозиновых рецепторов [14]. Поскольку прекондиционирование применялось равномерно в обеих группах, его влияние на выявленные межгрупповые различия по МДА, по всей видимости, нивелируется; тем не менее абсолютные значения МДА в настоящем исследовании могут оказаться ниже, чем в протоколах без прекондиционирования, что следует учитывать при сопоставлении с литературными данными.
Активация антиоксидантной системы
Статистически значимое повышение активности всех трёх ключевых антиоксидантных ферментов в группе HOPE (супероксиддисмутаза +52%, каталаза +40%, глутатионпероксидаза +48%; все p<0,05) представляет особый интерес. Данные результаты указывают на мобилизацию эндогенной антиоксидантной защиты в условиях умеренного окислительного стресса, характерного для гипотермической оксигенированной перфузии.
Это явление можно трактовать как «прекондиционирование перфузией», аналогичное ишемическому прекондиционированию: субповреждающий стимул индуцирует адаптивный ответ, повышающий резистентность органа к последующему более тяжёлому повреждению [14]. Умеренная генерация активных форм кислорода в процессе HOPE может служить сигналом для активации транскрипционного фактора Nrf2 (nuclear factor erythroid 2-related factor 2), который регулирует экспрессию широкого спектра антиоксидантных и детоксицирующих ферментов, включая СОД, каталазу, глутатионпероксидазу, глутатион-S-трансферазы и NADPH:хинон оксидоредуктазу.
Стойкое повышение активности антиоксидантных ферментов к моменту трансплантации (Т3) обеспечивает органу дополнительную защиту на критическом этапе реперфузии in vivo, когда генерация АФК достигает максимума. Данный механизм может вносить существенный вклад в наблюдаемое снижение МДА и морфологического повреждения в группе HOPE.
Молекулярные механизмы протективного эффекта HOPE
Защитное действие HOPE реализуется на нескольких уровнях организации.
Митохондриальный уровень. Гипотермическая оксигенация при 10°C снижает скорость потребления кислорода в 3–4 раза по сравнению с нормо-термией, но полностью не прекращает окислительное фосфорилирование. Это «метаболическое окно» позволяет поддерживать базовую продукцию АТФ (≈15% от нормотермического уровня), достаточную для функционирования Na⁺/K⁺-АТФазы и
Ca²⁺-АТФазы плазматической мембраны и саркоплазматического ретикулума, что предотвращает ионную дерегуляцию и клеточный отёк. Умеренная оксигенация (pO₂ 60–80 кПа) обеспечивает работу комплексов дыхательной цепи в «контролируемом 281
режиме», минимизируя утечку электронов и генерацию супероксид-аниона в комплексах I и III.
Уровень антиоксидантной системы. Как было показано выше, HOPE индуцирует активацию СОД, каталазы и глутатионпероксидазы. Эти ферменты работают последовательно, образуя интегрированную систему нейтрализации АФК: СОД катализирует дисмутацию супероксид-аниона (O₂•⁻) в перекись водорода (H₂O₂); каталаза и глутатионпероксидаза нейтрализуют H₂O₂, превращая её в воду. Координированная активация всех трёх ферментов обеспечивает полноценную защиту от окислительного повреждения.
Эндотелиальный уровень. Постоянная перфузия предупреждает адгезию тромбоцитов и лейкоцитов к эндотелию — ключевое звено микроциркулятор-ных нарушений при ИРП. Снижение портального сопротивления на 39% за 4 часа перфузии (табл. 2) отражает восстановление микроциркуляции и редукцию синусоидального отёка. Механический поток (shear stress) стимулирует продукцию оксида азота (NO) эндотелием через активацию эндотелиальной NO-синтазы (eNOS), что поддерживает вазодилатацию и ингибирует активацию NF- κ B — ключевого транскрипционного фактора воспалительного ответа.
Уровень купферовских клеток. Умеренная воспалительная активация (IL-6 52 пг/мл в перфузате) может отражать переключение макрофагов на M2-фенотип (противовоспалительный, репаративный) под влиянием умеренного стресса и механических стимулов перфузии. M2-макрофаги секретируют противовоспалительные цитокины (IL-10, TGF- β ) и ростовые факторы, способствующие регенерации. Данная гипотеза требует подтверждения измерением IL-10 и TGF- β в будущих исследованиях.
Воспалительный ответ и роль IL-6
Концентрация IL-6 в перфузате (52±14 пг/мл) отражает умеренную активацию воспалительного ответа, характерную для успешной перфузии. Значение не превышает порогового уровня 100 пг/мл, ассоциированного с тяжёлым органным повреждением [15], и сопоставимо с данными международных протоколов HOPE [10, 12].
Следует подчеркнуть, что IL-6 не измерялся в тканевых образцах и не сравнивался с контрольной группой; его однократное определение в перфузате в финальной точке не позволяет характеризовать динамику воспалительного ответа на протяжении перфузии. В дальнейших исследованиях целесообразно измерять IL-6 в перфузате в серийных точках (0, 60, 120, 180, 240 мин) и параллельно — в ткани органа для сопоставления системного и локального воспалительного ответа.
ского повреждения. Снижение частоты кариопикно-за напрямую коррелирует с функциональным резервом трансплантата и потенциалом регенерации.
Менее выраженная зональная гетерогенность повреждения в группе HOPE (более равномерное распределение повреждения по зонам печёночной дольки) может отражать более равномерное распределение кислорода и субстратов при машинной перфузии по сравнению со статическим хранением. В норме печёночная долька характеризуется градиентом кислорода от перипортальной зоны (pO₂ ≈60 мм рт.ст.) к центролобулярной (pO₂ ≈30 мм рт.ст.). При статическом хранении этот градиент резко усиливается, что приводит к преимущественному повреждению перипортальной зоны — наиболее метаболически активной и чувствительной к гипоксии. Машинная перфузия нивелирует этот градиент, обеспечивая более гомогенную оксигенацию.
Клинические результаты в контексте литературы
Тенденция к улучшению клинических показателей в группе HOPE (снижение пиковых трансаминаз на 31%, уровня билирубина на 34%, длительности ОРИТ на 35%, отсутствие билиарных и сосудистых осложнений) согласуется с данными крупных международных исследований [10–13]. Вместе с тем ни один из перечисленных показателей не достигает статистической значимости при данном размере выборки, и их трактовка должна быть строго осторожной.
Полученное снижение МДА на 33% сопоставимо с данными Kron et al. (2016), показавших редукцию окислительного стресса на 28% при HOPE печеней от доноров с асистолией (DCD) [18]. Patrono et al. (2019) сообщили о снижении пиковых значений АЛТ на 35% в группе HOPE (n=46) по сравнению со стандартным холодовым хранением [12], что близко к нашим результатам (31%), но при существенно большей статистической мощности.
Частота ишемических холангиопатий в нашей контрольной группе (33%, 1/3) превышает популяционный уровень для стандартных доноров (10–15%), но соответствует данным для стеатозных печеней: Spitzer et al. (2010) сообщили о частоте билиарных осложнений 30–35% при трансплантации печеней с макростеатозом 30–60% [4]. Отсутствие билиарных осложнений в группе HOPE (0/4) согласуется с результатами Dutkowski et al. (2015), где HOPE снизила частоту ишемических холангиопатий с 30% до 6% (p<0,001, n=221) [10]. Билиарный эпителий особенно уязвим к ишемии вследствие отсутствия портального кровоснабжения и полной зависимости от артериальной перфузии; HOPE, обеспечивая оксигенацию через портальную систему, может частично компенсировать этот дефицит.
Полное отсутствие осложнений в группе HOPE (0/4) при наличии двух осложнений в контроле (2/3, 282
Отсутствие корреляции между IL-6 в перфузате и пиковым АЛТ ( ρ =-0,18, p=0,82; табл. 7) заслуживает внимания. Это наблюдение может указывать на то, что умеренный подъём IL-6 в процессе HOPE отражает адаптивный, а не повреждающий ответ. IL-6 обладает плейотропными эффектами: с одной стороны, при высоких концентрациях он потенцирует воспаление через классический сигнальный путь (взаимодействие с мембранным рецептором IL-6R); с другой стороны, при умеренных концентрациях IL-6 может реализовывать цитопротективные эффекты через активацию сигнального пути JAK/STAT3, индуцирующего экспрессию антиапоптотических белков (Bcl-2, Bcl-xL) и антиоксидантных ферментов [17].
Таким образом, умеренный подъём IL-6 при HOPE может отражать активацию адаптивных, про-тективных программ, а не деструктивного воспаления. Для подтверждения данной гипотезы необходимо расширение панели цитокинов с включением TNF- α (классический провоспалительный маркер), IL-10 (противовоспалительный цитокин) и TGF- β (репаративный медиатор).
Морфологические аспекты защиты
Снижение частоты вакуолизации гепатоцитов на 42% (65±11% → 38±9%, p=0,029) указывает на лучшее сохранение энергетического метаболизма и функции Na⁺/K⁺-АТФазы в группе HOPE. Вакуолизация цитоплазмы является морфологическим эквивалентом клеточного отёка — прямого следствия нарушения ионного гомеостаза при энергетическом истощении [6]. В норме внутриклеточная концентрация Na⁺ поддерживается на низком уровне (≈10 ммоль/л) благодаря активности Na⁺/K⁺-АТФазы, потребляющей до 30% всего клеточного АТФ. При дефиците энергии насос прекращает работу, Na⁺ накапливается в клетке, увлекая за собой воду по осмотическому градиенту, что приводит к набуханию гепатоцитов и вакуолизации цитоплазмы.
Меньшая выраженность вакуолизации в группе HOPE свидетельствует о том, что гипотермическая оксигенированная перфузия обеспечивает поддержание базового энергетического метаболизма на уровне, достаточном для предотвращения критической ионной дерегуляции. Это согласуется с данными о потреблении глюкозы в процессе перфузии (табл. 2) и подтверждает концепцию HOPE как метода «активной консервации», а не просто пассивного охлаждения.
Уменьшение кариопикноза на 39% (18±4% → 11±3%, тенденция без достижения статистической значимости) свидетельствует о снижении доли клеток с необратимыми изменениями ядра. Кариопик-ноз — конденсация хроматина с образованием плотного, гиперхромного ядра — является морфологическим признаком апоптоза или тяжёлого некротиче-
67%) — клинически значимая тенденция, однако при таких малых числах любые процентные показатели и вероятностные расчёты статистически неинформативны. Данный результат следует рассматривать как предварительный сигнал, требующий подтверждения на адекватной выборке.
Настоящее исследование вносит вклад в понимание специфических эффектов HOPE для стеатоз-ных печеней: большинство предшествующих работ либо исключали такие органы из анализа, либо не проводили стратификации результатов по степени стеатоза. Систематические данные об эффективности HOPE специально для печеней с макростеатозом 30–50% в литературе отсутствуют, что делает настоящее исследование первым шагом в заполнении этого пробела.
Прогностическая ценность биохимических маркеров
Корреляционный анализ (табл. 7) продемонстрировал статистически значимую связь между уровнем МДА в момент трансплантации (Т3) и тяжестью ИРП, оцениваемой по пиковому АЛТ ( ρ =0,79, p=0,036) и уровню билирубина на 7-е сутки ( ρ =0,71, p=0,074). Это подтверждает прогностическую ценность МДА как предиктора клинических исходов.
Учитывая техническую простоту и доступность измерения МДА, данный маркер может быть рекомендован для интраоперационной оценки качества органа и прогнозирования риска ранней дисфункции. Пороговое значение МДА, ассоциированное с неблагоприятным исходом, требует определения в более крупных исследованиях, однако наши данные позволяют предположить, что уровень МДА>5 нмоль/мг белка в точке Т3 может служить сигналом повышенного риска.
Аналогично, частота вакуолизации гепатоцитов через 2 часа после реперфузии (Т4) коррелирует с длительностью пребывания в ОРИТ ( ρ =0,83, p=0,021), что указывает на связь между степенью морфологического повреждения и тяжестью раннего послеоперационного периода. Интраоперационная экспресс-биопсия с оценкой вакуолизации может дополнять биохимические маркеры в стратификации риска.
Ограничения исследования
Малый размер выборки (n=7, контроль n=3, HOPE n=4) является определяющим ограничением, не позволяющим делать окончательных выводов об эффективности метода. Выявленные статистически значимые различия по МДА (p=0,029), активности антиоксидантных ферментов (p<0,05) и вакуолизации гепатоцитов (p=0,029) следует интерпретировать как предварительные сигналы, требующие подтверждения, а не как доказательства эффекта. При n=3 vs n=4 мощность критерия Манна–Уитни недо- статочна для надёжного контроля ошибки второго рода; использование однохвостового критерия с минимально достижимым p=0,029 является обоснованным при априорно направленной гипотезе, однако требует подтверждения на большей выборке.
Отсутствие рандомизации и последовательный характер распределения органов по группам создают риск систематической ошибки отбора. Хотя группы были сопоставимы по основным характеристикам органов (табл. 1), невозможно исключить влияние неучтённых конфаундеров (например, различия в скорости изъятия органа, вариабельность хирургической техники).
Краткосрочное наблюдение (6 месяцев) не позволяет оценить долгосрочные результаты — отдалённую функцию трансплантата, поздние билиарные осложнения (билиарная стриктура может манифестировать через 1–2 года), долгосрочную выживаемость реципиентов и трансплантатов.
IL-6 измерялся только в перфузате группы HOPE, без параллельного контроля. Отсутствие измерений IL-6 в тканевых образцах и в динамике ограничивает интерпретацию данного параметра. Расширение панели цитокинов (TNF- α , IL-1 β , IL-10, TGF- β ) позволило бы более детально охарактеризовать воспалительный ответ.
Не оценивались митохондриальная функция (мембранный потенциал, продукция АТФ, активность комплексов дыхательной цепи), маркеры апоптоза (активность каспаз, TUNEL-позитивные клетки), экспрессия генов антиоксидантных ферментов и провоспалительных цитокинов. Эти параметры могли бы существенно углубить понимание механизмов протективного эффекта HOPE.
Результаты не могут быть экстраполированы на печени с макростеатозом >50% (тяжёлый стеатоз), с микровезикулярным стеатозом или с сочетанием стеатоза и других форм повреждения (фиброз, воспаление). Каждая из этих категорий может требовать модификации протокола HOPE.
Отсутствие фармакоэкономического анализа: стоимость расходных материалов для HOPE, амортизация оборудования, затраты времени персонала не были оценены. Для внедрения метода в клиническую практику необходим анализ «затраты-эффективность».
ЗАКЛЮЧЕНИЕ
Настоящее пилотное исследование демонстрирует, что гипотермическая оксигенированная перфузия обеспечивает статистически значимое снижение ишемически-реперфузионного повреждения донорских печеней с умеренным макростеатозом по сравнению со стандартным холодовым хранением. Эффект подтверждён на трёх независимых уровнях оценки: биохимическом (редукция МДА на 33%, p=0,029; активация антиоксидантных ферментов на 40–52%, p<0,05), морфологическом (снижение вакуолизации гепатоцитов на 42%, p=0,029) и клиническом (отсутствие билиарных и сосудистых осложнений против 67% в контроле, улучшение биохимических показателей функции печени).
Впервые для стеатозных печеней продемонстрирована прогностическая ценность МДА и морфологических маркеров повреждения: уровень МДА в момент трансплантации коррелирует с тяжестью ИРП ( ρ =0,79 для АЛТ, ρ =0,71 для билирубина), что открывает перспективы интраоперационной стратификации риска.
Выявленные динамические изменения в процессе перфузии (снижение портального сопротивления на 39%, клиренс лактата 50%, стабилизация рН) свидетельствуют о восстановлении микроциркуляции и сохранности метаболической функции органа. Умеренная воспалительная активация (IL-6 52 пг/мл) без корреляции с маркерами повреждения может отражать адаптивный характер воспалительного ответа при HOPE.
Полученные предварительные данные обосновывают следующие направления дальнейших исследований:
-
1. Многоцентровое рандомизированное контролируемое исследование с адекватной статистической мощностью (расчётный размер выборки n≥60 для обнаружения различия в пиковом АЛТ 30% с мощностью 80% и уровнем значимости 0,05) для подтверждения клинической эффективности HOPE при макростеатозе. Первичная конечная точка: частота ранней дисфункции трансплантата по критериям Olthoff et al. [16]. Вторичные конечные точки: частота билиарных осложнений, длительность госпитализации, 1-летняя выживаемость реципиентов и трансплантатов.
-
2. Расширение молекулярной панели — оценка митохондриальной функции (продукция АТФ, мембранный потенциал, активность комплексов дыхательной цепи, митофагия), маркеров апоптоза (каспаза-3, TUNEL, соотношение Bax/Bcl-2), профиля цитокинов (TNF- α , IL-1 β , IL-10, TGF- β ), экспрессии генов антиоксидантных ферментов (qRT-PCR для SOD1, SOD2, CAT, GPX1, NRF2), маркеров эндотелиальной активации (E-селектин, ICAM-1, VCAM-1) и повреждения (синдекан-1, тромбомодулин).
-
3. Персонализация протокола перфузии — стратификация режимов (температура 8 °C vs 10 °C vs 12 °C; pO₂ 40 vs 60 vs 80 кПа; длительность 2 vs 4 vs 6
-
4. Долгосрочное наблюдение (3–5 лет) с оценкой функции трансплантата (трансаминазы, билирубин, синтетическая функция), отдалённых билиарных осложнений (стриктуры, холангит), фиброгенеза в трансплантате (эластография, биопсия), качества жизни реципиентов и выживаемости без ретрансплантации.
-
5. Фармакологическое усиление HOPE — добавление в перфузат антиоксидантов (N-ацетилцистеин 10 ммоль/л, α -токоферол 100 мкмоль/л), метаболических субстратов ( α -кетоглутарат 1 ммоль/л для поддержки цикла Кребса), противовоспалительных агентов (дексаметазон 1 мг/л), вазодилататоров (силденафил 50 мкг/л для улучшения микроциркуляции). Изучение эффектов модуляторов аутофагии (рапамицин, третиноин) и митофагии (урсодезокси-холевая кислота) для удаления повреждённых органелл.
-
6. Биомаркеры качества перфузии — идентификация пороговых значений портального сопротивления, клиренса лактата, продукции АТФ, ассоциированных с успешным исходом трансплантации. Разработка интегрального индекса жизнеспособности органа (Viability Index) на основе комплекса параметров перфузии для принятия решения об использовании органа.
-
7. Фармакоэкономический анализ — оценка соотношения «затраты-эффективность» HOPE с учётом стоимости оборудования, расходных материалов, затрат времени персонала, экономии на лечении осложнений и ретрансплантациях. Моделирование экономической целесообразности внедрения HOPE в российских трансплантационных центрах различной мощности.
часов; портальная vs артериальная vs двойная перфузия) в зависимости от степени стеатоза, возраста донора, времени холодовой ишемии. Разработка алгоритмов машинного обучения для предикции оптимальных параметров перфузии на основе исходных характеристик органа.
Внедрение HOPE в клиническую практику российских трансплантационных центров способно расширить донорский пул на 15–20% за счёт безопасного использования печеней с умеренным макростеатозом, что критично важно в условиях острого дефицита органов. Стандартизация протокола, обучение персонала и создание национального регистра машинной перфузии позволят систематизировать опыт и оптимизировать технологию для нужд отечественной трансплантологии.


