Математическая модель процесса биодеструкции парацетамола как открытой системы
Автор: Вихарева Е.В., Селянинов А.А., Данилов Ю.Л., Рудакова И.П., Нечеухина Т.А., Ившина И.Б., Няшин Ю.И.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 2 (40) т.12, 2008 года.
Бесплатный доступ
Разработана математическая модель процесса биодеструкции парацетамола с учетом особенностей открытой системы. Модель представляет собой четыре кинетических уравнения, два из них решены аналитически, остальные - численно. В виде линейной зависимости от времени определены коэффициенты k1 и k2 - «константы» скорости реакций биокаталитического окисления парацетамола и его первичного метаболита n-аминофенола соответственно. При этом расчетные данные согласуются с опытными, полученными в процессе биодеструкции парацетамола свободными и иммобилизованными клетками родококков. Математическая модель позволяет прогнозировать поведение исходного субстрата и продуктов его разложения при заданной схеме реакций и известных константах скоростей, а также окончание процесса биодеструкции парацетамола по убыли n-аминофенола.
Парацетамол, n-аминофенол, биодеструкция, бактерии рода rhodococcus, константа скорости реакции, кинетические показатели
Короткий адрес: https://sciup.org/146215918
IDR: 146215918 | УДК: 531/534:[57+61]
Текст научной статьи Математическая модель процесса биодеструкции парацетамола как открытой системы
По данным авторов [3], процесс биодеструкции парацетамола с использованием клеток актинобактерий рода Rhodococcus осуществляется по схеме, приведенной на рис. 1. При этом гидролиз парацетамола, последующее дезаминирование и окисление п -аминофенола протекают в открытой системе, в которой происходит обмен реагентов и продуктов реакций с окружающей средой (воздухом и культуральной жидкостью). В реальных процессах ферментации парацетамола значения констант скорости указанных реакций являются функциями времени. Данные показатели могут быть подобраны эмпирически или определены экспериментально [2].
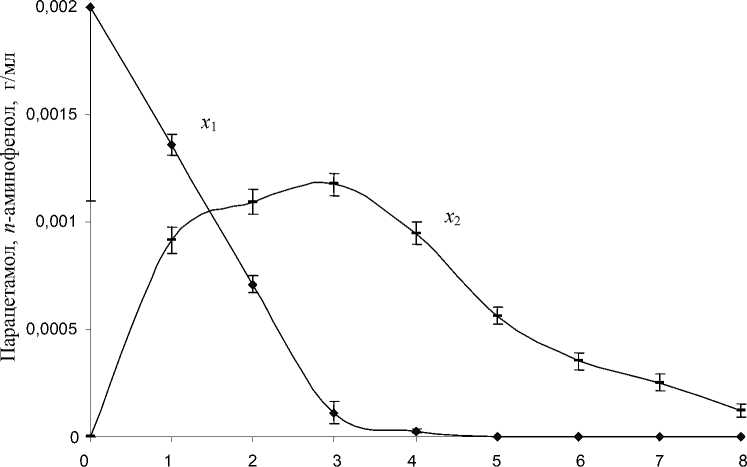
Первичным продуктом разложения парацетамола является п -аминофенол, который обнаруживается в среде культивирования родококков в течение первых часов после начала процесса биодеструкции парацетамола и накапливается до конца его ферментации в культуральной жидкости (рис. 2).
Особо следует отметить, что п -аминофенол является наиболее токсичным (минимальная подавляющая концентрация составляет 12 мг/мл) для клеток родококков
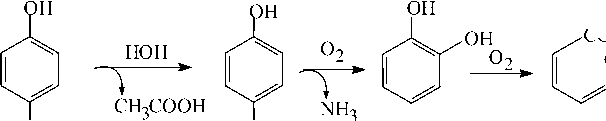
пирокатехин
NHCOCH3 парацетамол
NH2 п -аминофенол
COOH
OOH
цис, цис -муконовая кислота
NH3
OH
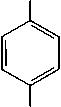
OH гидрохинон
О
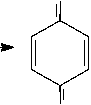
О бензохинон
Рис. 1. Схема биодеструкции парацетамола с использованием клеток R. rubber ИЭГМ 77
t , сут
Рис. 2. Изменение содержания парацетамола ( х 1 ) и п -аминофенола ( х 2 ) в процессе биодеструкции парацетамола клетками R. erythropolis ИЭГМ 767
по сравнению с парацетамолом (минимальная подавляющая концентрация составляет 500 мг/мл) и другими продуктами его разложения. В связи с этим имеются различия в процессах биодеструкции n -аминофенола как единственного источника углерода и энергии для бактериальных клеток и как продукта разложения парацетамола. Данное обстоятельство необходимо учитывать при прогнозе продолжительности процесса биодеструкции парацетамола по убыли п -аминофенола. Возможность прогнозирования содержания продукта реакции во времени обеспечивает математическая модель, построенная на основании системы кинетических уравнений.
В связи с этим целью настоящих исследований является разработка математической модели процесса биодеструкции парацетамола, которая учитывает особенности открытой системы и позволяет прогнозировать поведение объекта моделирования во времени.
Экспериментальное исследование процесса биодеструкции парацетамола
В лабораторных условиях эксперименты по биодеструкции парацетамола проводили в колбах Эрленмейера объемом 250 мл, закрепленных на платформе орбитального шейкера (160 об/мин) при 28 ºС. В колбы помещали минеральную среду состава (г/л): K 2 HPO 4 – 2,0; KH 2 PO 4 – 2,0; KNO 3 – 1,0; (NH 4 ) 2 SO 4 – 2,0; NaCl – 1,0; MgSO 4 ×7Н 2 О – 0,2; CaCl 2 ×2Н 2 О – 0,02; FeСl 3 ×7Н 2 О – 0,001, парацетамол в виде фармацевтической субстанции в концентрации 0,2% (0,2 г на 100 мл среды) и бактериальную суспензию в концентрации 107 клеток/мл. В экспериментах по биодеструкции n -аминофенола в качестве исходного субстрата первоначальная масса его варьировалась от 0,075 до 0,14 г. Последнее значение соответствует максимальному количеству данного вещества, которое может образоваться при разложении 0,2 г парацетамола. В работе использовали предварительно отобранные путем скрининга наиболее активные в отношении парацетамола штаммы родококков R. erythropolis ИЭГМ 767 и R. ruber ИЭГМ 77 [4].
Для активизации оксигеназ бактериальные клетки до начала процесса биодеструкции выращивали в минеральной среде вышеуказанного состава в присутствии 0,1% фенола – структурного аналога парацетамола. В опытах по биодеструкции парацетамола использовали свободные и иммобилизованные (закрепленные на носителе) клетки родококков. В качестве носителя использовали криогель поливинилового спирта [7]. Продолжительность экспериментов составляла от 12 часов до 8 суток. Качественный состав продуктов разложения анализировали методом тонкослойной хроматографии. Количественные характеристики процесса биодеструкции парацетамола изучали по приросту первичного метаболита п -аминофенола и степени исчезновения парацетамола. Содержание п -аминофенола в культуральных жидкостях определяли фотометрическим методом с помощью спектрофотометра Lambda EZ 201, (« Perkin-Elmer », США) при 450 нм по модифицированной методике, основанной на реакции конденсации п -аминофенола с n -диметиламинобензальдегидом [3]. Количество остальных метаболитов, содержащихся в осадке (шламе), рассчитывали с учетом закона сохранения молекулярных масс веществ. С целью определения класса опасности шлама его токсичность ( LD 50 ) исследовали при пероральном введении белым беспородным мышам в дозах от 1000 до 4000 мг/кг массы животного [9].
Класс опасности культуральной жидкости и шлама определяли расчетным методом в соответствии с «Критериями отнесения опасных отходов к классу опасности для окружающей природной среды» [5] на основании известных токсикологических [6] и эколого-гигиенических [1] показателей п -аминофенола и значения LD 50 осадка (шлама). Концентрацию парацетамола в культуральных жидкостях определяли методом высокоэффективной жидкостной хроматографии на хроматографе модели HP -1090 ( Hewlett Packard , США) с использованием колонки ZORBAX Extend -C18 (4,6×250 мм). Эксперименты проводили в трехкратной повторности. Математическую обработку полученных результатов осуществляли с использованием компьютерных программ Exсel 2000 и Statistica (версия 3.4 для Windows ).
Кинетические схемы процессов биодеструкции парацетамола И N - АМИНОФЕНОЛА В КАЧЕСТВЕ ИСХОДНЫХ СУБСТРАТОВ
Процесс биодеструкции парацетамола ранее описан авторами [1] кинетическим уравнением, в котором коэффициент скорости реакции [2] биокаталитического окисления парацетамола представлял собой константу k 1 . Для построения более адекватной модели данного процесса предлагается считать k 1 функцией времени.
dx
— = - k1( t) • xl, dt где x1 |t 0 = x10 = 0,002
г
мл
– начальная концентрация парацетамола.
Процесс биодеструкции п-аминофенола в качестве исходного субстрата может быть описан аналогичным кинетическим уравнением dx2
dt
- k 2 ( t ) • x 2,
где x 2 | t = 0 = x 0 = 0,00075
г мл
начальная концентрация п -аминофенола,
соответствующая максимальному содержанию данного вещества как продукта разложения в процессе биодеструкции парацетамола. Необходимо отметить, что в концентрациях более 0,001 г/мл п -аминофенол вызывает гибель бактериальных клеток.
Уравнения (1) и (2) интегрируются методом разделения переменных.
Для уравнения (1)
x 1 dx 1
x 0 x i
t
= - J k 1 (t ) dt , отсюда In | x 1|| x ‘0
0 x 1
1 t
- I k 1 ( t ) dt • t . t 0
Для среднеинтегрального выражения
t
-I k 1 ( i ) dt t 0
используем линейную
k аппроксимацию по времени в виде k ’ = — t + b .
Из физических соображений значения концентраций xk модуль опускаем. Тогда ln —р = -(b + — t)t и окончательно x01 2
биодеструкции парацетамола принимает вид
положительны, поэтому
кинетическое уравнение
U k — b + t t
X i = X i0 • e 2
Аналогично для процесса биодеструкции п -аминофенола в качестве исходного субстрата
d
—I c +— t 1 1
x 2 = x 0 • e ^ 2 2
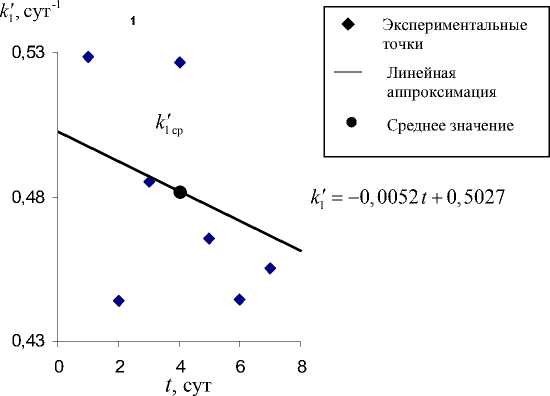
Рис. 3. Зависимость коэффициента к’ от времени в процессе биодеструкции парацетамола клетками R. ruber ИЭГМ 77 (медленный процесс).
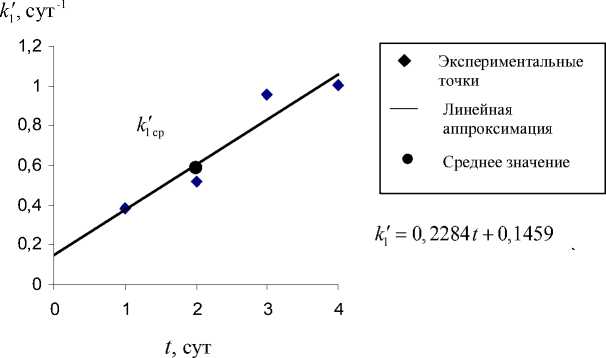
Рис. 4. Зависимость коэффициента к’ от времени в процессе биодеструкции парацетамола клетками R. erythropolis ИЭГМ 767 (средний процесс).
^^^^^^^^^^^^^^^^^в
♦
•
Экспериментальные точки
Линейная
аппроксимация
Среднее значение
Ц = 0,0187 1 + 0,0045
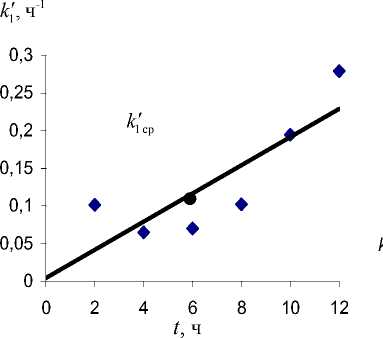
Рис. 5. Зависимость коэффициента к’ от времени в процессе биодеструкции парацетамола иммобилизованными клетками R. erythropolis ИЭГМ 767 (быстрый процесс)
В работе приведены определенный методом наименьших квадратов
k коэффициент к1 = 21 + b линейной зависимости от времени и средние значения
«константы» k 1cp скорости реакции разложения парацетамола с использованием свободных и иммобилизованных клеток родококков (рис. 3–5).
При этом следует отметить, что процесс биодеструкции парацетамола с использованием свободных клеток R. ruber ИЭГМ 77 (см. рис. 3), R. erythropolis ИЭГМ 767 (см. рис. 4) и иммобилизованных клеток R. erythropolis ИЭГМ 767 (см. рис. 5) протекает с разной скоростью и условно обозначен нами как медленный, средний и быстрый соответственно. Как видно из рис. 4, коэффициент к' имеет выраженную линейную зависимость от времени только в условиях среднего процесса. Однако во всех остальных случаях авторами использованы также линейные зависимости k1 (t), которые позволяют получить соответствие теоретических и экспериментальных данных.
♦ Экспериментальные точки
--- Линейная аппроксимация
• Среднее значение
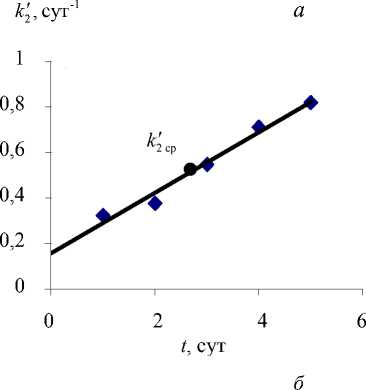
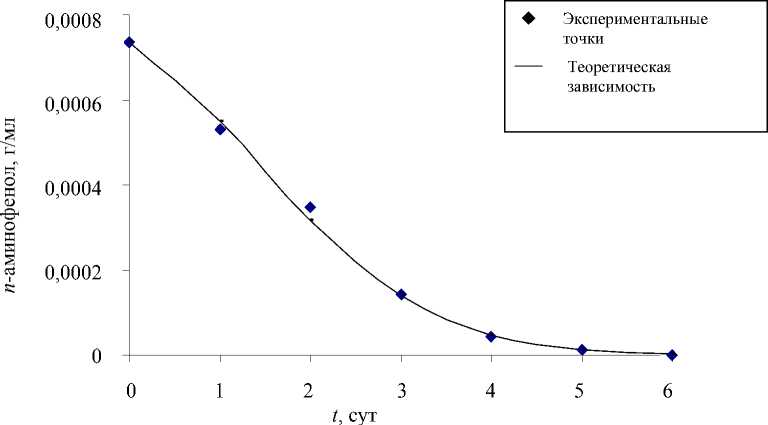
Рис. 6. Зависимость концентрации п -аминофенола ( а ) и коэффициента k 2 ( б ) от времени в процессе биодеструкции его как исходного субстрата клетками R. erythropolis ИЭГМ 767
к 2 = 0,1329 t + 0,1571
Таблица
Параметры «констант» скорости реакций разложения парацетамола к 1 (t ) и п -аминофенола к 2 (t)
|
Процесс биодеструкции парацетамола |
Значения параметров k 1 ( t ) и k 2 ( t ) |
|||
|
k |
b |
d |
c |
|
|
Медленный (с использованием свободных клеток R. ruber ИЭГМ 77) |
–0,0104 [сутки-2] |
0,5027 [сутки-1] |
0,095 [сутки-2] |
–0,11 [сутки-1] |
|
Средний (с использованием свободных клеток R. erythropolis ИЭГМ 767) |
0,4568 [сутки-2] |
0,1459 [сутки-1] |
0,115 [сутки-2] |
–0,15 [сутки-1] |
|
Быстрый (с использованием иммобилизованных клеток R. erythropolis ИЭГМ 767) |
0,0374 [час-2] |
0,0045 [час-1] |
0,01 [час-2] |
–0,04 [час-1] |
На рис. 6 представлено изменение содержания п -аминофенола и коэффициента к 2 от времени в процессе биодеструкции п -аминофенола как исходного субстрата клетками R. erythropolis ИЭГМ 767. Предложенное кинетическое уравнение (2) адекватно описывает процесс разложения п -аминофенола (см. рис. 6, а ), а коэффициент к 2 имеет явно линейную зависимость от времени (см. рис. 6, б ), как и коэффициент к ’ в процессе биодеструкции парацетамола клетками R. erythropolis ИЭГМ 767 (см. рис. 4).
При переходе от среднеинтегрального выражения к «константе» скорости реакции к 1 ( t ) получена ее зависимость от времени в виде к 1 (t ) = b + к • t для парацетамола и к 2( t ) = c + d • t для п -аминофенола соответственно. Параметры к 1 ( t ) (коэффициенты b, k ) и k 2 ( t ) (коэффициенты c, d ), полученные эмпирическим путем, приведены в таблице.
Как видно из таблицы, для медленного (с использованием свободных клеток R. ruber ИЭГМ 77) и среднего (с использованием свободных клеток R. erythropolis ИЭГМ 767) процессов биодеструкции парацетамола параметры k 2 ( t ) имеют близкие значения. Параметры к 2 ( t ) ( c = 0,1571 и d/2 = 0,1329), полученные при разложении п -аминофенола в качестве исходного субстрата, достоверно близки к эмпирически найденным для к 2 ( t ) в процессе биодеструкции парацетамола свободными клетками R. erythropolis ИЭГМ 767. В дальнейшем эмпирически найденные параметры k 2 ( t ) использовались авторами при разработке математической модели всего процесса биодеструкции парацетамола.
Математическая модель процесса биодеструкции парацетамола
Как было указано выше (см. рис. 1), процесс биодеструкции парацетамола представляет собой открытую систему. При этом скорость разложения парацетамола как исходного субстрата пропорциональна его концентрации [3]. Знак «–» в уравнении (1) означает убывание концентрации парацетамола со временем. Коэффициент k 1
является линейной функцией времени. Кинетическое уравнение для парацетамола как для исходного субстрата сохраняет вид (1).
На первой стадии процесса биодеструкции парацетамола (концентрация x1 ) в результате реакции его гидролиза (+Н2О) образуются п-аминофенол (концентрация x2 ) и уксусная кислота (концентрация x3 ). Суммарная скорость образования данных соединений увеличивается со скоростью разложения парацетамола (со знаком «+») и уменьшается за счет текущего разложения п-аминофенола. Кинетическое уравнение принимает вид d (x7 + x,) , . . , . .
----2---- — = k ( t ) • x - k ( t ) • x7 •
112 2
dt
Поскольку в реакции гидролиза участвует вода (система открытая), при постановке задачи биодеструкции парацетамола в терминах концентраций следует учесть прирост массы воды (11,9 %) в виде поправочного коэффициента KH2O. Расчёт масс, участвующих
K H 2 O может быть осуществлён на основании молекулярных в реакции соединений.
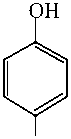
+ HOH
NHCOCH 3
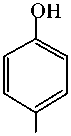
+
NH 2
x 2
CH 3 COOH
x 1
x 3
(молекулярная масса) 151,2 + 18,0 → 109,1 + 64,0 .
Отсюда коэффициент прироста массы за счет воды
K H 0 = 1,0 + -180- = 1,119.
H 2 O 151, 2
Для суммы концентраций х 2 и х 3 получаем кинетическое уравнение d ( x. + x. ) z .
-----------= K H2O • k 1 ( t ) • x 1 - k 2 ( t ) • x 2 , dt 2
где x 2 L = 0 = 0, x 3 I t = 0 = 0.
Доля уксусной парацетамола и воды. кислоты
кислоты составляет 35,5 % от суммы молекулярных масс В связи с этим коэффициент убыли масс за счет уксусной
K =--- 60,0--- = 0355
3 151,2 + 18,0 ,
Кинетическое
уравнение изменения содержания уксусной кислоты
(концентрация x 3 ) принимает вид
dx 3
d^" = K CH 3 COOH ‘ K H 2 O ‘ k ( t ) ‘ x •
Для прочих продуктов биодеструкции (в частности, пирокатехина и других в суммарной концентрации x 4 ) следует учесть прирост молекулярной массы кислорода и четырех протонов в количестве 33% от молекулярной массы п -аминофенола.
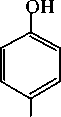
+ O 2 +4 H +
NH 2
+ NH 3 + HOH
x 2
x 4
(молекулярная масса) 109,1 + 32,0 + 4,0 ^ 110,1 + 17,0 + 18,0.
Исходя из значений молекулярных масс соединений, участвующих в реакции окисления п -аминофенола, находим коэффициент прироста массы.
= 1 + 32,0 + 4,0 = 1,330.
O 2 109,1
Кинетическое уравнение для остальных метаболитов принимает вид dx.
~£ = K02 • k2( t) • X2, где x4 It=0 = 0-
В результате система кинетических уравнений процесса биодеструкции парацетамола принимает вид dx
—1 = -( b + k • t) • x1, dt d (x 2 + x3)
dt dx = K dt
'H2O • ( b + k • t ) • x 1 - ( c + d • t ) • x 2 ,
CH 3 COOH " K H 2 O • ( b + k • t ) • x i ,
dx4 = Ko • ( c + d • t ) • x 2, I dt O 2
Где X 1 1 = 0 = X 10 , X 2 t = 0 = X 3 t = 0 = X 4 t = 0 = 0.
Система (8) включает четыре дифференциальных уравнения 1-го порядка с известными начальными условиями. Попытаемся решить данную систему аналитически. Первое уравнение в (8) проинтегрировано ранее (3), x1 = x0 • e
-I
I t
.
Подставив x1 в третье уравнение системы (8), получаем dx,
-73- = KCH3COOH • KH^ • (b + k • t) • x0 • e dt 32
-I
.
Интегрируем это дифференциальное уравнение методом разделения переменных, x3
t
CH 3 COOHH 2 O x 1
1 • e
1 1 dt ,
отсюда x3 KCH3COOH ' KH2O
• x 1
-I
• 1 - e
.
Далее системы (8),
подставляем третье уравнение из системы (8) во второе уравнение
dx 2 dt
'K CH 3 COOH • K „ 2 ° • ( b + k • 1 ) • x1 + K „ 2 ° • ( b + k • 1 ) • x 1 - ( c + d • 1 ) • x 2 =
= (1 - K CH 3 COOH ) • K H 2 O • ( b + k • 1 ) • x 1 - ( c + d • t ) • x 2 "
Заменив x 1 через зависимость (3), получаем неоднородное дифференциальное уравнение 1-го порядка для x 2 с коэффициентом в виде линейной функции времени
-f b + kt 1 1
• ( b + k • 1 ) • x 10 • e ^ 2 2 .
dx 2
—7“ + (c + d • t) • x2 = (1 - KCHCOOH ) • KH2O dt 32
Необходимо отметить, что после интегрирования уравнения (10) и подстановки результата в четвертое уравнение системы (8) для остальных метаболитов x 4 можно получить дифференциальное уравнение 1-го порядка с разделяющимися переменными.
Для концентрации парацетамола x 1 решение из системы кинетических уравнений (8) имеет естественный вид экспоненты (3). Для концентрации п -аминофенола x 2 в процессе биодеструкции его как исходного субстрата решение имеет такой же естественный вид (4).
Однако при разложении п-аминофенола в процессе биодеструкции парацетамола дифференциальное уравнение (10) не интегрируется в элементарных функциях. В связи с этим представляется необходимым решение системы (8) с применением численного метода. Для этого систему (8) преобразуем к стандартному виду для реализации на компьютере, dx,
";; ="( b + k • 1 )^ 1 -
"dt ^ = (1 - K CH 3 COOH ) • K H 2 O • ( b + k • 1 ) • x 1 - ( c + - ■1 ) • x 2 ,
-
d^ - K CH ,™ • K „ 2 ° • ( b + b1 ) • x„
dx
-
—4 = Ko • ( c + d • 1 ) • x 2,
I -1 ° 2 2
где x 1 L = 0 = xL x 2 L= 0 = x 3 I t = 0 = x 4 I t = 0 = 0’
Первое и третье уравнения проинтегрированы ранее (3), (9). Поэтому, подставив полученную функцию x1 (t) во второе уравнение системы (11), получаем систему двух уравнений dx^ Z1 \ ТЛ 0 /1 1 x -(b + t) t
—2 = (1 - Kth c ooh ) • K h о • x i • ( b + k • t ) • e 2
d^ CH 3 COOH / H 2 O 1 '
dx 4- = K O1 • ( c + d • t ) • x .1 1 = 0 = 0,
I dt 2
( c + d • t ) • x 2,
<
где x 2 L = 0 = x 4 I t = 0 = 0-
Формализованная запись системы (12) принимает вид
' dx^ f 2 ( t - x 2 ). dx 4 = f . ( t , x 2 ),
I dt где x2 |t=0 = x4 |t=0 = 0; f,, f 4 - известные функции от времени t и концентрации п-аминофенола x2 .
Одним из наиболее удобных и точных методов численного интегрирования дифференциальных уравнений является метод Рунге–Кутта, для которого используем стандартную программу интегрирования системы двух дифференциальных уравнений 1-го порядка.
Сравнение теоретических и экспериментальных данных
Результаты численного решения системы (12) для компонентов реакции x 2 и x 4 методом Рунге–Кутта и аналитические зависимости для компонента x 1 в сравнении с экспериментальными данными представлены на рис. 7–9. Как видно из рис. 7–9, разработанная модель адекватно описывает процесс биодеструкции парацетамола как открытой системы. Содержание парацетамола x 1 в процессе биодеструкции уменьшается сначала быстро, а затем медленно. При использовании клеток R. ruber ИЭГМ 77 исчезновение парацетамола из среды культивирования родококков наблюдается через 8 суток (см. рис. 7), R. erythropolis ИЭГМ 767 – через 4 суток (см. рис. 8), а при использовании иммобилизованных клеток R. erythropolis ИЭГМ 767 – через 14 часов (см. рис. 9). Различие в скорости процесса биодеструкции парацетамола при использовании свободных и иммобилизованных клеток родококков зависит от каталитической активности клеточных ферментов, которая инициируется предварительной индукцией оксигеназного комплекса и в еще большей степени иммобилизацией бактериальных клеток.
Содержание п- аминофенола x 2 как продукта разложения парацетамола сначала достаточно быстро увеличивается, достигая максимальных значений в культуральной жидкости на 3-и сутки при использовании свободных клеток родококков (см. рис. 7, 8) или через 12 часов при использовании иммобилизованных клеток (рис. 8), а затем плавно уменьшается до нуля на 8-е сутки или через 25 часов соответственно. Разработанная модель дает возможность прогнозировать окончание процесса
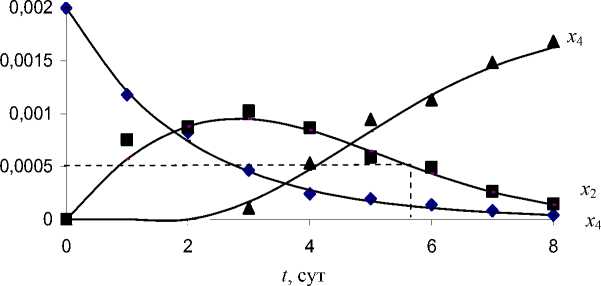
Рис. 7. Экспериментальные (точки) и теоретические (линии) зависимости от времени концентрации парацетамола x 1 , п- аминофенола x 2 и остальных продуктов разложения x 4 в процессе биодеструкции парацетамола клетками R. ruber ИЭГМ 77 (медленный процесс). Пунктирными линиями обозначены время окончания процесса и соответствующее ему содержание п -аминофенола.
биодеструкции парацетамола по убыли п- аминофенола. Так, по нашим данным, парацетамол и п- аминофенол относятся к I классу опасности для окружающей природной среды, то есть являются чрезвычайно опасными отходами. Культуральная жидкость становится малоопасным отходом (IV класс опасности для окружающей природной среды) и может быть размещена на санитарном полигоне по достижении в ней концентрации п- аминофенола, равной 0,0005 г/мл. Следовательно, процесс разложения парацетамола при использовании свободных клеток родококков может быть завершен через 6 суток (см. рис. 7, 8), а при использовании иммобилизованных клеток – через 19 часов (см. рис. 9).
Содержание уксусной кислоты x 3 как продукта реакции гидролиза парацетамола и практически не опасного в данной концентрации отхода в ходе экспериментов не регистрировалось, и на рис. 7–9 теоретические зависимости ее концентрации от времени не приводятся. Концентрация x 4 остальных продуктов разложения парацетамола, находящихся в осадке (шламе), заметно увеличивается, начиная с первых суток (см. рис. 7, 8) или нескольких часов (см. рис. 9) и достигает во всех случаях в конце процесса около 85% от начальной концентрации парацетамола. Образующийся осадок малотоксичен ( LD 50 > 4000 мг/кг), относится к V классу опасности (практически не опасен) для окружающей природной среды и наряду с культуральной жидкостью может быть размещен на санитарном полигоне.
Заключение
Таким образом, в результате проведенных исследований разработана математическая модель процесса биодеструкции парацетамола с учетом особенностей открытой системы. Модель представляет собой четыре кинетических уравнения, два из которых решены аналитически, остальные – численно. В виде линейной зависимости от времени определены коэффициенты k 1 и k 2 – «константы» скорости реакций биокаталитического окисления парацетамола и его первичного метаболита п -аминофенола соответственно. При этом расчетные данные согласуются с опытными, полученными в процессе биодеструкции парацетамола свободными и иммобилизован-
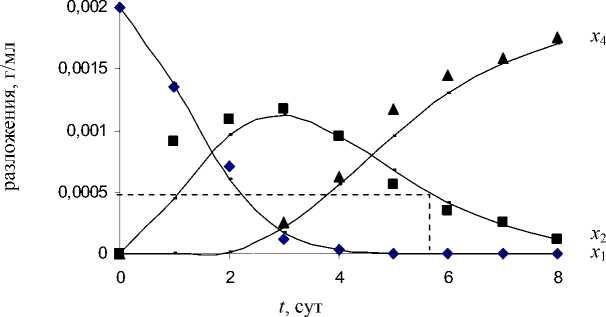
Рис. 8. Экспериментальные (точки) и теоретические (линии) зависимости от времени концентрации парацетамола х 1, п- аминофенола х 2 и остальных продуктов разложения х 4 в процессе биодеструкции парацетамола клетками R. erythropolis ИЭГМ 767 (средний процесс).
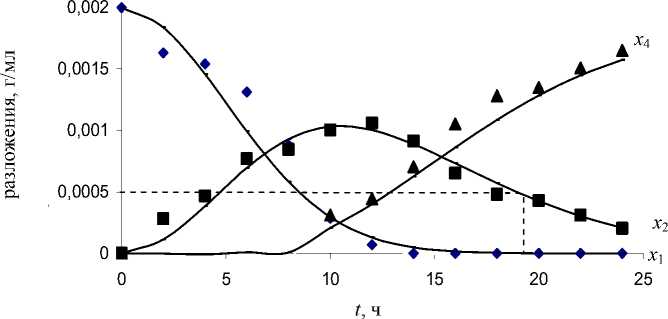
Рис. 9. Экспериментальные (точки) и теоретические (линии) зависимости от времени концентрации парацетамола х 1, п- аминофенола х 2 и остальных продуктов разложения х 4 в процессе биодеструкции парацетамола иммобилизованными клетками R. erythropolis ИЭГМ 767 (быстрый процесс).
ными клетками родококков. Разработанная математическая модель позволяет прогнозировать поведение исходного субстрата и продуктов его разложения, а также окончание процесса биодеструкции парацетамола по убыли п -аминофенола.
Благодарности
Исследования поддержаны грантом РФФИ № 07–04–96038–р–Урал.


