Математическое моделирование эволюции сферического клеточного агрегата в вязком матриксе. Формирование клеточных структур
Автор: Логвенков С.А.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 1 т.29, 2025 года.
Бесплатный доступ
Выполнено математическое моделирование развития сферически симметричных структур в клеточном агрегате, окруженном вязким внеклеточным матриксом. Постановка задачи использует разработанную нами ранее многофазную модель биологической сплошной среды, образованной двумя активно взаимодействующими твердыми фазами и жидкостью. Одна из твердых фаз образована клетками, другая – внеклеточным матриксом. Изменение радиуса сферической поверхности, ограничивающей агрегат, определяется условиями, которые учитывают перераспределение нагрузки между клеточной фазой и фазой матрикса по разные стороны от границы агрегата. Исследовано влияние активных взаимодействий клеток как между собой, так и с матриксом, а также начального состава клеточного агрегата на процесс перераспределения объемных концентраций клеток и матрикса. Процессы, связанные с делением клеток и выработкой протеолитических ферментов, не рассматриваются. Численные расчеты показали, что в случае доминирования межклеточных активных механических взаимодействий над перекрестными между клетками и матриксом происходит только уплотнение как рыхлых, так и плотных агрегатов – неинвазивное развитие. В случае доминирования перекрестных активных взаимодействий над межклеточными сценарий развития клеточных структур зависит от начальной объемной концентрации клеток. В рыхлых агрегатах формируется неоднородность распределения клеточной фазы, которая при определенных условиях может развиться в полую клеточную структуру. В плотных агрегатах происходит формирование плотного ядра и отрыв части клеточной фазы от основной массы.
Клеточные системы, активные среды, биологическое формообразование, континуальное моделирование
Короткий адрес: https://sciup.org/146283125
IDR: 146283125 | УДК: 532.5: 576.7 | DOI: 10.15593/RZhBiomeh/2025.1.07
Mathematical modeling of the evolution of a spherical cell aggregate in a viscous matrix. Formation of cell structures
Mathematical modeling of the development of spherically symmetrical structures in a cell ag-gregate surrounded by a viscous extracellular matrix was performed. The problem statement uses our previously developed multiphase continuum model of a biological medium formed by two ac-tively interacting solid phases and a liquid. One of the solid phases is formed by cells, the other by the extracellular matrix. The change in the radius of the spherical surface bounding the aggregate is determined by conditions that take into account the redistribution of the load between the cell phase and the matrix phase on opposite sides of the aggregate boundary. The influence of active interactions of cells both among themselves and with the matrix, as well as the initial composition of the cell aggregate on the process of redistribution of the volume concentrations of cells and matrix, was studied. Processes associated with cell division and the production of proteolytic en-zymes are not considered. Numerical calculations have shown that in the case of dominance of intercellular active mechanical interactions over cross interactions between cells and the matrix, only compaction of both loose and dense aggregates occurs - non-invasive development. In the case of dominance of active cross interactions over intercellular ones, the scenario of the devel-opment of cell structures depends on the initial volume concentration of cell phase. In loose ag-gregates, a heterogeneous distribution of the concentration of the cell phase is formed, which un-der certain conditions can develop into a hollow cell structure. In dense aggregates, a dense core is formed and part of the cell phase detaches from the main mass.
Текст научной статьи Математическое моделирование эволюции сферического клеточного агрегата в вязком матриксе. Формирование клеточных структур
RUSSIAN JOURNAL OF BIOMECHANICS
Развитию различных биологических тканей и органов в живых организмах зачастую предшествует организация клеток в агрегаты, окруженные внеклеточным матриксом. Дальнейшее развитие клеточных агрегатов при- водит к формированию различных клеточных структур. В частности, формирование новой сети кровеносных сосудов при кластерном васкулогенезе, имеющим место в условиях гипоксии, проходит стадию агрегации клеток-предшественников с последующим образованием просвета и слияния с ранее существовавшей сосудистой се-

се) ® ®
Эта статья доступна в соответствии с условиями лицензии Creative Commons Attribution-NonCommercial 4.0 International
License (CC BY-NC 4.0)
This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License (CC BY-NC 4.0)
тью [1]. Формированию полости в раннем эмбриональном развитии лягушки Xenopus Laevis также предшествует рыхлое скопление клеток [2; 3]. В качестве другого пути развития можно привести пример роста опухолей, характеризуемого существованием плотной основной массы клеток и инвазией отдельных групп клеток в окружающие ткани [4; 5]. Клеточные агрегаты, полученные в искусственных условиях, являются объектом изучения влияния активных взаимодействий клеток со своим окружением [6; 7].
Выбор пути развития определяется самыми разными факторами. В настоящее время существуют многочисленные данные, указывающие на то, что механические свойства внеклеточного матрикса играют значительную роль в организации клеточных структур в биологических тканях [8; 9]. Известно, что вязкоупругие свойства матрикса регулируют поведение одиночной клетки на плоском субстрате, однако влияние, в частности, вязких свойств матрикса на коллективную динамику клеток в тканях является предметом обсуждений. Следует отметить важную роль механических активных взаимосвязей, которые развиваются клетками при взаимодействии с матриксом.
Теоретические исследования, в которых методы механики сплошных сред использовались для моделирования развития клеточных сфероидов, в первую очередь связаны с ростом опухолей. Основной круг задач включает в себя описание развития неоднородности в опухолевых сфероидах, определяемой различной доступностью питательных веществ в разных областях сфероида и развитием напряжений в результате деления клеток. Рассматриваются задачи, связанные с распространением сфероида в окружающие ткани в результате ростовых процессов и взаимодействия с окружающим тканями. Предметом обсуждений являются законы роста, учитывающие взаимосвязь скорости деления клеток с напряженным состоянием среды. Математическое моделирование клеточных систем с учетом различных биологических и физических механизмов, принимающих участие в развитии клеточных агрегатов, представлено огромным количеством работ, которые различаются методами моделирования и детализацией описания процессов. Ниже приведены ссылки на небольшое количество публикаций, в которых присутствуют более полные обзоры существующих моделей.
Задача о распространении плоского фронта опухолевых клеток в недеформируемом матриксе рассматривалась в [10; 11]. Эволюция концентрации клеток описывалась уравнением неразрывности с учетом деления клеток. Поток плотности определялся эмпирическим соотношением, учитывающим, помимо диффузии, соответствующей случайным клеточным блужданиям, также активные нелокальные составляющие, определяемые активными взаимодействиями клеток между собой и матриксом. В основу модели положена аналогия между движением клеточной среды и фильтрационным течением жидкости, однако используемые при этом гипотезы справедливы только для очень разреженных клеточных сред.
В [12] представлена модель развития радиальной неоднородности клеточных сфероидов, характеризуемой различием свойств клеток. Формирование некротического ядра и областей с различной пролиферативной активностью клеток связано с неоднородностью распределения питательных веществ, которая описывается уравнением диффузии. Влияние механических параметров среды на развитие клеточных агрегатов не обсуждается. Обратная связь между скоростью роста и напряженным состоянием агрегата, контролируемая также доступностью питательных веществ, учитывается в [13], где клеточный агрегат рассматривается как пороупругое растущее тело. Этот класс моделей более подробно обсуждается в [14; 15]. Однако, несомненно, существенные механизмы активных взаимодействий клеток между собой и матриксом в этих моделях не рассматриваются.
В другой группе моделей [16–18] используются методы механики многофазных сплошных сред, которые учитывают присутствие активных механических взаимодействий клеток между собой и матриксом в процессе развития аваскулярных опухолей, а также зависимость скорости пролиферации клеток от напряжений, концентрации клеточной фазы и питательных веществ. Включение сократительных элементов в клеточную фазу позволило учесть влияние активных напряжений на процесс клеточных переупаковок, рассматриваемых как вязкое течение. Активные механические напряжения, создаваемые клетками, учитывались посредством немонотонной зависимости давления в клеточной фазе от ее объемной концентрации. Широкий обзор математических моделей, описывающих различные проявления роста аваску-лярных опухолей, представлен в статье [19]. Особое внимание уделяется роли механических взаимодействий опухолей с окружающим тканями.
Основные принципы построения континуальных моделей биологических сред, проявляющих механическую активность, были предложены в [20]. В работе представлены характеристики, позволяющие учитывать общие активные свойства клеточной среды и обсуждаются возможные механизмы, описываемые этими характеристиками. Предлагается введение вспомогательных фаз, которые соответствуют механически активным субклеточным элементам, связанным с созданием активных напряжений, контролирующим переупаковку клеток. Эта работа послужила основой построения континуальной модели биологической среды, образованной двумя активно взаимодействующими клеточными фазами и жидкостью [21], которая использовалась в задаче о сортировке двух типов клеток [22; 23] и образования полых структур [24; 25] в клеточных агрегатах.
В данной работе представлено теоретическое исследование системы «клетки – матрикс» как механической системы, исключая из рассмотрения эффекты, связанные с делением клеток и выработкой протеолитических ферментов. Будет исследовано влияние активных взаимодействий клеток как между собой, так и вязким матриксом, а также начального состава клеточного агрегата на процесс перераспределения объемных концентраций клеток и матрикса при развитии клеточных структур.
Постановка задачи и метод решения
Континуальная многофазная модель
Рассмотрим клеточный агрегат, образованный клетками и внеклеточным матриксом. В начальный момент времени агрегат имеет сферическую форму и окружен матриксом (рис. 1). Область, занятая агрегатом (совместно клетками и матриксом), в начальный момент времени ограничена сферой радиуса R , а область пространства, в которой присутствует только матрикс, считается неограниченной. Неограниченная область пространства, занятая матриксом, моделируется сферой большого постоянного радиуса R . В среде также присутствует внеклеточная жидкость.
Постановка задачи о перераспределении объемных концентраций клеток и матрикса будет использовать континуальную модель биологической многофазной среды, образованной двумя активно взаимодействующими твердыми фазами и жидкостью, разработанную в [5]. В данной задаче одна из твердых фаз образована клетками, а другая – внеклеточным матриксом. Истинные плотности фаз будем считать постоянными и равными между собой. Биологические особенности рассматриваемых фаз вносят некоторые отличия от [5]. Одним из них является отсутствие активных взаимодействий в фазе матрикса. Другое отличие состоит в изменении определяющих соотношений для активных механических взаимодействий между клетками и матриксом, которое в данном случае учитывает нелокальную стягивающую составляющую в этих взаимодействиях.
Все уравнения написаны в физическом базисе сферической системы координат с началом в центре сферы. Ниже приведены основные предположения, используемые в постановке задачи.
В уравнениях импульсов будем пренебрегать составляющей сил межфазного взаимодействия твердых фаз с жидкостью, которая обусловлена вязким трением. Оценки числовых значений соответствующих безразмерных параметров выполнены в [21; 28]. Эти оценки позволяют также пренебречь изменением гидростатического давления во внеклеточной жидкости, считая его равным нулю во всей занятой матриксом области (предполагается свободное перетекание жидкости через границу клеточного агрегата), и решать уравнения для клеточной фазы и матрикса отдельно от уравнений, описывающих движение жидкости. Уравнения, описывающие движения жидкости, далее не рассматриваются.
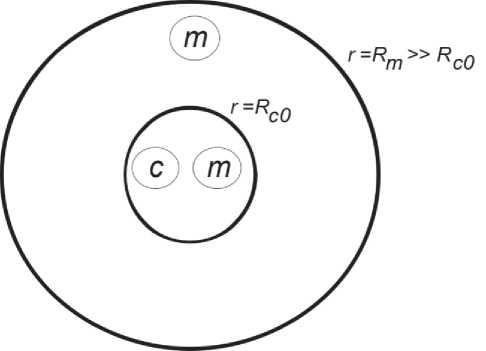
Рис. 1. Схематическое изображение клеточного агрегата, окруженного матриксом, в начальный момент времени. Буквенные обозначения c и m , обведенные маленькими кругами, обозначают присутствие клеток и матрикса в разных областях. Координата r = Rc0 является радиусом сферы, ограничивающей клетки, сфера радиуса Rm = const ограничивает матрикс
Активные механические взаимодействия клеток между собой и внеклеточным матриксом играют ключевую роль во многих биологических процессах, связанных с миграцией клеток и формированием тканей и органов. Развитие активных взаимодействий обеспечивается такими фундаментальными механизмами, как адгезия и сократимость клеточного скелета. Специфические поверхностные белки адгезии обеспечивают прочное сцепление участков клеточных поверхностей как между собой, так и с волокнами матрикса. Активная перестройка клеточного скелета и действие моторных белков генерирует силу, которая действует на соседние клетки и окружающий матрикс. В процессе взаимодействия с матриксом клетки образуют псевдоподии – выросты клеточной мембраны, которые устанавливают прочные контакты с волокнами матрикса [26; 27]. Активные механические взаимодействия между клетками и матриксом возникают под воздействием сократительных сил, развиваемых элементами клеточного скелета, расположенными в псевдоподиях. Активные силовые взаимодействия между клетками развиваются в результате более разнообразных проявлений механизмов адгезии и сократимости цитоскелета в зависимости от типа клеток и тканей (кратко изложено во введении [23]).
Описание активных взаимодействий клеток со своим окружением может быть выполнено путем введения вспомогательных фаз, отождествляемых с теми клеточными структурами, в которых развиваются активные силы взаимодействия [20].
Введем две вспомогательные фазы, первая из которых обеспечивает активные нелокальные взаимодействия между клетками и характеризуется тензором напряжений т(c). Вторая вспомогательная фаза с тензо- ром напряжений Тcm] = т(cm) + т(mc) обеспечивает нелокальные перекрестные активные взаимодействия между клеточной фазой и матриксом. Составляющие т(cm) и т( mc) перекрестного тензора напряжений описывают активные нелокальные взаимодействия между частицей клеточной фазы, находящейся в рассматриваемой точке, и матриксом, а также частицей матрикса в рассматриваемой точке и клеточной фазой соответственно. Объемы, занимаемые дополнительными фазами, считаются пренебрежимо малыми в сравнении с объемами основных фаз. Напряжения в клеточной фазе и фазе матрикса характеризуются тензорами a' c) и ст'm).
Уравнения импульсов для клеточной фазы и матрикса, пренебрегая инерционными эффектами, примем в следующем виде:
ризует эффективное расстояние, на котором происходит силовое взаимодействие клеток со своим окружением и имеет порядок одного или нескольких клеточных размеров.
В исследовании [3] использовалось предположение, что активные стягивающие взаимодействия развиваются только между клетками внутри фазы, а в перекрестных взаимодействиях учитывалась только расталкивающая составляющая. В данном случае составляющие т ' cm ) и т ( mc ) перекрестного тензора напряжений будут учитывать нелокальные стягивающие силы, действующие в данной точке на частицу одной фазы со стороны удаленных на определенное расстояние частиц другой фазы. Определяющие соотношения для активных напряжений примем в следующем виде:
V- ( Фсо ( c ) + т ( c ) + т ( cm ) ) + F = 0, V- ( Фио ( m ) + т ( m ) + т ( mc ) ) - F = 0.
т(с’ = -Пс -1 + mc —^-— -ФС[ФС- N0 Nds, с с 4п^2 с с sS
Здесь F – сила межфазного взаимодействия между клеточной фазой и матриксом, фс и фт — объемные концентрации клеточной фазы и матрикса соответственно. Второе и третье слагаемые в скобках учитывают силы взаимодействия с вспомогательными фазами.
Выражение для силы межфазного взаимодействия F , полученное в работе [5], имеет следующий вид:
т(cm’ = -Пcm -1 + mcm - Ф JФm ■ N ® Nds,
4 п R s S
Т ( mc ’ =-П cm - 1 + m cm ,' -Ф m ( Ф с ■ N ® N ds , 4 п R s S
П с
Ф 2
E ---Ф---,
1 -Ф с -Ф m
П cm
=E cm
ФФ cm
1 -Ф c -Ф m
F =Ф mPc V
ф 1
6 +ф J
\ т с т т /
Ф cPm V
Фт 1 + Uс +Фт J
+ Кт Ф с Ф т ( V ' m ’ — V ' c ) ), P c =- 1 1 . ( a ' с ) ), P m =- j I . ' a ' m ) ).
Здесь v ' c ) и v ( m ) - векторы скорости клеточной фазы и матрикса, I [ ( o ' с ) ) и I До ' m ) ) - первые инварианты тензоров напряжений в твердых фазах. Выражение (2) учитывает две составляющие силы межфазного взаимодействия, одна из которых связана с действием сил давления (первое и второе слагаемое), вторая – с силой вязкого трения на межфазных поверхностях.
Определяющие соотношения для активных напряжений в дополнительных фазах учитывают различные проявления активности клеток при взаимодействии со своим окружением: хаотическую активность при взаимодействии между собой и с матриксом, которая характеризуется давлениями П с ( Ф c , Ф m ), П cm ( Ф с , Ф m ) и проявляются в отталкивании частиц соответствующих фаз, а также и нелокальные стягивающие усилия, направленно реагирующие на неоднородность их микроокружения. Стягивающие составляющие определяются неоднородностью распределения соседних клеток или матрикса по сферической поверхности некоторого фиксированного для данной среды радиуса R (радиуса дальнодействия) с центром в рассматриваемой точке. Этот радиус характе-
Здесь I – единичный тензор. Интегрирование выполняется по сферической поверхности S фиксированного радиуса R с центром в рассматриваемой точке, N – единичный вектор нормали к поверхности сферы. Если интегрирование производится по той части поверхности, на которой подынтегральная функция не определена, то в этих точках она доопределяется нулем.
В общем случае тензоры скоростей деформации твердых фаз можно представить в виде суммы составляющих, связанных как с деформацией клеток и волокон матрикса (для них может быть принят один из законов упругости), так и с их переупаковкой [28]. В данной работе примем гипотезу о малости первой составляющей по сравнению со скоростью неупругого деформирования, связанного с переупаковками частиц фаз. Будем рассматривать неупругое деформирование фаз как течение, которым управляют активные напряжения и напряжения в фазах. Выражения для тензоров скоростей деформации e ' с ) и е ' m ) клеточной фазы и матрикса соответственно примем в следующем виде:
е ' с > = 1 (о ' с )
2щ (
—
__' m ) тО )
)—— т ' с ) 2 М 11
—
1 т ' cm )
2 И 12
e
,( m ) =
= — ( о ' m ) 2ц2V
—
Ф с о ' с ’
—
т ' mc ) ) .
Выбор знаков учитывает, что растягивающие напряжения во вспомогательных фазах стимулируют сближение частиц фаз, а растягивающие напряжения в
рассматриваемой фазе и сжимающие напряжения в соседней фазе этому уплотнению препятствуют.
Предполагается, что в среде отсутствуют деление и гибель клеток, а также потоки массы между твердыми фазами и жидкостью. Тогда уравнения неразрывности для клеточной фазы и матрикса примут следующий вид:
+ V- (Ф cv(c)) = 0, d t (5)
^ + ?• (Ф m V(m)) = 0.
d t
Система уравнений дополняется кинематическими соотношениями для компонент тензоров скоростей деформации твердых фаз:
e ( c * = 0,5( V v ( c * + ( V v ( c ) ) T ),
(6) e ( m ) = 0,5( V v ( m ) + ( V v ( m ) ) T ).
Уравнения (1)–(6) будут использованы для исследования эволюции перераспределения объемных концентраций клеток и матрикса в клеточном агрегате. Решение задачи будет выполнено в предположении сферической симметрии. У всех тензоров смешанные компоненты считаются равными нулю, а векторы скоростей будут иметь единственную отличную от нуля компоненту в радиальном направлении.
Граничные и начальные условия
Граничные условия учитывают независимое перемещения поверхности, ограничивающей клеточную фазу. Условие сферической симметрии обеспечивает сохранение сферической формы клеточного агрегата, и r = Rc (t ) является уравнением его границы.
Скорость матрикса на удаленной внешней границе считается равной нулю, и в качестве условия при r = Rm примем, что vm) = 0. (7)
Граница клеточной фазы r = Rc ( t ) является поверхностью разрыва для фазы матрикса. На этой границе должны быть сформулированы условие непрерывности потока массы матрикса и условия, учитывающие перераспределение нагрузки между твердыми фазами.
Условие непрерывности потока массы матрикса при r = Rc tt ) имеет вид:
[Ф m ( V m — R c ) ] = 0. (8)
Квадратные скобки обозначают разность соответственных величин по разные стороны разрыва, точкой обозначена производная по времени.
Условия для напряжений, учитывающие перераспределение нагрузки в результате силового взаимодействия частиц клеточной фазы и матрикса по разные стороны от разрыва, были предложены в [29]. Они имеют следующий вид:
ф c ^ rc ) +т : ) ■: ) =- p ’ф - Ф m ,
[ф m e ) +€ ) +e ) ]=- p *ф - Ф т , (9)
n * = P^m — P+mфc' p = ф ; +Ф m '
Здесь p * является средним давлением на поверхности межфазного контакта при r = Rc (t ) . Верхний индекс «плюс» или «минус» указывает на значение соответствующей величины справа или слева от разрыва.
Перемещение границы r = Rc (t ) определяется движением клеточной фазы, поэтому при r = Rc (t ) считается выполненным условие
R c ( t ) = v rc ) . (10)
Из уравнений неразрывности (5) и условия ограниченности скоростей фаз в центре сферы следует, что при r = 0 :
v ( c > = v ( m ) = 0. (11)
Граничные условия для объемных концентраций фаз не ставятся, так как их границы являются характеристиками уравнений (5). Соответствующие граничные условия получаются из решения уравнений (5), записанных в граничных точках.
В начальный момент времени будем задавать положение границы клеточной фазы Rc (0) = Rc0 и начальные распределения концентраций фаз фс (0, r ) = ф.0 ( r ), Ф m (0, r ) = Ф m 0( r ) .
Метод решения
Преобразуем систему уравнений (1)–(6), выразив тензоры напряжений для твердых фаз из уравнений (4) и подставив их в уравнения равновесия (1), используя (6). В области r < Rc (t ), занятой клеточным агрегатом, будут получены два уравнения второго порядка по r для единственной ненулевой радиальной компоненты векторов скорости клеточной фазы и фазы матрикса. Остальные уравнения равновесия будут выполнены тождественно в силу сферической симметрии задачи. Уравнение для радиальной компоненты вектора скорости матрикса в области Rc (t ) < r < Rm получается аналогично. При этом следует учитывать, что в этой области фс = 0, v ( c ) = 0 и q ' c ) = т ( c ) = т ( cm ) = 0 . Полная система уравнений для нахождения фс, фт и v ^c ) , v rm ) будет получена добавлением уравнений неразрывности (5).
Численное решение системы уравнений начинается с уравнений для v(c) и v(m), при этом значения фс и фт берутся с предыдущего шага по времени. Затем при найденных скоростях решаются уравнения (5) для фс, фш, и схема повторяется.
Для решения краевых задач для v( c ) и v ( m ) во внутренней области r < Rc tt ) , где присутствуют обе твердые фазы, и только для v ( m ) во внешней области Rc (t ) < r < Rm , в которой присутствует только матрикс, требуется шесть граничных условий. К их числу относятся условия (11), (8), оба условия (9) и условие (7).
Сложность задачи (помимо подвижности границы клеточной фазы) связана с тем, что во внутренней области присутствуют обе твердые фазы, в то время как во внешней области только одна, а на границе областей (при r = Rc (t ) ) используются условия на разрыве, которые связывают значения скоростей и концентраций фаз по разные стороны разрыва.
Решение уравнения для нахождения скорости фазы матрикса во внешней области ищется методом суперпозиции в виде линейной комбинации двух функций, для которых заданы «начальные» условия на внешней границе r = Rm [30]. Значение множителя в линейной комбинации определяется из условия непрерывности потока массы матрикса (8) на границе r = R c ( t ) . Это позволяет далее вычислить скорости фаз во внутренней области, используя граничные условия (11) и (9), которые будут содержать значение скорости матрикса только во внутренней области.
При расчете скоростей на отрезке [0; Rc ( t )] вводится безразмерная координата ^ = r / Rc ( t ) , что позволяет перейти от решения уравнений с подвижной верхней границей к решению уравнений на отрезке [0; 1].
Разностные схемы решения уравнений для v ( c ) и v ( m ' были получены интегро-интерполяционным методом [31]. Решение разностных уравнений во внутренней области было выполнено методом матричной прогонки. Для численного решения уравнений (5) для фс, фт использовалась TVD -схема Хартена [32; 33]. Вычисление интегралов в выражениях для активных напряжений выполнено с помощью пятиточечной квадратуры Гаусса [34], при этом учитывается различие пределов интегрирования для внутренних и граничных точек среды, то есть точек, удаленных от границы на расстояние, не превышающее R .
Числовые значения параметров
Введем безразмерные величины:
D*_ Rs F* _ E cm * _ P 1 * _ц 2 ..* _ Р 12
Rs D , Ecm 77, ^1 , ^2 , ц12
Rc 0 EC ц цц
• mc * mcm ,* kcmRc 02
mc = -c , m cm = -^ , k cm = ——
EC ECP
.
Здесь ц - характерное значение группы коэффициентов. Введение безразмерных неизвестных выполнено с использованием масштаба времени ц/ Ес , масштаба длины R и величины E в качестве масштаба для неизвестных, имеющих размерность напряжений.
Свойства системы будут исследованы в зависимости от значений безразмерных параметров, полученных на основе значений размерных величин, характерных для различных биологических сред.
Размер клеточных агрегатов, в которых проявляются различные структурные особенности, могут значительно варьироваться. Так, диаметр зародыша лягушки Xenopus Laevis на стадии, когда визуализируется образование первичной полости в рыхлом клеточном агрегате, составляет около 1,2-1,4 мм [2; 3]. Характерный размер кластеров клеток, образующихся при кластерном васку-логенезе, достигают величины порядка 400 мкм [1]. Изучение сортировки клеток разных тканей проводилось с использованием клеточных агрегатов размером 200500 мкм [6; 7]. Экспериментальное исследование закономерностей роста опухолей проводилось в [4] со сфероидами диаметром 200-600 мкм. Нарушение однородной структуры опухолевого агрегата, связанной с гибелью клеток и появлением некротического ядра, происходит в агрегатах, радиус которых превышает 200 мкм [35].
В дальнейшем примем, что Rc^ = 250 мкм. Последующие расчеты показали, что в качестве радиуса сферы, ограничивающей матрикс, достаточно принять Rm = 5 Rc 0. Для радиуса дальнодействия будет использовано значение Rs = 6,25 мкм, превышающее среднее значение радиуса клеток в [1] на 25 % .
Характерные значения коэффициента вязкости клеточной среды для эмбриональных тканей составляют 10 4 ^ 10 6 Па^с [36-38]. В дальнейшем примем ц = 8 • 105 Па^с в качестве характерного значения.
Оценка коэффициента межфазного трения между клеточной фазой и матриксом, выполненная в [39], дает значение 1,8 - 1014 Паю^м-2. В дальнейшем используется значение kcm = 1,8 - 1014 Паю^м-2.
Измерения в [24] показали, что клетки при взаимодействии с матриксом генерируют активные силы в диапазоне 10-200 нН в расчете на одну клетку. В [41] было показано, что активные силы, действующие со стороны клеток на матрикс, не превышают 100 нН. Если принять средний размер клетки ~10 мкм [1], то на единицу площади приходится -1010 клеток, и величина активных напряжений, отнесенных к единице поверхности среды , составит 100-2000 Па. Таким образом, получаем оценку коэффициентов m и m , которые характеризуют стяги- вающие составляющие активных напряжений в (3). В дальнейшем используются значения mc = 0,8 кПа и mcm = 1,5 кПа.
В настоящее время отсутствуют экспериментальные данные, позволяющие получить оценки параметров E и E . Рассмотрим состояние равновесия бесконечной ненагруженной сплошной среды, образованной только клетками, объемная концентрация которых является пространственно-однородной. Концентрация клеток будет определяться условием т(c) = 0 . Если принять, что пористость среды составляет 10-30 %, то получим оценку 0,1 < Ec / тс < 0,3 . Примем, что Ес = 0,1 кПа и Ecm = 0,05 кПа.
В дальнейшем звездочку при безразмерных параметрах будем опускать. В расчетах, если не сказано иначе, будут использоваться следующий базовый набор значения безразмерных параметров:
R 0 = 1; R m 0 = 5 ; Rs = 0,025; т с = 8 ; mC m = 15; E = 1;
E cm = 0’5 ; 0 1 = 1; М- 2 = 10 ; М 11 = М 12 = 1 ; k cm = 7,8 .
Числовые значения параметров учитывают, что матрикс является значительно более вязкой средой, чем клеточная фаза.
Результаты расчетов и обсуждение
Исследуем эволюцию объемных концентраций клеток и матрикса в клеточных агрегатах, различающихся начальным составом и активными взаимодействиями клеток между собой и c матриксом. Будут рассмотрены два случая, когда стягивающие активные взаимодействия клеток между собой сильнее или слабее перекрестных взаимодействий клеток с матриксом. В каждом из этих случаев будет рассмотрена эволюция рыхлых и плотных агрегатов, имеющих различный состав.
Последующие расчеты продемонстрировали быстрое уплотнение агрегатов и уменьшение их радиуса на начальном этапе во всех рассмотренных ниже случаях. Плотность агрегата в начальный момент времени будем характеризовать величиной уменьшения его радиуса вследствие быстрого начального уплотнения клеточной фазы. Клеточный агрегат будем называть рыхлым, если начальное уменьшение радиуса агрегата значительно превышает радиус дальнодействия R и плотным, если начальное уменьшение радиуса не превышает R . Степень уплотнения агрегата определяется как его составом, так и активными взаимодействиями клеток между собой и с матриксом.
Рассмотрение эволюции рыхлых и плотных агрегатов связано с различиями их происхождения. В одних случаях агрегаты первоначально формируются, напри- мер, в результате самоорганизации редко расположенных клеток. При этом клетки могут вырабатывать ферменты, разрушающие матрикс. Для этих случаев характерно формирование рыхлой клеточной массы, погруженной в матрикс, объемная концентрация которого в области, занимаемой совместно с клетками, может быть неоднородной. Такой сценарий реализуется, например, при кластерном васкулогенезе [1].
Для рыхлых клеточных агрегатов примем пространственно-однородное начальное распределение клеточной фазы в занимаемой ей области: ф. (0, r ) = фс0 при r < 1. Начальное распределение концентрации матрикса имеет вид сглаженной ступени ф m (0, r ) =Ф m 0 + ( Ф m 0 -Ф m 0 ) н s ( r - 1) , где н . ( r ) - сглаженная функция Хевисайда, заданная формулой:
0, r < -£
H ( r ) = < r +^ + — sin ( п r / s ) , | r | <£ , £ = 0,2 .
£ 2 e 2п x
1,
r > £
Здесь фт0 и ф+0 - начальные значения концентрации матрикса в агрегате и на бесконечности.
В других случаях формирование более плотных агрегатов, характерных для роста опухолей, может происходить в результате клеточных делений из небольшой компактной группы клеток. Содержание матрикса в этих агрегатах невелико, и будем считать его постоянным в области, занятой клетками. В этих случаях начальное распределение концентрации матрикса принято в следующем виде: ф m (0, r ) =Ф m 0 + ( Ф m 0 -Ф m 0 ) н £ ( r - 1 -£ ) , где £= 0,05. Начальное распределение клеточной фазы предполагается таким же, как и в рыхлых агрегатах.
-
1. Доминирование стягивающих активных взаимодействий в клеточной фазе над перекрестными взаимодействиями ( mc > mc ш, mc = 8 и mcm = 3 ). В случае доминирования стягивающих активных взаимодействий в клеточной фазе над перекрестными взаимодействиями численные расчеты показали сходную эволюцию концентрации клеточной фазы и матрикса как в рыхлых, так и в плотных агрегатах. Начальная стадия быстрого уплотнения сменяется медленным процессом дальнейшего роста концентрации клеточной фазы, перемещением матрикса на периферию и уменьшением радиуса клеточного агрегата. Такой тип эволюции клеточного агрегата можно охарактеризовать как неинвазивное развитие.
-
2. Доминирование перекрестных активных взаимодействий над межклеточными ( mcm > mc , здесь и далее используется базовый набор параметров). Увеличение перекрестных взаимодействий между клетками и матриксом приводит к изменению сценария эволюции концентрации клеточной фазы и формированию клеточных структур, отличных от простого уплотнения.
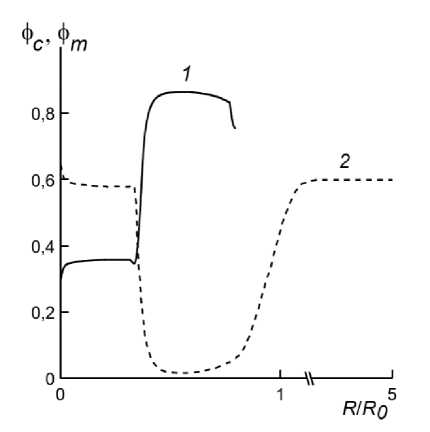
Рис. 2. Распределения концентраций клеточной фазы и матрикса ( 1 и 2 для фс и фя, соответственно) в момент времени t = 4,5 при начальных условиях ф c о = 0,4, ф т о = 0,05 и ф ^ 0 = 0,6
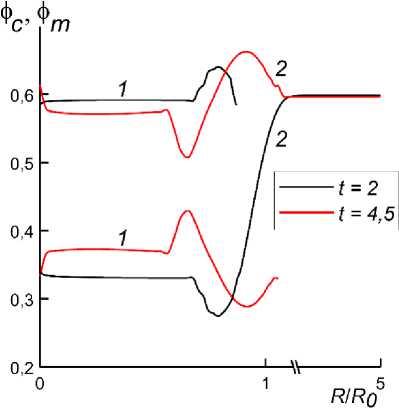
Рис. 3. Распределения концентраций клеточной фазы и матрикса ( 1 и 2 для фс и фя, соответственно) в моменты времени t = 2 и t = 4,5 при начальных условиях ф c 0 = 0,4, ф т 0 = 0,2 и ф т 0 = 0,6
A. Эволюция рыхлых клеточных агрегатов. Распределения концентраций клеточной фазы и фазы матрикса в момент времени t = 4,5 при фс0 = 0,4, фт0 = 0,05 и Ф+о = 0,6 показаны на рис. 2. При этих начальных значениях концентраций фаз уменьшение радиуса клеточного агрегата в результате начального уплотнения значительно превышает R и составляет приблизительно 8,5 • Rs . Последующее заполнение освободившегося пространства матриксом сопровождается его втягиванием в область, занятую клетками в результате доминирования сократительной составляющей в перекрестных активных взаимодействиях над межклеточными. Это способствует вытеснению клеточной фазы в радиальном направлении в сторону внешней границы фазы и формированию распределения концентрации клеточной фазы, которое можно рассматривать как начальную стадию формирования полости. Радиус клеточного агрегата незначительно растет. Обрыв кривой 1 (рис. 2) соответствует границе области, занятой клеточной фазой.
Дальнейшее развитие полости требует участия дополнительных механизмов, таких как повышенное гидростатическое давление и ферментативное разрушение матрикса. Исследование участия этих механизмов в рамках используемой модели выполнено в [25].
Влияние увеличения концентрации матрикса в агрегате. Увеличение концентрации матрикса в агрегате влияет на его уплотнение и приводит к уменьшению смещения границы клеточной фазы к центру, в область с меньшим содержанием матрикса. Это способствует меньшему ослаблению перекрестных взаимодействий между клетками и окружающим матриксом.
Распределения концентраций клеточной фазы и фазы матрикса в моменты времени t = 2 и t = 4,5 при ф c 0 = 0,4 , ф т 0 = 0,2 и ф т 0 = 0,6 показано на рис. 3. Начальное уменьшение радиуса агрегата в данном случае составляет приблизительно 7 • Rs .
Главным отличием от предыдущего случая является поддержание более сильных перекрестных взаимодействий в окрестности границы клеточного агрегата. Расчеты показали, что при данных начальных условиях, характеризуемых увеличением содержания матрикса в рыхлом агрегате, в эволюции концентрации клеточной фазы можно выделить несколько стадий. На начальном этапе, как и в предыдущем случае, начинает формироваться неоднородность распределения фазы, которая при определенных условиях может развиться в полую клеточную структуру. На более позднем этапе происходит внедрение небольшой части клеточной фазы в окружающий матрикс. Этот процесс можно рассматривать как проявление инвазивного развития, в котором небольшая группа клеток проявляет тенденцию отделиться от основной клеточной массы.
Влияние концентрации матрикса, окружающего клеточный агрегат. Распределения концентрации клеточной фазы в момент времени t = 4,5 при фс0 = 0,4 , фт0 = 0,2 и различных концентрациях окружающего матрикса ф +0 показаны на рис. 4. Расчеты показали, что при малой ф +0 происходит медленное распространение фронта клеток (кривая 1 ), ограничивающего внутреннее пространство, в котором концентрация клеточной фазы меньше. Увеличение ф+0 приводит к формированию структуры, имеющей тенденцию к формированию плато, окруженного
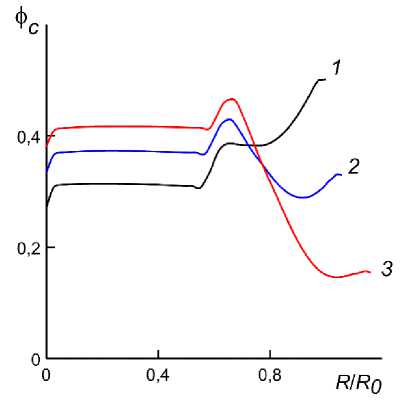
Рис. 4. Распределения концентраций клеточной фазы в момент времени t = 4,5 при фс0 = 0,4, ф-0 = 0,2 и различных ф+0 . Кривая 1 - ф+0 = 0,4,
2 — ф+ т о = 0,6, з — Ф т о = о,8
слоем клеточной фазы, и быстрого внедрения небольшой группы клеток в окружающий матрикс (кривые 2 и 3 ).
Из расчетов следует, что инвазии клеточной фазы способствуют более высокие значения концентрации окружающего матрикса, поскольку они обеспечивают более сильные перекрестные взаимодействия.
В результате вычислений также получено, что внедрение небольшой группы клеток рыхлого клеточного агрегата в окружающий матрикс является структурно неустойчивым. Некоторые изменения состава рыхлого агрегата, при которых величина начального уплотнения сохраняется, приводят к отсутствию внедрения группы клеток в окружающий матрикс. Так, при начальных условиях фс0 = 0,48 , фш0 = 0,035 быстрое начальное уменьшение радиуса агрегата в точности совпадает с уменьшением радиуса в предыдущем случае (фс0 = 0,4 , ф-0 = 0,2), однако эволюция концентраций фаз демонстрирует только формирование полости (как на рис. 2).
Дальнейшее увеличение плотности клеточного агрегата только за счет увеличения содержания в нем матрикса также показывает отсутствие инвазии. В результате вычислений получено, что при начальных условиях фс0 = 0,4 , ф-0 = 0,4 (начальное уплотнение приблизительно 3,5 • R S ) происходит распространение фронта клеточной фазы по матриксу: концентрация клеточной фазы на фронте либо превышает концентрацию в центральной части, либо остается приблизительно такой же (чем ниже концентрация окружающего матрикса, тем выше концентрация клеточной фазы на фронте).
Выполненные расчеты показывают, что устойчивой чертой развития рыхлых агрегатов, в которых начальное содержание клеточной фазы меньше некоторого критического значения, является создание предварительной разметки для последующего развития полой клеточной структуры. Эта особенность сохраняется при различных соотношениях начальных концентраций клеточной фазы и матрикса в рыхлых агрегатах.
Увеличение начальной плотности клеточной фазы выше некоторого критического значения приводит к формированию структуры, отличной от полости, даже если клеточный агрегат можно еще считать рыхлым ( фсо = 0,635 , ф-0 = 0,05, величина начального уплотнения приблизительно 3,5 • Rs , как в предыдущем случае). Формирующаяся в этом случае структура характерна для развития плотных клеточных агрегатов.
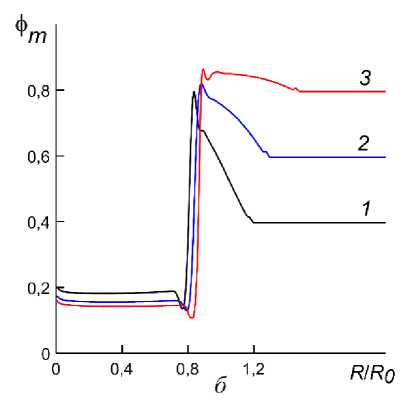
Б. Эволюция плотных клеточных агрегатов . Рассмотрим эволюцию объемных концентраций твердых фаз в плотном клеточном агрегате, в котором фс0 = 0,8 и ф-о = 0,08 при различных значениях ф+0 . Начальное уменьшение радиуса агрегата составляет приблизительно 0,1 • R . Расчеты показали, что в процессе формирования клеточной структуры происходит образование плотного ядра, окруженного кольцом клеточной фазы, где объемная концентрация клеток существенно отличается от центральной области (рис. 5, а ). Концентрация и распределение клеточной фазы в этом кольце зависит от концентрации окружающего матрикса. При невысокой концентрации матрикса распределение клеточной фазы характеризуется отделением небольшой группы клеток от основной массы (кривые 1 и 2 - рис. 5, а ), тогда как при высокой концентрации матрикса концентрация клеточной фазы в кольце является малой и практически неизменной (кривая 3 - рис. 5, а ). Радиус ядра слабо зависит от концентрации окружающего матрикса, а концентрация клеточной фазы в ядре является почти постоянной. Механические взаимодействия отделяющейся части клеточной фазы с матриксом создают условия для уплотнения матрикса вокруг ядра клеточной фазы (кривые 1 и 2 - рис. 5, б) , которое может быть рассмотрено как образование капсулы.
Эффект отделения группы клеток от основной массы был получен также и в теоретических работах [11; 42], в которых распространение клеток в матриксе описывалось уравнением диффузионного типа для концентрации клеток, учитывающим возможные механизмы активных клеточных взаимодействий. В этих работах было исследовано влияние активных взаимодействий клеток как между собой, так и с матриксом на распространение фронта клеток в недеформируемом матриксе в линейной геометрии. Существенным элементом моделей [11; 42] является ферментативное разрушение матрикса, которое создает неоднородность распределения его плотности.
Постановка задачи в данной работе позволяет получить этот эффект в реальной сферической геометрии с учетом деформируемости матрикса и без привлечения химической активности клеток.
Однако более реалистичное описание отделения группы клеток от основной массы должно быть выполнено в рамках 3 D -постановки без использования предпо-
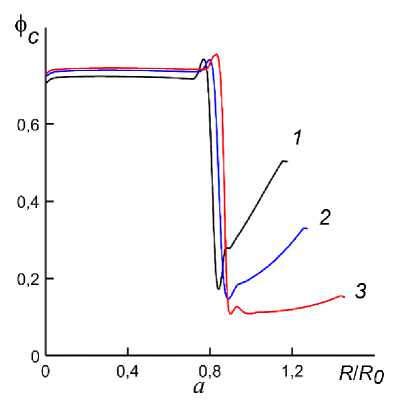
Рис. 5. Распределения концентраций клеточной фазы ( а ) и фазы матрикса ( б) в момент времени t = 4,5 при ф c о = 0,8 , ф т о = 0,08 и различных ф + 0 . Кривая 1 - ф т 0 = 0,4, 2 - ф т 0 = 0,6 , 3 - ф т 0 = 0,8
ложения о сферической симметрии. Должно быть исследовано развитие неустойчивости поверхностного слоя клеток, которая проявляется в образовании пальцеобразных клеточных структур.
Распределение клеточной фазы на рис. 5, б, кривая 3 характерно для развития глибластомы (опухоли мозга). Глиобластомы состоят из растущего плотного сфероида, окруженного зоной подвижных клеток низкой плотности, известной как инвазивная зона. Инвазивнная область клеток образует диффузный сферически-сим-метричный рисунок [5; 43; 44].
Во всех случаях инвазивный рост связан с изменением подвижности и адгезии клеток в поверхностном слое опухоли [45]. В рассмотренной задаче не потребовалось вводить пространственную неоднородность свойств клеток. Основными механизмами, контролирующим модель развития, являются активные межклеточные взаимодействия и активные взаимодействия клеток с матриксом, которые в свою очередь определяются составом среды.
Заключение
В работе исследована роль параметров, которые характеризуют систему «клетки - матрикс» только как механическую систему, исключая из рассмотрения эффекты, связанные с делением клеток и выработкой протеолитических ферментов.
Решена задача о развитии структур в клеточном агрегате сферической формы, который окружен вязким внеклеточным матриксом. Математическое моделирование выполнено в предположении сферической симметрии. Разработанная нами ранее континуальная многофазная модель биологической среды, образованной двумя активно взаимодействующими твердыми фазами и жидкостью [21], адаптирована для данного случая, когда одна из твердых фаз образована клетками, а другая -внеклеточным матриксом. Постановка задачи учитывает перемещение границы клеточного агрегата. Ее перемещение определяется условиями, которые учитывают перераспределение нагрузки между клеточной фазой и фазой матрикса по разные стороны от границы агрегата.
Исследована эволюция объемных концентраций клеточной фазы и матрикса в клеточных агрегатах, различающихся начальным составом и активными взаимодействиями клеток как между собой, так и с матриксом.
Численные расчеты показали, что в случае доминирования межклеточных активных механических взаимодействий над перекрестными между клетками и матриксом происходит только уплотнение как рыхлых, так и плотных агрегатов - отсутствие распространения клеток в окружающие ткани или неинвазивное развитие.
Доминирование перекрестных активных взаимодействий над межклеточными приводит к зависимости модели развития клеточных структур от начальной объемной концентрации клеточной фазы. В рыхлых клеточных агрегатах происходит вытеснение клеточной фазы в радиальном направлении в сторону внешней границы агрегата и формирование распределения концентрации клеточной фазы, которое можно рассматривать как начальную стадию формирования полости, окруженной слоем клеточной фазы. В плотных агрегатах происходит формирование плотного ядра и отрыв части клеточной фазы от основной массы - внедрение в окружающие ткани или инвазивное развитие. При этом формируется капсула из внеклеточного матрикса, окружающая агрегат. Более корректное описание развития плотных агрегатов должно быть выполнено в рамках 3 D -постановки без использования предположения о сферической симметрии. Должно быть исследовано развитие неустойчивости поверхностного слоя клеток, которая проявляется в образовании пальцеобразных клеточных структур. Исследование длительной эволюции системы не проводится, поскольку оно имеет смысл только с учетом механизмов, связанных с делением клеток и ферментативным разрушением матрикса.
Полученные результаты имеют значение для понимания роли различных механизмов в процессах образования и развития многоклеточных биологических структур.


