Математическое моделирование механического поведения биологических тканей и высокотехнологичных медицинских изделий, применяемых для лечения заболеваний сердечно-сосудистой системы
Автор: Антонова О.В., Рововой Э.Ю., Охотников А.О., Иванов С.Д., Кабин Н.А., Козаев А.В.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 1 т.30, 2026 года.
Бесплатный доступ
Стентирование и ангиопластика являются малоинвазивными методами, которые применяются для лечения широкого спектра заболеваний сердечнососудистой системы и позволяют восстановить нормальные функции артерий, например, нормальные просветы коронарных или сонных артерий при их сужении изза образования атеросклеротических бляшек. Применение методов математического моделирования может послужить основой для моделирования процессов установки стентов различного назначения и усовершенствования методик проведения данных медицинских вмешательств. Задачей данного исследования является проведение анализа механического поведения коронарных сосудов, в том числе пораженных атеросклерозом, и некоторых медицинских изделий, взаимодействующих с их фрагментами. Целью данного исследования является выявление закономерностей и формулировка рекомендаций по дальнейшему применению тех или иных реологических моделей. Было проведено численное моделирование и проанализировано поведение коронарного сосуда, коронарного сосуда с атеросклеротической бляшкой при взаимодействии с баллоном, а также численное моделирование процессов сворачивания и раскрытия баллона, применяемого в ангиопластике и стентировании коронарных сосудов. Рассмотрены гиперупругие реологические модели Хольцапфеля – Гассера – Огдена (HolzapfelGasserОgden), Огдена (Ogden) и Муни – Ривлина (Mooney – Rivlin), позволяющие максимально достоверно описать механическое поведение и напряженнодеформированное состояние данных объектов. На основании результатов численного моделирования проведен анализ влияния ключевых констант материалов на напряженнодеформированное состояние баллона, коронарной артерии и коронарной артерии с атеросклеротической бляшкой. Полученные результаты и рекомендации в дальнейшем могут быть использованы при построении математических моделей и описании механического поведения других высокотехнологичных медицинских изделий.
Коронарный стент, баллон для ангиопластики, атеросклеротическая бляшка, реологическая модель, напряженно-деформируемое состояние, математическое моделирование
Короткий адрес: https://sciup.org/146283275
IDR: 146283275 | УДК: 531/534: [57+61] | DOI: 10.15593/RZhBiomeh/2026.1.04
Mathematical modeling of mechanical behavior of biological tissues and high-tech medical devices used for the treatment of cardiovascular diseases
Stenting and angioplasty are minimally invasive methods that are used to treat a wide range of diseases of the cardiovascular system and allow restoring normal arterial functions, for example, normal coronary or carotid artery lumen when they narrow due to the formation of atherosclerotic plaques. The use of mathematical modeling methods can serve as a basis for modeling the processes of installing stents for various purposes and improving the methods of these medical interventions. The objective of this study is to analyze the mechanical behavior of coronary vessels, including those affected by atherosclerosis, and some medical devices interacting with their fragments. The purpose of this study is to identify patterns and formulate recommendations for the further application of certain rheological models. Numerical modeling was performed and the behavior of a coronary vessel, a coronary vessel with atherosclerotic plaque in interaction with a balloon, as well as numerical modeling of the processes of balloon folding and opening used in angioplasty and coronary stenting were analyzed. Hyperelastic rheological models of Holzapfel–Gasser-Ogden, Ogden, and Mooney-Rivlin are considered, which make it possible to describe the mechanical behavior and stress-strain state of these objects as reliably as possible. Based on the results of numerical modeling, the influence of key constants of materials on the stress-strain state of the balloon, coronary artery and coronary artery with atherosclerotic plaque was analyzed. The results and recommendations obtained can be used in the future to build mathematical models and describe the mechanical behavior of other high-tech medical devices.
Текст научной статьи Математическое моделирование механического поведения биологических тканей и высокотехнологичных медицинских изделий, применяемых для лечения заболеваний сердечно-сосудистой системы
RUSSIAN JOURNAL OF BIOMECHANICS
Развитие методов математического моделирования в данной области охватывает широкий спектр задач: от описания биомеханики желчевыводящих путей при патологиях [1] до создания сложных вычислительных моделей взаимодействия стента с многослойной артерией [2] и изучения геометрических параметров стентов, изготовленных как методом селективного лазерного плавления [3; 4], так и FDM-печати [5].
Для лечения широкого спектра заболеваний сердечно-сосудистой системы всё чаще используют высокотехнологичные медицинские изделия и процедуры: коронарное стентирование с применением различных конфигураций стентов [6–8] и ангиопластику [9; 10]. Данные процедуры являются малоинвазивными и эффективными методами, позволяющими вылечить или минимизировать последствия такой патологии, как атеросклеротическая болезнь сосудов. Применение методов математического моделирования ещё на этапах разработки медицинских рекомендаций и планирования оперативного вмешательства позволит снизить риски и минимизировать возможные негативные последствия.
В данной работе сделан акцент на такой важный этап моделирования, как выбор реологических моделей материалов, применяемых для описания поведения как медицинских изделий, в нашем случае баллона для проведения ангиопластики, так и биологических тканей: стенок сосудов. В то же время, для полного понимания механики сердечно-сосудистой системы и прогнозирования исходов вмешательств, крайне важно учитывать и характер кровотока [11]. С учетом строения стенок сосудов (здоровых и пораженных атеросклерозом), а также конструктивных особенностей баллона, для рассмотрения были выбраны несколько наиболее широко используемых гиперупругих моделей материала: Хольцапфеля – Гассера – Огдена [10], Огдена [13] и Муни – Ривлина [14; 15].
Отдельно отметим, что модель Хольцапфеля – Гассера – Огдена [12] является наиболее подходящей для моделирования именно сосудов, так как позволяет учесть анизотропию свойств, обусловленную физиологическими особенностями строения артерий и сосудов. При этом данная модель имеет ограничения, связанные с необходимостью выбора большого числа коэффициентов, входящих в нее и зависящих в первую очередь от качества и условий эксперимента по их определению [17]. Поэтому для моделирования сосуда была также рассмотрена и модель Муни – Ривлина [14; 15], имеющая более простую структуру, а для моделирования баллона – модель Огдена [13], использование которой обусловлено отсутствием необходимости на данном этапе учитывать анизотропные свойства.
Целесообразность анализа применения именно этих моделей подтверждается серий работ, где были продемонстрированы результаты для похожих задач [18-23].
Описание механического поведения коронарной артерии
Коронарные артерии являются сосудами, обеспечивающими кровоток к сердцу. Нарушение кровотока в связи с ограничением пропускной способности артерий может приводить к различным ишемическим болезням сердца (ИБС). Для решения проблемы окклюзии (сужения) сосудов активно применяется метод коронарного стентирования [24].
Коронарное стентирование – это наиболее современный метод инвазивного вмешательства, позволяющий восстановить проток физиологической жидкости к сердцу. Метод основан на имплантации стента в пораженный атеросклерозом участок артерии [25]. Стент – сетчатая трубчатая конструкция, устанавливаемая во внутренний просвет сосуда, тем самым обеспечивая необходимый объем проходящей жидкости. Схема процесса коронарного стентирования показана на рис. 1
В эндоваскулярных вмешательствах в современной медицине одной из ключевых проблем является недостаточное раскрытие или чрезмерное расширение коронарного стента, что может привести к осложнениям (тромбоз, рестеноз и т. д.). Для моделирования процесса и анализа возможных проблем необходимо наиболее достоверное описание поведения коронарной артерии.
Текущая часть исследования посвящена описанию механического поведения коронарной артерии с использованием модели Хольцапфеля – Гассера – Огдена [10], активно применяющейся при математическом моделировании сосудов, имеющих многослойную структуру.
Геометрическая модель. В качестве объекта исследования использована часть сосуда здорового пациента, взятая из открытых источников [26]. Длина сосуда в продольном направлении составляет 18 мм, внутренний диаметр сосуда в среднем составляет около 1,6 мм. В исходной 3 D -модели представлен только внутренний просвет сосуда, соответственно стенки сосуда были достроены самостоятельно. Толщина
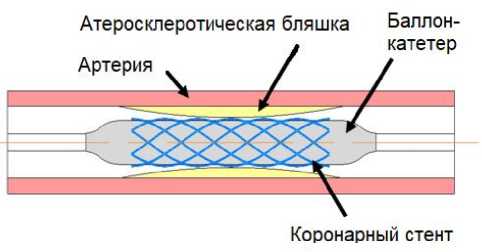
Рис. 1. Схема коронарного стентирования
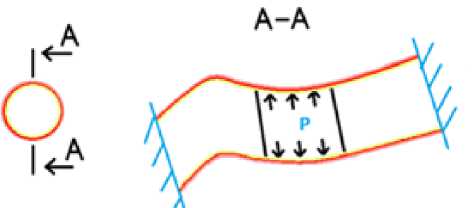
Рис. 2. Схема граничных условий (края закреплены по всем направлениям, давление приложено в проксимальной части сосуда)
внутреннего слоя артерии (интимы) составляет 0,27 мм, толщина среднего мышечного слоя (медии) – 0,35 мм, толщина наружного слоя (адвентиции) – 0,38 мм [27].
Модель материала Исследование строится на изучении механической модели Хольцапфеля – Гассера – Огдена [10]. Модель анизотропная, гиперупругая. Уравнение потенциальной энергии упругой деформации, используемое в математическом описании модели [29]:
U = C 10 ( 1 1 - 3) + ^ ^ J ^-1 - ln J e J , (1)
+Sexp[kiE4 ]-1(,
1 k 2 a= 1
где
К = k ( I - 3) + (1 - 3 k )( I ,( aa ) - 1).
В данном уравнении C , D , k , k , k являются параметрами материала, зависящими от температуры, N – число наборов волокон (N ≤ 3), I – инвариант C , J el – объемный модуль упругости, I – псевдо- инварианты C и A , C – модифицированный тензор деформаций Коши – Грина.
Целесообразность использования механической модели Хольцапфеля – Гассера – Огдена подтверждается большим количеством научных работ [40; 41], содержащих результаты валидации численных методов.
Параметры модели Хольцапфеля – Гассера – Огдена отображены в табл. 1 [28].
Граничные условия Постановка задачи заключается в моделировании процедуры ангиопластики, с использованием ранее описанной геометрической модели коронарной артерии.Края артерии закреплены по всем направлениям, в проксимальной части артерии к внутренней поверхности приложено давление в 2 МПа. Область прикладываемого давления ограничена 10 мм и выбрана таким образом, чтобы сымитировать место воздействия баллона. Схема граничных условий показана на рис. 2, где сечение А–А является поперечным разрезом сосуда.
Модель Хольцапфеля – Гассера – Огдена требует определения локальных систем координат по нормали для каждого элемента. В качестве упрощения применения модели Хольцапфеля – Гассера – Огдена необходимо разбить сосуд на несколько условно цилиндрических частей и задать для каждой части свою локальную систему координат. Это позволяет расставить системы координат согласно нормалям конечных элементов сосуда.
Результаты численного моделирования Для анализа интерес представляет напряженно-деформированное состояние артерии, так как полученная картина позволит оценить соответствие результатов численного моделирования реальному поведению артерии. Локализация максимальных напряжений, их распределение по толщине, деформации в радиальном направлении будут являться результатами, по которым можно будет вести валидацию.
Интенсивность напряжений по Мизесу отображена на рис. 3.
Значения максимальных напряжений по Мизесу составляют около 10–13 МПа по внутреннему радиусу в сечении с максимальными напряжениями. Анализируя подобные работы, можно сделать вывод, что порядок значений максимальных напряжений не отличается от полученных в данном исследовании [42].
Радиальные перемещения показаны на рис. 4.
Увеличение внутреннего диаметра коронарной артерии на 20–25% (штриховкой показана недеформированная форма артерии) соответствует результатам, получаемым при ангиопластике [28].
График распределения напряжений по Мизесу по толщине в сечении с максимальными напряжениями представлен на рис. 5.
Максимальное значение напряжений сосредоточено на внутренней поверхности сосуда, тогда как мышечная средняя часть практически не испытывает напряжений. Такое поведение не лишено логики – исходя из того, что средний мышечный слой является основной несущей частью сосуда, а интима при механическом воздействии достаточно быстро разрушается. Текущая гиперупругая постановка не позволяет описать вязкостно-пластические деформации. Такие деформации могут появляться ввиду различных патологических или возрастных изменений. Это нужно учесть в будущих исследованиях описания поведения коронарных артерий.
График распределения напряжений по Мизесу вдоль сосуда (рис. 6) позволяет оценить влияние закреплений на приложенное давление. В данном исследовании – левая и правая части сосуда в зоне закреплений испытывают крайне малые напряжения, что позволяет сделать вывод об отсутствии краевых эффектов.
Исходя из полученных в ходе анализа результатов, можно сделать вывод о возможности использования данной постановки задачи для описания использования данной постановки задачи для описания
Таблица 1
Параметры модели Хольцапфеля – Гассера – Огдена
|
Материал |
р , 10 6 кг / мм 3 |
C „ 10 - 3 МПа |
k 1 |
k 2,10 2 |
k , 10 - 2 |
D , 10 - 6 |
|
Интима |
1,07 |
23,2 |
25 |
12 |
31 |
0,90 |
|
Медиа |
1,07 |
1,40 |
0,18 |
1 |
31 |
5,31 |
|
Адвентиция |
1,07 |
8,32 |
4 |
10 |
31 |
4,67 |
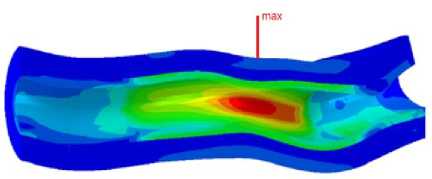
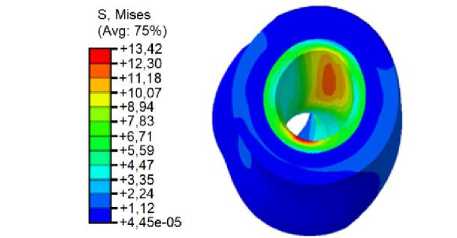
Рис. 3. Интенсивность напряжений по Мизесу (МПа): сверху – в продольном разрезе; снизу – в поперечном сечении с максимальными напряжениями
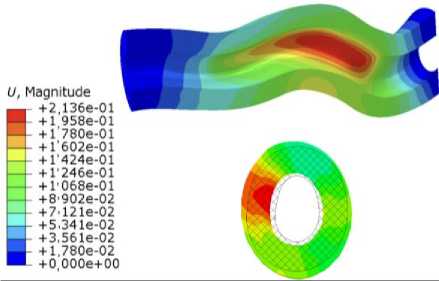
Рис. 4. Поле суммарных перемещений [мм]: сверху – в продольном сечении; снизу – в поперечном сечении
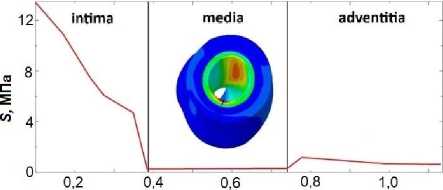
г, мм
Рис. 5. Распределение напряжений по Мизесу по толщине
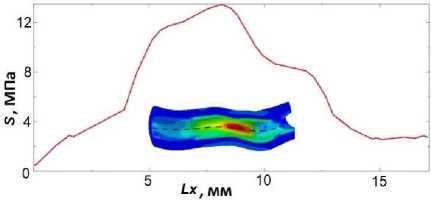
Рис. 6. Распределение напряжений по Мизесу вдоль сосуда, где Lx – длина сосуда вдоль его условной оси
поведение коронарной артерии.
поведения коронарных артерий при использовании механической модели Хольцапфеля – Гассера – Огдена. Краевые эффекты в области закреплений отсутствуют, уровень напряжений в области прикладываемого давления согласуется со статьями подобного рода.
Максимальные напряжения по Мизесу составили 10–13 МПа по внутреннему радиусу в сечении с максимальными напряжениями. Такие значения схожи со значениями в подобных исследованиях. Радиальные перемещения составляют 20–25 % от изначального внутреннего диаметра коронарной артерии. Это удовлетворяет результатам, получаемым в процессе ангиопластики [29], и отражает
Описание механического поведениякоронарной артерии, пораженнойатеросклерозом
Коронарная артерия является ключевым компонентом системы кровоснабжения миокарда, обеспечивая доставку кислорода и питательных веществ, необходимых для нормального функционирования сердца. При прогрессировании атеросклероза, характеризующегося формированием атеросклеротических бляшек в стенке сосуда, просвет артерии сужается, что ограничивает кровоток и
Type: Total Deformation Unit: mm
H O,4693 Max 0,41719 0,36509 0,31298 0,26088 0,20877
-0,'5667
-0,10456 0,052459

0.0035442 Min
Рис. 8 Поле суммарных перемещений атеросклеротической бляшки

Type: Equivalent (von-Mises) Stress Unit: MPa
-
■ 0,64346 Max
-
■ 0,57197 0,50048 0,42899 0,3575 0,28601 0,21453
-
■ 0,14304 ■ 0,071547
5,8507e-5 Min
Рис. 9. Поле распределения эквивалентных напряжений по Мизесу на атеросклеротической бляшке приводит к развитию ишемической болезни сердца (ИБС) [30]. Когда медикаментозная терапия оказывается недостаточно эффективной, чрескожное коронарное вмешательство (ЧКВ) со стентированием становится важным методом восстановления адекватного коронарного кровотока. В ходе процедуры стентирования в поражённый участок коронарной артерии имплантируется стент – металлическая сетчатая конструкция, которая механически расширяет просвет сосуда и обеспечивает восстановление перфузии миокарда.
Несмотря на выраженный положительный эффект, взаимодействие стента с атеросклеротической бляшкой и окружающими тканями инициирует сложные биологические процессы. Формирование неоинтимы, воспалительная реакция, а также морфологические и структурные особенности бляшки оказывают влияние на долгосрочную эффективность стентирования. В частности, неполное прилегание стента к сосудистой стенке или дистальная эмболизация фрагментами бляшки могут приводить к тяжёлым осложнениям и даже летальному исходу [31].
Целью данного исследования является анализ механического поведения атеросклеротической бляшки и оценка влияния выбранной модели материала на её напряжённо-деформированное состояние. В дальнейшем планируется расширение исследования за счёт более детального анализа механики коронарного сосуда.
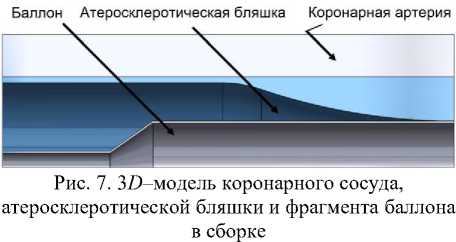
На рис. 7 представлена модель, включающая коронарную артерию, атеросклеротическую бляшку и баллон в симметричной постановке.
Геометрическая модель. В исследовании рассматривались трёхмерные модели коронарной артерии, атеросклеротической бляшки и баллона в симметричной постановке, представленной на рис. 9. Коронарная артерия моделировалась в виде однослойной цилиндрической трубки с наружным диаметром 4,4 мм, толщиной стенки 0,7 мм и длиной 7,5 мм. Атеросклеротическая бляшка задавалась с толщиной основания 0,1 мм и протяжённостью стеноза 3,5 мм [32]. Для моделирования баллона были выбраны следующие параметры: наружный диаметр 1,53 мм, толщина стенки 0,1 мм, длина 7,5 мм.
Численные расчёты выполнялись методом конечных элементов, реализованным в программном комплексе ANSYS [33]. Была создана серия конечно-элементных моделей. Проведено исследование сходимости. Для дальнейшего анализа выбрана модель, состоящая из 21 595 элементов второго порядка.
Модель материала. Для моделирования атеросклеротической бляшки применяются различные модели материалов, включая модели Муни – Ривлина, Огдена, Нео – Гука и другие [32; 34–37]. В данном исследовании использована гиперупругая модель Муни – Ривлина пятого порядка. Эта модель представляет собой разновидность полиномиальной функции плотности энергии деформации, применяемой для описания механического поведения гиперупругих материалов. Она характеризуется параметрами, связанными с модулем сдвига и модулем объёмной упругости [14 – 16].
W = cw ( 1 1 - 3) + c 01 ( 1 2 - 3) + c 20 ( 1 1 - 3)2 +
+ C 11( 1 1 - 3)( 1 2 - 3) + (2)
+ c02(12 - 3)2, где
W – потенциал энергии деформации;
I – инварианты тензора деформаций Коши – Грина; c – материальные константы.
В табл. 2 приведены параметры модели материала Муни – Ривлина, использованные в расчётах [32; 38].
Для описания коронарной артерии и баллона использовался изотропный материал. В таб. 3 приведены параметры модели материала, использованные для описания механики коронарной артерии [39; 42].
Граничные условия. В качестве граничных условий на границах используемых моделей: коронарной артерии, атеросклеротической бляшки и баллона были заданы условия удалённого смещения с запретом на перемещение по всем степеням свободы. Между внутренней поверхностью артерии и внешней поверхностью бляшки был задан склеенный контакт, чтобы атеросклеротическая бляшка деформировалось последовательно с артерией. Между баллоном и бляшкой использовался нелинейный контакт без трения. Расширение баллона внутри артерии осуществлялось путем задания на внешнюю поверхность баллона перемещения по нормали, равного 0,32 мм.
Результаты численного моделирования. Оценка влияния параметров модели материала Муни – Ривлина на напряженно-деформированное состояние атеросклеротической бляшки являлась одним из ключевых аспектов исследования. Сравнение проводилось на основе максимальных значений эквивалентных напряжений по Мизесу. Поле эквивалентных напряжений по Мизесу и поле перемещений для параметров материала Муни – Ривлина приведенных в табл. 2, представлено на рис. 8 и 9. Можем наблюдать, что полученные результаты соотносятся с теми, которые были получены в работе [32]. В зависимости от эксцентричности атеросклеротической бляшки напряжения, возникающие в бляшке при раскрытии баллона, находятся в диапазоне от 0,3 до 1,5 МПа. Далее было выполнено варьирование параметров модели материала Муни – Ривлина, результаты представлены на рис. 11–13.
На рис. 10, где представлено варьирование параметра C , наблюдается нелинейная зависимость максимальных напряжений по Мизесу от параметра C . В начальном диапазоне значений C (3–4,5 кПа) отмечается плавный и относительно небольшой рост напряжений. Это указывает на низкую чувствительность напряженного состояния к изменению C в этой области. Однако, после значения C = 4500 Па, скорость роста напряжений увеличивается, что свидетельствует о возрастающем влиянии параметра на деформационное поведение материала. Важно отметить наличие выраженного пика в области C = 6 кПа, после которого напряжения стабилизируются и демонстрируют
Таблица 2
Параметры модели материалов Муни-Ривлина
|
с 10 , кПа |
с 01 , кПа |
с 11 , кПа |
с 20 , кПа |
с 02 , кПа |
|
28,5 |
8,63 |
56,76 |
150,48 |
2721 |
Таблица 3
Параметры модели изотропно-упругих материалов
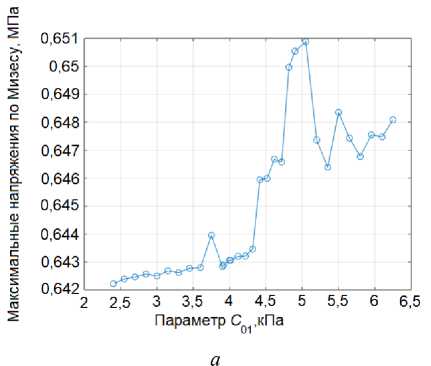
На рис. 11, а можем наблюдать, что зависимость максимальных напряжений по Мизесу от параметра C также демонстрирует нелинейный характер. В начальной области (2 – 4 кПа) наблюдается незначительное изменение напряжений при варьировании C , что свидетельствует о слабом влиянии параметра в данном диапазоне. Однако в диапазоне значений C от 4 до 5 кПа происходит резкий рост напряжений, достигающий максимума при C =5кПа.
После достижения пикового значения напряжения резко снижаются и стабилизируются, демонстрируя тенденцию к медленному росту при дальнейшем увеличении C . Подобное поведение может демонстрировать, что параметр C играет важную роль в определенном диапазоне деформаций.
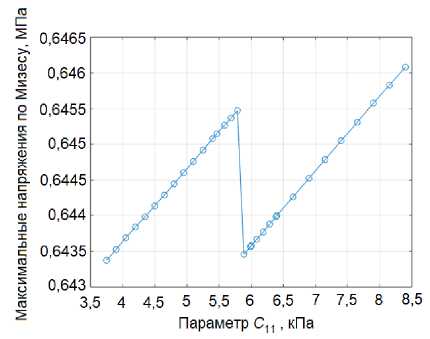
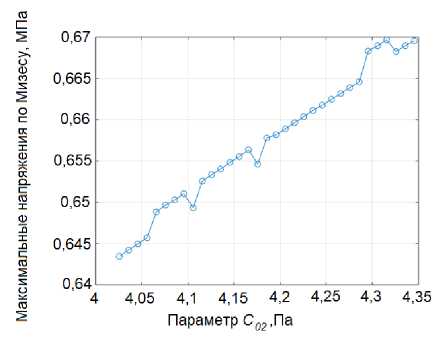
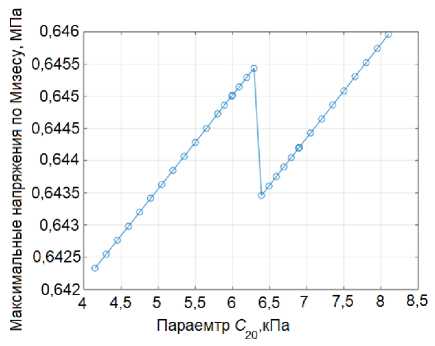
На рис. 11 б представлена практически линейная зависимость максимальных напряжений по Мизесу от параметра C в двух диапазонах значений, разделенных резким скачком. В первом диапазоне (4–6,2 кПа) и во втором диапазоне (6,5–8,5 кПа) наблюдается линейное увеличение напряжений с ростом C . Однако при C = 6,3 кПа происходит резкое снижение напряжений. Данный скачок может быть связан с изменением характера деформации или переключением на другой механизм деформирования, приводящий к внезапному снижению напряжения. Зависимость максимальных напряжений по Мизесу от параметра C , представленная на рис. 12, а, аналогична зависимости от C , см. рис. 11, а. В первом (3,5–5,8 кПа) и втором (6–8,5 кПа) диапазонах наблюдается линейный рост напряжений с увеличением параметра C . Между этими участками возникает резкое падение напряжений при значении C около 5,8 кПа. Данный скачок, вероятно, обусловлен теми же причинами, что и в случае с параметром C – изменением механизма деформации. На рис. 12, б наблюдается монотонное, но не совсем линейное увеличение максимальных напряжений по
Мизесу с ростом параметра C .
На основании проведенного анализа выявлено, что параметры модели Муни – Ривлина оказывают разное влияние на максимальные напряжения по Мизесу, что выражается в нелинейностях, пиках и скачках. Наиболее сложное и нелинейное воздействие выявляется у параметров C и C , в то время как C
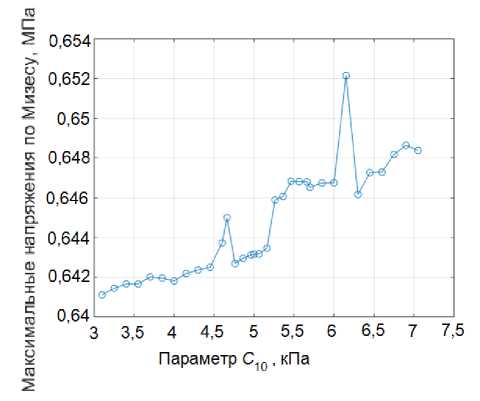
Рис. 10. Зависимость максимальных напряжений по Мизесу от C
и C демонстрируют линейную зависимость, осложненную резкими изменениями, вероятно, связанными с переходом к другому механизму деформации. Параметр C оказывает монотонное положительное воздействие. Важно отметить, что при использовании модели материала Муни – Ривлина необходимо проводить тщательный подбор параметров для получения адекватного результата.
Моделирование процессов сворачивания и раскрытия баллона для ангиопластики
Баллонный катетер представляет собой одно из ключевых медицинских устройств, применяемых при ангиопластике. Баллон крепится на дистальном конце тонкого гибкого катетера и изготавливается, как правило, из композитных полимерных материалов (например, нейлона, полиэтилентерефталата или полиуретана), обладающих высокой прочностью, устойчивостью к деформации и способностью выдерживать внутренние давления до 10–20 атмосфер.
Процедура начинается с введения катетера с баллоном в артериальное русло через небольшой прокол в области бедренной или лучевой артерии. Под рентгеноскопическим контролем катетер продвигается
а
Рис. 12. Зависимость максимальных напряжений по Мизесу от а – C , б – C
Рис. 11. Зависимость максимальных напряжений по Мизесу от а – C , б – C
б
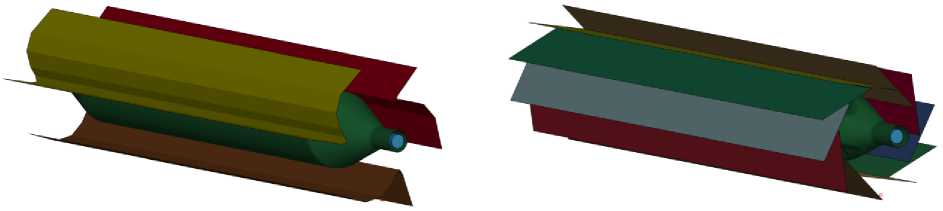
б к поражённому участку сосуда. На этом этапе баллон находится в спущенном состоянии и свернут в компактную форму, что обеспечивает минимальное сопротивление при продвижении по сосуду и снижает риск травмирования эндотелия.
Когда баллон достигает области стеноза, внутрь него подаётся жидкость под высоким давлением, вызывая его контролируемое радиальное расширение. На этом этапе баллон демонстрирует сложное механическое поведение, обусловленное как геометрией конструкции, так и реологическими свойствами материала. Под воздействием давления баллон равномерно разворачивается, прикладывая к стенке сосуда радиальное усилие, достаточное для раздвигания суженного участка и разрушения атеросклеротической бляшки. При этом важным параметром является радиальная жёсткость баллона – он должен обеспечивать необходимое давление без значительных отклонений от заданной формы.
Наиболее напряжённой фазой для материала баллона является момент максимального расширения, при котором он взаимодействует с неоднородной и часто кальцинированной внутренней поверхностью сосуда. Это требует от материала высокой прочности на разрыв и способности сохранять геометрическую стабильность без локализованных раздутий или деформаций. При моделировании баллон рассматривается как тонкостенная оболочка, подверженная внутреннему давлению, с гиперупругим или упругопластическим поведением в зависимости от выбранного материала.

Рис. 13. Геометрическая модель баллона
а б
Рис. 14. Этапы сворачивания баллона: а – стадия складывания; б – стадия плиссировки

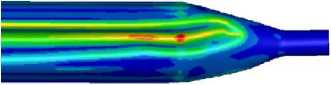
Рис. 15. Результаты численного моделирования: а – форма баллона на стадии плиссировки;
б – соответствующее поле напряжений по Мизесу [МПа]

6,829e+02-
6,146е+02-|
5,463е+02-4,780е+02-4,098е+02-
3,415е+02-2,732е+02-
2,049е+02
1,366е+02 -]
6,829е+01 -I 0,000е+00 ■
Рис. 16. Поле напряжений по Мизесу на стадии плиссировки: а – на проксимальном конце баллона;
б – на дистальном конце баллона [МПа]
Таблица 4
Параметры модели материала Огдена
|
Порядок модели Огдена |
µ , МПа |
α 1 |
|
1 |
1,72 |
4,55 |
Таблица 5
Значения параметров материала катетера
|
Материал |
E |
ν |
|
HDPE |
1000 |
0,46 |
После достижения требуемого диаметра сосуда часто в него имплантируется стент, задача которого – зафиксировать достигнутый просвет и предотвратить повторное сужение (рестеноз). Далее давление в баллоне снижается, и он возвращается к исходной геометрии. Эта фаза также требует от материала хорошей способности к обратимым деформациям и устойчивости к многократным циклам нагружения – разгрузки. После этого баллон и катетер аккуратно извлекаются из организма.
Таким образом, баллон в процессе ангиопластики проходит несколько стадий нагружения: начальное сжатое транспортное состояние, фазу активного радиального расширения при контакте с жёсткой сосудистой стенкой, удержание формы под давлением и последующее возвращение к исходным размерам. Каждая из этих стадий предъявляет особые требования к механическим характеристикам баллона, что необходимо учитывать при его проектировании, выборе материалов и построении численных моделей. В данной работе основное внимание уделяется описанию напряжённо-деформированного состояния баллона в различных фазах ангиопластики.
Цель исследования Данное исследование направлено на описание механического поведения и напряженно-деформированного состояния баллона при ангиопластике с целью выявить возможные области возникновения концентраторов напряжений или зоны повреждения баллона. В дальнейшем на основании полученных результатов исследование будет расширено для различных материалов баллона и методик сворачивания.
Геометрическая модель Для математического моделирования в рамках данного исследования была построена геометрическая модель баллона в соответствии с размерами, представленными в [7]. Итоговая модель изображена на рис. 13.
Численное моделирование проводилось с использованием метода конечных элементов. Модель содержит 28 800 твердотельных элементов (катетер) и 168 259 оболочечных элементов первого порядка (баллон) толщиной 0,03 мм [42].
Модель материала. Для описания поведения материала баллона, полиамида ( Grilamid L 25), была выбрана гиперупругая модель материала Огдена первого порядка. Данная модель используется для описания поведения гиперупругих материалов, потому что она хорошо подходит для моделирования больших нелинейных деформаций, характерных для таких материалов, как пластмассы и биологические ткани. Благодаря гибкой параметризации с помощью степенных зависимостей главных деформаций, она позволяет проводить точную настройку модели под экспериментальные данные, что делает её более универсальной по сравнению с другими гиперупругими моделями, такими как Нео – Гук или Муни – Ривлин.
Определяющие соотношения для модели материала
Огдена представлены формулами (3) и (4).
NN и=E-v (K‘ + я + ла - з|+Е к (Jel -i)2, (3)
,-=1 a ,=i Di где д = j ; д ^ д д13 = i, (4)
U – плотность энергии деформации; µ – модуль Огдена, Паскаль; α – параметр Огдена, безразмерный;
λ – удлинения в главных направлениях; J – объемная деформация; J – упругий объемный коэффициент деформаций; D – параметр материала, связанный с объемным сжатием, 1/Паскаль.
В табл. 4 приведены параметры модели материала Огдена [43].
Для описания материала катетера была выбрана линейно-упругая модель материала, полимера (HDPE), представленная формулами (5) и (6):
a = Л0Е + 2це, где
0 = tr e , Л =------------- , ц =------- .
(1 + v )(1 - 2 v ) 2(1 + v )
В данном уравнении E – модуль Юнга, а ν коэффициент Пуассона. Значения соответствующих параметров взяты из литературы [45] и представлены в табл. 5.
Граничные условия. Для моделирования процесса складывания баллона были заданы следующие граничные условия:
-
1) для узлов на дистальном конце катетера был задан запрет на перемещение по всем степеням свободы;
-
2) по внутренней поверхности баллона было приложено равномерно распределенное давление, равное -0,1 МПа, предотвращающее самопроизвольное расправление материала после удаления внешнего воздействия;
-
3) были созданы абсолютно жесткие пластины сжатия и плиссирующие пластины, рис. 14, которые обеспечивают формоизменение баллона [44].
Результаты численного моделирования. Сворачивание баллона осуществляется в два последовательных этапа — стадия складывания и стадия плиссировки, каждая из которых включает серию контролируемых механических воздействий с использованием пластин сжатия и вакуумной стабилизации.
На первом этапе (см. рис. 14, а) три пластины сжатия вращаются вокруг своих опорных точек на угол 4,58°, устанавливая контакт с внешней поверхностью баллона. Это вызывает деформацию стенок и придает баллону форму «трилистника». Вся операция выполня- ется за 1 с моделирования. После этого пластины сжатия возвращаются в исходное положение (поворот на -4,58°), и контакт между пластинами сжатия и баллоном прекращается.
На втором этапе, (рис. 15, б) происходит уплотнение складок и их наматывание вокруг катетера. Для этого десять плиссирующих пластин поворачиваются на угол -1,1°, вступая
Одной из основных задач данной работы являлось определение потенциально уязвимых участков баллона. Для этого было проанализировано поле распределения эквивалентных напряжений по Мизесу.
Соответствующие результаты представлены на рис. 16, б.
Из рис. 15, б видно, что напряжения возрастают в областях складок баллона, при этом вблизи концов баллона возникают концентраторы напряжений, которые стоит рассмотреть отдельно – рис. 16.
На рис. 16 представлены распределения эквивалентных напряжений по Мизесу в материале баллона в процессе его сворачивания. Анализ полученных данных показал наличие выраженных концентраторов напряжений вблизи проксимального и дистального концов баллона. В этих зонах наблюдается локальное повышение напряжений, значения которых существенно превышают напряжения в центральной части устройства.
Максимальные напряжения сосредоточены в переходных участках между цилиндрическим телом баллона и его коническими окончаниями, что обусловлено геометрическими особенностями конструкции и резким изменением формы. Данные концентраторы могут стать потенциальными точками начала разрушения материала или инициирования локальных повреждений при повторном использовании или в условиях чрезмерного нагружения.
По результатам проведенного исследования можно отметить, что были достаточно адекватно смоделированы различные этапы складывания баллона для ангиопластики, при этом были обнаружены концентраторы напряжений вблизи проксимального и дистального


