Математическое моделирование оптоакустического сигнала от агрегированных эритроцитов для оценки уровня агрегации
Автор: Кравчук Денис Александрович, Старченко И.Б.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Математические методы и моделирование в приборостроении
Статья в выпуске: 1 т.28, 2018 года.
Бесплатный доступ
Представлена модель формирования оптоакустического сигнала при воздействии лазера Nd: YAG на модельные образцы крови с агрегированными эритроцитами, для изучения того, как будет изменяться амплитуда оптоакустического (ОА) сигнала и спектр мощности в зависимость от уровня агрегации эритроцитов. Разработана математическая модель упаковки эритроцитов для моделирования агрегации красных кровяных телец. Установлено, что амплитуда оптоакустического сигнала возрастает с увеличением уровня агрегации и снижается частота спектральной плотности мощности сигнала.
Оптоакустический сигнал, агрегация, эритроциты, спектральная плотность мощности, лазер
Короткий адрес: https://sciup.org/142214842
IDR: 142214842 | УДК: 535.015 | DOI: 10.18358/np-28-1-i3036
Mathematical modeling of the optoacoustic signal from aggregated erythrocytes to assess the level of aggregation
The presented model of the formation of an optoacoustic signal under the influence of an Nd: YAG laser on model blood samples with aggregated erythrocytes, to study how the amplitude of the optoacoustic (OA) signal and the power spectrum will vary depending on the level of aggregation of erythrocytes. A mathematical model of the packing of erythrocytes has been developed for modeling the aggregation of red blood cells. It is established that the amplitude of the optoacoustic signal increases with increasing aggregation level and the frequency of the spectral power of the signal decreases.
Текст научной статьи Математическое моделирование оптоакустического сигнала от агрегированных эритроцитов для оценки уровня агрегации
Рассмотрим воздействие лазерного излучения Nd: YAG с длиной волны 1064 нм на математическую модель агрегированных эритроцитов при фиксированном гематокрите. Ранее в [1–4] была разработана модель формирования отклика оптоакустического сигнала от одиночного эритроцита и была смоделирована математическая модель формирования оптоакустического сигнала (ОАС) в результате воздействия лазерного излучения на модельные образцы крови с учетом изменения гематокрита. Было отмечено, что уровень ОА сигнала монотонно возрастал по мере увеличения концентрации эритроцитов. Амплитуда спектральной плотности мощности ОАС возрастала с увеличением количества источников формирования оптоакустического сигнала, что позволяет определять уровень гематокрита. В этой работе рассмотрим формирование ОАС от агрегированных эритроцитов, разработаем метод упаковки эритроцитов в кластеры различного размера и при различных уровнях агрегации.
Агрегация эритроцитов (АЭ) может служить диагностическим параметром для патологических состояний. При патологиях может возникать так называемый "гиперагрегационный синдром", при котором эритроциты аномально быстро и прочно агрегируют. Изменение АЭ при патологиях связывают в основном с изменением концентрации белков плазмы крови и в меньшей степени с изменением свойств самих эритроцитов.
Конфигурация кровяных тканей агрегированных эритроцитов может быть получена различны- ми путями. Например, в [5] эмпирически моделировали энергию взаимодействия клеточных пар как комбинацию стерического и притягивающего потенциалов, а затем применяли технику Монте-Карло для развития системы в течение большого количества итераций для получения двумерных распределений агрегированных эритроцитов. При случайной свободной упаковке в двух измерениях можно обеспечить плотность упаковки ячеек 54– 55 %, тогда как в трех измерениях она составляет около 60 %. Таким образом, эти методы не способны обеспечить компактные кластеры. Однако для создания плотно упакованных кластеров эритроцитов можно использовать обычные схемы упаковки. Например, в двух измерениях плотность упаковки кругов (сфер) почти 90 % может быть достигнута с помощью схемы гексагональной упаковки. Эту схему упаковки можно использовать для организации окружностей, представляющих эритроциты, для образования агрегат. Сформированный кластер помещали случайным образом для создания агрегированного образца крови и многократно повторяли вычисления для различных образцов ткани. Следует отметить, что это — очень быстрый метод, потому что ячейки размещаются в фиксированных местоположениях в агрегате, а также способны формировать компактные кластеры.
МАТЕМАТИЧЕСКАЯ МОДЕЛЬ
Волновое уравнение для давления, создаваемого при поглощении оптического лазерного излучения при условии термоизоляции, можно запи- сать в виде [6, 7]:
V2 p -
1 d 2 p v 1 d tt
в d H C p d t ’
где β — коэффициент изобарного теплового расширения, С p — теплоемкость, ν s — скорость звука в области действия лазера, H — тепловая энергия.
Пусть оптическое излучение интенсивности I 0 распространяется вдоль оси x , тогда функция нагрева H ( x , t ) = μI 0 e–ωt . Здесь μ — коэффициент оптического поглощения освещенной среды, ω — частота модуляции оптического луча.
Можно получить аналитические решения уравнения (1) для некоторых простых форм (цилиндра, сферы и т. д.) при использовании соответствующих граничных условий [1, 3, 4, 6]. Давление оптикоакустического сигнала для равномерно освещенного сферического поглотителя на расстоянии r можно найти как [1, 7, 8]
P \ ( 1 ) =
i ωµβI 0 ν s α c p ( r / a )
x
[ л л! i k ( (r -a )
sin 1 - 1 cos 1 ] e f
q 2
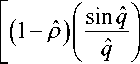
- cos 1 + i pv sin 1
где безразмерная частота определяется как q ˆ = ωα / ν s , α — радиус поглощающей сферы, k f — волновое число в жидкой среде для волны давления с частотой ω и определяется выражением k f = = ω / ν f . Аналогично, безразмерные величины ρ ˆ = = ρ s / ρ f и v ˆ = ν s / ν f представляют собой отношения плотности и скорости звука соответственно. Нижние индексы s и f используются для обозначения свойств поглотителя и окружающей жидкой среды соответственно, верхний индекс 1 в уравнении (2) означает, что рассматривается только один источник ОАС.
Предположим, что сферические поглотители освещались лазерным излучением с постоянной интенсивностью независимо от их пространственного положения и все многократные рассеяния светового пучка можно считать пренебрежимо малыми, а также ультразвуковые волны, генерируемые светопоглощающими сферическими частицами, не взаимодействуют друг с другом. При этих предположениях поле давления ОАС, создаваемое совокупностью поглощающих сфер, можно записать в виде линейной суперпозиции сферических волн, испускаемых отдельными источниками, поле давления от времени принимает вид
p } ( T )
∞
xJ d1 ]
-^
i^eFv s 2 x 2nCp ( r / a )
sin 1 - 1 cos 1 ]
1 (1 - p))
sin 1 ] „ „
----I- cos 1 + ipv sin 1
1 )
-4- x
Суммарный член в приведенном выше уравнении учитывает интерференцию волн давления, генерируемых сферическими источниками, распределенными в пространстве. При этом r n — вектор положения n -й частицы и содержит N источников ОАС. Здесь k f определяет направление наблюдения [7].
МЕТОД УПАКОВКИ ЭРИТРОЦИТОВ
Зададимся размерами агрегируемого кластера и фиксированной величиной гематокрита. Модельные исследования будем проводить для образцов крови при 40 %-м гематокрите и при различных условиях кластеризации, или агрегации, и исследуем полученный ОА сигнал. Уровень гематокрита выбран 40 %, потому что он близок к нормальному уровню гематокрита 45 % в нормальной крови человека. [9]
Следующий шаг заключался в том, чтобы найти пространственные положения случайно распределенных, хорошо разделенных изотропных кластеров одинакового размера в пределах размеров образца ткани в периодических граничных условиях с использованием того же алгоритма. Количество кластеров также фиксировало число ячеек, которые могли быть присоединены к одному кластеру. Количество ячеек на кластер определялось делением общего количества ячеек на количество кластеров и усечением этого численного значения до ближайшего меньшего целочисленного значения. Это количество ячеек было позиционировано с использованием гексагональной упаковки для каждого кластера.
После этого были выбраны координаты центра круга, расположенного в центральной области этой прямоугольной области. Координаты центров других кругов регистрировались в соответствии с их расстояниями относительно этой контрольной точки для формирования таблицы поиска. Следующим шагом было взять координаты требуемо-
го количества кругов, прикрепленных к кластеру, из этой таблицы поиска и поместить их относительно центра кластера. В таблице поиска были указаны координаты окружностей относительно центра кластера. Для вычисления же уравнения (3) необходимы координаты этих окружностей относительно начала кластера, и это легко получить, суммируя координаты этих кругов (доступные из таблицы) и центра кластера. Точно так же координаты окружностей, связанных с другими кластерами, были взяты из справочной таблицы, и они были преобразованы в систему координат кластеров. Круги, не принадлежащие какому-либо кластеру, были размещены в пределах образца при неперекрывающихся условиях с другими кругами. Таким образом, были получены пространственные распределения неперекрывающихся, изотропных и идентичных кластеров, содержащих неперекры-вающиеся ячейки. Кроме того, для каждого агрегирующего условия был рассчитан средний радиус вращения кластеров для количественного определения среднего размера кластера. Радиус вращения кластера Rg определяли, используя квадрат расстояний ячеек от центра кластера. Численные значения Rg были получены для всех кластеров, связанных с реализацией ткани, и среднее значение было вычислено впоследствии. Неагрегиро-ванные эритроциты не рассматривались для оценки среднего радиуса агрегации кластеров.
Среднее число частиц, связанных с кластером, лежало в диапазоне от 7 до 61 и очень мало эритроцитов (< 4 %) ячеек не были частью агрегатов. Минимальное значение среднего радиуса вращения кластеров оценивалось в 5.51 мкм, а наивысшего агрегата — 16.06 мкм.
МОДЕЛИРОВАНИЕ
Предполагалось, что клетки были в сходных биофизических и биохимических условиях, которые в свою очередь позволили считать числовые значения физических параметров ( β , Сp и µ ) одинаковыми для всех ячеек, поэтому эти параметры ( β , Сp , µ и F ) считались константами [8].
Эритроциты находились в интересующей области 100 × 100 мкм для создания условия агрегации при моделировании реализаций двумерной ткани. Для каждого испытания было смоделировано 200 случаев ткани, представляющих возможные конфигурации тканей, и вычислены с помощью уравнения (3). Интеграл в (3) в каждой временнόй точке оценивали численно с использованием метода трапеций, и рассчитанное давление ОАС было комплексным количеством. Кривая ОАС была получена из реальных частей данных временнόго ряда давления ОАС, а огибающая сигнала была определена из соответствующих величин.
В Приложении на рис. 1–3 представлена пространственная расчетная модель структур из сферических отражателей (эритроцитов), порождающих оптоакустический сигнал при облучении лазером Nd: YAG [10–13]. Модель была простроена и рассчитана в программе Matlab.
ЗАКЛЮЧЕНИЕ
Представленная модель использовалась для изучения того, как амплитуда ОА сигнала и спектр мощности будут изменяться в зависимости от уровня агрегации эритроцитов. Было отмечено, что амплитуда ОА сигнала возрастает с увеличением уровня агрегации и уменьшается частота сигнала с увеличением размеров агрегата. Рассчитанная модель позволяет сделать вывод о возможности регистрации уровня агрегации эритроцитов в крови с помощью оптоакустического эффекта, возникающего в результате воздействия лазерного излучения с длинной волны 1064 нм на модельные образцы клеток. Тем не менее в разработанной модели пока не учитывался ряд факторов, таких как эффекты потока, ширина полосы ультразвукового приемного преобразователя и т. д., которые могут влиять на чувствительность предлагаемой модели. После уточнения всех этих факторов модель может быть скорректирована для измерения уровней агрегации эритроцитов, связанных с широким спектром патологий. Полученные результаты дополняют математическую модель рассчитанную ранее в [3, 13, 14] для неагрегированных эритроцитов.
ПРИЛОЖЕНИЕ
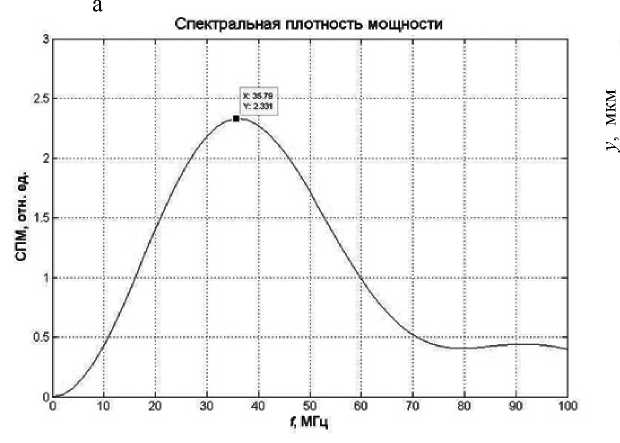
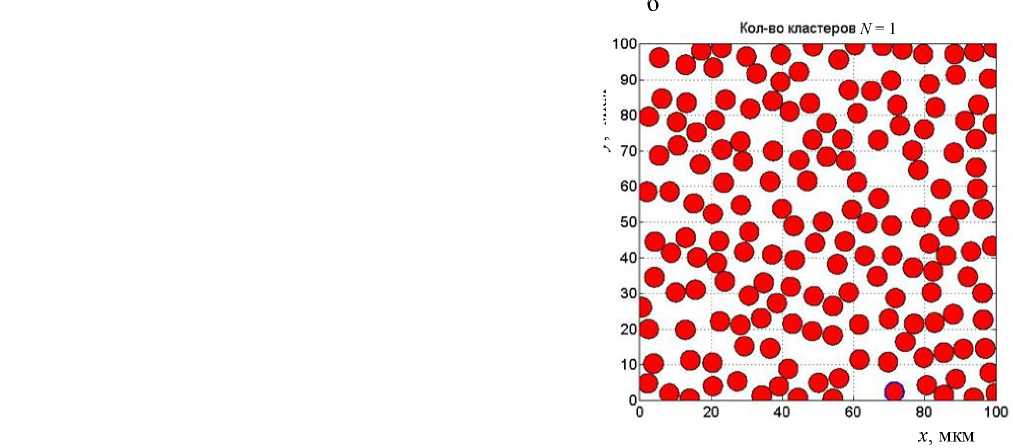
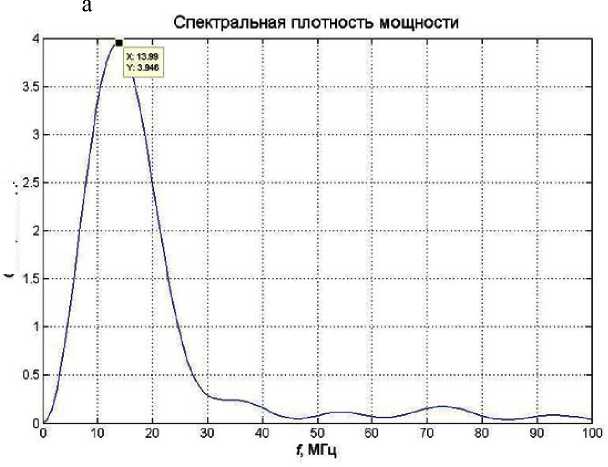
Рис. 1. Спектральная плотность мощности ОАС неагрегированных эритроцитов (а) и двумерная реализация образца ткани (б).
Количество неагрегированных эритроцитов 168
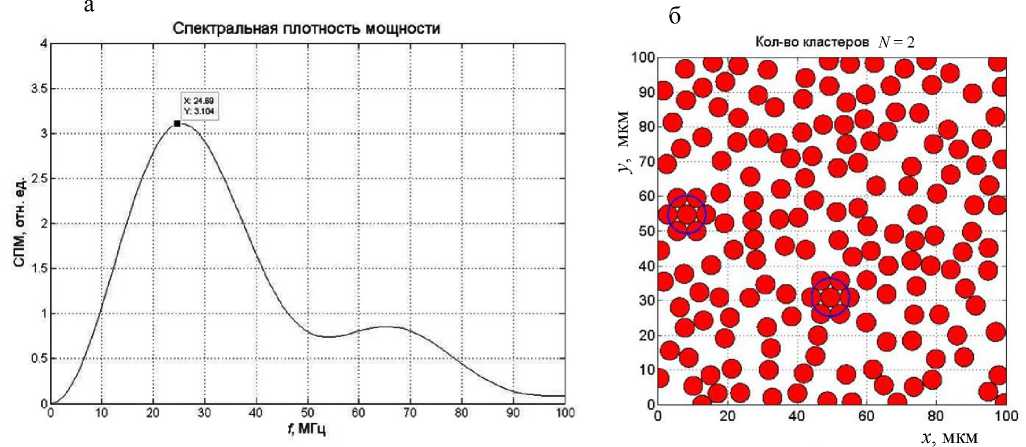
Рис. 2. Спектральная плотность мощности ОАС агрегированных эритроцитов (а) и двумерная реализация образца ткани (б).
Количество эритроцитов в кластере N = 7, радиус агрегата R g = 5.51 мкм. Неагрегированных эритроцитов 154. Процент агрегации 8.3 %
СПМ, отн. ед.
90 § И 80
^70
б
Кол-во кластеров N = 2
x , мкм
Рис. 3. Спектральная плотность мощности ОАС агрегированных эритроцитов (а) и двумерная реализация образца ткани (б).
Количество эритроцитов в кластере N = 61, радиус агрегата R g = 16.06 мкм. Неагрегированных эритроцитов 47. Процент агрегации 73 %
Список литературы Математическое моделирование оптоакустического сигнала от агрегированных эритроцитов для оценки уровня агрегации
- Кравчук Д.А., Старченко И.Б. Математическое моделирование оптикоакустического сигнала от сферических поглотителей на примере эритроцитов//Известия Юго-Западного государственного университета. Серия: Управление, вычислительная техника, информатика. Медицинское приборостроение. 2017. Т. 7, № 3. C. 101-107.
- Старченко И.Б., Кравчук Д.А., Кириченко И.А. Прототип оптоакустического лазерного цитомера//Медицинская техника. 2017. № 5. C. 4-7.
- Кравчук Д.А. Система проточной лазерной диагностики жидкостей при генерации оптоакустического сигнала на рассеивателях сферической формы//Качество и жизнь. Москва, 2017. № 4. C. 74-78.
- Кравчук Д.А. О методе моделирования оптоакустических сигналов от источников сферической формы на примере эритроцитов//Качество и жизнь. Москва, 2017. № 4. C. 78-80.
- Savery D., Cloutier G. Effects of red cell clustering and anisotropy on ultrasound blood backscatter: a Monte Carlo study//IEEE Trans. Ultrason. Ferroelectr. Freq. Control. 2005. Vol. 52, no. 1. P. 94-103 DOI: 10.1109/TUFFC.2005.1397353
- Zhang H.F., Maslov K., Sivaramakrishnan M., Stoica G., Wang L.V. Imaging of hemoglobin oxygen saturation variations in single vessels in vivo using photoacoustic microscopy//Appl. Phys. Lett. 2007. Vol. 90, no. 5 DOI: 10.1063/1.2435697
- Diebold G.J. Photoacoustic monopole radiation: Waves from objects with symmetry in one, two and three dimensions//Photoacousti'c Imaging and Spectroscopy/L.V. Wong (ed.). Taylor & Francis Group, LLC, London, 2009. P. 3-17.
- Saha R.K., Kolios M.C. A simulation study on photoacoustic signals from red blood cells//The Journal of the Acoustical Society of America. 2011. Vol. 129, no. 5 DOI: 10.1121/1.3570946
- Meiselman H.J. Red blood cell aggregation: 45 years being curious//Biorheology. 2009. Vol. 46, no. 1. P. 1-19 DOI: 10.3233/BIR-2009-0522
- Кравчук Д.А. Экспериментальные исследования и моделирование процесса генерации оптоакустических волн//Электронный научный журнал "Инженерный вестник Дона". 2017. Т. 45, № 2. URL: http://www.ivdon.ru/ru/magazine/archive/n2y2017/4234.
- Кравчук Д.А. Теоретические исследования генерации оптоакустических волн в жидкости цилиндрическими поглотителями//Электронный научный журнал "Инженерный вестник Дона". 2017. Т. 46, № 3. URL: http://www.ivdon.ru/ru/magazine/archive/N3y2017/4350. ISSN 2073-8633.
- Кравчук Д.А. Аналитический результат генерации оптоакустических волн для сферических поглотителей в дальнем поле//Электронный научный журнал "Инженерный вестник Дона". 2017. Т. 47, № 4. URL: http://www.ivdon.ru/ru/magazine/archive/n4y2017/4436.
- Starchenko I.B., Kravchuk D.A., Kirichenko I.A. An optoacoustic laser cytometer prototype//Biomedical Engineering. Springer, 2018. Vol. 51, no. 5. P. 308-312.
- Кравчук Д.А. Применение оптоакустических методов в биомедицинских исследованиях//Электронный научный журнал "Инженерный вестник Дона". 2017. № 4. URL: http://www.ivdon.ru/ru/magazine/archive/n4y2017/4484.


