Механизмы нарушения функции эндотелия и внутренних органов на фоне экспозиции хлоридом кобальта (экспериментальное исследование)
Автор: Гиголаева Л.В., Тибилов А.Г.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Экспериментальные модели и инструментальные исследования для оценки риска в гигиене и эпидемиологии
Статья в выпуске: 3 (15), 2016 года.
Бесплатный доступ
Поступление кобальта в организм человека является фактором риска развития легочных и сердечно-сосудистых нарушений здоровья. В данной работе отражены результаты исследований функциональных и биохимических механизмов развития эндотелиальной дисфункции и патологии внутренних органов при кобальтовой интоксикации в эксперименте. Выявлен системно-органный характер активации окислительных процессов по данным повышения вторичного продукта малонового диальдегида в эритроцитах и гомогенатах внутренних органов, а также участие дисбаланса антиокислительной системы в развитии липопероксидации, изучены особенности нарушения NO-образующей функции эндотелия и участие в этом процессе L-аргинина и аналога эндогенного ингибитора экспрессии eNOS -L-NC-аргинина, метилового эфира (L-NAMEилиL-nitro-arginin-methil-ester) при кобальтовой интоксикации в условиях активации окислительных процессов. Хроническая кобальтовая интоксикация у крыс приводит к активации окислительных процессов, при этом происходит угнетение активности супероксиддисмутазы, а концентрация каталазы и церулоплазмина повышается. Нарушаются обмен холестерина, продукция оксида азота и его биодоступность, что сопровождается изменением микроциркуляторной гемодинамики висцеральных органов. Проведена оценка функционального состояния внутренних органов по данным активности Na+,К+-АТФ-азы в гомогенатах, а также по активности органоспецифических и экскреторного ферментов в сыворотке крови на фоне кобальтовой интоксикации и выявлена роль изменений обмена холестерина как фактора риска атерогенеза в нарушении биодоступности оксида азота. Для патогенетической коррекции выявленных нарушений применен способ с использованием эндогенного антиоксиданта коэнзима Q10 и регуляторов экспрессии eNOS: L-аргинина, L-NAME, а также их комбинаций с коэнзимом Q10.
Атерогенез, оксид азота, перекисное окисление липидов, антиокислительная система, микроциркуляторная гемодинамика, хлорид кобальта, холестерин
Короткий адрес: https://sciup.org/14237963
IDR: 14237963 | УДК: 577.352.3
Mechanisms of endothelium and internal organs dysfunction associated with exposure to cobalt chloride (experimental study)
Cobalt administration in the human body is a risk factor for developing pulmonary and cardiovascular health problems. In this paper we report the results of functional studies and biochemical mechanisms of endothelial dysfunction and pathology of internal organs in cobalt intoxication in experiment. System-organ nature of the activation of oxidative processes is identified according to the increase of MDA secondary product in erythrocytes and homogenates of internal organs as well as the participation of AOC imbalance in the development of lipid peroxidation, the peculiarities of the violations of NO release endothelial function and participation in this process of L-arginine and an analogue of endogenous inhibitor of expression eNOS -L-NC - arginine methyl ester (L-NAME or L-nitro-arginine-methil-ester) with cobalt intoxication in conditions of activation of oxidative processes. Chronic cobalt intoxication in rats leads to the activation of oxidative processes, thus there is inhibition of superoxide dismutase activity and the concentration of catalase and ceruloplasmin increased. Cholesterol metabolism is disturbed, as well as impaired nitric oxide production and its bioavailability, which is accompanied by the change of the microcirculatory hemodynamics of the visceral organs. The evaluation of the internal organs' functional state according to the activity of the Na+,K+-ATPase in homogenates is performed, as well as due to the activity of organ-specific and excretory enzymes in blood serum on the background of cobalt toxicity. The role of changes of cholesterol metabolism is established - as a risk factor of atherogenesis in violation of the bioavailability of nitric oxide. For the pathogenetic correction of violations we applied the method using the endogenous antioxidant coenzyme Q10 and regulators of the expression eNOS L-arginine, L-NAME and their combination with coenzyme Q10.
Текст научной статьи Механизмы нарушения функции эндотелия и внутренних органов на фоне экспозиции хлоридом кобальта (экспериментальное исследование)
кантом являются предприятия цветной металлургии.
Токсичность высоких концентраций кобальта обусловлена его гипоксическим действием, активацией перекисного окисления липидов (ПОЛ) и истощением антиоксидантной защиты (АОЗ) [1, 2, 7, 8]. Избыточное поступление в организм кобальта индуцирует перекисное окисление липидов и способствует формированию окислительного стресса, сопровождающегося дисфункцией эндотелия, повреждением биологических макромолекул, мембранных структур клеток и ферментов [8, 17]. Принимая на себя действие солей тяжелых цветных металлов, эндотелий становится прямой мишенью для повреждения, и эндотелиальная дисфункция играет патогенетическую роль в повреждении мембран клеток внутренних органов в условиях окислительного стресса. В механизме развития эндотелиальной дисфункции в условиях активации окислительных процессов играет роль снижение продукции оксида азота – основного вазодилатирующего фактора и его биодоступность [2, 6, 8, 14–16]. В нарушении транспорта NO в гладкомышечную клетку сосуда может быть значимо изменение метаболизма холестерина как фактора риска атерогенеза [6].
Исследованиями Peters K. et al. [16] показано, что двухвалентные ионы кобальта (Co2+) индуцируют экспрессию генов, реагирующих с гипоксией. В силу этого соединения кобальта используются даже для имитации гипоксии [11]. В свою очередь дисбаланс в оксидантно-антиоксидантной системе является существенным фактором риска развития патологии легочных структур, к примеру, бронхолегочной дисплазии [2].
Высокие дозы кобальта, попадающие в организм через дыхательные пути на вредных производствах, приводят к повышению содержания в крови холестерина, бета-липопротеидов, общих липидов и снижению лецитин-холестеринового коэффициента [17].
Вместе с тем в литературе весьма недостаточно представлены данные о влиянии окислительных процессов на метаболизм оксида азота как фактора риска развития сосудистых осложнений на фоне кобальтовой интоксикации, патогенетическим звеном которых становится нарушение функции эндотелия. В механизмах развития дисфункции эндотелия несомненную роль играет изменение метаболизма оксида азота – важного вазодилатирующего фактора. Изучение причинно-следственных связей акти- вации окислительных процессов метаболизма оксида азота при сосудистых осложнениях и разработке способов патогенетической коррекции – актуальная научная задача.
Учитывая вышеизложенное, цель исследования определяли как изучение влияния хлорида кобальта на биохимические показатели дисфункции эндотелия у крыс в эксперименте с кобальтовой интоксикацией.
Материалы и методы. Исследования проводились на 275 крысах-самцах линии «Вис-тар» одной возрастной группы (10–14 мес.), массой 175–220 г. Подопытные крысы были разбиты на 10 групп по 15–20 голов. Содержание животных и проведение экспериментов осуществляли в полном соответствии с «Правилами проведения работ с использованием экспериментальных животных» (Минобразования СССР, 1984), а также принципами Хельсинкской декларации (2000) и международными рекомендациями (этический кодекс) по проведению медико-биологических исследований с использованием животных (Совет международных научных организаций, 1985) В контрольную группу 1 входили интактные животные (n = 22), по возрасту и массе сопоставимые с основной группой, 55 голов составляли резервную группу. Кобальтовую интоксикацию у крыс опытных групп моделировали введением хлорида кобальта в дозе 6 мг/кг массы животного (исходя из DL50). Данная доза была оптимальной (подбирали по степени убывания), так как не влекла за собой гибели животного и в то же время вызывала соответствующие изменения со стороны изучаемых процессов. Развитие токсических влияний прослеживали в течение 30 дней. Во время эксперимента крысы находились на стандартном пищевом рационе и имели свободный доступ к питьевой воде, световой режим – естественный.
В эксперименте исследовались следующие показатели: интенсивность ПОЛ в мембранах эритроцитов по данным изменения концентрации малонового диальдегида (МДА) колориметрическим методом с тиобарбитуровой кислотой [1]; состояние антиокислительной системы (АОС) оценивали по активности каталазы [4] и супероксиддисмутазы (СОД) по методу аутоокисления адреналина, концентрацию церулоплазмина (ЦП) в сыворотке крови – по методу Равина [3]. О нарушении обмена холестерина судили по концентрации общего холестерина (ОХС) в сыворотке крови и его содержа- нии в липопротеидах низкой плотности (ЛНП) и липопротеидах высокой плотности (ЛВП). Концентрацию суммарных метаболитов NOХ определяли по реакции диазотирования Грисса [2].
Результаты и их обсуждение. У экспериментальных крыс на фоне длительной кобальтовой интоксикации, вызванной парентеральным введением хлорида кобальта, развиваются системные окислительные процессы. Зарегистрировано повышение концентрации МДА не только в эритроцитах, но и в гомогенатах почечной ткани: в корковом слое – на 212 %, в мозговом слое – на 92 % (при р <0,001); печеночной ткани – на 48,3 % и миокардиальной ткани – на 52,1 % (при р <0,001). Изучение корреляционных взаимосвязей между содержанием кобальта в плазме крови и активностью ПОЛ в эритроцитах выявило прямую корреляцию между этими показателями при затравке хлоридом кобальта в течение месяца. Анализ активности ферментов АОС показал достоверное ( р <0,001) снижение активности СОД в сыворотке крови и эритроцитах (на 27,7 %), повышение активности каталазы (на 64,1 %) и концентрации церулоплазмина (на 11,9 %), что следует рассматривать как возможное проявление клеточной компенсаторной реакции.
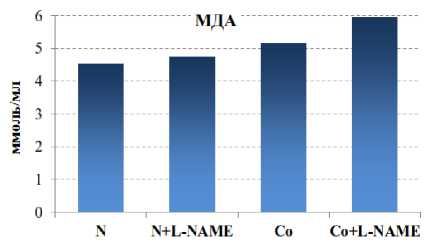
При интоксикации хлоридом кобальта у крыс на фоне активации окислительных процессов выявлено снижение концентрации суммарных метаболитов NO на 19,7 % ( р <0,001) и повышение при этом концентрации МДА – продукта ПОЛ – на 10,9 % (рис. 1). Для подтверждения роли этих химических факторов проведен корреляционный анализ, который показал наличие отрицательной сильной связи между повышением МДА в крови и снижением концентрации суммарных метаболитов NO ( r = –0,72).
В цепи механизмов, ведущих к развитию дефицита NO и дисфункции эндотелия, ключевым звеном является концентрация L-аргинина [10]. Для выяснения роли доступности субстрата L-аргинина для фермента NO-синтазы в специальной серии экспериментов вводили ежедневно в течение 4 недель крысам с кобальтовой интоксикацией L-аргинин в дозе 10 мг/кг веса тела. По окончании эксперимента определяли в сыворотке крови концентрацию оксида азота и показатели активации окислительных процессов. Полученные результаты продемонстрировали повышение концентрации NO в крови на фоне введения L-аргинина крысам с длительной интоксикацией сравнительно с данными,
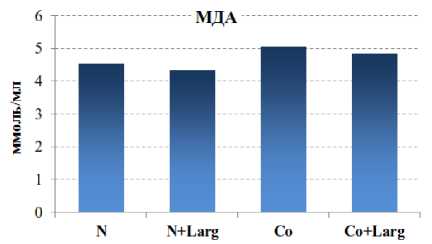
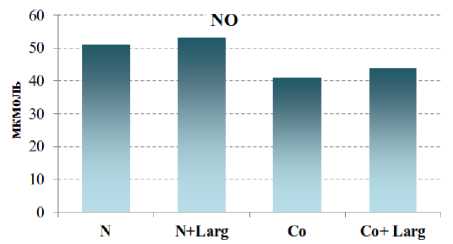
1 – контроль; 2 – N+L-аргинин;
3 – Со; 4 – Со+L-аргинин
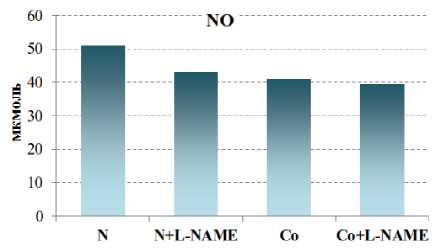
1 – контроль; 2 – N+L-NAME;
3 – Co; 4 – Co+L-NAME
б
а
Рис. 1. Изменения концентрации МДА и суммарных метаболитов NO на фоне донора NO-L-аргинина ( а ) и ингибитора eNOS – L-NAME при кобальтовой интоксикации ( б )
полученными только при кобальтовой интоксикации ( р <0,001). Введение L-аргинина крысам с длительной интоксикацией хлоридом кобальта вызвало уменьшение степени выраженности дисбаланса в системе «свободнорадикальное окисление (СРО) – АОЗ» и одновременно статистически достоверное повышение концентрации суммарных метаболитов NO в сыворотке крови. Введение же интактными затравленным крысам ингибитора еNOS–L-NAME показало, что содержание метаболитов ПОЛ возрастает, одновременно снижается концентрация суммарных метаболитов NO.
Выявленная активация СРО при введении интактным и особенно затравленным животным ингибитора еNOS – L-NAME может быть обусловлена так называемым «разобщением» ре-дуктазного и оксидазного доменов еNOS, когда фермент вместо NO продуцирует активные формы кислорода (АФК). Следовательно, в сыво- ротке крови концентрация NO может определяться содержанием субстрата синтеза L-аргинина, экспрессией эндотелиальной NO-синтазы, уровнем эндогенного ингибитора экспрессии еNOS и нарушением биодоступности NO.
Еще одним важным процессом, в определенной степени детерминирующим эффективность образования NO, является влияние окисленных ЛНП и лизофосфатидилхолина (продукта реакции, катализируемого фосфолипазой и ассоциированной с ЛНП) на транспорт L-аргинина в эндотелиальную клетку (ЭК) (рис. 2–4).
Анализ данных показал статистически достоверное повышение концентрации ОХС на 105,8 % ( р <0,001) в сыворотке крови у крыс с кобальтовой интоксикацией. Анализ распределения ХС в липопротеинах различной плотности показал снижение его уровня в ЛВП на 25,3 % и повышение в ЛНП на 186,3 %, т.е. в атерогенных ЛП-комплексах.
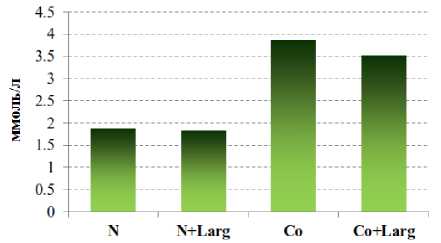
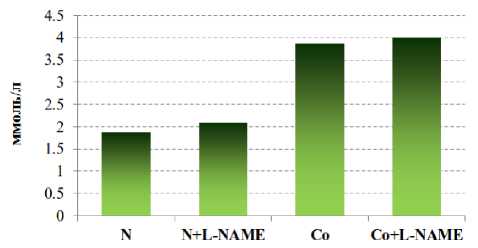
a б
Рис. 2. Изменение концентрации общего холестерина на фоне донора NO-L-аргинина ( а ) и ингибитора eNOS – L-NAME ( б ) при кобальтовой интоксикации (N – контроль)
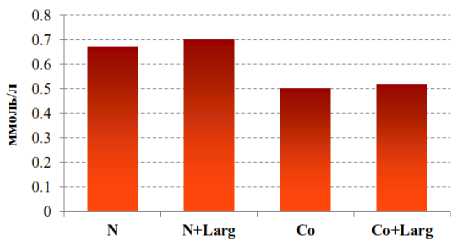
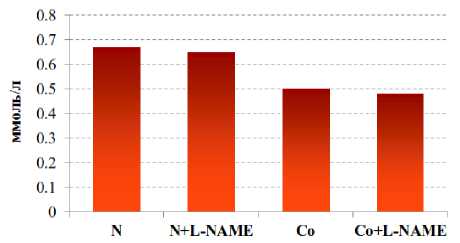
a б
Рис. 3. Изменение концентрации липопротеидов высокой плотности на фоне донора NO-L-аргинина ( а ) и ингибитора eNOS – L-NAME ( б ) при кобальтовой интоксикации (N – контроль)
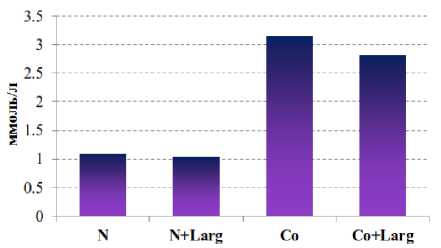
а
Рис. 4. Изменение концентрации липопротеидов низкой плотности на фоне донора NO-L-аргинина ( а ) и ингибитора eNOS – L-NAME ( б ) при кобальтовой интоксикации (N – контроль)
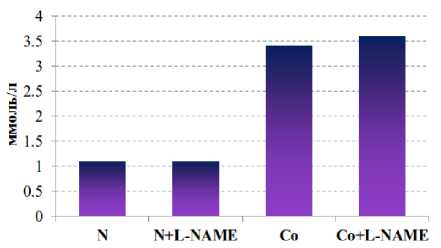
б
В стадии длительного воздействия хлоридом кобальта происходит гиперхолестеринемия и гипер-β-липопротеинемия, а это вследствие атерогенеза способствует повреждению эндотелия сосудов. Следует предположить, что в условиях повышенного содержания в крови реактивных форм кислорода, особенно радикала гидроксила ОН - - как наиболее реакционноспособного и вторичного продукта ПОЛ–МДА, происходит окислительная модификация ЛНП, включая пе-реокисление липидов и образование конъюгированных диенов, углеродная модификация (apо) β, а также энзиматическое превращение фосфолипазой фосфатидилхолина в лизофосфатидил-холин. Измененные, окисленные ЛНП (оЛНП) нарушают транспорт L-аргинина из сыворотки крови в ЭК, имеется и дефицит L-аргинина, субстрата синтеза NO, в результате снижается образование оксида азота и его биодоступность.
Исследовали показатели ПОЛ, активность мембранного фермента – Na,K-АТФ-азы, а также активность органоспецифических ферментов: АлАТ, АсАТ, ГГТП и экскреторного фермента – щелочной фосфатазы у крыс в длительной стадии кобальтовой интоксикации.
Полученные данные показали снижение активности Na,K-АТФ-азы в обоих слоях почечной ткани ( р <0,001), а также в печеночной и миокардиальной тканях. О повреждении кардиомиоцитов свидетельствует увеличение концентрации МДА в них, снижение активности Na,K-АТФ-азы, а также повышение в сыворотке крови АсАТ, являющейся наиболее органоспецифической для миокарда.
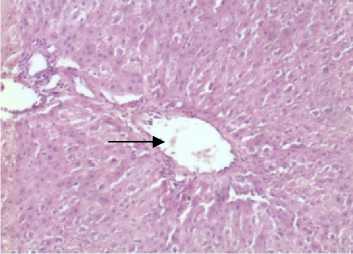
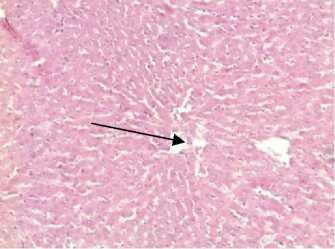
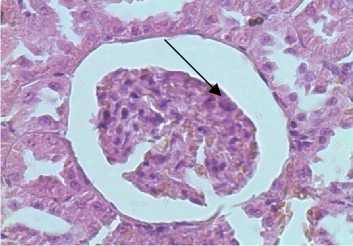
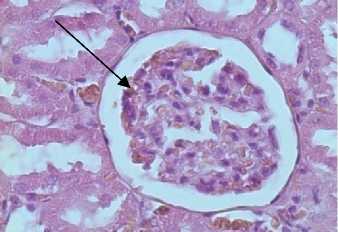
Токсические эффекты реализуются путем развития и прогрессирования эндотелиальной дисфункции и нарушением висцеральных органов: почек, печени, миокарда. Кобальтовая интоксикация вызывает, помимо функциональных изменений, нарушения морфологической структуры эндотелия сосудов и клеток внутренних органов. Полученные результаты были подтверждены гистологическими данными почечной, печеночной, миокардиальной тканей и эндотелия сосудов микроциркуляторного русла (рис. 5).
На срезах тканей внутренних органов у крыс с кобальтовой интоксикацией на фоне L-аргинина отмечались: частичная фрагментация кардиомиоцитов; умеренная паренхиматозно-белковая дистрофия и частичное исчезновение гликогена в гепатоцитах; умеренная гиалиновокапельная дистрофия канальцев и расширение мочевых пространств; умеренное утолщение сосудов микроциркуляторного русла.
На срезах тканей крыс с кобальтовой интоксикацией на фоне L-NAME (на рис. 5 фотографии справа) изменения более выражены. Отмечается: фрагментация и распад кардиомиоцитов, исчезновение поперечной исчерченности в большинстве кардиомиоцитов; расширение мочевых пространств, полнокровие клубочков, выраженная гиалиново-капельная дистрофия мочевых канальцев; выраженная паренхиматозно-белковая дистрофия печеночной ткани, умеренная жировая дистрофия (капли в виде прозрачных включений); умеренное утолщение эндотелия сосудистой стенки, неравномерность (шероховатость) сосудистой стенки.
Для коррекции выявленных нарушений, мы использовали коэнзим Q 10 и его комбинацию с L-аргинином и L-NAME. Исследование влияния коэнзима Q 10 и его комбинации с L-аргинином на состояние ПОЛ выявили существенное угнетение ПОЛ – статистически достоверное снижение концентрации МДА ( р <0,001) в крови на фоне коэнзима Q10 и его комбинации с L-аргинином. В другом варианте исследований на фоне L-NAME – ингибитора фермента
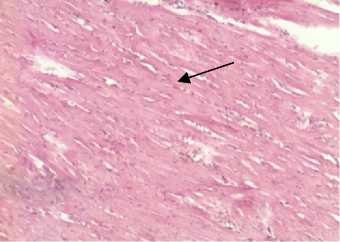
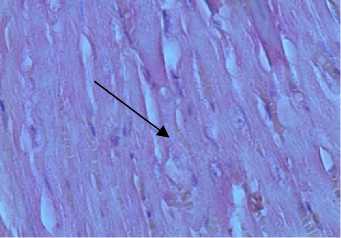
а
б
в
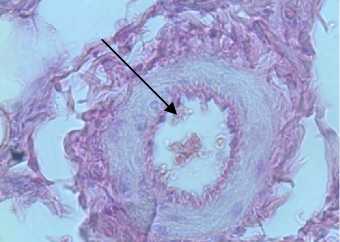
Рис. 5. Изменения морфологической структуры тканей внутренних органов и эндотелия сосудов микроциркуляторного русла у крыс с кобальтовой интоксикацией на фоне L-аргинина (слева) и на фоне ингибитора eNOS - L-NAME (справа) (окраска - гематоксилином и эозином, ув. х 400): а – миокардиальная ткань; б – печеночная ткань; в – почечная ткань; г – эндотелий сосудов микроциркуляторного русла
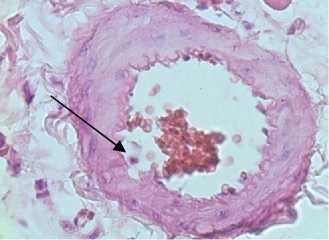
г
еNOS, эндогенный антиоксидант вызвал менее значимое угнетение интенсивности ПОЛ и снижение концентрации МДА в эритроцитах. При сравнительном анализе результатов ингибирования ПОЛ наиболее эффективным является коэнзим Q10 и его комплекс с L-аргинином.
Выводы. На фоне длительной индуцированной кобальтовой интоксикации активируются окислительные процессы. Повышается концентрация МДА в эритроцитах, в печеночной и миокардиальной тканях, гомогенатах коркового и мозгового вещества почек. В антиокисли-тельной системе отмечается дисбаланс, характеризующийся снижением активности суперокси-ддисмутазы в эритроцитах и компенсаторным повышением активности каталазы и концентра- ции церулоплазмина в сыворотке крови. Активация окислительных процессов сопровождается снижением концентрации суммарных метаболитов NO вследствие дефицита субстрата синтеза L-аргинина и повышения в крови ингибитора экспрессии eNOS-АДМА, установленные исследованиями на фоне введения аналога эндогенного ингибитора L-NAME.
Отмечается снижение активности Na,K-АТФ-азы в гомогенатах почечной, печеночной и миокардиальной тканях, а также повышение активности в сыворотке крови следующих ферментов: трансаминаз – АлАт, АсАт, а также ГГТП и щелочной фосфатазы, что свидетельствует о нарушении гидрофобности цитоплазматических мембран клеток и повышении их проницаемости.
Список литературы Механизмы нарушения функции эндотелия и внутренних органов на фоне экспозиции хлоридом кобальта (экспериментальное исследование)
- Бондаренко Л.В. Генетическая токсикология//Экологическая генетика. -2007. -Т. 5, № 1. -С. 39-41.
- Горюнов И.А., Джиоев И.Г. Особенности состояния перекисного окисления липидов и антиоксидантной активности при респираторном дистресс-синдроме у новорожденных//Вестник Международной академии наук экологии и безопасности жизнедеятельности. -2009. -Том 14, № 5. -С. 208-211.
- Камышников В.С. Определение содержания (активности) церулоплазмина//Справочник по клинико-биохимической лабораторной диагностике. -Минск, 2003. -Т. 2. -С. 71-79.
- Метод определения каталазы/М.А. Королюк, Л.И. Иванова, И.Г. Майорова, В.Ц. Токарев//Лабораторное дело. -1988. -№ 1. -С. 16-19.
- Oксид aзота: рoль в рeгуляции биoлoгичeских функций, мeтoдыoпрeдeлeния в крoви чeлoвека/В.А. Мeтeльскaя, Н.Г. Гумaнoва, Н.В. Перова, Р.Г. Оганов//Лабoрaтoрная мeдицинa. -2005. -№ 7. -С. 19-24.
- О санитарно-эпидемиологической обстановке в Республике Северная Осетия-Алания в 2014 г. . -Владикавказ, 2015. -URL: http://15rospotrebnadzor.ru/upload/document/1375867985.pdf (дата обращения: 15.06.2016).
- Отиев М.А., Дзугкоев С.Г., Можаева И.В. Биохимические маркеры дисфункции эндотелия на фоне экспозиции хлоридом кобальта в эксперименте у крыс//Здоровье и образование в ХХI веке. -2017. -Т. 17, № 3. -С. 67-71.
- Системный окислительный стресс и биохимические маркеры повреждения внутренних органов/С.Г. Дзугкоев, И.В. Можаева, Л.В. Гиголаева, Е.А. Такоева, Ф.С. Дзугкоева, О.И. Маргиева//Фундаментальные исследования. -2014. -№ 7. -С. 478-481.
- Аsakаwа T., Mаtsushitа S. Cоlоring cоnditiоns of thiоbarbituric аcid tеst, fоr dеtеcting lipidhyd11rоperоxides//Lipids. -1980. -Vol. 15. -P. 137-140.
- Böger R.H., Bode-Böger S.M. The clinical pharmacology of L-arginine//Annu. Rev. Pharmacol. Toxicol. -2001. -Vol. 41. -P. 79-99.
- Cobalt chloride-induced signaling in endothelium leading to the augmented adherence of sickle red blood cells and transendothelial migration of monocyte-like HL-60 cells is blocked by PAF-receptor antagonist/C. Sultana, Y. Shen, C. Johnson, V.K. Kalra//J. Cell. Physiol. -1999. -Vol. 179. -P. 67-78.
- Heavy metal ion induction of adhesion molecules and cytokines in human endothelial cells/M. Wagner, C.L. Klein, H. Kleinert, C. Euchenhofer, U. Forstermann, C.J. Kirkpatrick//The role of NF-kappaB, I kappaB-alpha and AP-1. Pathobiology. -1997. -Vol. 65. -P. 241-252.
- In vivo study of the effect of systemic hypoxia on leukocyte-endothelium interactions/N. Baudry, G. Danialou, J. Boczkowski, E. Vicaut//Am. J. Respir. Crit. Care. Med. -1998. -Vol. 158. -P. 477-483.
- Krantz S.B. Erythropoietin//Blood. -1991. -Vol. 77. -P. 419-434.
- Miranda K.M., Espey M.G., Wink D. A rapid, simple spectrophotometric method for simultaneous detection of nitrate and nitrite//Nitrtic Oxide: Biol & Chem. -2001. -№ 5. -P. 62-71.
- Paradoxical effects of hypoxia-mimicking divalent cobalt ions in human endothelial cells in vitro/K. Peters, H. Schmidt, R.E. Unger, G. Kamp, F. Pröls, B.J. Berger, C. Kirkpatrick//Molecular and Cellular Biochemistry. -2005. -Vol. 270, № 1. -Р. 157-166.
- Van Hinsbergh V.W. Regulatory functions of the coronary endothelium//Mol. Cell. Biochem. -1992. -Vol. 116. -P. 163-169


