Механизмы влияния экотоксикантов на здоровье населения города Владикавказа
Автор: Дзугкоева Ф.С., Хетагурова Л.Г., Дзугкоев С.Г., Чопикашвили Л.В., Такоева Е.А., Битарова Ж.Р., Тедтоева А.И., Касохов А.Б.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Ликвидация последствий антропогенного загрязнения
Статья в выпуске: 1-8 т.12, 2010 года.
Бесплатный доступ
Экотоксиканты - соли тяжелых металлов, содержание которых превышает ПДК в атмосфере г. Владикавказа, оказывают мембрано- и ферментотоксическое действие, вызывают функциональные изменения в нефроне и периферической сосудистой системе, активацию перекисного окисления липидов (ПОЛ) в условиях эксперимента. В районах г. Владикавказа загрязнение металлопо- лютантами повышает заболеваемость бронхиальной астмой у детей и является причиной хромосомных аберраций, свидетельствующих о их генотоксических нарушениях. В механизме развития приступов бронхиальной астмы участвуют провоспалительные цитокины (ИЛ-4; ИЛ-8; Фно-ά), содержание которых повышается, и изменяется концентрация противовоспалительных (повышается Инф- и снижается ИЛ-10).
Перекисное окисление липидов, гемодинамика, антиокислительная защита, хромосомные аберрации, соли тяжелых металлов, цитокины
Короткий адрес: https://sciup.org/148199198
IDR: 148199198 | УДК: 577.352.3
Mechanisms of ecotoxicants influence on health of the population in Vladikavkaz city
Ecotoxicants - salts of heavy metals which contents in Vladikavkaz atmosphere exceeds maximum per-missible concentration, render membrane and enzyme-toxical action, cause functional changes in a nephron and peripheric vascular system, activation of peroxide oxidations of lipids (POL) in conditions of experiment. In Vladikavkaz districts metals pollution increases a case rate of bronchial asthma at chil-dren and is the reason of chromosomal aberrations testifying about their genetoxical disturbances. Proin-flammatory cytokines participate in the mechanism of development of bronchial asthma attacks (IL-4; IL-8; FNO-a) which contents increases, and concentration of antiinflammatory cytokines increase and IL-10 decrease.
Текст научной статьи Механизмы влияния экотоксикантов на здоровье населения города Владикавказа
Битарова Жанна Руслановна, аспирантка Тедтоева Анжелика Ираклиевна, аспирантка Касохов Анатолий Борисович, доктор медицинских наук, заведующий отделом лаборатории детской патологии атмосферы оказывают воздействие на человека в виде аэрозолей, образующиеся вследствие конденсации и окисления на воздухе, оседают на волосах, коже и всасываются в кровь. Другим путем их поступления в организм является дыхательная система и желудочно-кишечный тракт. Благодаря липофильности эти соли легко всасываются через клеточные мембраны, взаимодействуют с сульфидными группами белков мембран и субклеточных органелл, что определяет их стойкость и способность к накоплению, т.е. кумуляции в клетках органов в больших концентрациях. Основными токсикантами являются Ni, Co, Cd и др., способные вызывать токсические эффекты при относительно низких уровнях воздействия, которые раньше считались безопасными. Проникая в кровеносную систему, поражают практически все висцеральные системы, в том числе и почки, как основной экскреторный орган; при этом оказывают прямое воздействие на эндотелиальные и мезангиальные клетки, тубулярный эпителий, базальные мембраны как гло-мерул, так и канальцев. Проявляют мембрано-, ферментотоксичность и генотоксичность, в динамике воздействия могут вызывать функциональные и морфологические изменения, приводящие к нефропатии и почечной недостаточности, вызывают приступы бронхиальной астмы, нарушения со стороны сердечнососудистой, иммунобиологической и эндокринной систем. Особенно чувствительна к их влиянию детская популяция нашего населения.
Цель исследования: изучение медикобиологических аспектов влияния солей тяжелых цветных металлов и разработка методологии их коррекции.
Соли тяжелых цветных металлов как ионы с переменной валентностью генерируют активные метаболиты кислорода: О 2 –, ОН–, Н 2 О 2 , О 2 2, индуцируя ПОЛ. Существует ряд источников супероксид анион-радикала О 2 –: митохондрии, мембраны ЭПР, фагоциты, но основной путь их образования – утечка О 2 – из дыхательной цепи на уровне коэнзима Q. Одноэлектронное восстановление О 2 является результатом ответвления от основного пути переноса электронов по дыхательной цепи, происходящее на уровне коэнзима Q, цитохрома С, а также при микросомальном окислении токсических веществ с участием НАДФ-зависимых оксидаз и цитохрома Р450. Эти радикалы и продукты ПОЛ атакуют структуры клеточной мембраны, митохондрии, ядро. Основной точкой приложения их негативного влияния являются ПНЖК фосфолипидов биологических мембран, они подвергаются пере-окислению, что приводит к нарушению физико-химической структуры мембран, вплоть до полного разрыва.
Материалы и методы. Эксперименты проведены на 350 крысах-самцах линии Вис-тар с хронической интоксикацией солями тяжелыми металлами: хлоридом никеля, кобальта и сульфатом кадмия. Определенная серия исследований проведена на взрослом и детском населении, проживающем в экологически неблагополучных районах г. Владикавказа. У детей, страдающих бронхиальной астмой, исследовали содержание цитокинов: провоспа-лительных и противовоспалительных. У взрослых исследовали генетические повреждения по данным хромосомных аберраций. Исследовали основные процессы мочеобразо-вания: скорость клубочковой фильтрации по клиренсу эндогенного Cr, рассчитывали канальцевую RH2O, используя формулы Ю.В. На-точина (1974). Для анализа электролитовыделительной функции почек определяли экскрецию Na и K с мочой, их концентрацию в крови, Фз ионов, рассчитывали канальцевую RNa в %. Изучали активность Na,K,АТФ-азы в корковом и мозговом слоях почечной ткани по приросту неорганического фосфора в среде инкубации по методу Scou ТС (1957). Для выяснения патогенетического механизма нарушений исследовали интенсивность ПОЛ в мембранах эритроцитов и в гомогенатах коркового и мозгового слоев почечной ткани по данным изменения концентрации малонового диальдегида (МДА), который определяемого методом Аsakаwa T., (1980). О состоянии ан-тиокислительной защиты судили по активности СОД методом аутоокисления адреналина и каталазы в сыворотке крови, определяемую методом М.А. Королюка и соав., (1988). Влияние никелевой интоксикации на различные звенья сосудистой системы: магистральные сосуды и микроциркуляторное звено – изучали в 6 точках локации. Кровоток регистрировали ультразвуковым портативным допплерогра-фом ММ-Д-Ф фирмы «МИНИМАКС» на наркотизированных интактных животных и крысах с никелевой интоксикацией. Использовали датчик с частотой 10 МГц. Для каждой зоны локации прибор регистрировал основные параметры кровотока: среднюю (М), систолическую (S) и диастолическую (D) скорости кровотока, пульсовой индекс (Pi), градиент давления (GD). Результаты всех серий опытов обработаны статистически с применением t-критерия Стьюдента с использованием программы Microsoft Excel, проводили корреляционный анализ.
Результаты и их обсуждение. Анализ наших данных показал, что на фоне экспозиции тяжелыми цветными металлами действительно отмечается активация процессов свободно-радикального окисления в клетках крови – эритроцитах. Сравнительный анализ данных полученных при интоксикации различной длительности показал, что интенсивность процессов СРО нарастает, в соответствии со сроками влияния.
Изменения носят системно-органный характер, и соответственно происходит интенсификация процесса СРО не только в крови, но и в почечной ткани – основного пути экскреции ксенобиотиков. В гомогенатах коркового и мозгового вещества повышается концентрация МДА, свидетельствующая об интенсификации СРО на фоне Cd , Co и Ni. Хроническая интоксикация этими солями в течение месяца выявила равнозначные показатели ПОЛ в корковом и мозговом веществе почечной ткани под влиянием Ni и Co, и менее выраженные на фоне экспозиции сульфатом кадмия.
Активность ферментов АОЗ – суперок-сиддисмутазы снизилась, хотя возросла активность каталазы в сыворотке крови компенсаторно, причем изменения имеют однонаправленный характер как при введении сульфата кадмия, хлорида кобальта, так и при никелевой интоксикации.
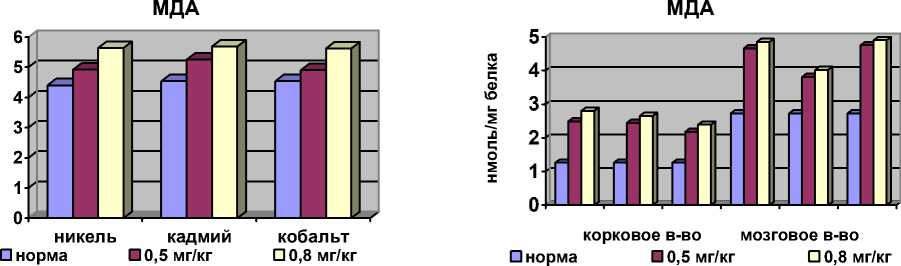
Рис. 1. Концентрация МДА в эритроцитах и в гомогенатах коркового и мозгового слоев почечной ткани на фоне введения хлорида никеля, сульфата кадмия и хлорида кобальта
СОД
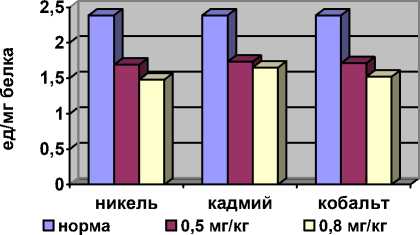
КАТАЛАЗА
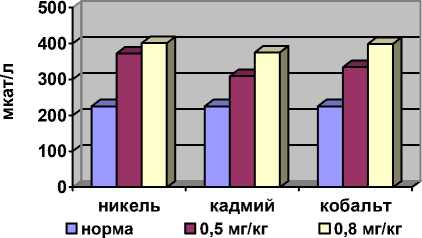
Рис. 2. Состояние антиокислительной системы на фоне интоксикации солями тяжелых и цветных металлов
Образовавшиеся метаболиты ПОЛ, МДА изменяют физико-химические и функциональные свойства биологических мембран, что проявляется в следующих нарушениях:
-
- окислительная модификация SH-NH 2 –групп белков: структурных, транспортных, ферментов в частности ФЛ А 2 ;
-
- окисление ферментов ЦТК, поставляющие восстановленные эквиваленты в дыхательную цепь;
-
- повышение проницаемости липидного бислоя: появление в гидрофобной области гидроксилов и полярных продуктов ПОЛ ПНЖК приводит к образованию водных пор, нарушению стабильности мембраны, вплоть до ее полного разрыва;
-
- увеличение протонной проводимости: разобщение процессов биологического окисления и окислительного фосфорилирования и потеря способности аккумулировать АТФ;
-
- нарушение синтеза АТФ – уменьшение соотношения АТФ/АДФ;
-
- набухание митохондрий;
-
- снижение активности мембранных ферментов.
Примером изменения активности мембраносвязанных ферментов является, в частности, Na-транспортирующий энзим. Анализ данных активности Na+,K+-АТФ-азы как в мозговом, так и в корковом слоях почечной ткани показал, что угнетается его активность, как в мозговом, так и корковом слоях почечной ткани на фоне интоксикации солями тяжелых цветных металлов.
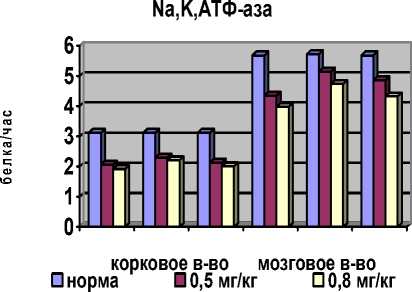
Рис. 3. Показатели активности Na+,K+-АТФ-азы в гомогенатах коркового и мозгового слоев почечной ткани на фоне интоксикации солями тяжелых и цветных металлов
На фоне оксидативного стресса изменяется функциональное состояние почек, выражающееся в снижении СКФ и уровня каналь- цевой реабсорбции воды и изменении объема диуреза. Одновременно нарушается и электролито-выделительная функция, данные свидетельствуют о достоверном повышении экскреции натрия и калия с мочой на фоне всех ис- следуемых солей тяжелых цветных металлов, вследствие снижения уровня канальцевой реабсорбции иона, на фоне снижения фильтрационного заряда натрия. Одновременно снижается и фильтрационный заряд калия.
Таблица №1.
Изменения функционального состояния почек и гемодинамики на фоне хронической интоксикации солями тяжелых металлов (M±m Показатели контроль Ni контроль Cd диурез, мл/час/100 г 0,091±0,003 0,060±0,0071111) 0,091±0,003 0,132±0,0071111) скорость клубочковой фильтрации, мл/час/100 г 14,69±0,40 9,296±0,511111) 14,69±0,40 11,56±0,33 канальцевая реабсорбция воды, % 99,37±0,037 99,351±0,015- 99,37±0,037 98,82±0,0521111) экскреция Na, мкмоль/ч/100 г 9,38±0,26 10,742±0,181111) 2) 9,38±0,26 11,02±0,44111) фильтрационный заряд Na, мкмоль/ч/100 г 1658,16±52,93 1305,37±24,131111) 1658,16±52,93 1465,19±50,44111) канальцевая реабсорбция Na, % 99,49±0,092 99,172±0,0261111) 99,49±0,092 99,29±0,0741) экскреция К, мкмоль/ч/100 г 6,32±0,36 7,75±0,115- 6,32±0,36 6,87±0,23- фильтрационный заряд К, мкмоль/ч/100 г 53,85±1,47 80,306±1,8241111) 53,85±1,47 44,61±1,31111) средняя скорость кровотока (М), см/с 4,95±0,21 3,7±0,111111) 1,41±0,14 1,068±0,1031) систолическая скорость (S), см/с 12,74±0,42 11,69±0,34- 9,37±0,39 6,78±0,9811) диастолическая скорость (D), см/с 6,335±0,19 2,49±0,211111) 6,94±0,27 6,91±0,12- индекс Гослинга (Pi) 7,28±0,38 9,18±0,321111) 13,16±0,43 17,42±1,28111) градиент давления (GD), мм.рт.ст. 0,054±0,002 0,038±0,0031111) 0,039±0,003 0,028±0,008- реографический индекс (RI) 0,49±0,04 0,897±0,051111) 1,59±0,061 1,78±0,071) Примечание:1111) - p<0,001; 111) - p<0,01; 11) - p<0,02; 1) - p<0,05 достоверность относительно контроля Системные изменения, вызванные солями тяжелых металлов, проявлялись в дисциркуляторных гемодинамических нарушениях вследствие изменения тонуса сосудов и повреждения эндотелиоцитов. Данные показали, что на фоне интоксикации солями тяжелых цветных металлов выявляется снижение жидкостного обмена тканей (А) – перфузии, систолической и диастолической скоростей кровотока в сосудах микроциркуляции. При анализе перфузии на фоне хронической интоксикации выявлено повышение пульсаторного индекса (индекса Гослинга - Pi), который отражает упруго-эластические свойства (плотность) сосудистой стенки. Реографический индекс Пурсело (RI)снижался. В крупных артериальных сосудах (БА, ПА) отмечено повышение средней и систолической скоростей кровотока (М и S, соответственно), градиент давления также повышен (GD). Но в отличие от сосудов микроциркуляторного звена, отмечено снижение и пульсаторного и реографического индексов (Pi и RI|, соответственно), что свидетельствует о тенденции к увеличению сердечного выброса. Повышение средней и систолической скоростей кровотока, отмечалось в артериях (БА, ПА) на фоне снижения реографи-ческого и пульсаторного индексов, вероятно, является механизмом компенсации жидкостного обмена в данной ситуации. Соли тяжелых металлов оказывают выраженный генотоксический эффект: на фоне Cd – 15,0±1,5% хромосомных аберраций, на фоне Pb 14,3±3,2% и Zn 12,0±3,3%. Выявлены хромосомные аберрации хроматидного типа (одиночные делеции) и хромосомного типа: парные делеции, дицен-трическое слияние хромосом, кольцевые хромосомы, реже встречались геномные мутации. Эти изменения касаются здоровья взрослого и детского населения г. Владикавказа. У 27,9% обследованных фенотипически здоровых молодых людей за период с 2001 по 2008 гг. уровень хромосомных аббераций превышал контроль в 1,5-2 раза и варьировал в пределах 36%, а у 14,7% уровень поражения наследственных структур превышал контроль в 2,5-3 раза, то есть был представлен 7-8 %. Результаты указанного генетического груза проявляются и соответствуют итогам диспансеризации, согласно которым из числа обследованных только 36,4% признаны здоровыми, у остальных выявлены различные отклонения в здоровье. Рождаются дети с врожденными пороками развития, из всего числа новорожденных 73,6% имели кариотип в пределах нормы, у 19,5% отмечено увеличение генетического дисбаланса в 2 раза на фоне контроля, а 4,9% обследованных детей имелся уровень хромосомных аберраций более 6-7%, что превышало контроль в 2-3 раза (контроль 2-3%). Таблица №2. Содержание цитокинов в сыворотке крови в приступном периоде при различном течении бронхиальной астмы (M±m Показатели Легкое (n=22) Среднетяжелое (n=20) Тяжелое (n=20) Ил-4 11,11 ±4,61 Р1>0,01 12,56±7,36 Р2>0,01 25,67 ±18,48 Р3>0,01 Ил-8 34,77±15,09 Р1>0,01 33,18 ±14,09 Р2>0,01 40,41 ±19,33 Р3>0,01 Ил-10 11,15 ±3,87 Р1>0,01 10,03 ±3,64 Р2>0,01 10,14 ±5,47 Р3>0,01 ИФ-γ 18,4±7,86 Р1>0,01 22,09 ±15,46 Р2>0,01 21,62±17,08 Р3>0,01 ФНО-ά 1,77±0,28 Р1>0,01 1,84±0,63 Р2>0,01 2,0±0,86 Р3>0,01 Примечание: Р1 - достоверность различий показателей между легким и среднетяжелым течением; Р2 -достоверность различий показателей между среднетяжелым и тяжелым течением; Р3 – достоверность различий показателей между легким и тяжелым течением Металлополютанты вызывают иммунобиологическую несостоятельность, способствуют развитию хронических и аутоиммунных заболеваний: бронхиальной астмы, хронических заболеваний почек, сахарного диабета, ИБС. Анализ данных заболеваемости бронхиальной астмой показал ее повышение у детей, проживающих в экологически неблагоприятном районе г. Владикавказа. Иммуносупрессия связана с нарушением репарации ДНК лимфоцитов, нарушением синтеза Т1 хелперами цитокинов: ИФ –γ, ИЛ-2 и экспрессии клеточных рецепторов. При интоксикации солями тяжелых металлов происходят изменения порфиринового обмена, инактивация ферментов синтеза Hb, дельта-аминолевулинат синтетаза, феррохелатазы и нарушение содержания Hb в крови. Исследование цитокинового статуса и показателей иммунобиологического состояния показало, что в период обострения отмечается повышение провоспалительных цитокинов ИЛ-4, ИЛ-8 и ФНО-α и снижение содержания противовоспалительных: ИЛ-10, ИНФ-γ. Разработаны новые технологии профилактики и лечения патологических состояний в эксперименте и клинике с использованием природных ресурсов РСО-Алании: ирлит-1,7, а так же современные антиоксиданты и мембранотропные вещества: НУМС, милдронат, L-карнитин и афобазол. Выводы: соли тяжелых металлов способствуют формированию различных патологических состояний со стороны висцеральных систем, нарушая их функционирование и вызывая развитие хронических заболеваний, таких как хронические заболевания почек, ИБС, бронхиальная астма, сахарный диабет и др. Патогенетической основой этих нарушений является активация процессов ПОЛ солями тяжелых цветных металлов, повреждение физико-химических свойств клеточных мембран основных систем жизнеобеспечения, иммуно-компонентных клеток и генетического аппарата.
Список литературы Механизмы влияния экотоксикантов на здоровье населения города Владикавказа
- Гильденскиольд, Р.С. Изменения структурно-функциональных показателей клеток системы крови мышей при длительном воздействии свинца и кадмия/Р.С. Гильденскиольд, Ю.В. Новиков, Р.С. Хамидулин и др.//Токсикол. Вестник. 2001. №5. С. 2-5.
- Кацнельсон, Б.А. Связь доклинических проявлений в почках у детей дошкольного возраста с содержанием кадмия и свинца в моче/Б.А. Кацнельсон, Л.И. Привалова, С.В. Кузьмин и др.//Токсикологический вестник. 2006. №4. С. 35-41.
- Киреев, Р.А. Влияние ионов кадмия на свободно-радикальные процессы и активность Na+, К+-АТФ-азы в тканях крыс//Токсикологический вестник. 2005. №4. С. 12-15.
- Ларкин, А.А. Оценка эффективности средств индивидуальной защиты кожи при воздействии соединений никеля//Медицина труда и промышленная экология. 2007. №9. С. 23-26.


