Механосинтез полимерных a-аминофосфонатов
Автор: Аль-итхави В.К.А., Аль-саммаррайи И.Ш.А., Копчук Д.С., Ковалев И.С., Криночкин А.П., Рыбакова С.С., Никонов И.Л., Зырянов Г.В., Поспелова Т.А., Матерн А.И.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 2 т.16, 2024 года.
Бесплатный доступ
Реакция Кабачника - Филдса широко используется для получения α-аминофосфонатов, в том числе полимерных. Кроме того, развитие получают методы механосинтеза α-аминофосфонатов. В рамках статьи были изучены методы получения арил-замещенных полимерных α-аминофосфонатов путем взаимодействия изомерных диаминобифенилов, терефталевого альдегида и диэтилфосфоната в шаровой мельнице. В результате были получены целевые поли(α-аминофосфонаты) 4. Строение продуктов было установлено на основе данных спектров ЯМР 1Н, 31P и ИК-. В спектре ЯМР 1Н следует отметить наличие характеристичных сигналов протонов ароматических фрагментов в виде мультиплетов при 8,62; 8,07 и 7,54 м.д., сигнала протонов при sp3-гибридизованном атоме углерода в виде уширенного синглета при 3,75 м. д., а также сигнала протонов группы OСH2CH3 в виде мультиплетов при 4,14 м. д. и 1,20 м. д. В спектре 31P имело место присутствие сигнала фосфора при 22,96 м.д. В ИК-спектрах наблюдались полосы поглощения при 1161 см-1 (P=O), 1051 см-1 (P-C-O), 2957 см-1 (OCH3) и 3445 см-1 (NH амидного фрагмента). Дополнительно была исследована возможность пост-модификации поливинилхлорида (ПВХ) фрагментами α-аминофосфонатов путем реакции первого с 2-аминотиофенолом, бензойным альдегидом и диэтилфосфонатом в шаровой мельнице, а также посредством реакции с 2-аминотиофенолом, терефталевым альдегидом и диэтилфосфонатом в аналогичных условиях. В результате были получены соответствующие α-аминофосфонат-содержащие поливинилхлориды 8-9. Таким образом, была продемонстрирована принципиальная возможность механосинтеза α-аминофосфонатов, а также возможность постмодификации ПВХ фрагментами α-аминофосфонатов.
Реакция кабачника - филдса, диаминобифелилы, диэтилфосфонат, механосинтез, поливинилхлорид, полимерные α-аминофосфонаты
Короткий адрес: https://sciup.org/147244625
IDR: 147244625 | УДК: 678.85 | DOI: 10.14529/chem240213
Mechanosynthesis of polymer a-aminophosphonates
Kabachnik-Fields reaction is widely used to obtain α-aminophosphonates, including polymeric ones. In addition, methods for the mechanosynthesis of α-aminophosphonates under mechanosynthesis conditions are being developed. The article examined methods for the preparation of aryl-substituted polymeric α-aminophosphonates by reacting isomeric diaminobiphenyls, terephthalic aldehyde and diethylphosphonate in the absence of a solvent in a ball mill. As a result, polymeric α-aminophosphonates 4 were obtained. The structure of the products was established on the basis of 1H, 31P and IR NMR spectra. In the 1H NMR spectrum, it should be noted the presence of characteristic signals of the protons of aromatic fragments in the form of multiplets at 8.62, 8.07 and 7.54 ppm, signals of the proton at the sp3 -hybridized carbon atom in the form of a broadened singlet at 3.75 ppm, as well as a signal of the protons of the group OCH2CH3 as a multiplet at 4.14 ppm. and a multiplet at 1.20 ppm. In the 31P spectrum there was the presence of a phosphorus signal at 22.96 ppm. Absorption bands at 1161 cm-1 (P=O), 1051 cm-1 (P-C-O), 2957 cm-1 (OCH3) and 3445 cm-1 (NH amide fragment) were observed in the IR spectra. Additionally, the possibility of post-modification of polyvinyl chloride (PVC) with fragments of α-aminophosphonates was investigated by reacting the former with 2-aminothiophenol, benzoaldehyde and diethylphosphonate in the absence of a solvent in a ball mill, as well as by reacting with 2-aminothiophenol, terephthalic aldehyde and diethylphosphonate under similar conditions. Thus, a possibility of mechanosynthesis of α-aminophosphonates was demonstrated, as well as the possibility for the post-modification of PVC with fragments of α-aminophosphonates .
Текст научной статьи Механосинтез полимерных a-аминофосфонатов
α-Аминофосфонаты представляют собой структурные аналоги (антагонисты) аминокислот. Основная их роль связана с ингибированием ферментов, участвующих в обмене аминокислот, что влияет на физиологическую активность клеток, в связи с чем α-аминофосфонаты могут проявлять широкий спектр биологической активности [1], в том числе антибактериальную [2–4] и противогрибковую активность [5]. Имеются данные о применении α-аминофосфонатов в качестве регуляторов роста растений [6] и в качестве нейромодулирующих средств [7, 8]. Наконец, α-аминофосфонаты могут быть использованы в качестве лигандов для катионов металлов [9], а их металлокомплексы могут быть использованы в медицинских целях [10].
Наиболее распространенным методом синтеза α-аминофосфонатов является реакция Кабач-ника – Филдса между аминами, альдегидами или кетонами и P(O)H-компонентами в растворителях или в их отсутствие [11, 12]. Также α-аминофосфонаты могут быть получены в условиях реактора непрерывного действия [13], а также в условиях механосинтеза [14]. Следует также отметить примеры получения полимерных α-аминофосфонатов [15].
В данной работе нами продолжено изучение возможностей механосинтеза полимерных α-аминофосфонатов путем мультикомпонентной реакции между диаминобифенилами, терефталевым альдегидом и диэтилфосфонатом в условиях шарового измельчения, а также путем постмодификации коммерчески доступного полимера – поливинилхлорида
Экспериментальная часть
-
3,3’-Диаминобифенил получен по ранее описанной процедуре [16]. Все остальные реагенты коммерчески доступны.
Спектры ЯМР 1H записаны на спектрометре Bruker Avance-400 (400 МГц, внутренний стандарт – SiMe 4 ).
Спектры ЯМР 31P записаны на спектрометре Bruker Avance-600 (243 МГц, внутренний стандарт – H 3 PO 4 ).
Механосинтез был осуществлен на планитарной мельнице Retsch PM-100 с использованием стального помольного стакана на 25 мл и 4 стальных мелющих шаров (диаметр 10 мм).
Механосинтез полимеров α-аминофосфонатов (4а–б). Смесь изомерных диаминодифенилов 1а или 1б (130 мг, 0,70 ммоль, 1 экв.), терефталевого альдегида 2 (95 мг, 0,70 ммоль, 1 экв.) в присутствии 200 мкл сухого 1,4-доксана перемешивали при 500 об/мин в течение 2 ч. Добавляли диалкилфосфонат 3 (6 экв.) в 100 мкл сухого ДМСО и смесь снова перемешивали в течение 2 ч. Полученные осадки суспендировали в ТГФ, осадок отфильтровывали, промывали диэтиловым эфиром. Процедуру повторили 3 раза. После этого осадок сушили в течение 24 ч.
Полимер 4а . Желтый осадок. Выход 70 %. Т пл > 250 °C. ИК (КВr), ν, cm–1: 1171 (P=O), 1011 (P-C-O), 3411, 3362 (NH), 2978, 2873 (OCH3).
Полимер 4б . Желтый осадок. Выход 62 %. Т пл > 250 °C. ЯМР 1H (400 MHz, CDCl 3 + ДМСО-d 6 , δ): 8,60 (уш. c., 2H); 8,06 (уш. с., 4H); 7,51 (м., 6H); 4,17(c., 2H); 3,75 (c., 3H); 1,38 (c., 3H). ЯМР 13P (400 MHz, ДМСО-d 6 , δ): 22,99. ИК (КВr), ν, cm–1: 1161 (P=O), 1051 (P-C-O), 3445, (NH), 3024– 2874 (OCH 3 ).
Синтез полимеров (8–9). Смесь о -аминотиофенола 6 (88 мг, 0,70 ммоль, 1 экв.), бензойного альдегида 7 (для полимера 8 ) (72 мг, 0,70 ммоль, 1 экв.) или терефталевого альдегида 2 (для полимера 9 ) (95 мг, 0,70 ммоль, 1 экв.) в присутствии 200 мкл сухого 1,4-доксана перемешивали при 500 об/мин в течение 2 ч. Добавляли диалкилфосфонат 3 (6 экв.) в 100 мкл сухого ДМСО и смесь снова перемешивали при 500 об/мин в течение 2 ч. Добавляли поливинилхлорид (1 г), К 2 СО 3 (0,966 мг, 7 ммоль), 200 мкл сухого 1,4-доксана и смесь перемешивали при 500 об/мин в течение 2 ч. Полученные осадки суспендировали в воде, осадок отфильтровывали и промывали метанолом. Процедуру повторили 3 раза. После этого осадок сушили в течение 24 ч.
Обсуждение результатов
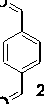
В качестве исходных соединений в данной работе были использованы коммерчески доступные бензидин ( 1a ), 4,4’-диаминобифенил, а также 3,3’-диаминобифенил ( 1б ). Взаимодействие осуществлялось путем трехкомпонентной реакции между диаминобифенилами ( 1 ), терефталевым альдегидом ( 2 ) и диэтилфосфонатом ( 3 ) в присутствии небольших количеств со-растворителя (1,4-диоксан или ДМСО) в условиях шарового измельчения при 500 об/мин в течение 4 ч (схема 1).
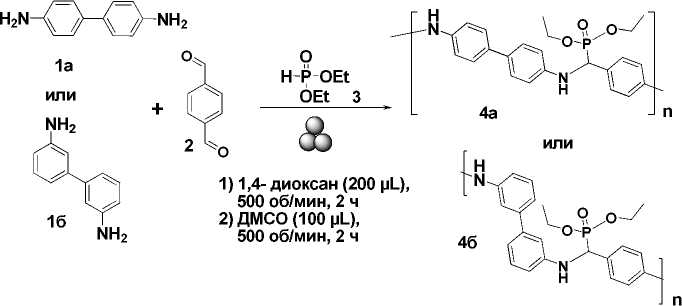
Схема 1. Трехкомпонентный синтез полимеров 4а, б
Полученные полимеры ( 4 ) были выделены в виде желтых осадков, бол е е рас тв ори мый п олимер ( 4б) был ох а рак те ризов а н Я МР 1Н анализом. Так, в спектре ЯМР 1Н (рис. 1) присутствуют си гналы а рома ти чес к и х фра гм е н тов в в и д е му л ьтиплетов при 8,62; 8,07 и 7,54 м. д., сигнал протона при sp3-г ибри д и з ованн ом атоме углерода (уширенный синглет при 3, 75 м. д.) и сигналы группы OСH 2 CH 3 ( м у льти п ле ты п ри 4, 14 м. д. и 1,20 м. д.) фрагмента α-аминофосфоната. К сож а л е н и ю , оп ред е ле н ие моле к у ля рного веса полимеров ( 4 ) методом гель-проникающей хроматог ра фи и ок аз ал ос ь не в озм ож н ым и з -за низкой растворимости в ТГФ.
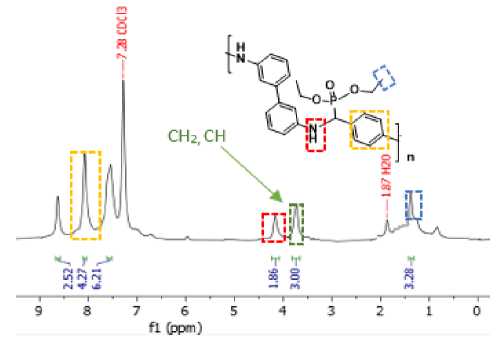
Рис. 1. ЯМР 1Н спектр полимера 4б
Данными спектров ЯМР 3 1P было подтверждено присутствие фосфорсодержащего фрагмента в составе полимера ( 4б ) ( а и менно имел место сигнал атома фосфора при 22, 96 м. д., рис. 2). В больш и нс тв е ли те ра ту р н ых и с точн и к ов для α-аминометилфосфонатов наблюдался пик в спектрах 31P в диапазоне 20–30 м. д . [ 17, 18 ].
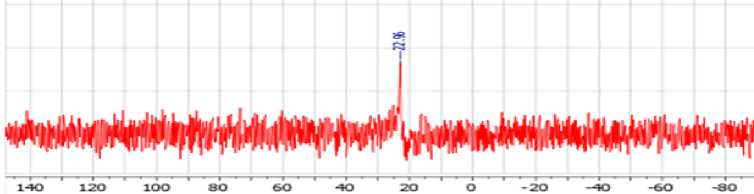
Рис. 2. ЯМР 31P спектр полимера 4б
В ИК-с п е к тра х н а б лю да л и сь полосы поглощения группы P=O при 1161 см–1, а также фрагментов P-C-O при 1051 см–1, O C H 3 при 2957 см–1 и NH фрагмента амида при 3445 см–1.
Доп олн и те л ьн о была и с сл едована возможность модификации коммерч е ск и доступного ПВХ ( 5 ) фрагментами α-амин ом етилфосфонатов. Для этого была осуществлена ч е тыре х к омп он е н тн ая реакция между ПВХ ( 5 ), 2-а мин оза ме ще н н ым ти офен олом ( 6 ), диэтилфосфонатом ( 3 ) и бензойным альдегидом ( 7) в п ри с у тс тви и K 2 CO 3 в условиях шарового измельчения при 500 об/мин в течение 4 ч (схема 2).
OO
OP

O
H P OEt
OEt
+
Cl

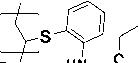
O P ^O
O
n K2CO3, 1,4-диоксан - ДМСО, 5 K2CO3, 1,4-диоксан - ДМСО, O O
500 об/мин, 6 ч 500 об/мин, 6 ч
O
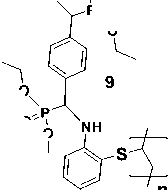
Схема 2. Четырехкомпонентный синтез полимеров 8, 9
Полученный ПВХ-модифицированный полимер ( 8 ) был выделен в виде бесцветного осадка и охарактеризован методами ЯМР 1Н и ИК-спектроскопии. Так, в спектре ЯМР 1Н присутствуют сигналы протонов ароматических фрагментов в виде мультиплета при 7,25–7,55 м. д., протона при sp3-гибридизованном атоме углерода (уширенный синглет при 3,75 м. д.) и протонов группы OСH 2 CH 3 (мультиплет при 4,14 м. д. и мультиплет при 1,20 м. д.) фрагмента α-аминофосфоната.
В ИК-спектрах соединений 4а–б и 8 наблюдались полосы поглощения группы P=O при 1165 см–1, а также фрагментов P-C-O при 1055 см–1, OCH 3 при 2960 см–1 и NH фрагмента амида при 3460 см–1.
Наконец, в рамках работы была осуществлена попытка получения кросс-связанного полимерного α-аминометилфосфоната, а именно полимера ( 9 ), путем четырехкомпонентной реакции между ПВХ ( 5 ), 2-аминозамещенным тиофенолом ( 6 ), диэтилфосфонатом ( 3 ) и терефталевым альдегидом ( 2 ) в присутствии K 2 CO 3 в условиях шарового измельчения при 500 об/мин в течение 6 ч (см. схему 2). В итоге был выделен бесцветный осадок, нерастворимый в органических растворителях.
Выводы
Таким образом, продемонстрирована возможность механосинтеза полимерных α-аминометилфосфонатов путем мультикомпонентной реакции Кабачника – Филдса между изомерными амино(би)фенилами, ароматическими (ди)альдегидами и диэтилфосфонатом в отсутствие расторителя в шаровой мельнице. При этом наряду с непосредственным конструированием полимерного каракаса из мономерных фрагментов было осуществлено построение фрагментов α-аминометилфосфонатов на каркасе поливинилхлорида. Полученные полимеры были охарактеризованы методами ЯМР- и ИК-спектроскопии. Предложенный метод может рассматриваться как альтернатива для проведения реакции Кабачника – Филдса в условиях механосинтеза, а также как возможность для утилизации/постмодификации коммерчески доступного поливинилхлорида, в том числе в составе бытовых отходов, с использованием ресурсосберегающих методов.
Список литературы Механосинтез полимерных a-аминофосфонатов
- Orsini F., Sello G., Sisti M. // Curr. Med. Chem. 2010. Vol. 17, Iss. 3. P. 264. DOI: 10.2174/092986710790149729.
- Litim B., Djahoudi A., Meliani S. et al. // Med. Chem Res. 2022. Vol. 31, Iss. 1. P. 60. DOI: 10.1007/s00044-021-02815-5.
- Koszelewski D., Kowalczyk P., Śmigielski P. et al. // Materials 2022. Vol. 15, Iss. 11. 3846. DOI: 10.3390/ma15113846.
- Bahadi R., Berredjem M., Benzaid C. et al. // J. Mol. Struct. 2023. Vol. 1289. 135849. DOI: 10.1016/j.molstruc.2023.135849.
- Rezaei Z., Khabnadideh S., Zomorodian K. et al. // Int. J. Med. Chem. 2011. Vol. 2011. 678101. DOI: 10.1155/2011/678101.
- Nadiveedhi M.R., Nuthalapati P., Gundluru M. et al. // ACS Omega. 2021. Vol. 6, Iss. 4. P. 2934. DOI: 10.1021/acsomega.0c05302.
- Uparkar J.J., Dhavan P.P., Jadhav B.L. et al. // J. Iran. Chem. Soc. 2022. Vol. 19. P. 3103. DOI: 10.1007/s13738-022-02515-w.
- Yelamanda Rao K., Shaik Jeelan B., Kallubai M. et al. // Eur. J. Med. Chem. 2023. Vol. 253. 115288. DOI: 10.1016/j.ejmech.2023.115288.
- Bálint E., Tajti A., Tripolszky A. et al. // Dalton Trans. 2018. Vol. 47. P. 4755. DOI: 10.1039/C8DT00178B.
- Tušek-Božić L.J. // Curr. Med. Chem. 2013. Vol. 20, Iss. 16. P. 2096. DOI: 10.2174/0929867311320160004.
- Sravya G., Balakrishna A., Zyryanov G.V. et al. // Phosphorus Sulfur Silicon Relat. Elem. 2021. Vol. 196, Iss. 4. P. 353/ DOI: 10.1080/10426507.2020.1854258.
- Varga P.R., Keglevich G. // Molecules. 2021. Vol. 26, Iss. 9. 2511. DOI: 10.3390/molecules26092511.
- Bálint E., Tajti Á., Ladányi-Pára K. et al. // Pure Appl. Chem. 2019. Vol. 91, Iss. 1. P. 67. DOI: 10.1515/pac-2018-0923.
- Fiore C., Sovic I., Lukin S. et al. // ACS Sustainable Chem. Eng. 2020. Vol. 8, Iss. 51. P. 18889. DOI: 10.1021/acssuschemeng.0c05744.
- Zhang Y., Zhao Y., Yang B. et al. // Polym. Chem. 2013. Vol. 5. P. 1857. DOI: 10.1039/C3PY01486J.
- Al-Ithawi W. K. A., Khasanov A. F., Kovalev I. S. et al. // Chem. 2023. Vol. 5, Iss. 2. P. 978. DOI: 10.3390/chemistry5020066.
- Hirschmann R., Yager K.M., Taylor C.M. et al. // J. Am. Chem. Soc. 1997. Vol. 199, Iss. 35. P. 8177. DOI: 10.1021/ja962465o.
- Kakuchi R., Theato P. // ACS Macro Lett. 2014. Vol. 3, Iss. 4. P. 329. DOI: 10.1021/mz500139c.


