Меланофоры рыб в реализации свободнорадикальных клеточно-тканевых механизмов онкогенеза
Автор: Сахаров А.В., Лошенко В.И., Макеев А.А., Арбузова Е.Н.
Статья в выпуске: 3 т.259, 2024 года.
Бесплатный доступ
Работа посвящена изучению роли хроматофор рыб в реализации клеточных и органно- тканевых механизмов, их адаптации к действию повреждающих факторов. В работе дана морфологическая характеристика патологического новообразования в области жаберной крышки карася (Саrаssius gibеliо), добытого из депрессивного водоема с высоким уровнем антропогенной нагрузки. Клеточная атипия, нарушение дифференцировки клеток и дезорганизация структуры покровного эпителия жаберной крышки характеризует развитие дисплазии покровного эпителия жаберной крышки на начальных этапах развития процесса. При манифестации процесса в структуре эпителия отдельных сосочков обнаруживается фрагментация базальной мембраны, нарушение стратификации эпителия и развитие гиперкератоза. Данная морфологическая картина характерна для плоскоклеточного ороговевающего рака.
Серебряный карась, жаберная крышка, эпителий, меланофоры, онкогенез, свободные радикалы, антиоксидантная защита
Короткий адрес: https://sciup.org/142242489
IDR: 142242489 | УДК: 591.2; 639.371.5 | DOI: 10.31588/2413_4201_1883_3_259_211
Fish melanophores in the implementation of free radical cell-tissue mechanisms of oncogenesis
The work is devoted to studying the role of fish chromatophores in the implementation of cellular and organ-tissue mechanisms of their adaptation to the action of damaging factors. The work provides a morphological characteristic of a pathological neoplasm in the area of the gill cover of silver prussian carp (Carassius gibelio), obtained from a depressed reservoir with a high level of anthropogenic load. Cellular atypia, impaired cell differentiation and disorganization of the structure of the integumentary epithelium of the gill cover characterize the development of dysplasia of the integumentary epithelium of the gill cover at the initial stages of the development of the process. When the process manifests itself in the structure of the epithelium of individual papillae, fragmentation of the basement membrane, disruption of the stratification of the epithelium and the development of hyperkeratosis are detected. This morphological picture is typical for squamous cell keratinizing carcinoma.
Текст научной статьи Меланофоры рыб в реализации свободнорадикальных клеточно-тканевых механизмов онкогенеза
В настоящее время не вызывает сомнений, что клетки, синтезирующие пигменты в различных тканевых компартментах, обеспечивают реализацию важнейших физиологических процессов у позвоночных и беспозвоночных животных, растений и грибов [1]. По мере расширения имеющихся представлений о биологической роли пигментов становится совершенно очевидным их важное участие в реализации активности всех без исключения функциональных систем организма. Целесообразность существования огромного многообразия окрасок покровов тела рыб остается до настоящего времени одним из не решенных вопросов [9]. Результаты, полученные С. Ю. Петуховым и Ю. П. Толмачевым (2015), Д. В. Праздниковым и Ф. Н. Шкилем (2018) весьма убедительно объясняют причины и значение возникающих межвидовых и внутривидовых различий окраски тела отдельных групп рыб и особенности их преобразований в филогенезе [10-11]. Эти материалы имеют важное значение для понимания фундаментальных закономерностей биологии и экологии водных животных. Однако использование современных методов исследований позволило сместить акцент работ в направлении изучения различных классов пигментов с популяционно-видового и онтогенетического, до клеточного и молекулярно-генетического уровней организации живой системы. Такой подход позволил приблизиться к пониманию значения пигмент-синтезирующих клеток в реализации морфофункциональных преобразований в организме водных животных уже на ранних этапах онтогенеза, начиная от оплодотворения икры, периоды эмбрионально-личиночного развития и более поздние сроки онтогенеза [4]. Сведения по данной проблематике, накопленные в результате наблюдений на различных видах живых организмов, указывают на способность пигментных клеток посредством экспрессии специфических белков обеспечивать осуществление гораздо более важных, чем предполагалось ранее морфогенетических преобразований, как в норме, так и при изменении параметров среды обитания рыб или воздействии на организм патогенов [3].
Считается, что синтензирующие меланин клетки у различных живых организмов принимают активное участие в окислительно-восстановительных процессах и регуляции редокс-гомеостаза как в норме, так патологии [14]. Анализ публикаций отечественных и зарубежных авторов указывает на крайне недостаточную информации относительно участия хроматофор рыб в реализации клеточных и органно-тканевых механизмов адаптации к действию повреждающих факторов [4]. В этой связи изучение значения меланофоров рыб в реализации свободнорадикальных клеточно-тканевых механизмов онкогенеза определяет высокую актуальность настоящего исследования.
Целью работы являлось изучение роли меланофоров у рыб вида серебряный карась ( Саrаssius gibеliо ) в морфогенезе опухолевого роста покровного эпителия.
Материал и методы исследований. Исследование проводилось в период октября 2020 – март 2021 гг. на 32 особях рыб серебряного карася ( Саrаssius gibеliо ) средней массой 1431, 41±12 граммов. Рыбы добыты из экологически депрессивного водоема с высоким уровнем антропогенной нагрузки [5]. Объектом изучения являлись участки неопластических образований, локализованных в области костей жаберной крышки, которые забирали единым комплексом. Материал фиксировали в 10 % растворе нейтрального формалина и далее декальцинировали в насыщенном растворе трилона Б. При вырезке патологического материала соблюдали предельную осторожность и сохраняли целостность тканевого комплекса, включающего костную ткань и зоны опухолевого роста. Образцы обезвоживали в изопропиловом спирте и заливали в гистомикс по стандартной методике. Срезы толщиной 510 мкм готовили на ротационном полуавтоматическом микротоме SLEE CUT 5062 (Германия), а затем окрашивали гематоксилином Бемера и эозином. Распределение суммарных кислых гликозаминогликанов (ГАГ) изучали путем постановки гистохимической реакции с альциановым синим по Стидмену. Реакцию на коллаген определяли по Маллори.
Исследование гистологических препаратов осуществляли с использованием комплекса оптикоструктурного анализа Axio Imager.M2 c программным обеспечением для анализа изображений AxioVision Z2 M2 (CARL ZEISS, Германия). Цифровая обработка материала осуществлялась при помощи CCD-камеры AxioCam HR c программным обеспечением Zen Lite (CARL ZEISS, Германия).
Содержание первичных и вторичных продуктов свободнорадикального перекисного окисления липидов (СПОЛ), активность ключевых ферментов системы антиоксидантной защиты (АОЗ) изучали в рекомендации Е. Б. Меньщиковой с соавт. (2006) [8]. Уровень диеновых конъюгатов (ДК) определяли в реакции с гептанизопропаноловой смесью. Содержание малонового диальдегида (МДА) исследовали в реакции с трихлоруксусной и 2-тиобарбитуровой кислотами. Активность каталазы (КАТ) выявляли в реакции перекиси водорода с добавлением молибдата аммония. Активность супероксидисмутазы (СОД) определяли по ингибированию скорости восстановления тетразолия нитросинего в системе феназинметасульфата и НАД∙Н. [7]. Статистическую обработку результатов исследования проводили на основе вычисления средних величин (M) и их ошибок (m) с учетом объема выборки (n). Различия всех исследуемых показателей оценивали методом вариационной статистики по t-критерию Стьюдента и считали достоверными при Р ≤ 0,05. Все расчеты проводили по общепринятым формулам с использованием пакета программ Miсrosoft Excel 2010.
Результаты исследований. По уровню развития патологического процесса в области жаберных крышек карася обнаружены особи, как с незначительными, так и чрезмерно развитыми по площади новообразованиями. В случае слабо выраженного патологического процесса измененная ткань имеет площадь до 11,31±1,98 см3 (Рисунок 1 А). Ее поверхность преимущественно гладкая или слегка бугристая, бледно-розового или серого цвета. Морфология патологических образований представлена паренхимой в форме многочисленных эпителиальных разрастаний сферической формы и стромой (Рисунок 1 Б.) На светооптическом уровне паренхима состоит из активно пролиферирующих клеток многослойного плоского эпителия (Рисунок 1 В). В структуре ткани заметны очаговые пигментные образования чернозеленого цвета (рис 1 А). В зависимости от выраженности процесса морфологическая картина измененной ткани покровного эпителия жаберной крышки соответствует либо гиперплазии, либо слабовыраженной дисплазии. Морфологические критерии дисплазии в данном случае основываются на наличие трех основных диагностических признаков – клеточная атипия, нарушение дифференцировки клеток эпителия и, в целом дезорганизация структуры покровного эпителия жаберной крышки (Рисунок 1 Г).
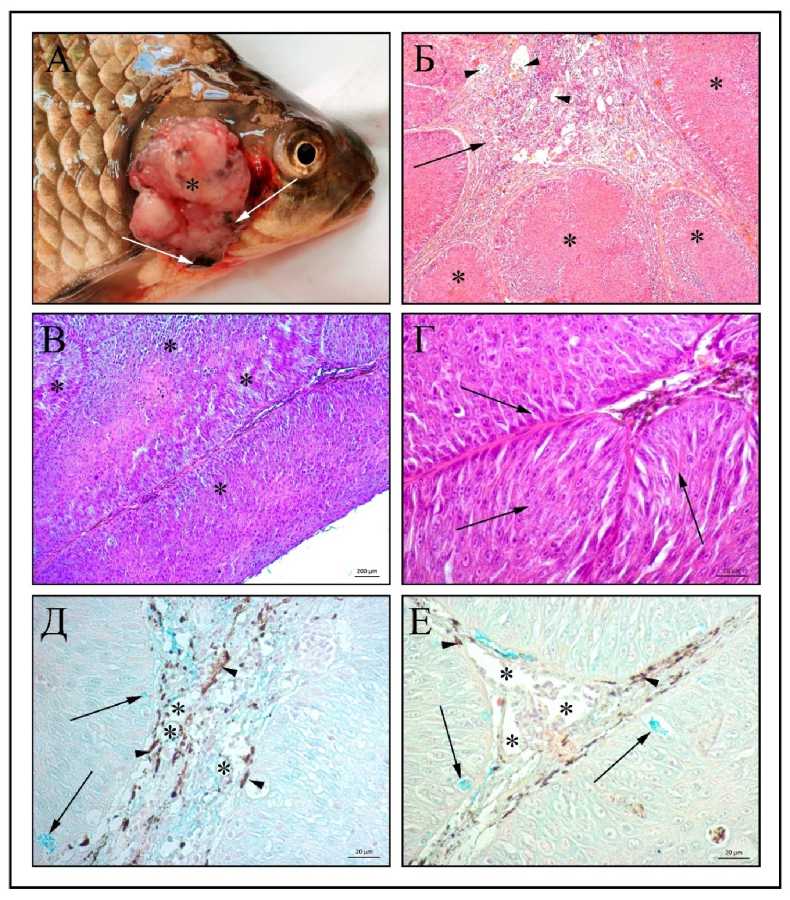
Рисунок 1 – А. Звездочкой обозначено новообразование, стрелками – участки гиперпигментации новообразования; Б. Звездочками обозначены эпителиальные узелки новообразования, стрелкой – строма новообразования, головками стрелок – кровеносные сосуды; В. Звездочками обозначены участки активно-пролиферирующих клеток многослойного плоского эпителия; Г. Стрелками обозначены участки дезорганизации покровного эпителия жаберной крышки; Д, Е. Звездочками обозначены кровеносные сосуды, стрелками – положительная реакция цитоплазмы кератиноцитов на кислые ГАГ, головками стрелок – локализация меланофоров
Наличие многочисленных межклеточных щелей, вероятно, обусловлено потерей или снижением темпов экспрессии интенсивно пролиферирующими клетками эпителия молекул адгезии и замедлением времени формирования межклеточных контактов.
Строма патологического образования обильно васкуляризирована (Рисунок 1 Б, Е, Д). В просвете кровеносных сосудов и периваскулярном пространстве идентифицируются многочисленные лейкоциты, среди которых преобладают клетки лимфоцитарного профиля. На препаратах, окрашенных альциановым синим, отчетливо видны многочисленные активно пролиферирующие кератиноциты, цитоплазма которых дает положительную реакцию на ГАГ (Рисунок 1 Д). В межклеточном веществе стромы заметно обилие меланофоров, локализованных в области формирования кровеносных капилляров (Рисунок 1 Д, Е).
При наличии у обследованных рыб обширных новообразований в области костей жаберной крышки последние имеют бугристую поверхность темнозеленого или черного цвета неправильной формы с нечеткими контурами.
Дезорганизация эпителия новообразования по уровню атипии клеток и их дифференцировки отличается вариабельностью структурнофункциональных преобразований. Одни имеют схожее строение с описанной выше тканью рыб, у которых патологический процесс ограничен гиперплазией и начальными этапами дисплазии. В исследуемых образцах рыб с массивными новообразованиями морфологическая картина эпителия имеет признаки глубокого нарушения структурной организации. Неоплазма возвышается над поверхностью жаберной крышки и ее размеры варьируют от 11,31±1,98 см3 и до 33,15 см3 (Рисунок 2 А). На светооптическом уровне опухоль состоит из множества сосочков, что само по себе является проявлением атипизма ткани (Рисунок 2 Б).
На обзорных препаратах, окрашенных гематоксилином и эозином, отчетливо заметно, что клетки базального слоя теряют характерное для нормального эпителия строение. Вытянутые, призматической формы эпителиоциты выстраиваются перпендикулярно базальной мембране и между клетками становятся заметными широкие межклеточные щели (Рисунок 2 В). Среди эпителиоцитов, лежащих выше базального слоя, заметны фигуры атипического митоза, клетки с признаками летального повреждения. В структуре эпителия отдельных сосочков обнаруживается фрагментация базальной мембраны и нарушение стратификации эпителия (Рисунок 2 Г, Д). Кроме того, обращает внимание наличие многочисленных кератиноцитов с оксифильной цитоплазмой и участками ее просветления в околоядерной зоне (Рисунок 2 Е).
В центре эпителиального сосочка видны обширные полости, содержащие клеточный детрит и субстрат, по тинкториальным свойствам напоминающий меланин или липофусцин (Рисунок 3 А). Клеток воспаления в таких образованиях и на их периферии не обнаружено. На поверхности сосочка эпителий имеет признаки гиперкератоза (Рисунок 3 Б).
Применение гистохимической реакции на ГАГ и коллаген удачно демонстрирует возможность реализации дифференциального патоморфологического подхода к идентификации структуры новообразования. В реакции с альциановым синим среди клеточного состава эпителия заметно высокое содержание эпителиоцитов, синтезирующих слизистый секрет. В структуре опухоли паренхима преобладает строму по объему, коллагеновые фибриллы которой интенсивно окрашиваются в реакции по Маллори (Рисунок 3 В). Строма образована типичной рыхловолокнистой соединительной тканью с развитой сетью кровеносных сосудов. Капилляры чрезмерно расширены. В просвете кровеносных сосудов и периваскулярном пространстве идентифицируется высокое содержание лимфоцитов (Рисунок 3 Г). По ходу капиллярной сети периваскулярно располагаются многочисленные меланофоры (Рисунок 3 Д). Изменение тинкториальных свойств патологически измененного покровного эпителия и костной ткани в области os paraeoperculum и os operculum, указывает на чрезмерное увеличение темпов ремоделирования костного матрикса и повышение порозности костей жаберной крышки (Рисунок 3 Е).
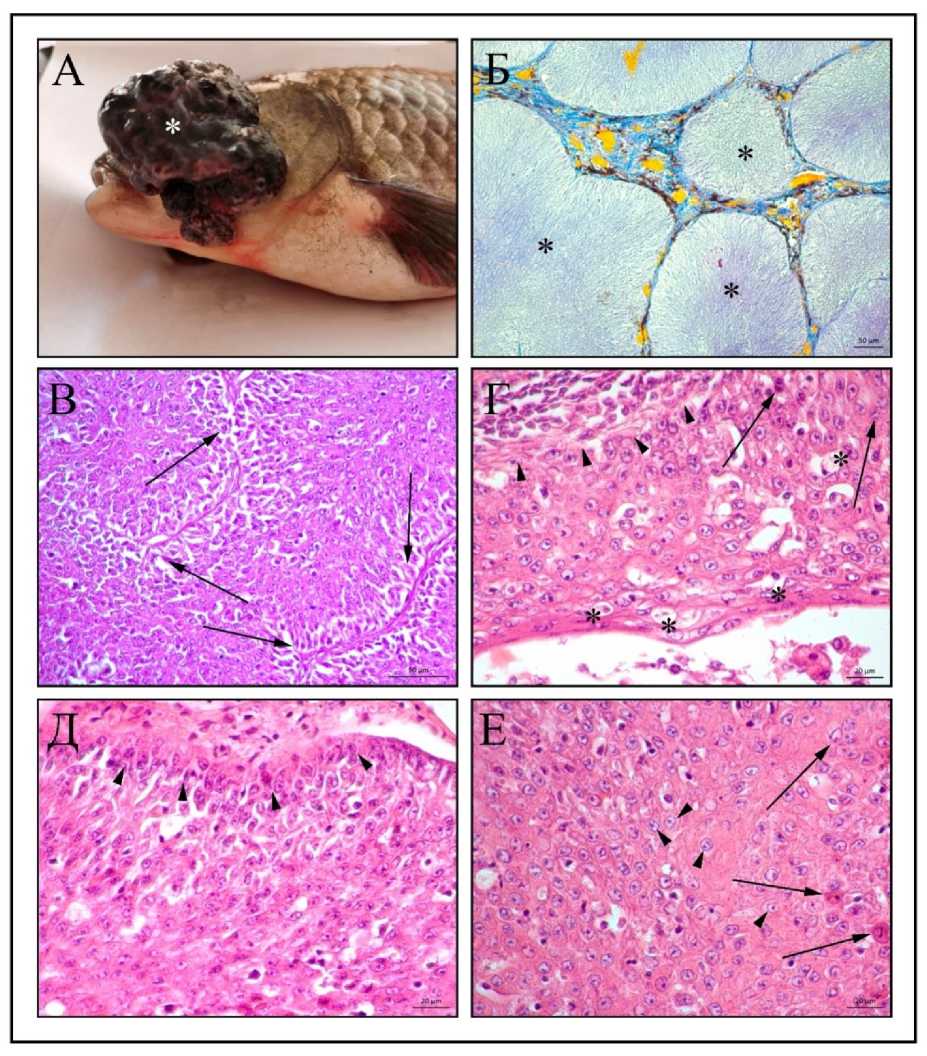
Рисунок 2 – А. Звездочкой обозначено новообразование; Б. Звездочками обозначены эпителиальные узелки новообразования; В. Стрелками обозначены межклеточные щели; Г. Головками стрелок обозначено нарушение целостности базальной мембраны, стрелками – фигуры атипического митоза, звездочками – клетки с признаками летального повреждения; Д. Головками стрелок обозначено нарушение целостности базальной мембраны; Е. Головками стрелок обозначены клетки с оксифильной цитоплазмой и участками её просветления в околоядерной зоне, стрелками – фигуры атипического митоза
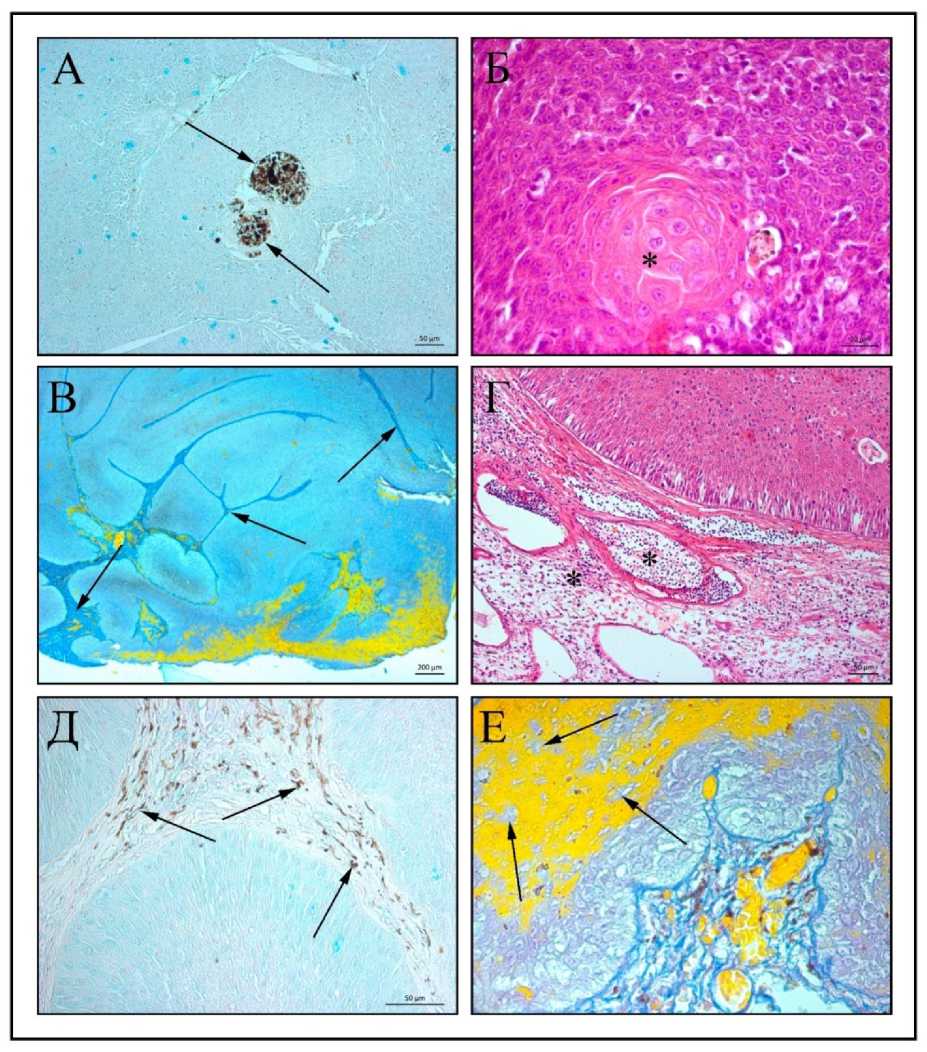
Рисунок 3 – А. Стрелками обозначены локализация клеточного детрита в центре эпителиального сосочка; Б. Звездочкой отмечен участок гиперкератоза в структуре эпителия; В. Стрелками обозначена интенсивная реакция на коллаген; Г. Звездочками обозначена локализация лимфоцитов в просвете кровеносных сосудов стромы; Д. Стрелками обозначена локализация меланофоров; Е. Стрелками обозначены участки остеолиза костного матрикса
При изучении состояния системы АОЗ в гомогенатах ткани опухоли нами установлена депрессия ключевых ферментов системы антоксидантной защиты СОД, КАТ и превышение уровня ДК и МДА по сравнению с интактными участками эпителия жаберной крышки карася (Таблица 1).
Оценивая полученные результаты, с позиции единства структуры и функции, закономерно возникает вопрос относительно природы данного патологического образования в области жаберной крышки карася. На ранних этапах развития процесса в структуре эпителия опухолевого образования рыб пролиферация клеток эпителия происходит без нарушения целостности базальной мембраны и структуры эпителиального пласта в целом. По мере дальнейшего развития патологического процесса в цитоплазме клеток обнаруживается не характерное для нормы усиление реакции на ГАГ. Структура такого эпителия напоминает муцинпродуцирующее интраэпителиальное поражение шейки матки у человека SMILE (stratified mucin – producing intraepithelial lesion) при инфицировании вирусом папилломы человека (ВПЧ). В публикации J. J. Park с соавторами (2000) приводится мнение, что поражение мультипотентной стволовой клетки эпителиального пласта ВПЧ приводит к развитию гиперплазии, плоскоклеточной интраэпителиальной неоплазии и малигнизации in situ [12]. В нашем исследовании на причастность к неопластическому процессу вирусного патогена указывает наличие среди клеток эпителия жаберной крышки кератиноцитов с зоной просветления цитоплазмы в околоядерной зоне, которые напоминают койлоциты – клетки инфицированные ВПЧ.
Таблица 1 – Показатели липопероксидации и активности системы антиоксидантной защиты в гомогенатах эпителиальной ткани жаберной крышки карася
|
Исследуемые показатели |
Локализация |
|
|
эпителий интактных участков |
эпителиома |
|
|
ДК, нмоль/г |
4,47±0,27 |
25,11±1,46 * |
|
МДА, нмоль/г белка |
32,93±6,35 |
205,41±15,80* |
|
КАТ, моль/мин/мг белка |
11,22±0,91 |
1,47±0,29 ** |
|
СОД, усл. ед./ мг белка |
1,47±0,34 |
0,32±0,13* |
Примечание. Различия статистически достоверны между показателями образцов интактных участков жаберной крышки и эпителиомы, *Р≤0,05, **Р≤0,01
В структуре эпителиальных узлов отмечаются признаки избыточного ороговения в виде интенсивно оксифильных концентрических образований, которые дают картину плоскоклеточного ороговевающего рака. Описанные особенности гистотопографии тканевого комплекса в строме патологического образования карася свидетельствуют о существовании причинно-следственной связи между функциональной активностью меланофоров и повреждением кератиноцитов, предположительно NO.
Опираясь на собственные результаты и данные литературных источников инфицирование покровного эпителия вирусным патогеном начинается с клеток базального слоя. В случае вирусного папилломатоза, например, человека инфицирование происходит в результате травмы глубоких слоев эпителия слизистой оболочки. В нашей работе наличие в сосудах стромы опухоли, расположенных на границе с базальным слоем эпителия высокого содержания лимфоцитов, которые, как известно, принимают активное участие в механизмах противовирусной защиты клеток не исключает возможности проникновения вируса гематогенным путем. Предпринятый ранее нами патоморфологический анализ образцов печени, почек, кишечника и жабер рыб с опухолевыми образованиями не позволил выявить характерных признаков их повреждения. Следовательно, в рамках настоящей работы без проведения специальных исследований однозначно ответить на этот вопрос не представляется возможным. Вместе с тем, факт активной пролиферации кератиноцитов является стереотипной реакцией клеток на их сублетальное повреждение. В зависимости от тяжести процесса морфологическая картина повреждения развивается в направлении от гиперплазии эпителия к дисплазии и очаговой малигнизации. По мнению C. Romero-Graillet с соавторами (1997) пролиферирующие кератиноциты экспрессируют паракринные факторы, активирующие пролиферацию муцинсекретирующих клеток. Данные литературы и результаты иммуногистохимии свидетельствуют об участии кератиноцитов и меланофор в синтезе NO [13].
С точки зрения функциональной морфологии повышение количества меланисинтезирующих клеток в опухолевой ткани имеет дуалистическую природу. С одной стороны, рост опухоли требует ее адекватного кровоснабжения. В этом плане экспрессия меланофорами NO обеспечивает активный рост сосудов в строме неоплазмы. С другой стороны, биологический смысл увеличения меланофор связан со способностью свободнорадикальной молекулы NO повреждать инфицированные вирусным патогеном клетки эпителия. Анализ состояния активности свободнорадикальных процессов в опухолевой ткани карася подтверждает наличие высокого уровня окислительных процессов и развитие окислительного стресса (Таблица 1).
Необходимо отметить, что у более низко организованных животных, например, насекомых меланин участвует в инкапсуляции проникшего в организм патогена и заживление ран [5]. При таком варианте в ходе инкапсуляции чужеродный объект заключается в капсулу из разрушенных и меланизированных клеток. Подобную реакцию можно наблюдать при ранении мягких тканей тела насекомого, где меланин выступает в качестве мощного механического барьера, изолирующего чужеродные объекты, предотвращающий рост паразитов и ингибирующий микробиальные хитиназы и протеазы [6, 15]. Кроме того, во время каскада ферментативных реакций, приводящих к образованию меланина, возникает также ряд промежуточных высокореактивных продуктов, опосредующих киллерный механизм при инкапсуляции и гранулообразовании.
Считается, что меланины, особенно эумеланины, демонстрируют выраженные окислительно-восстановительные свойства и могут принимать участие в одноэлектронных и двухэлектронных окислительно-восстановительных реакциях, приводящих к генерации супероксидных радикалов. Последние, как известно, способствуют необратимому повреждению молекулы ДНК, летальному повреждению клеток и субклеточных структур, развитию опухолевого процесса [2].
Заключение. Таким образом, результаты исследования дают все основания считать, что в основе молекулярных механизмов развития опухолевого процесса у рыб важная роль принадлежит активным метаболитам кислорода, а меланин синтезирующие клетки выступают в роли клеточнотканевых регуляторов онкогенеза.
Список литературы Меланофоры рыб в реализации свободнорадикальных клеточно-тканевых механизмов онкогенеза
- Грачева, Н. В. Меланины. Перспективы и проблемы использования в промышленности / Н. В. Грачева, В. Ф. Желтобрюхов. – Волгоград: Волгоградский государственный технический университет, 2019. – 92 с.
- Вострикова, С. М. Активные формы кислорода и антиоксиданты в канцерогенезе и терапии опухолей / С. М. Вострикова, А. Б. Гринев, В. Г. Гогвадзе // Биохимия.– 2020.– Т. 85.– №. 10.– С. 1474-1488.
- Кеберлайн, О. В. Изменение содержания естественных антиоксидантных соединений в икре зеркального карпа при различных технологиях обесклеивания / О. В. Кеберлайн, А. В. Сахаров, А. Е. Просенко // Проблемы биологии и биологического образования в педагогических вузах. – 2013. – С. 53-54.
- Кеберлайн, О. В. Роль каротиноидов в механизмах адаптации эмбрионов зеркального карпа к технологическим нагрузкам при разведении в аквакультуре / О. В. Кеберлайн, А. В. Сахаров, А. А. Макеев, А. Е. Просенко // Современные проблемы науки и образования. – 2012. – №. 6. – С. 543-543.
- Кофанова, А. С. Карась серебряный как индикатор состояния акваторий, подвергнутых деструктивному влиянию мегаполиса / А. С. Кофанова, И. В. Перминов, В. И. Лошенко и др. // Актуальные проблемы биологической и химической экологии: Материалы VII Международной научно-практической конференции. – Москва: МГОУ, 2021. – С. 187-191.
- Крюков, В. Ю. Иммуносупрессия насекомых ядом паразитоида Habrobracon hebetor увеличивает чувствительность метода выделения энтомопатогенных грибов из почв / В. Ю. Крюков, М. В. Тюрин, О. Г. Томилова, О. Н. Ярославцева, Н. А. Крюкова, Б. А. Дуйсембеков, Ю. С. Токарев, В. В. Глупов // Известия Российской академии наук. Серия биологическая. – 2017. – № 4. – С. 401-405.
- Лошенко, В. И. Экспериментальное обоснование роли активных метаболитов кислорода в формировании экотоксичности в акватории приплотинного участка гидроэлектростанции / В. И. Лошенко, А. В. Сахаров, А. Е. Просенко, Е. И. Рябчикова // Современные проблемы науки и образования. – 2014. – №. 5. – С. 589-589.
- Меньщикова, Е. Б. Окислительный стресс. Прооксиданты и антиоксиданты. / Е. Б. Меньщикова, В. З. Ланкин, Н. К. Зенков и др. – М: Фирма «Слово», 2006. – 556 с.
- Павлов, Д. А., Изменчивость Upeneus tragula (Mullidae): цветовые морфы острова Том (Сиамский залив, Южно-Китайское море) / Д. А. Павлов, Н. Г. Емельянова // Вопросы ихтиологии. – 2018. – Т. 58. – №. 3. – С. 331-341.
- Петухов, С. Ю. Исследование разнообразия окраски обыкновенного окуня Perca fluviatilis в разнотипных водоёмах Байкальского региона / С. Ю. Петухов, Ю. П. Толмачева // Вопросы ихтиологии. – 2015. – Т. 55. – №. 6. – С. 734-734.
- Праздников, Д. В. Роль гетерохроний в формировании разнообразия окрасок костистых рыб: экспериментальные данные на примере цихловых рыб (Сichlidae: perciformes) / Д. В. Праздников, Ф. Н. Шкиль // Биологическое разнообразие: изучение, сохранение, восстановление, рациональное использование. – 2018. – С. 32-35.
- Park, J. J. Stratified mucinproducing intraepithelial lesions of the cervix: adenosquamous or columnar cell neoplasia? / J. J. Park, D. Sun, B. J. Quade, C. Flynn, E. E. Sheets, A. Yang, F. McKeon, C. P. Crum // The American journal of surgical pathology. – 2000. – Т. 24. – №. 10. – P. 1414-1419.
- Romero-Graillet, C. Nitric oxide produced by ultraviolet-irradiated keratinocytes stimulates melanogenesis / C. Romero-Graillet, E. Aberdam, M. Clement, J. P. Ortonne, R. Ballotti // The Journal of clinical investigation. – 1997. – Т. 99. – №. 4. – P. 635-642.
- Sichel, G. Relationship between melanin content and superoxide dismutase (SOD) activity in the liver of various species of animals / G. Sichel, C. Corsaro, M. Scalia, S. Sciuto, E. Geremia // Cell Biochemistry and Function. – 1987. – Т. 5. – №. 2. – P. 123-128.
- Söderhäll, K. Prophenoloxydase activating system and melanization / K. Söderhäll // Developmental and comparative immunology. – 1982. – Vol. 6. – № 4. – P. 601-611.


