Метаболомное исследование гликоалкалоидов методом тандемной масс-спектрометрии в восьми сортах цветного картофеля Solanum tuberosum L
Автор: Разгонова Майя Петровна, Куликова Валентина Ивановна, Ходаева Вера Петровна, Захаренко Александр Михайлович, Голохваст Кирилл Сергеевич
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Агрономия
Статья в выпуске: 2, 2023 года.
Бесплатный доступ
Цель - метаболомное исследование гликоалкалоидов методом тандемной масс-спектрометрии в восьми сортах цветного картофеля. В данной работе исследуются экстракты цветного картофеля, селекционные образцы которого получены из Сибирского федерального научного центра агробиотехнологий РАН, на предмет присутствия разнообразия гликоалкалоидов. Использовано восемь сортообразцов: Тулеевский, Кузнечанка, Памяти Антошкиной, Томичка, Гибрид 15/F-2-13, Гибрид 22103-10, Гибрид 17-5/6-11, Синильга. Гликоалкалоиды представляют собой растительные метаболиты, содержащие олигосахарид, стероид С27 и гетероциклический компонент азота. Первоначальный скрининг методом ВЭЖХ-МС показал, что среди сотен соединений, обнаруженных в клубнях, состав гликоалкалоидов был особенно разнообразным. Картофельные гликоалкалоиды можно разделить на два основных класса: соланидановые или спиросолановые агликоны. Считается, что соланин и чаконин составляют более 90 % от общего количества гликоалкалоидов одомашненного картофеля, при этом чаконина часто больше, чем соланина. Методом тандемной масс-спектрометрии (высокоэффективная жидкостная экстракция и ионная ловушка BRUKER DALTONIKS) проанализированы экстракты данных сортообразцов на присутствие в них соединений из семейства гликоалкалоидов. Результаты исследования показали присутствие 22 гликоалкалоидов в предложенных сортообразцах, некоторые из выявленных гликоалкалоидов пока не описаны в мировой научной литературе.
Вэжх-mс/mс, тандемная масс-спектрометрия, картофель, гликоалкалоиды
Короткий адрес: https://sciup.org/140297966
IDR: 140297966 | УДК: 633.491:631.53 | DOI: 10.36718/1819-4036-2023-2-81-87
Metabolic research of glycoalkaloids by tandem mass spectrometry in eight varieties of colored potatoes Solanum tuberosum L
The purpose of research is a metabolomic study of glycoalkaloids by tandem mass spectrometry in eight varieties of colored potatoes. In this work, extracts of colored potatoes, the breeding samples of which were obtained from the Siberian Federal Scientific Center for Agrobiotechnologies of the Russian Academy of Sciences, are studied for the presence of a variety of glycoalkaloids. Eight varieties were used: Tuleevskij, Kuznechanka, Pamyati Antoshkinoj, Tomichka, Hybrid 15/F-2-13, Hybrid 22103-10, Hybrid 17-5/6-11, Sinilga. Glycoalkaloids are plant metabolites containing an oligosaccharide, a C27 steroid, and a heterocyclic nitrogen component. Initial screening by HPLC-MS showed that among the hundreds of compounds found in tubers, the composition of glycoalkaloids was particularly diverse. Potato glycoalkaloids can be divided into two main classes: solanidane or spirosolan aglycones. It is believed that solanine and chaconine make up more than 90 % of the total glycoalkaloids of domesticated potatoes, with chaconine often more than solanine. Using tandem mass spectrometry (high-performance liquid extraction and BRUKER DALTONIKS ion trap), extracts of these varieties were analyzed for the presence of compounds from the glycoalkaloids family. The results of the study showed the presence of 22 glycoalkaloids in the proposed varieties, some of the identified glycoalkaloids have not yet been described in the world scientific literature.
Текст научной статьи Метаболомное исследование гликоалкалоидов методом тандемной масс-спектрометрии в восьми сортах цветного картофеля Solanum tuberosum L
Acknowledgments : the work has been carried out according to the research plan of the FSBRI Federal Research Center N.I. Vavilov All-Russian Institute of Plant Genetic Resources according to R&D (RK) Collection of vegetatively propagated crops (potatoes, fruits, berries, grapes) and their wild relatives VIR – study and rational use No. 0662-2019-0004".
Введение. Зародышевая плазма картофеля характеризуется обширным генетическим разнообразием, включающим около 200 диких видов, обитающих в чрезвычайно разнообразных местообитаниях по всей Америке [1]. Однако лишь небольшая часть этого генетического разнообразия была включена в выведение современных сортов картофеля, что привело к очень узкому генетическому коридору. Следовательно, дикие виды представляют собой в значительной степени неиспользованный ресурс, который, вероятно, содержит много новых генов, полезных для улучшения свойств одомашненного картофеля. Относительно мало известно о степени разнообразия метаболитов, присутствующих в зародышевой плазме картофеля. Методы метаболомного исследования дают возможность понять изобилие и разнообразие по-лифенольного состава и соединений других классов в растениях. Было показано, что методы метаболомного исследования нескольких сортов картофеля с помощью ГХ-МС и ВЭЖХ-МС/МС являются эффективным инструментом исследования [2, 3].
Предварительный анализ семи генотипов в исследовании [4] показал, что гликоалкалоиды являются большим источником разнообразия метаболитов. Гликоалкалоиды представляют собой растительные метаболиты, содержащие олигосахарид, стероид С27 и гетероциклический компонент азота. Считается, что соланин и чако-нин составляют более 90 % от общего количества гликоалкалоидов одомашненного картофеля, при этом чаконина часто больше, чем соланина.
Пути биосинтеза гликоалкалоидов не полностью очерчены, даже для основных гликоалкалоидов картофеля, соланина и чаконина. Гликоалкалоиды, полученные из мевалонатного пути через холестерин, встречаются по всему клубню, но в основном синтезируются в феллодерме [5]. На удивление мало известно о генах и энзимологии, участвующих в превращении холестерина в различные гликоалкалоиды. Идентификация генов биосинтеза гликоалкалоидов позволила использовать трансгенные подходы к снижению содержания гликоалкалоидов в картофеле, поскольку гликоалкалоиды обычно считаются антипитательными соединениями [6]. Карто- фель со сверхэкспрессией стеролметилтранс-феразы сои показал снижение количества как холестерина, так и гликоалкалоидов [7].
Первоначальный скрининг методом ВЭЖХ-МС показал, что среди сотен соединений, обнаруженных в клубнях, состав гликоалкалоидов был особенно разнообразным. Картофельные гликоалкалоиды можно разделить на два основных класса: соланидановые или спиросола-новые агликоны, в связи с этим исследование [8] было сосредоточено на соланидиновых или соланиданоподобных гликоалкалоидах.
В данном исследовании был использован метод тандемной масс-спектрометрии для определения метаболомного профиля присутствующих гликоалкалоидов в восьми сортах цветного картофеля, выращенного Сибирским федеральным научным центром агробиотехнологий (Краснообск Новосибирской области) Российской академии наук. Внешний вид сортов цветного картофеля Гибрид 15/F-2-13 и Синиль-га из Сибирского федерального научного центра агробиотехнологий представлен на рисунке 1.

А B
Рис.1. Внешний вид сортов цветного картофеля: A – Гибрид 15/F-2-13; B – Синильга
Цель исследования – метаболомное исследование гликоалкалоидов методом тандемной масс-спектрометрии в восьми сортах цветного картофеля Solanum Tuberosum L.
Объекты и методы. Объектом исследования являлись восемь сортов сибирского цветного картофеля S. tuberosum, полученные методом селекционного отбора из Сибирского федерального научного центра агробиотехнологий Россий- ской академии наук. Это сорта: Тулеевский, Куз-нечанка, Памяти Антошкиной, Томичка, Гибрид 15/F-2-13, Гибрид 22103-10, Гибрид 17-5/6-11, Синильга. Картофель был собран на полях Сибирского федерального научного центра агробиотехнологий РАН в конце сентября 2020 г.
Для получения высококонцентрированных экстрактов применяли фракционную мацерацию. При этом общее количество экстрагента (спирт метиловый ХЧ) делили на 3 части и последовательно настаивали на картофеле первую часть, затем вторую и третью. Время настаивания каждой части экстрагента составило 7 сут.
Для выполнения разделения многокомпонентных смесей использовался жидкостный хроматограф высокого давления Shimadzu LC-20 Prominence HPLC (Shimadzu, Япония), оборудованный UV-детектором и обратнофазной колонкой Shodex ODP-40 4E. Программа элюции градиента следующая: 0,0 – 4 мин, 100 % CH 3 CN; 4 – 60 мин, 100 % – 25 % CH 3 CN; 60 – 75 мин, 25 % – 0 % CH 3 CN; контрольная промывка 75– 120 мин 0 % CH 3 CN. Весь ВЭЖХ-анализ сделан с UV-VIS-детектором SPD-20A (Kanda-Nishikicho 1-chrome, Shimadzu, Chiyoda-ku, Токио, Япония) при длинах волн 230 и 330 r/м ; температура 17 °С. Объем впрыска составлял 1 мл.
Масс-спектрометрические данные получены с помощью ионной ловушки amaZon SL (производство фирмы «BRUKER DALTONIKS», Германия), оснащенной источником ионизации электрораспылением ESI в режимах отрицательных и положительных ионов. Оптимизированные параметры получены следующим образом: температура источника ионизации – 70 °С, поток газа – 4 л/мин, газ-небилайзер (распылитель) – 7,3 psi; капиллярное напряжение – 4500 V; напряжение на изгибе торцевой пластины – 1500 V; фрагментатор – 280 V; энергия столкновения – 60 eV. Масс-спектрометр использовался в диапазоне сканирования m/z 100 – 1,700 для MС и МС/МС.
Результаты и их обсуждение. Для экспериментальных исследований были отобраны восемь наиболее эффективных сортов, полученных методом селекционного отбора из Сибирского федерального научного центра агробиотехнологий Российской академии наук. Это сорта: Тулеевский, Кузнечанка, Памяти Антошкиной, Томичка, Гибрид 15/F-2-13, Гибрид 22103-10, Гибрид 17-5/6-11, Синильга. Картофель был собран на полях в конце сентября 2020 г.
Данные масс-спектрометрии высокой точности регистрировали на ионной ловушке amaZon SL BRUKER DALTONIKS, оснащенной источником ESI в режиме отрицательных и положительных ионов. Реализован четырехступенчатый режим разделения ионов (режим МС/МС). Все химические профили образцов были получены методом ВЭЖХ – ESI – MS/MS. Сочетание обоих режимов ионизации (положительного и отрицательного) в режиме полного сканирования МС дает дополнительную достоверность определения молекулярной массы (рис. 2.). Данное сочетание режимов ионизации обеспечивает самую высокую чувствительность и приводит к ограниченной фрагментации, что делает этот метод наиболее подходящим для определения молекулярной массы разделяемых гликоалкалоидов, особенно в случаях, когда концентрация низкая. Идентификация производилась путем сравнения значений m/z, RT и моделей фрагментации со спектральными данными MS2, взятыми из научной литературы, или путем поиска в базах данных (MS2T, MassBank, HMDB).
Полученные масс-спектрометрические данные позволяют составить подробную таблицу присутствия и относительной скорости ионизации идентифицированных соединений у разных сортов сибирского картофеля S. tuberosum (табл.). Примененный в жидкостной хроматографии градиент замещения ацетонитрила водой позволил расщепить все стероидные алка-лоиды-гликозиды за достаточно короткое время.
I $2
ф
|
2 о 1— |
О co 05 OO О LO CO OO т— |
OO о CXI LO |
OO 3 LO CO CD CXI |
CXI 05 LO CD 05 CD |
CXI CXI LO 05 CD CO т— |
CD CD CD CXI |
||||||||||||||||
|
LO Cl KO 1_______ |
CXI LO 05 CD CO CO OO |
CO LO 05 CO 05 CXI т— |
CO LO 05 CO 05 CXI т— |
CO LO 05 CO 05 CXI т— |
CO LO 05 CO 05 CXI т— |
CD CD CD 05 CD т— |
||||||||||||||||
|
о о CXI CXI Cl x KO x 1_______ |
LO СО CXI LO CO о co |
СХ| т— СО LO СО со |
т— CXI о ? OO |
CO 05 CO LO CO 3 co |
T- 3 OO т— LO т— |
OO OO co CD CD т— |
OO OO co CD CD т— |
OO OO co CD CD т— |
CD т— CO 05 LO |
05 CXI CO OO т— |
CO 05 3 |
CO LO CO |
CD 3 |
|||||||||
|
co ^ LO Cl x KO |
о о о Т- со LO |
О О О СО СХ| ОО |
co 05 О CXI CXI co CXI |
co LO CXI co т— CO 05 |
CO LO CO LO CXI |
CO LO CO LO CXI |
CD CD CD CD LO |
|||||||||||||||
|
2 q x о |
LO со со СХ| 3 |
о co о о T- CXI |
CO LO CO OO о |
CXI LO CD CXI CO LO LO |
LO CD т— 05 CD CO |
LO CD т— 05 CD CO |
co 05 CXI т— CO LO CXI |
CO 05 CXI т— CO LO CXI |
CO 05 CXI т— CO LO CXI |
OO co co CXI |
CXI 3 co CXI LO |
cxi 05 co 05 T- |
||||||||||
|
2 (U CD X co ^ |
со LO о о ОО о LO Т- |
со 05 05 СО LO т— |
CXI LO CXI LO OO LO О CXI |
CXI LO LO OO 05 LO CO |
OO CXI 05 CD CXI CD N т— |
LO CO CXI co co |
OO CXI 05 CD CXI CD N т— |
CD CD CD CXI т— |
CD CD CD OO |
CD CD CD 05 |
||||||||||||
|
О X X £ s < |
со LO о LO 05 |
о о CXI 05 О CO |
OO 05 OO |
05 CXI CD 05 CO |
OO CXI LO CO OO co |
3 LO CD т— |
CXI OO co CD CXI LO |
CD CD CD т— |
т— CXI CD |
co CD CO CD CO CXI |
||||||||||||
|
CD CD |
о со 05 о Т- |
СО ОО со |
CO LO OO LO о co T- CXI |
T- 3 LO co |
т— О о CXI о co |
CO LO LO 05 CXI |
CO LO CD т— 3 3 T- |
CO LO CD т— 3 3 T- |
CO co co CXI co OO co |
|||||||||||||
|
DC О 5. ¥ s s Э |
о т (XI о |
о Z т см о |
ОО о Z £ см о |
о co ZE СП о |
о co ZE CO о |
о z ZE co cJ |
О ZE LO cJ |
LO о z ZE LO cJ |
LO О z ZE LO cJ |
LO О z ZE LO cJ |
LO О ZE LO cJ |
LO о ZE LO cJ |
LO О ZE LO cJ |
LO о ZE LO cJ |
co о z ZE LO cJ |
co о ZE LO cJ |
co о ZE LO cJ |
co о z LO ZE LO cJ |
co о z ZE LO cJ |
co о z LO ZE CO cJ |
о z co ZE LO cJ |
OO о z CO ZE CO cJ |
|
CD Cl CD О О О 05 5 |
CD С Ъ с 05 О О |
"о "со Е о 1— |
СЕ X О 2 05 g Е >х X 1— CD CD m CO X CD ZE |
CD C c о CD 05 CD -2 о СП |
Cl X О 2 05 2 E >x X 1— CD CD m CO X CD ZE |
CD C c о CD 05 CD 2 "O X CD Q |
CD C c о CD 05 X CD 05 X CD. < |
CD CD О "о CD 05 xz CD "o 2 TD 05 C 05 О GO |
CD CD О О CD CD 2 Ъ 05 C 05 О GO |
CD CD О "о CD 05 CD CD C О CD c 05 О GO |
CD C c 05 О CD 05 xz CD < |
CD C c Q CD _l |
CD CD О "о CD 05 xz CD "o cz CD 'cz 05 О CD |
CD CD О О CD CD CZ 2 Ъ 05 'cz 05 О CD |
CD CD О О CD "о CZ 2 Ъ 05 'cz 05 О CD |
CD C c Q. CD _l |
CD CD О О CD "о CZ CD 'cz 05 О CD |
СЕ s о 2 05 g s E >x X 1— CD CD m CO s CD ZE |
er s о 2 05 2 s E >x X 1— CD CD m CO s CD ZE |
d s о 2 05 2 s E >x X 1— CD CD m CO s CD ZE |
CE s о 2 05 2 s E >x X 1— CD CD m CO s CD ZE |
CE s о 2 05 2 s E >x X 1— CD CD m CO s CD ZE |
Разрешение отдельных пиков стероидных алкалоидных гликозидов в применяемом градиенте жидкостной хроматографии было удовлетворительным, и идентификация соединений на основе зарегистрированных масс-спектров была од- нозначной. В экстрактах в качестве основных гликоалкалоидных компонентов идентифицированы α-чаконин и α-соланин, их пики легко распознавались в суммарном ионном токе (рис. 2, 3).
Intens. x10 7
x10 07
x10 05
x10 05
0.5
0.0
1+ 868.41
PotatoTuleevsky MeOH #2_-1_01_849.d: +MS, 32.1min #1195
1+ 2+
297.40 445.67
1+ 398.26
1+ 706.32
1+ 560.33
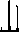
1+ 851.39
PotatoTuleevsky MeOH #2_-1_01_849.d: +MS2(868.41), 32.1min #1196
PotatoTuleevsky MeOH #2_-1_01_849.d: +MS3(868.41->398.26), 32.2min #1200
15 1 7 + .04 1+
253.19
327.22 о

312.27
706.40
PotatoTuleevsky MeOH #2_-1_01_849.d: +MS4(868.41->398.26->327.22), 32.3min #1204
150.13
204.13
1400 1600
1800 m/z
Рис. 2. Масс-спектр α -соланина из экстракта S. Tuberosum (сорт Тулеевский), m/z 868.41
Intens. x108
0.5
x100.07
x1007
1.0
0.5
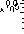
ОАА
^™
PotatoTuleevsky MeOH #2_-1_01_849.d: +MS, 32.6min #1217
PotatoTuleevsky MeOH #2_-1_01_849.d: +MS2(852.41), 32.7min #1219
PotatoTuleevsky MeOH #2_-1_01_849.d: +MS3(852.41->706.40), 32.8min #1223
PotatoTuleevsky MeOH #2_-1_01_849.d: +MS4(852.41->706.40->560.32), 32.9min #1227
л ДАА
.ААА
Рис. 3. Масс-спектр α -чаконина из экстракта of S. Tuberosum (сорт Тулеевский), m/z 852.41
Заключение. Научные исследования, представленные в данной работе, показали присутствие большой разновариантности гликоалкалоидов в сортах сибирского цветного картофеля S. tuberosum L. Это сорта: Тулеевский, Кузнечан-ка, Памяти Антошкиной, Томичка, Гибрид 15/F-2-13, Гибрид 22103-10, Гибрид 17-5/6-11, Синильга. Все селекционные образцы получены в Сибирском федеральном научном центре агробиотехнологий Российской академии наук. Для идентифицирования целевых аналитов из экстрактов картофеля была использована тандемная масс-спектрометрия (высокоэффективная жидкостная экстракция в соединении с ионной ловушкой BRUKER DALTONIKS). Данный метод позволил идентифицировать 22 соединения, относящихся к группе гликоалкалоидов.
Список литературы Метаболомное исследование гликоалкалоидов методом тандемной масс-спектрометрии в восьми сортах цветного картофеля Solanum tuberosum L
- Spooner D.M., Hijmans R.J. Potato systematics and germplasm collecting, 1989-2000 // Am. J. Potato Res. 2001. T. 78. P. 237-268.
- Roessner U., Willmitzer L., Fernie A.R. High-resolution metabolic phenotyping of genetically and environmentally diverse potato tuber systems. Identification of phenocopies // Plant Physiol. 2001. T. 127. P. 749-764.
- Monitoring changes in anthocyanin and steroid alkaloid glycoside content in lines of transgenic potato plants using liquid chromatography/mass spectrometry / M. Stobiecki [et al.] // Phytochem. 2003. T. 62. P. 959-969.
- Griffiths D.W., Bain H., Dale M.F.B. The effect of low-temperature storage on the glycoalkaloid content of potato (Solanum tuberosum) tubers // J. Sci. Food Agric. 1997. T. 74. P. 301-307.
- Krits P., Fogelman E., Ginzberg I. Potato steroidal glycoalkaloid levels and the expression of key isoprenoid metabolic genes // Planta. 2007. T. 227. P. 143-150.
- Shakya R., Navarre D.A. LC-MS Analysis of Solanidane Glycoalkaloid Diversity among Tubers of Four Wild Potato Species and Three Cultivars (Solanum tuberosum) // J. Agric. Food Chem. 2008. T. 56. P. 6949-6958.
- Reduction of cholesterol and glycoalkaloid levels in transgenic potato plants by overexpression of a type 1 sterol methyltransferase cDNA / L. Arnqvist [et al.] // Plant Physiol. 2003. T. 131. P. 1792-1799.
- Friedman M., McDonald G.M. Potato glycoalkaloids: chemistry, analysis, safety, and plant physiology. Crit. ReV // Plant Sci. 1997. T. 16. P. 55-132.


