Металл-аффинная хроматография. Основы и применение
Автор: Кельциева Ольга Александровна, Гладилович В.Д., Подольская Е.П.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Хроматография, ПЦР-, ДНК-анализ
Статья в выпуске: 1 т.23, 2013 года.
Бесплатный доступ
В обзоре рассмотрен принцип действия и основные возможности применения металл-аффинной хроматографии, которые включают в себя очистку гистидин-меченных белков, металл-связывающих белков, нуклеотидов и антител. Описаны преимущества и недостатки как самого метода, так и различных сорбентов.
Металл-аффинная хроматография, металл-аффинные сорбенты, очистка белков, фосфопротеомика
Короткий адрес: https://sciup.org/14264847
IDR: 14264847 | УДК: 543.544.414
Immobilized metal ion affinity chromatography (IMAC). Principle and applications
This article reviews the basic principle of operation and the possibility of using immobilized metal affinity chromatography which include cleaning of histidine-tagged proteins, metal-binding proteins and antibodies. The advantages and disadvantages of this method and various sorbents are described.
Текст обзорной статьи Металл-аффинная хроматография. Основы и применение
В последние годы активное развитие получают высокоспецифичные и высокоселективные методы выделения органических и биоорганических соединений из биологических образцов и объектов окружающей среды. В первую очередь к таким методам можно отнести металл-аффинную хроматографию (МАХ, IMAC — immobilized-metal affinity chromatography). В научной литературе на русском языке используют также названия: металлхе-латная, или лигандобменная хроматография. В основе этого хроматографического метода лежит различное сродство органических соединений к ионам некоторых металлов. Ионы, в большинстве случаев это — ионы металлов, хелатируют поли-дентантными лигандами, иммобилизованными на вспомогательной подложке (силикагель, агароза, сефароза, сшитый сополимер полистирола и диви-нилбензола).
Концепция металл-аффинной хроматографии была впервые сформулирована и представлена Поратом [1]. Она была основана на известном сродстве ионов переходных металлов, таких как Zn2+, Cu2+, Ni2+ и Co2+ к гистидину и цистеину в водных растворах. Впоследствии появилась идея использовать прочно зафиксированные ионы металлов для фракционирования белков. Реакция образования комплекса иона металла и некоторых функциональных групп (например, фосфатных групп) органических молекул, как правило, обратима. Следовательно, иммобилизованные ионы металлов можно использовать как сорбент. Взаимодействие между сорбентом и аналитом pH-зависимое, поэтому связанные вещества можно элюировать, изменяя рН, уменьшая ионную силу буфера или используя другие хелатирующие агенты, такие как ЭДТА или имидазол.
Одним из самых известных приложений МАХ является очистка гистидин-меченных белков(His).
В последнее время наблюдается увеличение применения МАХ при проведении предварительной обработки образца для обнаружения наркотиков, таких как тетрациклины, фторхинолоны, макролиды, β-лактамы, аминогликозиды [2]; при пробо-подготовке для выявления биомаркеров в сыворотке крови, моче и тканях для диагностики заболеваний с последующим применением методов масс-спектрометрии [3, 4].
ПРИНЦИП ДЕЙСТВИЯ МЕТОДА МЕТАЛЛ-АФФИННОЙ ХРОМАТОГРАФИИ
Ионы металлов чаще всего классифицируются согласно теории ЖКМО (Жестких кислот мягких оснований) Пирсона [5]. Жесткие кислоты (например, ионы Fe3+, Ca2+, Al3+) легче всего координируют кислород и фтор функциональных групп, мягкие кислоты (ионы Cu+, Hg+, Ag+) — серу. Промежуточные по жесткости (Cu2+, Ni2+, Zn2+, Co2+) — азот, кислород и серу. Селективность жестких и промежуточных ионов различна: при оптимальном для их связывания рН (кислом и нейтральном соответственно) они координируются с разными функциональными группами. Такие группы могут содержаться в белках и нуклеиновых кислотах. "Мишенями" жестких кислот могут являться аспарагиновая и глутаминовая кислоты, тирозин или фосфорилированные серин, треонин или тирозин.
Адсорбция белков и пептидов методом МАХ основана на обратимом взаимодействии между аминокислотами, выступающими в качестве доноров электронов, и ионами металла, хелатированными лигандами, которые иммобилизованы на поверхности твердого носителя [5]. Несмотря на значительное количество аминокислот, которые могут участвовать в процессе связывания (в том числе глицин, аргинин, лизин, тирозин, гистидин, цистеин, аспарагиновая кислота), фактически сорбция белка определяется наличием гистидина.
Наиболее часто используемыми при приготовлении металл-аффинных сорбентов являются ионы переходных металлов. Электрон-доноры (N, S и O) в хелатирующих соединениях могут координировать ионы металлов с получением металл-хелатов в диапазоне от бидентатных до пентаден-татных соединений в зависимости от числа занятых координационных связей.
Были разработаны различные подложки для МАХ. Традиционно в качестве подложки использовался мягкий гель, такой как агароза. Полисаха- риды, например целлюлоза, обладают преимуществом из-за хорошей биологической совместимости. Но они демонстрируют низкую механическую прочность и, следовательно, не могут быть использованы в системах высокого давления. Напротив, неорганическая матрица, такая как диоксид кремния, обладает превосходными механическими свойствами, но имеет недостаток в виде необратимой неспецифической сорбции белков [6].
Основной механизм взаимодействия His-меченных белков с иммобилизованным ионом металла представлен на рисунке.
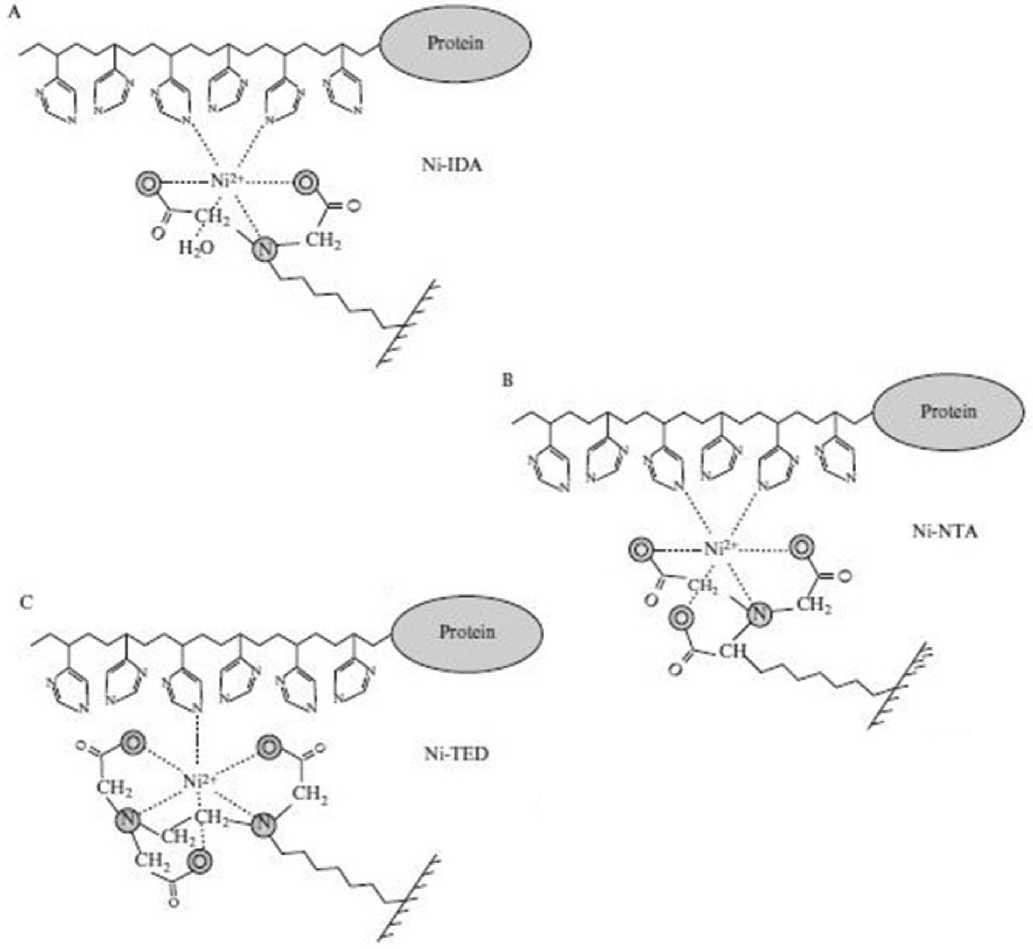
Модель взаимодействия между остатками гистидина и ионами металлов в три-(IDA), тетра-(NTA) и пентадентатных IMAC лигандах (TED) [5]
Такой лиганд, как нитрилотриуксусная кислота (nitrilotriacetic acid, NTA), удерживает ион Ni2+ четырьмя валентностями (рис., В), и две валентности иона металла доступны для взаимодействия с кольцами имидазола гистидиновых остатков. Это соотношение оказалось наиболее эффективным для очистки гистидин-меченных белков. Другой тетрадентатный лиганд — карбоксиметиласпартат [7], имеющийся в продаже как кобальтсодержащая смола Talon [http://www.clontech. com/]. В отличие от тетрадентатных лигандов иминодиуксусная кислота (iminodiacetic acid, IDA) координирует двухвалентные ионы тремя валентностями (рис., A), оставляя третью валентность иона металла свободной для взаимодействия с кольцом имидазола, хотя неясно, будет ли имидазол иметь пространственную возможность участвовать во взаимодействии.
По всей видимости, координационное число играет важную роль в отношении качества очищения белковых фракций. Степень очистки белка с применением IDA и NTA-матриц, как правило, дает различный результат, поскольку часто наблюдается сильное выщелачивание ионов металлов из IDA-лигандов по сравнению с NTA [5]. Самое низкое выщелачивание металлов показано при использовании пентадентатного лиганда, который координирует ионы особенно сильно (рис., С).
Как было указано выше, выбор металла для МАХ зависит от структуры анализируемых соединений. Наряду с тем что трехвалентные катионы, такие как Al3+, Ga3+ и Fe3+ [8, 9], или четырехвалентный Zr4+ предпочтительны для сорбции фосфорсодержащих белков и пептидов, двухвалентные ионы Cu2+, Ni2+, Zn2+ и Co2+ используют для очистки гистидин-меченных белков. Комбинация тетрадентатного лиганда, который обеспечивает сильное связывание, и иона металла, который оставляет два координационных сайта свободными для взаимодействия с биополимерами (Ni2+, Co2+), получила наиболее широкое признание и приводит к высокой степени извлечения и чистоте выделенного белка.
Металл-аффинные сорбенты могут быть как на основе хелатированных лигандами ионов металлов, так и нанесены на функциональные поверхности, например чипы, в методе SELDI (активированная поверхностью лазерная десорбция / ионизация). Методы на основе чипов (например, поверхностный плазмонный резонанс (SPR)) позволяют иммобилизовать His-меченные белки (белки, меченные гистидиновым остатком-тэгом) для количественных и кинетических исследований. Кроме того, МАХ была использована на этапе ингибитора истощения до ПЦР-амплификации нуклеиновых кислот из сложных образцов, таких как кровь, в технологии, названной Chelex [1]. Были предложены и методы МАХ для профилирования протеома на основе чипов [10], и эти методы используют в качестве инструмента в клинической практике обследования на наличие фосфатных групп и гистидин-содержащих белков и пептидов (SELDI).
Наиболее важные из многочисленных приложений металл-аффинной хроматографии будут рассмотрены далее.
ПРИМЕНЕНИЕ МЕТАЛЛ-АФФИННОЙ ХРОМАТОГРАФИИ ДЛЯ ОЧИСТКИ БЕЛКОВ
Изначально разработанная для очистки нативных белков [1] МАХ оказалась технологией с очень широким спектром применения, в том числе в случае хроматографического очищения: возможность метода позволяет очищать наиболее распространенные металлопротеины, антитела, фосфорилированные и рекомбинантные His-меченные белки. В попытке использовать специфичность и высокое сродство His-меченных белков к иммобилизованным ионам металлов металл-аффинные лиганды были применены для изучения белок-белковых взаимодействий, где белки должны быть стабильно иммобилизованы на поверхности. В качестве примера приведем ниже два приложения этого подхода: ELISA (иммунофермент-ный анализ) — в качестве диагностического инструмента, и технологии на основе чипов для функциональных исследований.
Одной из наиболее важных областей применения МАХ является очистка рекомбинантных белков вследствие относительно высокого сродства и специфичности некоторых металлов к эпитопу, содержащему шесть или более остатков гистидина. Даже один шаг очистки в большинстве случаев приводит к той степени чистоты препарата белка, которая достаточна для решения наиболее распространенных задач в биохимии. Структура меченного конца, т. е. его положение, последовательность и длина, может влиять на процесс производства белка на нескольких стадиях: скорость экспрессии, доступность для привязки к металл-аффиному сорбенту, образование трехмерной белковой структуры, формирование белковых кристаллов и в меньшей степени на растворимость и активность. Наиболее распространенная форма His-конца состоит из шести последовательных остатков гистидина (Н 6 ), которые связываются с металлами достаточно хорошо, чтобы сместить равновесие ассоциации / диссоциации больше в сторону ассоциации, ведущей к стабильному связыванию в большинстве случаев [11].
Есть несколько преимуществ применения ме-талл-аффинной хроматографии для очистки His-меченных белков по сравнению с другими видами аффинной хроматографии [12]. Кроме простоты и низкой стоимости использования наиболее поразительной особенностью является надежность МАХ:
-
• метод работает как в нативных, так и денатурирующих условиях, таких как 8 М мочевина или 6 М гуанидингидрохлорид [13], и позволяет осуществлять последовательный рефолдинг на колонке [14];
-
• метод работает в окислительно-восстановительных условиях;
-
• связанные с сорбентом белки способны выдерживать воздействие широкого спектра различных химических веществ;
-
• относительно высокое сродство и специфичность позволяют обеспечивать высокую эффективность сорбции даже при наличии высоких титров белка;
-
• процедуры очистки масштабируемы.
Несмотря на такие преимущества, МАХ имеет свои ограничения. Очевидно, что использования хелатообразователей в анализируемом образце следует избегать, что может быть недостатком, поскольку, например, ЭДТА — мощный ингибитор металлопротеаз — может быть применена только в низких концентрациях. Следует также проявлять осторожность при использовании других потенциально хелатных групп, таких как Трис, соли аммония и некоторые аминокислоты.
До недавнего времени использование сильных восстановителей, таких как дитиотреитол (ДТТ), в металл-аффинном анализе считалось проблематичным из-за вымывания никеля из сорбента, и как следствие подозревалось увеличение концентрации никеля в белковых препаратах. Тем не менее было обнаружено, что умеренные концентрации ДТТ полностью совместимы с очисткой на Ni-NTA [5]. Даже если ДТТ может восстановить ионы никеля, это приведет к изменению цвета смолы, а не к вымыванию лигандов, и смолы, обрабатываемые в восстановительных условиях, могут быть регенерированы и повторно использованы. Эти результаты показывают, что, несмотря на изменение цвета вследствие восстановления никеля ДТТ, сорбент по-прежнему функционирует.
Для того чтобы МАХ приводила к высокой степени очистки за один этап, требуется высокая корреляция количества гистидин-меченного белка-рекомбинанта в образце с количеством металл-аффинного сорбента [15]. Стоит отметить, что существуют белки, проявляющие поверхностные свойства, подходящие для взаимодействия с иммобилизованными ионами металлов, которые могут образовывать связи с сорбентом, хотя их сродство к сорбенту ниже, чем у гистидин-меченных белков. Соответственно избыток сорбента может привести к тому, что препарат будет загрязнен такими белками. Более того, существуют некоторые белки, в которых локальная плотность хелатирующих аминокислот, таких как гистидин, настолько велика, что они практически неизбежно будут связываться с ионами иммобилизованных металлов. Для избавления от соэлюирую-щихся белков или предотвращения их адсорбции существуют несколько процедур:
-
• проводить дополнительные этапы очистки перед МАХ;
-
• подбирать соотношение гистидин-мечен-ного белка и сорбента;
-
• использовать альтернативную подложку;
-
• дополнительно очищать целевой белок после МАХ методом обращенно-фазовой хроматографии.
Дополнительная очистка перед стадией МАХ возможна методами ион-обменной (ИОX) или эксклюзионной хроматографии (ЭХ). ИОХ имеет лучшие возможности разделения, но ЭХ не только способна разделять молекулы по их размерам и помогает отделить совокупность молекул с высокой молекулярной массой, но и может быть использована для обессоливания препарата [16]. Хотя ЭХ-МАХ (в отличие от ИОХ-МАХ) может быть представлена как стандартизованная процедура без учета биохимических свойств белка, таких как диапазон разделения и pI, для ее проведения необходим набор различных ЭХ-колонок. Кроме того, чтобы использовать все возможности этих технологий, требуется дорогостоящее оборудование, в частности автоматизированная хроматографическая система, что часто существенно снижает скорость проведения большого количества параллельных измерений. Аффинную очистку методом МАХ обычно выполняют в режиме связывание— промывка—элюирование. Это позволяет легко ввести второй сорбент в процедуру двухэтапной очистки, приводящей к получению высокоочи-щенного белкового препарата [17].
Повысить чистоту белков при проведении МАХ возможно использованием в качестве матрицы для сорбента покрытых декстраном гранул агарозы, которые составляют материал большинства хроматографических носителей (Sepharoses, Superflow, Agaroses), что предотвращает соэлю-цию белков с выраженной аффинностью к перечисленным матрицам [18]. К недостаткам метода можно отнести коммерческую недоступность дек-стран-покрытых гранул и как следствие необходимость в приготовлении металл-аффинного сорбента в лабораторных условиях. Подложки на основе силикагеля также предотвращают адсорбцию белков с аффинностью к агарозе и, кроме того, обладают хорошей устойчивостью к давлению, что делает их походящими для применения в ВЭЖХ, но силикагелевые смолы часто страдают от низкой связывающей способности и ограниченной устойчивости к высоким значениям рН, что критично при проведении МАХ.
Недавно был разработан новый подход, позволяющий избегать использования твердых хроматографических носителей, получивший название "аффинное осаждение", и было показано, что МАХ также может быть проведена этим методом [19]. Хелатирующий лиганд химически связывается с полимером, который после сорбции гисти-дин-меченного белка агрегирует при изменении внешних условий (рН, температура), после чего вместе с белком может быть осажден центрифугированием. Протокол его использования все еще относительно сложен, но со временем, возможно, данный метод будет широко использован при очищении белков методом МАХ.
МЕТАЛЛ-АФФИННАЯ ХРОМАТОГРАФИЯ В ИММУНОХИМИИ
Сорбент Ni(II)-NTA, лиганды которого иммобилизованы на поверхности луночных планшетов, используют для задерживания His-меченных антигенов в их растворяемой и структурно не поврежденной форме при серологических исследованиях. Иммобилизация с помощью гистидиновых остатков может быть выгодна и удобна для стандартной процедуры иммуноферментного анализа ELISA. В стандартной методике белки-антигены адсорбируются на пластиковых поверхностях планшета случайно, часть активных сайтов присоединения антител (эпитопов белка) маскируется. ELISA с применением металл-аффинного подхода позволяет отбирать конформационно-зависимые моноклональные антитела [20] и проводить иммуносорбцию с повышенной чувствительностью [21].
Иммобилизация His-меченных белков на поверхности чипа для исследования взаимодействия с другими молекулами, например, в методе SPR является широко используемым методом характеризации белка или межбелковых взаимодействий. Фактор устойчивого заякоривания и стабильности на поверхности чипа для плазмонного резонанса может быть важен для снижения утечки молекул белка с поверхности [11, 22]. Существенные улучшения в стабильности функциональной иммобилизации His-меченных белков на стеклянных поверхностях даже при низкой концентрации были достигнуты в соответствии с концепцией мультивалентных хелатирующих головок, где одна молекула лиганда несет три фрагмента NTA (tris-NTA) [23, 24]. Эта разработка позволяет использовать His-меченные белки без маркировки биотином после очистки.
Металл-аффинные лиганды также успешно используют в качестве детектирующего соединения в методе иммуноблоттинга, заменяя дорогостоящие антитела. His-меченные белки, перемещенные в нитроцеллюлозную мембрану, могут быть обнаружены с помощью Ni-NTA, сопряженной со щелочной фосфатазой или с особыми указывающими ферментами [25] по хромогенной или хемилюминесцентной реакции или с квантовыми точками для флуоресцентной детекции [26]. Такой подход представляет собой быструю и экономически выгодную альтернативу реакции обнаружения на основе антител в случаях, когда высокая специфичность антител не требуется. Специфичность обнаружения при использовании сопряженной NTA была увеличена на порядок при использовании tris-NTA [27, 28].
ИСПОЛЬЗОВАНИЕ МЕТАЛЛ-АФФИННОЙ ХРОМАТОГРАФИИ В ПРОТЕОМНЫХ ИССЛЕДОВАНИЯХ
Как было описано выше, МАХ первоначально была разработана как метод разделения металл- и гистидин-содержащих белков [1], но сегодня эти возможности используют и в других протеомных исследованиях, в которых снижение сложности (компонентности) системы является необходимым условием при анализе и идентификации малораспространенных белков. МАХ прочно заняла свое место среди других методов предварительного разделения сложных смесей, таких как жидкостная обращенно-фазовая, ионообменная, аффинная хроматографии и гель-электрофорез [29, 30]. В зависимости от целей и задач в процессе пробо-подготовки МАХ комбинируют с двухмерным гель-электрофорезом при анализе белков или с обращенно-фазовой хроматографией для дополнительного разделения пептидов.
Таким образом, в протеомике металл-аффин-ную хроматографию используют в исследованиях, где фракции клеточного белкового пула обогащают для дальнейшего анализа. Так, например, белки со сродством к металлам могут быть обогащены либо с учетом их способности связываться с определенным иммобилизованным ионом металла (например, Me2+-NTA), либо путем связывания иона металла с белком (Ме2+-белок) на незаряженном металл-аффинном лиганде (например, NTA) [31, 32]. В качестве ионов, пригодных для металл-аффинного анализа металло-протеома, чаще всего используют Cu2+, Ni2+, Zn2+.
Также этот метод может быть использован для связывания и разделения моно- и динуклеотидов за счет сложного явления, объясняемого дифференциальным взаимодействием потенциальных сайтов связывания — кислорода в фосфатной группе, азота и кислорода на азотистых основаниях, гидроксильных групп в рибозе с иммобилизованным металлом [33].
Совершенно иным представляется применение МАХ для очищения антител, основанное на сродстве последних к ионам металлов. Молекулярные основы такого взаимодействия металл-содержащих сайтов на тяжелой цепи были рассмотрены авторами [34]. Об адсорбции иммуноглобулинов из различных образцов на металл-аффинных сорбентах сообщалось многими авторами (humanized murine IgG [34], человеческий IgG [35], козий IgG [36]). Очистка антител успешно осуществляется с помощью различных форматов МАХ, включая гели [34, 37], полиметакрилат [38] и мембранные полые волокна (Cu2+, Ni2+, Zn2+, Co2+) [39]. Мягкий способ элюирования белка солями, низкая стоимость и высокая надежность металл-аффинных сорбентов определенно способствовали увеличению популярности этого метода по сравнению с традиционными подходами [39].
Однако на сегодняшний день основным приложением МАХ является фосфопротеомика [31]. Обратимое фосфорилирование белков по остаткам серина, треонина и тирозина имеет важное биологическое значение. Как правило, ферментативное фосфорилирование /дефосфорилирование клеточных белков контролирует ключевые внутриклеточные процессы, связанные с делением, дифференцировкой или гибелью клеток. Направление протеомики, которое занимается анализом таких посттрансляционных модификаций белков, как фосфорилирование, получило название "фосфопротеомика". Активно развиваемая отрасль подобных исследований — изучение пула модифицированных белков при различных клеточных состояниях и в различных субклеточных компарт-ментах позволяет вычленять ключевое событие в каскаде фосфорилирований /дефосфорилирований.
Металл-аффинная хроматография была предложена как простой, экономичный и универсальный метод выделения различных типов фосфорилированных пептидов [23, 41, 42] и быстро нашла свое применение в исследованиях фосфопротеома [43, 44]. Как было указано выше, самыми распространенными хелатирующими лигандами в ме-талл-аффинных сорбентах являются нитрилотри-уксусная (NTA) и иминодиуксусная (IDA) кислоты. Эти кислоты хелатируют ионы Ni2+, Zn2+, Fe3+, Ga3+ и др. [41, 45–47], при этом свободные орбитали атомов металлов способны участвовать в координационном взаимодействии с отрицательно заряженными пептидами, в частности с фосфорилированными пептидами. Было отмечено, что сорбент на основе Fe3+-NTA показывает более высокую селективность к фосфопептидам по сравнению с Fe3+-IDA [42]. Однако серьезным недостат- ком метода МАХ является неспецифичное связывание с сорбентом таких кислых аминокислот, как глутаминовая кислота, аспарагиновая кислота, гистидин и цистеин, и других отрицательно заряженных соединений. На протяжении последних десятилетий предпринимаются попытки уменьшить неспецифическую сорбцию различными способами [49]. Так, можно варьировать рН раствора, в котором происходит связывание (связывающий буфер) [41, 45], или рН промывочного раствора [46, 47]. Несмотря на успешное применение этого подхода на стандартных белках, при переходе на уровень протеома селективность метода снижается до 60–70 %, что приводит к недостаточно эффективной идентификации фосфорилированных белков. Альтернативно возможно использование реакции этерификации для получения метиловых эфиров пептидов, что позволяет определять большее число сайтов фосфорилирования в сложных биологических смесях [46, 48–50]. Однако введение дополнительной реакции может привести к большим потерям в образце [51, 52].
Недавно были разработаны методики предварительной очистки образцов катион- или анион-обменной хроматографией [53, 54]. Такой подход позволил увеличить селективность МАХ до 75 %. Однако к недостаткам такого метода можно отнести возможность слишком сильного удерживания неполностью ферментативно гидролизованных пептидов, а также значительное удерживание других модифицированных пептидов, например N-ацетилированных пептидов и гликопептидов. Кроме того, было показано, что нормальнофазовая хроматография в качестве предварительного этапа пробоподготовки может быть эффективна при фосфопротеомной идентификации [55]. Поскольку фосфатная группа является сильно гидрофильной, фосфорилированные пептиды слабо удерживаются на нормальной фазе, что приводит после металл-аффинного обогащения к 99 % селективности.
На сегодняшний день наиболее успешной оказалась разработка так называемого метода металлооксидной аффинной хроматографии (МОАХ) на основе оксида титана TiO2 [56]. При использовании предколонки с TiO2, соединенной с обращен-нофазовой капиллярной колонкой, авторами [56] была показана возможность извлечения фосфорилированных пептидов казеина из гидролизата суммарного белка молока коровы. Однако селективность этого метода была снижена из-за неспецифического связывания кислых нефосфорилиро-ванных пептидов. В работе [57] авторы использовали 2,5-дигидроксибензойную кислоту (2,5-dihydroxybenzoicacid, DHB) для удаления неспецифично связавшихся пептидов, что повысило селективность и чувствительность метода. В работе [58] была впервые показана возможность приме- нения оксида циркония при МОАХ, причем ZrO2 имеет большую селективность к монофосфорили-рованным пептидам, тогда как TiO2 — к мульти-фосфорилированным. Был сделан вывод, что комбинация двух сорбентов имеет потенциал для исчерпывающего профилирования фосфопротеома [59]. При добавлении в связывающий и промывочный буферы молочной кислоты в элюате после МОАХ на TiO2 содержится, как правило, более 90 % фосфорилированных пептидов; для ZrO2 это значение ниже [60].
Сорбенты на основе оксидов металлов могут быть использованы в различном аппаратурном исполнении. Наиболее распространен "офф-лайн" вариант, обеспечивающий гибкость в подборе растворителей и масштабируемости эксперимента. Частицы оксидов металлов могут быть упакованы в носики для автоматических пипеток (сорбция достигается путем многократного пропускания образца через сорбент) [61] либо помещены в спиновые колонки (образец пропускают через сорбент с помощью центрифуги). Альтернативно возможен batch-вариант, в котором сорбент помещен в микропробирку, что позволяет веществу дольше взаимодействовать с ним. В "он-лайн"-режиме оксиды металлов помещают в предколонки для ВЭЖХ-систем [62].
Недавно появились разработки наночастиц на основе оксидов металлов, в которых на нанораз-мерные магнитные шарики или на полимерную подложку наносят тонкий слой оксида [63, 64]. Такая структура обладает большой удельной поверхностью и повышенной сорбционной емкостью по сравнению с традиционными металл-аффин-ными сорбентами, однако есть сомнения по поводу воспроизводимости таких структур. Также имеются сведения о создании модифицированных сорбентов мишеней для MALDI-масс-спектрометрии [65, 66].
Сравнение методов МАХ и МОАХ вызывает все больший интерес. Так, было показано [60], что оксид титана более устойчив к влиянию солей, детергентов и малых молекул, чем классические металл-аффинные сорбенты. Добавление детергента в связывающий буфер может увеличить производительность МАХ из-за уменьшения адгезии на поверхности микропробирок и, более того, благоприятствовать обогащению мультифосфори-лированных пептидов по сравнению с TiO2. Авторы [67] показали новый подход — последовательное элюирование с сорбента для разделения моно-и мультифосфорилированных пептидов при варьировании элюентов. По сравнению с проточным вариантом МОАХ batch-анализ (в пробирке) продемонстрировал прекрасную степень извлечения и моно-, и мультифосфорилированных пептидов. Таким образом, экспериментальные условия силь- но влияют на производительность и селективность МАХ. Масштабное сравнение МАХ и МОАХ TiO2 при профилировании фосфопротеома клеток Drosophila melanogaster Kc167 было проведено авторами [68]. МАХ с предварительным метилированием пептидной смеси продемонстрировала 80 % селективность, так же как и МОАХ. Особенно важно небольшое перекрывание результатов идентификации фосфорилированных белков (35 %), что говорит о возможности комбинирования двух методов для более полного профилирования. Авторы работы [69] использовали последовательное элюирование 5 % водным аммиаком, 5 % пиперидином и 5 % пирролидином, что существенно увеличило число идентифицированных фосфорилированных белков в клеточной линии HeLa.
К настоящему времени известно об использовании в качестве металл-аффинных сорбентов оксидов многих металлов. Самым распространенным является TiO 2 , которому посвящено большое число работ по оптимизации условий проведения анализа [70–73], также много внимания уделено ZrO 2 [74, 75]. Были предприняты успешные попытки использовать в качестве сорбента для обогащения фосфорилированных пептидов гидроксид алюминия Al(OH) 3 [76], оксид галлия Ga 2 O 3 [77], оксид ниобия Nb 2 O 5 [78], оксид олова SnO 2 , который показал более низкий уровень неспецифического связывания по сравнению с TiO 2 [79], оксид тантала Ta 2 O 5 [80]. Также перспективным следует признать использование оксида железа как в варианте магнитных шариков Fe3O4 [81], так и микрораз-мерного Fe 2 O 3 [82]. Метод МОАХ имеет большое значение в фосфопротеомных исследованиях для выделения фосфорсодержащих пептидов без дополнительных процедур пробоподготовки, таких как этерификация и ионообменная хроматография [83].
Широкое развитие хромато-масс-спектрометрических методов в фосфопротеомике привело к возможности изучения и решения таких фундаментальных задач в биологии, как передача сигналов в клетках и их механизм регулирования, а также исследование различных заболеваний, при которых меняется качественный и количественный состав фосфорилированных белков, и других биохимических задач. Обратимый процесс фосфорилирования / дефосфорилирования белков чрезвычайно важен для проведения межклеточных сигналов. Нарушение сигнальных систем приводит к таким тяжелым заболеваниям, как диабет [84, 85], рак [86], болезнь Альцгеймера [86, 87], сердечная недостаточность [87], и многим другим.
Поскольку клеточные сигнальные системы, в которых большую роль играют фосфобелки, существуют практически во всех живых системах, включая высокоразвитые организмы, фосфопроте- омные исследования таких систем имеют огромное значение. Немаловажное место среди методов пробоподготовки занимает металл-аффинная хроматография. Например, применение МОАХ TiO2 для обогащения фосфопептидов позволило установить типы киназ, задействованных в развитии эмбрионов рыбы данио-рерио [88].
Фосфорилирование белков в тканях мышей (мозг, сердце, печень и пр.) было изучено с применением металл-аффинного сорбента, содержащего железо (идентифицировано 12000 белков и 36000 сайтов фосфорилирования), и позволило, во-первых, установить специфичность фосфорилирования в различных тканях, во-вторых, определить активность нескольких киназ, что позволило авторам в конечном итоге создать атлас фосфобелков мыши [89].
Важной областью биомедицины, в которой задействована фосфопротеомика, является изучение стволовых клеток, а именно понимание сигнальных механизмов в них. В работе [90] рассмотрены протеомный и фосфопротеомный (с использованием комбинации ион-обменной хроматографии и МОАХ TiO 2 ) ответ стволовых клеток человеческих эмбрионов при дифференцировании. А в работе [91] приведены данные о 10 844 сайтах фосфорилирования белков стволовых клеток. Эти данные помогают установить природу уникальности стволовых клеток.
В последние годы активно развивается направление, связанное с анализом посттрансляционных модификаций белков различными токсикантами и ксенобиотиками, которое получило собственное название — "аддуктомика", в рамках которого методы МАХ и МОАХ также нашли свое применение.
Особое внимание уделяется аддуктам бутирил-холинэстеразы (БХЭ) с фофсфорсодержащими соединениями, в том числе и с ОВ, такими как зарин и зоман [92, 93]. Было показано, что специфичное выделение аддукта БХЭ с остатком 3- орто -крезил фосфата из образца плазмы или сыворотки крови на TiO 2 возможно даже в случае ингибирования 0.05 % БХЭ [92].
Кроме БХЭ мишенью присоединения фосфорорганических соединений является сывороточный альбумин. Причем зачастую можно обнаружить несколько сайтов модификации альбумина фосфорорганическими соединениями. Возможность обогащения образцов аддуктами пептидов сывороточного альбумина методом МАХ на сорбенте с иммобилизироваными ионами железа (III) была показана на примере параоксона [93]. Авторы работы [94] успешно идентифицировали пептиды сывороточного альбумина человека, модифицированные зарином и зоманом, после их выделения из образца с помощью TiO 2 .
Кроме того, авторами [95] была показана принципиальная возможность применения металл-аффинной хроматографии для специфичной сорбции алкилированных аддуктов сернистого иприта с глобином на сорбенте, содержащем ионы Cu2+.
ЗАКЛЮЧЕНИЕ
Таким образом, металл-аффинная хроматография является специфичным, надежным и воспроизводимым методом. Несмотря на относительно недолгую историю существования, метод получил быстрое развитие во многих направлениях биоор-ганического анализа, и последние годы круг задач, решаемых с помощью МАХ и МОАХ, стремительно расширяется. В ближайших перспективах можно ожидать, что метод будет широко использоваться в ретроспективном токсикологическом анализе, для разработки новых методов диагностики различных заболеваний, производстве новых лекарственных препаратов. В то же время появление современных высокотехнологичных материалов и нанотехнологий позволяет надеяться, что будут разрабатываться и производиться новые эффективные металл-аффинные сорбенты.


