Метод альтернативной канюляции при протезировании аортального клапана у пациента с "фарфоровой аортой". Клинический случай
Автор: Козлов Б.Н., Насрашвили Г.Г., Панфилов Д.С., Кузнецов М.С., Михеев С.Л., Шипулин В.М.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: В помощь практическому врачу
Статья в выпуске: 3 т.32, 2017 года.
Бесплатный доступ
Атеросклеротическое поражение корня и восходящего отдела аорты, в особенности крайняя его выраженность - «фарфоровая аорта», представляет большую проблему при кардиохирургических вмешательствах. Данная патология чревата возможными тромбоэмболическими осложнениями, а также диссекцией аорты при интраоперационных манипуляциях на аорте, в частности, при ее канюляции по принятой методике. Данная ситуация требует от хирурга нестандартного подхода как в отношении тактики оперативного вмешательства, так и в обеспечении искусственного кровообращения (ИК). В данной статье представлен клинический случай интраоперационно выявленной «фарфоровой аорты» с описанием примененной альтернативной методики подключений ИК для минимизации осложнений.
Фарфоровая аорта, атеросклероз аорты, канюляция брахиоцефального ствола
Короткий адрес: https://sciup.org/149125172
IDR: 149125172 | DOI: 10.29001/2073-8552-2017-32-3-67-70
Alternative method of cannulation for aortic valve replacement in patient with porcelain aorta. Clinical case
Atherosclerotic damage of the aortic root and ascending aorta, especially in case of such extreme manifestation as porcelain aorta, is a major problem in cardiac surgery. This pathology is associated with potential thromboembolic complications and aortic dissection during intraoperative manipulation of the aorta, in particular, in case of standard cannulation technique. This situation requires surgeon to use nonstandard approaches to tactics of surgical intervention and cardiopulmonary bypass. This article presents a clinical case of intraoperatively detected porcelain aorta and describes an alternative technique for cardiopulmonary bypass connections to minimize complications.
Текст научной статьи Метод альтернативной канюляции при протезировании аортального клапана у пациента с "фарфоровой аортой". Клинический случай
Атеросклеротическое поражение коронарных артерий, а также стеноз аортального клапана атеросклеротической этиологии зачастую сопровождаются поражением корня аорты и восходящего отдела грудной аорты [1]. Крайняя выраженность данного поражения, вплоть до формирования так называемой «фарфоровой аорты», не только увеличивает риски таких осложнений, как тромбоэмболия и диссекция аорты, но также может влиять на тактику хирургического лечения и объем оперативного вмешательства [2].
На сегодняшний день наиболее информативным методом диагностики атеросклеротического поражения восходящего отдела аорты является компьютерная томография [1], однако рутинно в отсутствии подозрений на аневризматическую трансформацию аорты или ее диссекцию в обследовании пациентов данный метод не применяется.
Большую сложность и опасность представляет дооперационно не диагностированное поражение стенок восходящего отдела аорты. При интраоперационном выявлении атеросклеротической трансформации аорты с ее кальцинозом резко возрастает риск неврологических осложнений при ее типичной канюляции и пережатии в восходящем отделе, а также риск диссекции аорты. Такая ситуация сопряжена с возможным незапланированным возрастанием объема оперативного вмешательства, в том числе с использованием циркуляторного ареста (ЦА) [3]. ЦА — методика антигипоксиче-ской защиты организма, используемая при операциях с ИК, основанная на частичной или полной временной остановке кровообращения в условиях различной степени гипотермии.
В литературе описаны случаи завершения операции при выявлении «фарфоровой аорты» после выполненной стернотомии [4].
На сегодняшний день существуют методики альтернативной канюляции при операциях с ИК. Данные методики обычно применяются при вмешательствах на дуге аорты, а также в нисходящем ее отделе у пациентов с аневризмами грудной аорты и ее диссекцией, однако в то же время они способны снизить описанные риски при кальцинозе восходящей аорты у пациентов, оперируемых по поводу ишемической болезни сердца (ИБС) и клапанной патологии [5].
В данной статье представлен опыт хирургического лечения пациента с атеросклеротическим стенозом аортального клапана и интраоперационно выявленной «фарфоровой аортой» с применением нестандартной методики подключения аппарата ИК.
Клинический случай
Пациент Л., 71 год, 10.01.2017 г. в плановом порядке госпитализирован в кардиохирургическое отделение НИИ кардиологии для проведения хирургического лечения — протезирования аортального клапана.
При поступлении предъявлял жалобы на давящие, сжимающие боли за грудиной и одышку смешанного характера при незначительной физической нагрузке (ходьба до 50–100 м) и иногда в покое. Также отмечал выраженную слабость, утомляемость, отеки нижних конечностей, больше по вечерам, ощущение перебоев в работе сердца.
Из анамнеза известно, что пациент страдает гипертонической болезнью более 10 лет, с максимальным отмеченным повышением АД до 240/110 мм рт. ст. Длительное время пациент принимал гипотензивные препараты в разных комбинациях по назначению терапевта. Клиника стенокардии манифестировала с 2011 г., после чего по результатам коронарографии выполнено стентирование правой коронарной артерии. С 2013 г. отмечен рецидив стенокардии, при обследовании выявлен стеноз стента, выполнена баллонная ангиопластика. В том же году выявлен аортальный стеноз с пиковым градиентом 62 мм рт. ст. После этого сохранялась стенокардия на уровне 3-го функционального класса. С сентября 2016 г. отмечает появление отдышки, в то же время у пациента выявлены пароксизмы мономорфной желудочковой тахикардии, отмечено нарастание градиента на аортальном клапане.
В клинике были проведены общеклинические анализы. Отклонений от нормальных значений не обнаружено. При рентгенологическом исследовании органов грудной клетки очагово-инфильтративных изменений легочной ткани легких, нарушений гемодинамики малого круга кровообращения не выявлено. Аорта уплотнена, умеренно расширена больше в восходящем отделе.
По данным эхокардиографии выявлена небольшая дилатация левого предсердия (ЛП) — 48х57 мм, небольшая гипертрофия левого желудочка (ЛЖ) — масса миокарда составила 255 г. Общая сократимость желудочков в норме (фракция выброса ЛЖ в В-режиме составляет 70%). Нарушений локальной сократимости не выявлено. Диастолическая дисфункция ЛЖ (небольшое замедление расслабления миокарда). Выявлен кальциноз корня аорты, выраженный кальциноз створок аортального клапана с резким снижением подвижности створок. Выраженный аортальный стеноз с пиковым градиентом 82 мм рт. ст. (индекс площади отверстия аортального клапана 0,4 см/м2), аортальная регургитация небольшая, до первой степени. Остальные клапаны без изменений, функционируют нормально.
При ультразвуковом исследовании сонных артерий стенозов не определяется. Стенозов в бедренных артериях не отмечено. Спирография также не выявила отклонений от нормы.
По данным коронарографии (от 23.09.17) стенозов коронарных артерий не выявлено. В правой коронарной артерии стент проходим.
После проведенного обследования пациенту установлен диагноз дегенеративного сложного порока аортального клапана с преобладанием стеноза с пиковым градиентом на клапане 82 мм рт. ст.
18.01.2017 г. пациенту было выполнено оперативное лечение в объеме протезирования аортального клапана механическим протезом «Мединж 2» диаметром 19 мм в условиях ИК и антеградной холодовой кардиоплегии раствором кустодиол.
При интраоперационной ревизии корень аорты и восходящий ее отдел циркулярно кальцинированы. В связи с крайне высоким риском эмболии и диссекции аорты принято решение отказаться от принятой методики канюляции восходящей аорты в пользу альтернативного артериального доступа для ИК (рис. 1). Выделен брахиоцефальный ствол от устья до бифуркации. В условиях системной гепаринизации выполнено боковое пережатие брахиоцефального ствола в проксимальном сегменте под контролем церебральной оксиметрии системой INVOS Cerebral Oximeter (Somanetics Corporation).
Сформирован анастомоз между синтетическим протезом диаметром 8 мм и брахиоцефальным стволом по типу «конец в бок». Область анастомоза тщательно осушена и обработана клеем BioGleu. В свободный конец синтетического протеза установлена канюля соответствующего диаметра для проведения ИК. Установлена венозная канюля в полость правого предсердия. Начато ИК по схеме «брахиоцефальный ствол — правое предсердие». Аорта пережата непосредственно проксимальнее устья брахиоцефального ствола. С техническими трудностями иссечены кальцинированные створки аортального клапана, в аортальную позицию имплантирован механический протез «Мединж 2» диаметром 19 мм. После проведения основного этапа операции выполнено клипирование вшитого в БЦС протеза металлическими скобками без риска повреждения стенки сосуда при деканюляции.
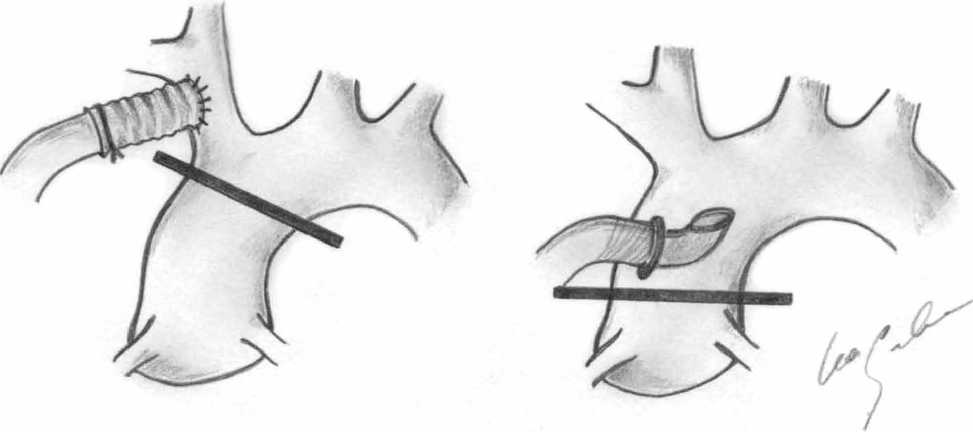
Рис. 1. Схема типичной канюляции восходящей аорты (справа) и канюляции в БЦС, через синтетический протез (слева). Стрелками указаны места пережатия аорты
Послеоперационный период протекал обычно. Согласно контрольной эхокардиографии, механический протез в аортальной позиции функционирует нормально. Пациент выписан из стационара в удовлетворительном состоянии на 14-е сутки после операции.
Обсуждение
Анализируя представленный клинический случай, необходимо отметить важность дооперационного обследования пациентов с мультифокальным атеросклеротическим поражением, в особенности при наличии приобретенного аортального стеноза на предмет вовлеченности восходящего отдела аорты в атеросклеротический процесс. Оперируя подобных пациентов, хирург должен иметь настороженность в отношении манипуляций на измененной стенке аорты, а также техническую возможность и высокую квалификацию для возможного применения методик альтернативного подключения аппарата ИК, а также работы в условиях гипотермической антигипоксической защиты организма. В то же время необходимо помнить о все более широко применяющихся методиках эндоваскулярных вмешательств как на коронарных артериях, так и при коррекции патологии аортального клапана, и в этой связи тщательно взвешивать риски при определении тактики лечения пациентов с «фарфоровой аортой» [4].
Заключение
Настоящий клинический пример иллюстрирует факт возможного интраоперационного выявления выраженного атеросклеротического поражения аорты с высоким риском ее канюляции по принятой методике. Одним из возможных вариантов решения возникшей проблемы для обеспечения ИК может быть альтернативная канюляция в брахиоцефальный ствол, что обеспечивает безопасное кровоснабжение головного мозга и внутренних органов на основном этапе операции без дополнительного риска тромбоэмболии и диссекции аорты.
Список литературы Метод альтернативной канюляции при протезировании аортального клапана у пациента с "фарфоровой аортой". Клинический случай
- Abramowitz Y., Jilaihawi H., Chakravarty T. et al. Porcelain Aorta: A Comprehensive Review // Circulation. - 2015. - Vol. 131. - P. 827-836- 10.1161/Circulation AHA.114.011867. DOI: 10.1161/CIRCULATIONAHA.114.011867
- Leyh et al. "No touch" technique and hypothermic circulatory arrest for porcelain aorta in combined valve surgery // J. Cardiothorac. Surg. - 2015. - Vol. 10 (Suppl. 1). - P. A173- DOI: 10.1186/1749-8090-10-S1-A173
- LeMaire S.A. Individualized treatment strategies for patients with aortic valve disease and porcelain aorta // J. Thorac. Cardiovasc. Surg. - 2015. - Vol. 149. - P. 134-136.
- Idrees J., Roselli E.E., Raza S. et al. Aborted sternotomy due to unexpected porcelain aorta: Does transcatheter aortic valve replacement offer an alternative choice? // J. Thorac. Cardiovasc. Surg. - 2014. - Vol. 149, Issue 1. - P. 131-134.
- Ken Okamoto, Toshihiro Fukui. Bilateral axillary artery cannulation for severely calcified aorta and branches: a case report // J. Cardiothorac. Surg. - 2016. - Vol. 11. - P. 98- DOI: 10.1186/s13019-016-0492-1


