Метод лапароскопии для прижизненной диагностики Т-2 токсикоза у кроликов
Автор: Хайруллин Д.Д., Валиуллин Л.Р., Идиятов И.И., Бирюля В.В., Иванов В.В., Трифонов А.Ю., Тремасов М.Я.
Статья в выпуске: 1 т.233, 2018 года.
Бесплатный доступ
В связи с высокой распространённостью микроскопических грибов, их метаболиты вызывают при этом тяжелые патологические процессы в организме животных. В наших исследованиях была изучена прижизненная диагностика токсического воздействия Т-2 токсина на кроликах методом лапароскопии брюшной полости. Для проведения видеолапароскопических исследований брюшной полости и для прижизненной биопсии печени при Т-2 токсикозе пользовались однопрокольной методикой. В качестве параметров контроля течения токсикоза служили клинические признаки и гистологические исследования. Исследуемые показатели сравнивали с контрольными данными. В результате проведенных исследований видно, что при лапароскопии возможно определить не только прижизненное морфологию внутренних органов животных, но и проводить биопсию печени для последующих гистологических исследований с целью выявления отрицательного воздействия различных препаратов на живой организм.
Лапароскопическая хирургия, диагностика отравлений, яды природного происхождения
Короткий адрес: https://sciup.org/142213005
IDR: 142213005 | УДК: 619:615.9;
Method of laparoscopy for injected diagnosis of T-2 toxicosis in rabbits
Due to the high prevalence of microscopic fungi, their metabolites cause with severe pathological processes in the organism of animals. In our studies, was studied in vivo diagnosis of toxic effect of T-2 toxin on kalikamata laparoscopy the abdominal cavity. To conduct video studies of the abdomen and for in vivo biopsy of the liver in T-2 toxicosis used odnoprestolnoj method. As control parameters, flow toxicity served as the clinical signs and histological examination. Investigated parameters were compared with control data. The result of the research shows that during laparoscopy it is possible to determine not only the in vivo morphology of the internal organs of animals, but also to carry out a liver biopsy for further histological studies to identify adverse effects of various drugs on the living organism.
Текст научной статьи Метод лапароскопии для прижизненной диагностики Т-2 токсикоза у кроликов
Одним из основных загрязнителей продовольственного сырья токсичными веществами биологического происхождения являются вторичные метаболиты микроскопических грибов (микотоксины) которые представляют большую угрозу для животных и человека.
В связи с высокой распространенность микроскопических грибов рода Fusarium в средней широтах (Франция, Германия, Канада, Российская Федерация, серверная часть США, и др. страны) часто встречающимися микотоксинами являются фузариотоксины (дизоксиневаленол (ДОН), фумонизины, зеараленон, Т-2 токсин). Они очень часто встречаются в продовольственном сырье (овощах, фруктах, мясе, молоке и молочных продуктах, орехах, вине и др.) и кормах (сено, силос, фуражное зерно и др,) в сочетании друг с другом на уровне или не превышающие ПДК [3, 6], Трихоте ценовые микотоксины могут вызывать подавление иммунитета, повреждение митохондрий за счет уменьшения митохондриального мембранного потенциала и индуцировать апоптоз путем повышающей регуляции генов, связанных с апоптозом [5, 8]. Зеараленон вызывает эмбриотоксический, тератогенный эффект, а в сочетании с трихотеценовыми микотоксинами может вызывать синергетическое воздействие даже при дозах ниже ПДК. Который приводит к дегенеративным и некротическим изменениям в печени, почках, иммунокомпетентных органов животных и человека [4, 7]. Однако, не смотря па широкую распространённость фузариотоксинов и высокие токсические свойства на организм животных и человека ранняя диагностика отравления микотоксина является мало изученной и весьма актуальной проблемой как для микотоксикологии так и для эпидемиологии. В связи с этим целью наших исследований была прижизненная диагностика токсического воздействия микотоксина Т-2 токсина на кроликов.
Материалы и методы исследований. Опыты по изучению хронического воздействия Т-2 токсина были проведены на 6 кроликах в течение 14 суток. Животные первой группы служили биологиче ским контролем. Животные второй группы получали Т-2 токсин в виде 5% спиртового раствора внутрижелудочно, (1/10 ДД50). Для эксперимента микотоксины были синтезированы в ФГБНУ ФЦТРБ-ВНИВИ, которые по физико-химическим параметрам и токсическим свойствам не отличались от существующих стандартов. В качестве продуцента микотоксинов использовали F. sporotrichiella 2 м 15, предоставленный Котиком А.Н. Для проведения видеолапароскопических исследований брюшной полости и для прижизненной биопсии печени при Т-2 токсикозе пользовались классической мегодикой (контроль) и новой одноирокольной методикой (опыт) представленной в монографии [1, 2]. Гистологическое исследование проводились согласно методической рекомендации по изучению микрокартины внутренних органов [9, 10). В качестве параметров контроля течения токсикоза служили клинические признаки и гистологические исследования. Исследуемые показатели сравнивали с контрольными данными.
Результаты исследований. Клинические признаки отравления начали проявляться у животных получавших Т-2 токсин, и характеризовались угнетением, снижением аппетита, взъерошенностью шёрстного покрова шаткостью походки, диареей. К концу опыта, получавших Т-2 токсин, к окончанию эксперимента отмечались эрозии и некрозы кожи губ и слизистых оболочек ротовой полости.
Подготовка для введения хирургических инструментов в классическом и опытном варианте лапароскопии в брюшную полость, что для лапароскопии делаются маленькие разрезы 4 мм в брюшной стенке (два при классической методике, или один в новой, однопрокольной методике), для троакаров, через которые в брюшную полость вводятся видеолапароскоп и манипуляторы (биопсийные зажимы). Введение в брюшную полость двух троакаров, первый для камеры и инсуффляции газа в брюшную полость, второй для манипулятора для биопсии печени представлены на рисунке 1.
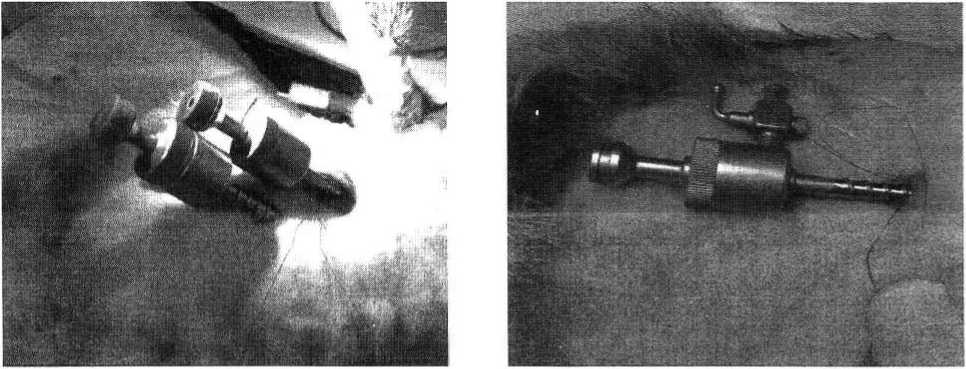
Рисунок 1 - Введение в брюшную полость двух зондов с лева на право, первый троакар для лапароскопаи инсуффляции газа в брюшную полость, а второй троакар для пункций печени.
В новой методике биопсийные зажимы вводятся через один порт (в щель между корпусом троакара и корпусом лапароскопа). Пункция печени были отобраны для гистологических исследований у животных получавших Т-2 токсина в дозах 1/10 ЛДзо. При диффузном поражении паренхиматозного органа биопсию в опытной и контрольной методике проводили с краевых участков печени, где риск биопсийных осложнений наименьший. Для гемостаза участков биопсий проводиться электрокоагуляция места пункции печени тем же манипулятором, которым проводили биопсию.
Гепатоциты печени у кролика контрольной и исследуемой группы имеют обычное строение, по линии соединяющей центральные вены наблюдается не значительный визуализирующийся стеаТоз.' В микрофотографии видно, что печень ' кролика получавших Т-2 токсин в дозе 1/10 ЛД50, определяется капельный стеатоз.
Заключение. В результате проведенных исследований видно, что при лапароскопии методом одного прокола брюшной полостикролика возможно определить не только прижизненное морфологию внутренних органов животных, по и проводить биопсию печени для последующих гистологических исследований с целью выявления отрицательного воздействия различных препаратов на живой организм. Работа выполнена за счет гранта Российского научного фонда (проект №16-15-00141).
Резюме
В связи с высокой распространённостью микроскопических грибов, их метаболиты вызывают при этом тяжелые патологические процессы в организме животных. В наших исследованиях была изучена прижизненная диагностика токсического воздействия Т-2 токсина на кроликах методом лапароскопии брюшной полости.
Для проведения видеолапароскопических исследований брюшной полости и для прижизненной биопсии печени при Т-2 токсикозе пользовались однопрокольной методикой. В качестве параметров контроля течения токсикоза служили клинические признаки и гистологические исследования. Исследуемые показатели сравнивали с контрольными данными.
В результате проведенных исследований видно, что при лапароскопии возможно определить не только прижизненное морфологию внутренних органов животных, но и проводить биопсию печени для последующих гистологических исследований с целью выявления отрицательного воздействия различных препаратов на живой организм.
METHOD OF LAPAROSCOPY FOR INJECTED DIAGNOSIS OF T-2 TOXICOSIS
Список литературы Метод лапароскопии для прижизненной диагностики Т-2 токсикоза у кроликов
- Валиуллин, Л.Р. Комбинированное воздействие микотоксинов на физиологические показатели крыс/Валиуллин Л.Р., Хайруллин Д.Д., Семенов Э.И., Егоров В.И., Шуралев Э.А., Рагинов И.С.//Ученые записки Казанской государственной академии ветеринарной медицины им. Н.Э. Баумана. -2015. -Т. 221. №1. -С. 45-48.
- Иванов В.В., Равилов Р.Х., Папуниди К.Х. Эндоскопическая хирургия мелких домашних животных. -Казань, 2016.-164 с.
- Тремасов, М.Я. Проблемы ветеринарной экотоксикологии/М.Я. Тремасов//Материалы международной конференции ветеринарных фармакологов и токсикологов, посвящённой 125-летию H.A. Сошественского. -Казань, 2001. -С. 10-14.
- Хайруллин, Д.Д. Идентификация кормового антибиотика цинкбацитрацина методом ВЭЖХ/Хайруллин Д.Д., Галяутдинова Г.Г., Босяков В.И., Шангараев Н.Г., Егоров В.И.//Ученые записки Казанской государственной академии ветеринарной медицины им. Н.Э. Баумана. Казань, 2017. -Т. 232 (4). С. -147-150.
- Banati H. Determination of mycotoxinproduction of Fusariumspecies in genetically modified by quantitative flow immunocytometry/Banati H., Darvas В., Feher-Toth S., Czeh A., Szekacs A. Toxins (Basel). -2017. -Feb 22; 9(2).
- Deng, C. Deoxynivalenol inhibits proliferation andinduces apoptosis in human umbilicalvein endothelial cells/Deng С, Ji С, Qin W, Cao X, et. al.//Environ Toxicol Pharmacol. -2016 Mar 26.
- Marie-Caroline. S. Natural Co-Occurrence of Mycotoxins in Foods and Feeds and Their in vitro Combined Toxicological Effects/Marie-Caroline S., Stephanie M., Emmanuel C. Nolwenn H.//Toxins (Basel). -2016 Mar 26. -8(4). pii: E94. doi: 10. 3390.
- Zhu, C.C. Toxic effects of IIT-2 toxin on mouse oocytes and its possible mechanisms/Zhu C.C., Zhang Y., Duan X, Han J., Sun S.C.//Arch Toxicol-2016 Jun; 90(6).
- Raginov L.S. Morphofunctional analysis of experimental model of esophageal achalasia in rats/Sabirov A.G., Burmistrov M.Y., Chelyshev Y.A., Khasanov R.Sh., Moroshek A.A., Grigoriev P.N., Zciirov A.L., Mukhamedyarov M.A.//Bull Exp Biol Med. -2010 Oct; 149(4):466-70.
- Elder, E. Atlas and synopsis levers of histopathology of the Skin/E. Elder, R. Elenitsas, A. Rubin et. al.//Skin Diseases. -2013.


