Метод местного отрицательного давления с инстилляцией химотрипсина в лечении гнойно-некротических заболеваний мягких тканей туловища и конечностей
Автор: Чиников М.А., Кисляков В.А., Мохареб А., Веретник Г.И., Аль-Арики М., Мишарина Л.К., Кравченко К.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Гнойная хирургия
Статья в выпуске: 1 (95), 2026 года.
Бесплатный доступ
Введение. Гнойно-некротические заболевания мягких тканей (ГНЗМТ) остаются сложной проблемой гнойной хирургии с летальностью 25–50 %. Метод местного отрицательного давления с инстилляцией (NPWT-i) является современным стандартом лечения сложных ран. Применение химотрипсина в рамках NPWT-i преодолевает недостатки традиционной ферментотерапии благодаря контролируемой доставке и быстрой эвакуации продуктов лизиса. Цель исследования: анализ эффективности метода местного отрицательного давления с инстилляцией химотрипсина по сравнению с применением физиологического раствора у больных ГНЗМТ туловища и конечностей. Материалы и методы. В исследование включено 27 пациентов с ГНЗМТ туловища и конечностей. В 1 группе (n=15) применялось NPWT-i с химотрипсином, во 2 группе (n=12) – NPWT-i с физиологическим раствором. Группы были сопоставимы по основным показателям. Результаты. В 1 группе к 3-м и 7-м суткам отмечены значимо меньшие уровни лейкоцитоза и СРБ (p<0,05). По данным цифровой планиметрии в 1 группе к 7-м суткам площадь некрозов и фибрина была значимо меньше, а площадь грануляций – больше (p<0,05). Клинические исходы у больных I группы также были лучше по количеству вторичных хирургических обработок (3 [2;3] vs 4 [3;5], p=0,015) и длительности госпитализации (21 [16;25] vs 31 [21;33] дней, p=0,013). Заключение. Использование метода местного отрицательного давления с инстилляцией (NPWT-i) раствора химотрипсина является эффективным средством в комплексном лечении больных гнойно-некротическими заболеваниями мягких тканей туловища и конечностей.
Метод местного отрицательного давления с инстилляцией (NPWT-i), гнойно-некротическая рана, протеолитические ферменты, химотрипсин, планиметрический анализ
Короткий адрес: https://sciup.org/142247253
IDR: 142247253 | УДК: 006.617–089 | DOI: 10.17238/2072-3180-2026-1-157-164
Negative Pressure Wound Therapy with Chymotrypsin Instillation in The Treatment of Purulent-Necrotizing Soft Tissue Infections of The Trunk and Extremities
Introduction. Purulent-necrotic diseases of soft tissues (PNDST) remain a challenging problem in purulent surgery with a mortality rate of 25–50 %. The method of local negative pressure wound therapy with instillation (NPWT-i) is a modern standard for treating complex wounds. The use of chymotrypsin within the NPWT-i framework overcomes the shortcomings of traditional enzyme therapy due to controlled delivery and rapid evacuation of lysis products. Objective: To analyze the efficacy of the method of local negative pressure wound therapy with instillation of chymotrypsin compared to the use of physiological saline in patients with PNDST of the trunk and limbs. Materials and methods. The study included 27 patients with PNDST of the trunk and limbs. In group 1 (n=15), NPWT-i with chymotrypsin was applied; in group 2 (n=12) – NPWT-i with physiological saline. The groups were comparable in terms of baseline characteristics. Results. In group 1, significantly lower levels of leukocytosis and C-reactive protein (CRP) were noted on days 3 and 7 (p<0,05). According to digital planimetry data, by day 7 in group 1, the area of necrosis and fibrin was significantly smaller, and the area of granulation tissue was larger (p<0.05). Clinical outcomes in patients of group I were also better in terms of the number of secondary surgical debridements (3 [2;3] vs 4 [3;5], p=0,015) and the duration of hospitalization (21 [16;25] vs 31 [21;33] days, p=0,013). Conclusion. The use of the method of local negative pressure wound therapy with instillation (NPWT-i) of chymotrypsin solution is an effective tool in the comprehensive treatment of patients with purulent-necrotic diseases of soft tissues of the trunk and limbs.
Текст научной статьи Метод местного отрицательного давления с инстилляцией химотрипсина в лечении гнойно-некротических заболеваний мягких тканей туловища и конечностей
Гнойно-некротические заболевания мягких тканей (ГНЗМТ), включая обширные флегмоны, абсцессы и инфицированные раны различного генеза, представляют собой одну из наиболее сложных и ресурсоемких проблем современной хирургии [1, 2]. Несмотря на значительный прогресс в области асептики, ГНЗМТ остаются серьёзной проблемой, сопровождающейся высоким уровнем послеоперационной летальности, достигающей, по данным различных авторов, 25–50 % [3, 4].
Метод местного лечения отрицательным давлением (Negative Pressure Wound Therapy – NPWT) стал общепринятым и очень важным способом лечения сложных ран за последние годы [5, 6]. В ходе развития метода появилась технология местного лечения ран отрицательным давлением с инстилляцией растворов (NPWT-i), которая объединяет в себе вакуумную аспирацию и возможность направленной подачи лекарственных растворов в рану [7, 8]. Обычно для инстилляции используют физиологический раствор, однако поиск более эффективных агентов для преодоления фазы гидратации и некролиза остается областью активных исследований [9, 10].
Кроме того, хорошо известна роль протеолитических ферментов в лечении гнойных ран [11–12]. Протеолитические ферменты, такие как трипсин и химотрипсин, играют ключевую роль в гнойной хирургии, избирательно расщепляя некротические ткани и фибрин, что ускоряет очищение раны, снижает воспаление и стимулирует репарацию [13–16].
В доступной литературе нами не найдено сравнительных исследований, оценивающих эффективность NPWT-i с инстилляцией раствора протеолитических ферментов в сравнении с применением для инстилляции физиологического раствора при лечении ГНЗМТ.
Цель исследования: анализ эффективности метода местного отрицательного давления с инстилляцией химотрипсина по сравнению с применением физиологического раствора у больных ГНЗМТ туловища и конечностей.
Материалы и методы
В исследование включено 27 больных с гнойно-некротическими заболеваниями мягких тканей туловища и конечностей, находившихся на лечении в отделении гнойной хирургии ГКБ им. А.К. Ерамишанцева с ноября 2024 г. по декабрь 2025 г. Критериями включения больных в исследование были возраст старше 18 лет, клиническая картина гнойно-некротизирующей инфекции мягких тканей туловища и конечностей. Критерии исключения: аллергические реакции на компоненты систем отрицательного давления или протеолитические ферменты, дисциркуляторная энцефалопатия II–III ст., декомпенсированные заболевания сердечно-сосудистой и дыхательной систем, коагулопатия, тромбоцитопения, язвенная болезнь или желудочно-кишечное кровотечение, признаки сепсиса (прирост ≥2 баллов по шкале SOFA), пациенты с хронической болезнью почек стадии G5 (по классификации KDIGO/KDOQI), психические расстройства и отказ пациента.
У всех пациентов, включённых в исследование, применяли метод местного отрицательного давления с инстилляцией (NPWT-i).
Техника применения NPWT-i была унифицирована. Использовался аппарат «ВИТ Ультра» (VIT Medical, г. Москва). Его использование позволяет контролировать параметры, включая уровень и длительность вакуумного воздействия, дозировку и скорость подачи раствора, а также продолжительность контакта инстилляционного раствора с раневой поверхностью, что обеспечивает воспроизводимость и надежность процедуры.
Исследование было проспективным одноцентровым рандомизированным. Рандомизация пациентов на группы выполнена с помощью метода конвертов.
В зависимости от используемого для инстилляции раствора все пациенты были разделены на две группы: в 1 группе (15 пациентов) для инстилляций применяли 10 мг химотрипсина, растворённого в 15 мл физиологического раствора, во 2 группе (12 пациентов) проводили инстилляции 15 мл физиологического раствора. Объём раствора для инстилляции (15 мл) был подобран в соответствии с рекомендациями производителя и был одинаковым в обеих группах.
Согласно международным рекомендациям один цикл работы аппарата (2 часа 40 мин.) включает: время воздействия отрицательным давлением (–125 mmHg) – 2 часа 30 мин.; время подачи раствора – 20 секунд (объем инстилляции 15 мл); экспозиция раствора – 10 минут [17]. Все пациенты лечились по единому протоколу, подробно описанному нами ранее [18].
Таблица 1
Сравнение изучаемых групп больных
Table 1
Comparison of the studied patient groups
|
Признак / Parameter |
1 группа (n =15) / 1 group |
2 группа (n =12) / 2 group |
р-value |
|
Возраст, лет (Me [Q25; Q75]) / Age, years |
58,60 ± 4,38 |
63,17 ± 3,42 |
р = 0,558 |
|
Мужчины, % / Men, % |
60 % |
58 % |
χ² = 0,083 р = 0,774 |
|
Женщины, % / Women, % |
40 % |
42 % |
|
|
Размер раны, см² (Me [Q25; Q75]) / Wound size, cm2 |
76.0 [52,0; 124,0] |
88,0 [48,0; 115,0] |
р = 0,759 |
|
Вид возбудителя / Type of pathogen |
|||
|
S.aureus |
60 % |
66 % |
χ² = 0,81 р = 0,846 |
|
Ps.aeuginosa |
16 % |
14 % |
|
|
Kl.pneumonia |
15% |
13 % |
|
|
A.banumannii |
9 % |
7 % |
|
|
Основной диагноз / Main diagnosis |
|||
|
Облитерирующий атеросклероз артерий нижних конечностей, % / Obliterating atherosclerosis of the arteries of the lower limbs, % |
39 % |
38 % |
χ² = 0,44 р = 0,801 |
|
Флегмона, % / Phlegmon, % |
41 % |
45 % |
|
|
Абсцесс, % / Abscess, % |
20 % |
17 % |
|
Окончание Таблицы 1 / End of Table 1
|
Признак / Parameter |
1 группа (n =15) / 1 group |
2 группа (n =12) / 2 group |
р-value |
|
Сопутствующее заболевание / Concomitant disease |
|||
|
Цереброваскулярная болезнь (ОНМК, ДЭП) / Cerebrovascular disease (ACVA, DEP) |
34 % |
30 % |
χ² = 0,77 р = 0,525 |
|
Болезни сердечно-сосудистой системы, Cardiovascular diseases |
31 % |
35 % |
|
|
Сахарный диабет 2-го типа / Type 2 diabetes mellitus |
20 % |
17 % |
|
|
Другие (Анемия) / Other (Anemia) |
15 % |
18 % |
|
Как показано в таблице (табл. 1), по возрасту, полу, размеру раны, основному и сопутствующему диагнозу и основному возбудителю группы были сопоставимы. Надо отметить, что у некоторых больных было 2 и более сопутствующих заболеваний.
Хирургическая тактика и общая схема лечения были одинаковыми для всех пациентов. Первичная хирургическая обработка (ПХО) проводилась в срочном порядке и включала санацию гнойно-некротического очага, максимально возможное иссечение некротизированных тканей и его адекватное дренирование. Вторичная хирургическая обработка (ВХО) выполнялась на 2–3 сутки, и далее с периодичностью 3–4 суток. В ходе каждой такой обработки осуществлялась тщательная ревизия раны, оценка динамики заживления и дополнительная некрэктомия. Всех пациентов лечили системными антибиотиками в зависимости от диагноза и предполагаемого возбудителя, а в последующем, с учётом результатов бактериологического исследования экссудата.
Методы оценки эффективности лечения включали динамику количества лейкоцитов в общем анализе крови и сывороточного уровня С-реактивного белка при поступлении, на 3-и, 7-е сутки после ПХО. Для объективного измерения площади раны и анализа темпов репарации тканей применялась методика цифровой планиметрии с использованием мобильного приложения «RAN.PRO» (Смарт Эквити, Россия). Фотография раны с эталонной линейкой загружалась в приложение, которое автоматически рассчитывало общую площадь дефекта, а также процентное соотношение некротических тканей, фибрина и грануляций. Микробиологическое исследование раневого отделяемого с целью идентификации возбудителя и оценки динамики бактериальной обсеменённости проводилось во время первичной хирургической обработки (ПХО) раны при поступлении. В обеих группах также анализировали количество вторичных хирургических обработок (ВХО) и сроки госпитализации пациентов.
Статистическая обработка полученных данных осуществлялась с применением программного обеспечения SPSS Statistics 23.0. Для описания количественных показателей использовались медиана и интерквартильный размах (Me [Q25; Q75]), так как распределение большинства признаков отличалось от нормального. Сравнение количественных данных между двумя независимыми группами проводилось с использованием непараметрического U-критерия Манна-Уитни. Для анализа качественных признаков применялся критерий χ² с поправкой Йетса. Статистически значимыми считались различия при достижении уровня p <0,05.
Результаты
Динамика лабораторных показателей у больных обеих групп показана в таблице (табл. 2).
Таблица 2
Динамика лабораторных маркеров воспаления в процессе лечения, Ме [Q25; Q75]
Table 2
Dynamics of laboratory markers of inflammation during treatment, Ме [Q25; Q75]
|
Время / Группа Time / Group |
Исходно Initially |
3-е сутки At day 3 |
7-е сутки At day 7 |
|
Лейкоцитоз, ×10⁹/л, Leukocytosis, ×10⁹/L |
|||
|
1 группа / 1 group |
11 [9; 13] |
8 [7; 9] |
7 [5; 10] |
|
2 группа / 2 group |
10.5 [6.5;13.75] |
12 [8.25; 17.25] |
10.5 [8; 13] |
|
P- value |
(р1=0,558) |
(р2=0,001) |
(р3=0,019) |
|
С-реактивный белок, мг/л, C-reactive protein, mg/L |
|||
|
1 группа / 1 group |
110 [59.25;164] |
21 [8; 60] |
13 [7; 19] |
|
2 группа / 2 group |
56 [15; 174] |
61.5 [28.25;111,5] |
43.5 [16.75;71] |
|
P- value |
(р4=0,479) |
(р5=0,017) |
(p6=0,025) |
Примечание: значимость отличий лейкоцитоза между группами р1 – исходно, р2 – на 3-и сут., р3 – на 7-е сут.; значимость отличий уровня С-реактивного белка между группами р4 – исходно, р5 - на 3-и сут., р6 – на 7-е сут.
Note: p-values denote the significance of intergroup differences: p1 (leukocytes at baseline), p2 (leukocytes on day 3), p3 (leukocytes on day 7); p4 (CRP at baseline), p5 (CRP on day 3), p6 (CRP on day 7).
Как показано в таблице (табл. 2), исходные уровни лейкоцитоза и С-реактивного белка (СРБ) в группах значимо не отличались (р1 и р4 >0,05). Анализ лабораторных показателей выявил более выраженную положительную динамику маркеров системного воспаления в 1 группе. К 3-м суткам лечения уровень лейкоцитов крови в 1 группе снизился до 8×10⁹/л, что было значимо ниже, чем во II группе (12×10⁹/л, при р2=0,001). К 7-м суткам этот показатель был также значимо ниже у больных 1 группы (7×10⁹/л против 10,5×10⁹/л, при р3=0,019).
Аналогичная тенденция наблюдалась и в динамике С-реактивного белка (СРБ). К 3-м суткам его концентрация в 1 группе составила 21 мг/л, что было значимо ниже, чем во 2 группе (61 мг/л, при р5=0,017). К 7-м суткам лечения уровень СРБ в I группе достиг 13 мг/л, оставаясь достоверно ниже, чем во 2 группе (43 мг/л, при p6=0,025).
Эти данные свидетельствуют о более эффективном купировании системного воспалительного ответа при использовании NPWT-i с инстилляцией протеолитических ферментов.
Результаты планиметрического анализа раневой поверхности на 7-е сутки после ПХО у больных обеих групп показаны на рисунке 1.
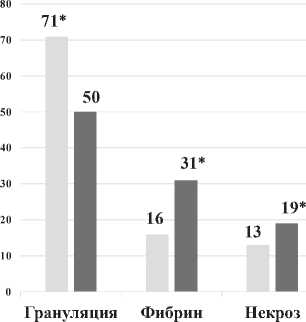
Рис.1. Результаты планиметрического анализа ран на 7 сут. после ПХО, % (* – при р <0,05)
I Группа
■ II Группа
Fig. 1. Results of planimetric analysis of wounds on day 7 after Primary surgical debridement’s, % (* – when p<0.05)
Как показано на рисунке 1, к 7-м сут. после ПХО площадь фибрина и некрозов в ране была статически значимо меньше в 1 группе больных, у которых применяли NPWT-i с инстилляцией протеолитических ферментов, а количество грануляций у больных этой группы было значимо больше. Это говорит о большей эффективности NPWT-i с инстилляцией протеолитических ферментов.
Результаты основных клинических исходов сравниваемых групп показаны в таблице 3.
Таблица 3
Основные клинические исходы лечения в сравниваемых группах, Ме [Q25; Q75]
Table 3
Main clinical outcomes of treatment in the compared groups, Ме [Q25; Q75]
|
Показатель эффективности, Efficacy indicator |
1 группа (n=15) 1 group |
2 группа (n=12) 2 group |
p-value |
|
Количество вторичных хирургических обработок (ВХО), Number of secondary surgical debridements |
3 [2; 3] |
4 [3; 5] |
0,015 |
|
Сроки госпитализации, дни, Hospital stay duration, days |
21 [16; 25] |
31 [21; 33] |
0,013 |
Как показано в таблице (табл. 3), в группе, получавшей NPWT-i с химотрипсином, потребовалось меньшее количество вторичных хирургических обработок (3 против 4; p=0,015), а средняя длительность стационарного лечения была значимо короче (p=0,013).
Таким образом, результаты исследования демонстрируют статистически и клинически значимые преимущества комбинированного NPWT-i с инстилляцией химотрипсина по сравнению со стандартным режимом NPWT-i с физиологическим раствором по всем основным критериям эффективности.
Обсуждение
Эволюция подходов к лечению ГНЗМТ отражает поиск наиболее эффективных методов, способных преодолеть ключевые клинические вызовы, связанные с антибиотикорези-стентностью, коморбидным фоном пациентов и значительными экономическими затратами на лечение [3, 4]. Основным и незаменимым методом лечения остается радикальная хирургическая обработка гнойного очага [1, 19]. Однако при обширных поражениях полная первичная некрэктомия часто невозможна, что диктует необходимость применения эффективных методов местного лечения раны [19, 20].
В качестве биохимической альтернативы механическому иссечению некротизированных тканей было предложено местное применение протеолитических ферментов, в частности, трипсина и химотрипсина. Их синергичное действие, основанное на гидролизе пептидных связей, обеспечивает эффективный протеолиз в очаге воспаления и модуляцию местного иммунного ответа [13–16]. Однако традиционные способы аппликации ферментов имеют принципиальные недостатки: быстрая инактивация в кислой среде раны и короткий период их ферментативной активности [19, 20].
Значительным технологическим шагом вперед стало внедрение NPWT-i, который интегрирует физические прин- ципы вакуум-терапии с возможностью контролируемого орошения [7, 8]. Применение физиологического раствора в рамках этой системы, как показали результаты исследований, способствует механическому очищению и поддержанию влажной среды, превосходя стандартные перевязки [9, 10]. Тем не менее, биохимическая пассивность физиологического раствора ограничивает его способность воздействовать на плотные некротические массы, что замедляет очищение ран и созревание грануляций.
Настоящее исследование подтверждает гипотезу о том, что интеграция протеолитического фермента (химотрипсина) в цикл NPWT-i создает синергичный эффект, преодолевающий ограничения каждого метода в отдельности. NPWT-i выступает в роли идеальной технологической платформы: он решает проблему быстрой инактивации химотрипсина за счет контролируемой подачи свежего раствора и своевременной эвакуации продуктов лизиса, поддерживая более благоприятный для ферментативной активности pH-баланс [20]. В свою очередь, химотрипсин усиливает очищающий потенциал самой вакуумной системы, осуществляя лизис некротических тканей и фибринозных наложений, которые остаются в ране после хирургической обработки, и облегчая их удаление в вакуумной фазе. Это прямое биохимическое воздействие объясняет полученные результаты: более быстрое снижение системных маркеров воспаления (лейкоцитоз, СРБ), ускоренное очищение раны от некротических тканей, активное формирование грануляционной ткани, сокращение потребности в повторных хирургических обработках и уменьшение длительности стационарного лечения [15, 16]. Клиническая эффективность напрямую коррелирует с экономической целесообразностью, снижая общие затраты на лечение [8, 10].
Таким образом, хирургическая обработка гнойного очага является основным методом лечения ГНЗМТ, а сочетание NPWT-i с инстилляцией протеолитических ферментов представляет собой качественно новый эффективный подход местного лечения ран, осуществляемого в оптимальных условиях. Это позволяет не только ускорить местные процессы заживления ран, но и позитивно влиять на системный воспалительный ответ, что особенно актуально для пациентов с отягощенным коморбидным фоном.
Заключение
Настоящее исследование подтверждает эффективность комбинации NPWT-i с протеолитическими ферментами (химотрипсин) для лечения гнойно-некротических заболеваний мягких тканей. Полученные результаты демонстрируют достоверное преимущество данного метода перед стандартным NPWT-i с физиологическим раствором по ключевым показателям: отмечается более быстрый регресс маркеров системного воспаления, сокращаются сроки очищения раны, уменьшается количество хирургических обработок, снижа- ются сроки госпитализации. Таким образом, применение раствора протеолитических ферментов при использовании метода местного отрицательного давления с инстилляцией создает синергетический эффект, оптимизируя методику лечения сложных ран.


