Методические и практические аспекты определения общей ртути в образцах цельной крови, мочи и волос методом масс-спектрометрии с индуктивно связанной плазмой
Автор: Уланова Т.С., Стенно Е.В., Вейхман Г.А., Недошитова А.В.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Экспериментальные модели и инструментальные исследования для оценки риска в гигиене и эпидемиологии
Статья в выпуске: 2 (22), 2018 года.
Бесплатный доступ
Точный, селективный и достаточный по чувствительности количественный метод определения химических веществ в объектах окружающей среды и организме человека зачастую является залогом корректной оценки рисков для здоровья. Оптимизированы условия проведения анализа образцов цельной крови, мочи и волос при определении содержания общей ртути методом масс-спектрометрии с индуктивно связанной плазмой (условия отбора и хранения проб, схема подготовки к анализу, параметры инструментальных настроек прибора, условия анализа). Количественное определение ртути в пробах крови, мочи и волос осуществлялось на масс-спектрометре Agilent 7500cx с октопольной реакционной/столкновительной ячейкой (Agilent Technologies, USA). Для подготовки к анализу образцов цельной крови использовали метод кислотного растворения в концентрированной азотной кислоте с последующим центрифугированием. Образцы мочи напрямую проанализированы после разведения 1/10 (V/V) 1 % раствором азотной кислоты. Предложенные условия рутинного анализа биосред при определении содержания общей ртути методом ИСП-МС позволяют выполнять определение элемента в крови в диапазоне концентраций 0,5-100 мкг/л при погрешности измерений 29,4 %, в моче 0,4-100 мкг/ л при погрешности измерений 24,2 %, в волосах 0,001-100 мкг/г при погрешности измерений 22,4 %. При валидации методики установлены пределы обнаружения (LOD) для крови 0,0015 мкг/л, для мочи 0,012 мкг/л, для волос 0,003 мкг/г. Правильность результатов подтверждена исследованием стандартных образцов крови SERONORM (Sero AS, Norway) blood L1 (LOT 1103128), L2 (LOT 1103129), L3 (LOT 1112691), мочи SeronormTM (Sero AS, Norway) urine (LOT 0511545) и волос Reference Material in Human Hair (IAEA-086,Vienna, Austria). Содержание общей ртути в крови детей определено в диапазоне 0,02-1,2 мкг/л, в моче 0,45-0,8 мкг/л. В моче экспонированных взрослых найдено 0,65-8,2 мкг/л, в волосах 0,29-0,49 мкг/г.
Ртуть, количественное определение, масс-спектрометрия, индуктивно связанная плазма, цельная кровь, моча, волосы, кислотное растворение
Короткий адрес: https://sciup.org/142212869
IDR: 142212869 | УДК: 543.064:616-074 | DOI: 10.21668/health.risk/2018.2.14
Methodical and practical aspects related to total mercury determination in whole blood, urine and hair with mass-spectrometry with inductively coupled plasma
A precise, selective, and sufficiently sensitive quantitative procedure for determining chemicals contents in environmental objects and a human body is often a key to correct health risk assessment. The authors describe optimized conditions for analyzing whole blood, urine, and hair samples used for determining total mercury contents with mass-spectrometry with inductively coupled plasma (sampling, samples storage, preparations to analysis, instrumental settings of a device, analysis conditions). We quantitatively determined mercury in blood, urine, and hair samples with Agilent 7500cx mass spectrometer with octopole reaction/collision cell (Agilent Technologies, USA). To prepare for whole blood samples analysis, we applied acid dilution in concentrated nitric acid with consequent centrifuging. Urine samples were directly analyzed after 1/10 (V/V) dilution with 1 % nitric acid solution. The suggested conditions of conventional biological media analysis applied in total mercury determining with mass spectrometry with inductively coupled plasma allow to determine the element in blood within 0.5-100 µg/l with measurement error being equal to 29.4 %; in urine, within 0.4-100 µg/l with measurement error being equal to 24.2 %; in hair, within 0.001-100 µg/l with measurement error being equal to 22.4 %. When validating the procedure, we found the following limits of detection (LOD): 0.0015 µg/l for blood; 0.012 µg/l, for urine; and 0.003 µg/l, for hair. Correctness of the results was confirmed by examination of standards blood samples SERONORM (Sero AS, Norway) blood L1 (LOT 1103128), L2 (LOT 1103129), L3 (LOT 1112691), urine samples SeronormTM (Sero AS, Norway) urine (LOT 0511545), and hair samples Reference Material in Human Hair (IAEA-086, Vienna, Austria). Total mercury contents in children's blood was determine within 0.02-1.2 µg/l; within 0.45-0.8 µg/l in urine. Contents in urine taken from exposed adults amounted to 0.65-8.2 µg/l, and to 0.29-0.49 µg/l in hair.
Текст научной статьи Методические и практические аспекты определения общей ртути в образцах цельной крови, мочи и волос методом масс-спектрометрии с индуктивно связанной плазмой
века связана с агглютинацией эритроцитов, ингибированием ферментов и нарушением белкового обмена. Ртуть попадает в организм ингаляционным, пероральным, трансдермальным путями и обнаруживается во всех органах и тканях человека [2–4]. По содержанию ртути в крови можно судить о недавнем или текущем заражении всеми формами ртути, по содержанию в моче – оценить текущее, недавнее заражение элементарной и неорганической ртутью, анализ волос позволяет определить поступление элемента в различные периоды времени [1, 5].
Референтные уровни содержания ртути в различных биосредах по данным научных изданий приведены в табл. 1.
Таблица 1
Референтные уровни содержания ртути в крови, моче (мкг/л) и волосах (мкг/г)
|
Автор (метод анализа) |
Кровь, мкг/л |
Моча, мкг/л |
Волосы, мкг/г |
|
ВОЗ, 2010 [5] |
5–10 |
5,6 (<10) |
<10 |
|
Н.У. Тиц (AAС) [3] |
0,6–59 |
<20 |
<15 |
|
Н.И. Калетина [4] |
3–11 |
2 |
0,5–1,5 |
|
А.В. Скальный [2] |
– |
0,1–2,0 |
0,05–2,0 |
|
C. Schulz (ИСП-МС) [6] |
0,8–1,0 |
0,4–0,7 |
– |
|
ALS Scandinavia (ИСП-МС) [7] |
0,46–7,5 |
0,14–4,2 |
0,05–0,93 |
|
J.P. Goulle (ИСП-МС) [8] |
0,94–8,13 |
0,14–2,22 |
0,31–1,66 |
По мнению исследователей Л.М. Каримовой, Т.К. Ларионовой и Г.Р. Башаровой [9], максимальный уровень содержания ртути в крови, при котором не наблюдаются сдвиги в гематологических, биохимических и иммунологических показателях, составляет 1 мкг/л. В методических рекомендациях по ранней диагностике токсического действия ртути в дозах малой интенсивности у детей (МР 2000/140), утвержденных Минздравом РФ, приводится фоновое содержание ртути в утренней моче детей
0,56 ± 0,07 мкг/л (диапазон 0,3–0,9 мкг/л)1. Комиссией по БМЧ Федерального агентства по окружающей среде Германии предложены референтные значения БМЧ-1 и БМЧ-2, составляющие для ртути в крови 5 и 15 мкг/л, а в моче – 7 и 25 мкг/л [1]. БМЧ-1 представляет собой концентрацию в биологическом материале, ниже которой нет риска для здоровья. При достижении концентрации уровня БМЧ-2 существует повышенный риск неблагоприятного воздействия, требующего устранения токсического воздействия. Очевидно, что значительные отличия в приведенных значениях и данных табл. 1 связаны не только с особенностями обследуемых популяций, но и с использованием различных методов анализа.
Для определения ртути в биосредах необходимы высокочувствительные и высокоэффективные методы анализа. К таким методам, в первую очередь, относятся масс-спектрометрия с индуктивно связанной плазмой и атомноабсорбционная спектрометрия с электротермическим вариантом атомизации (ААС-ЭТ)2 [10]. Атомно-абсорбционная спектрометрия при определении ртути обычно применяется в варианте абсорбции холодных паров ртути с использованием специальных ртутно-гидридных приставок (РГП) к атомно-абсорбционным спектрометрам или в ртутных анализаторах [11]. Метод атомной абсорбции холодных паров обладает высокой чувствительностью (пределы обнаружения не уступают ИСП-МС) и селективностью за счет отгонки паров элементной ртути от матрицы пробы. В то же время в работе Н.Б. Иваненко с соавт. [12] указано, что из-за невысокой производительности данные методы уступают место методу ИСП-МС. В РФ в 2003 г. утверждены и введены в действие МУК 4.1.1483-03 по определению содержания химических элементов, в том числе ртути, в биосубстратах методом ИСП-МС3. Диапазоны определения ртути в различных биосредах и БАД составляют: 0,1–10 мкг/л, погрешность оп- ределения 40 %, 10–100 мкг/л, погрешность определения 20 %, ПО 0,01 мкг/л.
Вместе с тем при количественном определении ртути методом ИСП-МС возникают некоторые трудности, обусловленные физико-химическими свойствами элемента. Ртуть представляет собой жидкий металл серебристого цвета, летучий, устойчивый к действию воздуха и воды. Высокая летучесть ртути определяет необходимость консервирования образца на стадии пробоотбора. Ртуть обладает очень высоким потенциалом ионизации 10,44 эВ, что при масс-спектрометрическом анализе существенно ограничивает эффективность ее ионизации в плазме и приводит к низкой чувствительности метода. Кроме того, существенное затруднение вызывает «эффект памяти». Данное мешающее влияние объясняется плохой смываемостью остаточных количеств ртути на подающих путях масс-спектрометра, распылительной камере и горелке, деталях интерфейса [12, 13].
Использование МУК 4.1.1483-033 в клинико-лабораторной практике для определения содержания ртути оказалось затруднительным, так как методика не устанавливает точных параметров подготовки образцов и условий анализа.
Таким образом, актуальность вышесказанного определила цель исследования – оптимизация условий рутинного анализа биосред при определении содержания общей ртути методом масс-спектрометрии с индуктивно связанной плазмой.
Материалы и методы. Количественное определение ртути в пробах крови, мочи и волос осуществляли на масс-спектрометре Agilent 7500cx с октопольной реакционной/столкно-вительной ячейкой (Agilent Technologies, USA) с транзисторным генератором 27,12 мГц. Для введения проб использовали двухканальную распылительную камеру Скотта, которая охлаждалась с помощью элемента Пельтье до 2 ° С. Скорость подачи образца в распылительную камеру составляла 0,4 мл/мин. Масс-спектрометр был оснащен плазменной горелкой Fassel с диаметром инжекторной трубки 2,5 мм. Использовался жидкий аргон высокой чистоты 99,998 % (ТУ-2114-005-00204760-99). Максимальная скорость потока аргона составляла 20 л/мин, давление в канале подводки газа 700 ± 20 кПа, Т плазмы=8000–10000 К. Автоматизация процесса проведения анализа обеспечивалась автосэмплером марки G3160B (Германия).
Для настройки чувствительности прибора использовали раствор 7Li, 59Co, 89Y, и 205Tl в 2 %-ной азотной кислоте с концентрацией 1 мкг/л для каждого элемента (Tuning Solution, USA). В качестве газа-реактанта применялся гелий газообразный высокой чистоты (99,995 %). Для приготовления растворов элементов внутреннего сравнения (IS) использовали комплексный стандартный раствор 209Bi, 73Ge, 115In, 6Li, 45Sc, 159Tb, 89Y с концентрацией 10 мг/л в 5 % водном растворе азотной кислоты (Internal Standard Mix, USA), а также стандартный раствор 103Rh с концентрацией 10 мг/л в 2 % водном растворе соляной кислоты (Rhodium Internal Standard, USA). Использовали кислоту азотную особо чистую с содержанием: As, Cd, Cu, Mn, Pb, Sr, V ≤ ≤ 0,01 мг/кг, Cr, Ni ≤ 0,02 мг/кг, Tl, Zn ≤ 0,05 мг/кг (Nitric acid 69 %, Sigma-Aldrich, США).
Для разбавления применяли деионизованную воду с удельным сопротивлением 18,22 Мом - см, очищенную в системе Milli-Q Integral (Millipore SAS, France). Лабораторную посуду из стекла, тефлона, полипропилена промывали в ультразвуковой мойке Elmasonic S 100H (Germany) при температуре 45-50 ° С: 3-4 раза в дистиллированной воде по 10 мин со сменой воды; затем 30 мин – в азотной кислоте, разбавленной дистиллированной водой 1:5; далее посуду промывали 2–3 % раствором соляной кислоты или раствором 1 %-ной азотной кислоты, содержащим 5 мкг/л хлорида золота.
Важным этапом химико-аналитических исследований является стадия отбора и хранения пробы, особенно при условии летучести исследуемых элементов. Так, для предотвращения потери ртути при хранении и транспортировке пробы необходимо замораживать или вносить раствор хлорида золота (III). При добавлении AuCl 3 в образцы необходимо использовать реакционно/столкновительные ячейки, поскольку ионы хлора ведут к интерференционным наложениям при определении ванадия, мышьяка и селена. Для эффективной ионизации ртути в плазменном потоке, для повышения чувствительности масс-спектрометра важно установить значение мощности частотного генератора 1500–1600 Вт и расстояние от горелки до отбирающего конуса порядка 7,0–7,5 мм. Перед проведением анализа осуществляли настройку прибора в режиме No Gas (без газа-реактанта), проверяли чувствительность, уровень фона, уровень вторичных оксидных и двухзарядных ионов, производили переключение на режим работы с реакционной ячейкой (Reaction mode).
Перед проведением анализа необходимо, чтобы гелий заполнил все подающие пути и реакционную ячейку со скоростью 10 мл/мин, далее прибор оставляли на 30 минут для стабилизации.
Для приготовления градуировочных растворов использовали стандартный раствор ионов ртути с концентрацией 10 мг/л в 5 % растворе азотной кислоты (Calibration Standard 2A – HG, USA).
Одним из способов минимизации «эффекта памяти» является определенный порядок измерения градуировочных растворов и непосредственно самих образцов: в плазму сначала подаются реальные пробы с низким содержанием ртути, а затем растворы для градуировки от самого низкого к более концентрированному. В настоящее время нами при исследовании ртути в образцах верхняя точка градуировочного графика не превышает 1,0 мкг/л, это также минимизирует загрязнение прибора, а следовательно, и «эффект памяти». Построение градуировочного графика проводили по точкам 0,0; 0,1; 0,5; 1,0 мкг/л (рисунок).
Для получения точных и достоверных результатов анализа необходимо, чтобы инструментальный фоновый уровень был минимальный. Из представленного на рисунке градуировочного графика видно, что концентрация, эквивалентная фону (BEC), не вносит вклад в результаты анализа. Коэффициент корреляции r равен 0,9995, а предел инстру- ментального обнаружения (DL) составляет 0,00478 мкг/л.
Одним из инструментальных приемов, позволяющих нивелировать матричное влияние насыщенной структуры матрицы крови, дрейф чувствительности прибора во время анализа, разность плотностей градуировочных и исследуемых растворов, низкую степень ионизации определяемых ионов, является установление оптимального элемента внутреннего сравнения ( IS ). Для этого использовали образцы крови с аттестованным значением содержания ртути и подвергали пробоподготовке с добавлением раствора комплексного внутреннего стандарта. Минимальные погрешности определения ртути в крови в различных диапазонах концентраций установлены при использовании в качестве внутреннего стандарта 159Tb и 103Rh. Немаловажным также является значение холостого опыта, в особенности при определении элемента на уровне нг/л. Так, при использовании159Tb и 103Rh холостая проба составляла порядка 8 мкг/л, при использовании 115In и 209Bi – порядка 18–19 мкг/л.
Кровь. Отбор проб крови производили из локтевой вены в вакуумные пробирки из полипропилена c напылением лития гепарина (PUTH, China). Возможно хранение проб в холодильнике (от 0 ° С до 4 ° С) в герметично закрытой пробирке до трех суток или длительное хранение при замораживании.
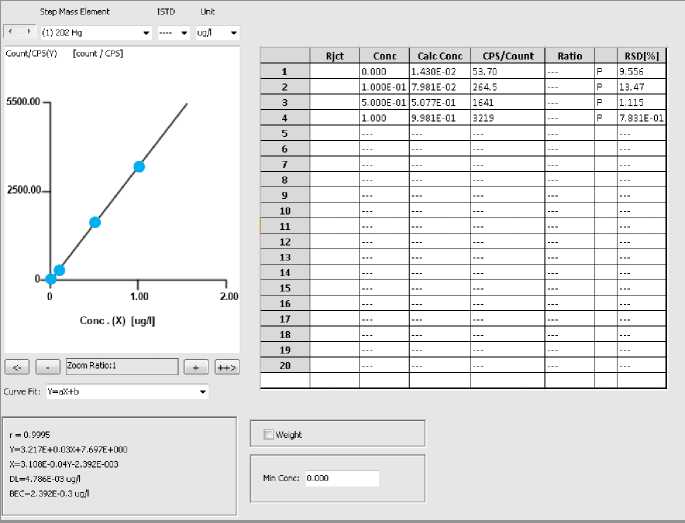
Рис. Градуировочный график для ионов ртути
Таблица 2
Метод «введено/найдено» для проб крови, мочи и волос
|
Образец |
ПО (LOD) в растворе |
В пробе без добавки |
В пробе с добавкой |
Введено/ найдено |
∆ , % |
|
Кровь (№ 1), мкг/л |
0,0015 |
0,012 |
0,03 |
0,02/0,018 |
10 |
|
Кровь (№ 2), мкг/л |
0,0015 |
0,042 |
0,065 |
0,02/0,023 |
15 |
|
Моча (№ 1), мкг/л |
0,012 |
0,080 |
0,19 |
0,1/0,11 |
10 |
|
Моча (№ 2), мкг/л |
0,012 |
0,045 |
1,18 |
1,0/1,14 |
14 |
|
Волосы (№ 1), мкг/г |
0,003 |
0,087 |
0,19 |
0,1/0,103 |
3 |
|
Волосы (№ 2, мкг/г |
0,003 |
0,147 |
0,253 |
0,1/0,105 |
5 |
Для разложения проб крови исследуемый образец объемом 0,1–0,2 мл вносили в конические центрифужные пластиковые пробирки с завинчивающейся крышкой, добавляли 0,2–0,4 мл азотной кислоты (68 %) и 0,1 мл комплексного внутреннего стандарта, далее тщательно перемешивали. Пробирки оставляли на 2–3 часа, далее доводили объем до 10 мл, центрифугировали 10 минут со скоростью 2700–3000 об./мин на центрифуге ЦЛМН–Р10–01– «Элекон» (Россия) и переносили в виалы для последующего масс-спектрометрического анализа. Параллельно для каждой серии проб готовили холостой опыт, который подвергался всем стадиям пробоподго-товки и включал все используемые реактивы, что и анализируемые пробы.
Моча. Отбор проб утренней мочи производили в стерильные полипропиленовые контейнеры на 125 мл с винтовой крышкой (F.L. Medical S.r.l., Torreglia, Italy). Образцы мочи напрямую анализировались после разведения 1/10 1 % раствором азотной кислоты: к 0,5 мл мочи добавляли 4,45 мл 1 % водного раствора HNO 3 и 0,05 мл раствора внутреннего стандарта.
Волосы. Волосы состригали с затылочной части головы на всю длину в количестве, позволяющем получить аналитическую пробу 0,1–0,2 г. Образцы волос хранили в бумажных пакетах. Разложение проб волос осуществляли в открытых пробирках: навеску волос массой 0,1–0,2 г помещали в конические пробирки из полипропилена вместимостью 15 мл, дозатором добавляли 0,1 мл раствора IS, добавляли 1–2 мл концентрированной азотной кислоты плотностью 1,415 г/см3, выдерживали 3–6 часов до растворения, добавляли 1–2 мл концентрированной перекиси водорода. Пробирку с содержимым взбалтывали, выдерживали 3–4 часа, затем доводили до 10 мл деионизованной водой и центрифугировали 10 мин на центрифуге ЦЛМН–Р10–01–«Элекон» (Россия) со скоростью 2700–3000 об./мин.
Контроль правильности результатов анализа образцов крови, мочи и волос проводили методом «введено/найдено» (табл. 2). Добавка вводилась в анализируемый образец перед про-боподготовкой. В табл. 2 приведены пределы обнаружения (LOD), рассчитанные по 3σ-кри-терию. Погрешность определения не превышала 15 %.
Проанализированы стандартные образцы крови SERONORM (Sero AS, Norway) blood L1 (LOT 1103128), L2 (LOT 1103129), L3 (LOT 1112691), мочи SeronormTM (Sero AS, Norway) urine (LOT 0511545) и волос Reference Material in Human Hair (IAEA-086, Vienna, Austria). Перед проведением анализа сертифицированные контрольные материалы подвергались той же процедуре подготовки, что и рабочие пробы. Контрольные образцы анализировались после каждой пятой реальной пробы. Данные табл. 3 свидетельствуют о достоверном совпадении между найденными и аттестованными значениями.
Таблица 3
Аттестованные и найденные средние значения содержания ртути в стандартных образцах крови, мочи и волос
|
Уровень |
Аттестованное значение |
Найденное среднее значение |
∆ , % |
|
SeronormTM urine ( n =5), мкг/л |
39,8 |
39,3 |
1,2 |
|
Seronorm blood L1 ( n =5), мкг/л |
1,5 |
1,71 |
14,0 |
|
Seronormblood L2 ( n =5), мкг/л |
16,0 |
17,3 |
8,1 |
|
Seronorm blood L3 ( n =4), мкг/л |
37,1 |
39,6 |
6,7 |
|
Reference Material in Human Hair ( n =10), мкг/г |
0,573 |
0,635 |
10,8 |
Предложенная методика была апробирована в рамках международной программы испытаний LAMP, организованной Агентством по охране окружающей среды США (CDC, Atlanta, USA). Результаты исследования образцов крови на содержание ртути представлены в табл. 4.
Результаты внешнего контроля качества свидетельствуют об удовлетворительных результатах, что подтверждает приемлемый Z -индекс, значение которого по модулю | Z |≤2.
Проведена метрологическая аттестация предлагаемой методики определения ртути в крови, моче, волосах, выполненная в соответствии с нормативными документами РМГ 61-2010, ГОСТ Р ИСО 5725-1-2002, ГОСТ Р ИСО 57252-2002, ГОСТ Р ИСО 5725-3-2002, ГОСТ Р ИСО 5725-4-2002, ГОСТ Р ИСО 5725-5-2002 и ГОСТ Р ИСО 5725-6-20024.
Методика выполнения измерений ртути в крови, моче и волосах обеспечивает получение результатов измерений с погрешностью, не превышающей значений, приведенных в табл. 5.
Таблица 4
Содержание ртути в образцах крови LAMP (CDC, Atlanta, USA)
|
Раунд/код пробы |
Аттестованное значение, мкг/л |
Найденное значение, мкг/л |
Z -индекс |
|
31/1402 |
3,13 |
3,43 |
0,6 |
|
31/1403 |
8,00 |
8,6 |
0,7 |
|
32/1404 |
4,13 |
4,6 |
0,2 |
|
32/1406 |
2,57 |
3,7 |
–0,4 |
|
33/1407 |
1,68 |
1,38 |
–0,6 |
|
33/1408 |
6,24 |
5,58 |
–0,3 |
|
33/1409 |
10,52 |
9,58 |
–0,2 |
Таблица 5
Метрологические характеристики методики определения ртути в растворе, мкг/л
|
Наименование определяемого компонента и диапазон измерений в растворе |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σ r , % |
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости) σ R , % |
Показатель точности (границы относительной погрешности при вероятности р =0,95), ±δ, % |
|
Кровь, мкг/л, от 0,005 до 1,0 вкл. |
9,19 |
13,23 |
29,42 |
|
Моча, мкг/л, от 0,04 до 1,0 вкл. |
10,36 |
10,42 |
24,25 |
|
Волосы, мкг/г, от 0,1 до 1,0 вкл. |
9,52 |
9,74 |
22,43 |
Таблица 6
Содержание ртути в диагностируемых биосредах
|
Материал |
Группа |
Пермский край |
Канада [16] |
Россия [14] |
Германия [6, 17] |
БМЧ-1 [1, 6] |
|
Кровь, мкг/л |
Взрослые |
– |
0,12–4,7 |
0,89–2,39 |
0,02–16 |
5 |
|
Дети |
0,02–1,2 |
0,27–6,39 |
0,2–0,43 |
0,8–1,0 |
||
|
Моча, мкг/ л |
Взрослые |
0,65–8,2 |
0,2–3,5 |
0,27–0,94 |
– |
7 |
|
Дети |
0,45–0,8 |
0,2–2,82 |
– |
0,4–0,8 |
||
|
Волосы, мкг/г |
Взрослые |
0,29–0,49 |
– |
0,21–0,54 |
– |
1 |
Разработанная методика определения ртути в биосредах на базе метода ИСП-МС позволяет выполнять определение элемента в крови в диапазоне концентраций 0,5 – 100 мкг/л при погрешности измерений 29,4 %, в моче – 0,4 – 100 мкг/л при погрешности измерений 24,2 %, в волосах – 0,001 – 100 мкг/г при погрешности измерений 22,4 %. Установлены ПО (LOD) для крови 0,0015 мкг/л, для мочи 0,012 мкг/л, для волос 0,003 мкг/л.
Результаты и их обсуждение. Апробация предлагаемой методики проведена при обследовании пациентов стационара и поликлиники ФБУН «ФНЦ медико-профилактических технологий управления рисками здоровью населения» (табл. 6). В таблице представлены данные о содержании ртути в биосредах жителей Канады, России и Германии. В обследуемой нами группе детей содержание ртути в крови и моче ниже уровня БМЧ-1. В моче экспонированных взрослых содержание ртути превышает уровень БМЧ-1.Уровни ртути в моче у неэкспонируемых жителей России составляют 0,27–0,94 мкг/л [14], а в группе рабочих промышленного предприятия 0,2–25,3 мкг/л [15].
В группе детей содержание ртути в моче, найденное нами, находится на уровне такового у детей Германии [6].
Найденное нами содержание ртути в волосах взрослых соответствует всем приведенным литературным данным [1, 6].
Выводы:
-
1. На основании проведенных исследований предложены оптимальные условия рутинного анализа биосред при определении содержания общей ртути методом масс-спектрометрии с индуктивно связанной плазмой, позволяющие выполнять определение элемента в крови в диапазоне концентраций 0,5 – 100 мкг/л при погрешности измерений 29,4 %, в моче – 0,4 – 100 мкг/ л при погрешности измерений 24,2 %, в волосах – 0,001 – 100 мкг/г при погрешности измерений 22,4 %.
-
2. Получена высокая сходимость результатов определения ртути в крови при участии в международной программе испытаний LAMP (| Z |≤2).
-
3. Предлагаемая методика определения ртути в крови, моче и волосах методом ИСП-МС апробирована при обследовании детей и экспонированных взрослых. Полученные результаты удовлетворительно корреспондируются с литературными данными.
-
4. Уровни ртути в биосредах неэкспонированных жителей Пермского края не превышают рекомендованных ВОЗ уровней БМЧ-1.
Финансирование. Исследование не имело спонсорской поддержки.
Список литературы Методические и практические аспекты определения общей ртути в образцах цельной крови, мочи и волос методом масс-спектрометрии с индуктивно связанной плазмой
- Биомониторинг человека: факты и цифры . -Копенгаген: Европейское региональное бюро ВОЗ, 2015. -URL: http://www.euro.who.int/ru/health-topics/environment-and-health/health-impact-assessment/publications/2015/human-biomonitoring-facts-and-figures (дата обращения: 18.01.2018).
- Скальный А.В., Рудаков И.А. Биоэлементы в медицине. -М.: Мир, 2004. -272 с.
- Тиц Н.У. Клиническое руководство по лабораторным тестам. -М.: Юнимед-пресс, 2003. -960 с.
- Токсикологическая химия. Метаболизм и анализ токсикантов/под ред. Н.И. Калетиной. -М.: Издательская группа ГЭОТАР-Медиа, 2008. -1016 с.
- Программа Организации Объединенных Наций по окружающей среде. UNEP (DTIE)/Hg/INC.2/6,2/9. 22 October 2010 //DocPlayer.ru. -URL: http://docplayer.ru/72077878-Programma-organizacii-obedinennyh-naciy-po-okruzhayushchey-srede.html (дата обращения: 18.01.2018).
- Revised and new reference values for environmental pollutants in urine or blood of children in Germany derived from the German Environmental Survey on Children 2003-2006 (GerESIV)/Ch. Schulz, J. Angerer, U. Ewers, U. Heudorf, M. Wilhelm//Int. J. Hyg. Environ. Health. -2009. -Vol. 212. -P. 637-647.
- Trace elements in human biological material //ALS Scandinavia. -URL: https://www.alsglobal.se/media-se/pdf/reference_data_biomonitoring_120710.pdf (дата обращения: 18.01.2018).
- Goulle J.P., Mahieu L., Castermant J. Metal and metalloid multi-elementary ICP-MS validation in whole blood, plasma, urine and hair: Reference values//Forensic Science International. -2005. -Vol. 153. -P. 39-44.
- Карамова Л.М., Ларионова Т.К., Башарова Г.Р. Критерии экологической безопасности тяжелых металлов в крови человека//Медицина труда и промышленная экология. -2010. -№ 6. -С. 21-23.
- Иваненко Н.Б., Иваненко А.А., Носова Е.Б. Определение токсических и фоновых содержаний ртути в крови атомно-абсорбционным методом с электротермической атомизацией и Зеемановской модуляционной поляризационной коррекцией фона//Вестник Санкт-Петербургского университета. Физика и химия. -2010. -№ 4. -С. 97-104.
- Использование Зеемановского спектрометра для определения ртути в моче/С.Е. Погарев, В.В. Рыжов, Т.В. Древаль, Н.Р. Машьянов//Экологическая химия. -1994. -Т. 3. -С. 227.
- Иваненко Н.Б., Ганеев А.А., Соловьев Н.Д. Определение микроэлементов в биологических жидкостях (Обзор)//Журнал аналитической химии. -2011. -Т. 66, № 9. -С. 900-915.
- Определение химических форм микроэлементов в биологических объектах/Н.Б. Иваненко, Н.Д. Соловьёв, А.А. Иваненко, Л.Н. Москвин//Аналитика и контроль. -2012. -Т.16, № 2. -С. 108-133.
- Применение стандартизованной методологии биомониторинга человека для оценки пренатальной экспозиции к ртути/А.И. Егоров, И.Н. Ильченко, С.М. Ляпунов, Е.Б. Марочкина, О.И. Окина, Б.В. Ермолаев, Т.В. Карамышева//Гигиена и санитария. -2014. -Т. 93, № 5. -С. 10-18.
- Оценка биомаркеров экспозиции к сварочному аэрозолю/Е.В. Зибарев, М.В. Чащин, С.М. Никонова, З.С. Кусраева, А.В. Кузьмин, D.G. Ellingsen, Y. Thomassen//Медицина труда и промышленная экология. -2010. -№ 4. -С.14-17.
- Results of the Canadian Health Measures Survey Cycle 1 (2007-2009) [Электронный ресурс] // Government of Canada. - URL: https://www.canada.ca/en/health-canada/services/environmental-workplace-health/reports-publications/environmental-contaminants/report-human-biomonitoring-environmental-chemicals-canada-health-canada-2010.html (дата обращения: 18.01.2018).
- Heitland P., Koster H.D. Biomonitoring of 37 trace elements in blood samples from inhabitants of northern Germany by ICP -MS//J. of Trace Elements in Medicine and Biology. -2006. -Vol.20. -P. 253-262.


