Методика прогнозирования прогрессирующего фиброза печени у больных коинфекцией вируса иммунодефицита человека и вирусного гепатита С
Автор: Масляков В.В., Аристанбекова М.С.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Оценка риска в организации здравоохранения
Статья в выпуске: 2 (30), 2020 года.
Бесплатный доступ
Разработана система прогнозирования характера фиброзного процесса у больных, коинфицированных вирусом иммунодефицита человека (ВИЧ) и вирусным гепатитом С (ВГС), и оценена ее эффективность с позиций особенностей противовирусной терапии инфекционного процесса. В исследование вошли 459 больных с верифицированным диагнозом коинфекции ВИЧ / ВГС, которые в течение года наблюдались в Государственном учреждении здравоохранения «Саратовский областной центр профилактики и борьбы со СПИД». Среди пациентов преобладали мужчины в возрастной группе моложе 36 лет. У 72-78 % больных были диагностированы стадии 3-4А ВИЧ-инфекции. Остальные пациенты находились на стадиях 4Б-4В. 32 % больным проводилась только антиретровирусная терапия с использованием комбинации препаратов из групп нуклеозидных и ненуклеозидных ингибиторов обратной транскриптазы, ингибиторов протеазы и ингибиторов интегразы в различных сочетаниях. 14 % коинфицированных ВИЧ и вирусным гепатитом С получали только противовирусную терапию, направленную на вирусный гепатит С, на основе пегилированного интерферона α и рибавирина или препаратов прямого действия - софосбувира и даклатасвира...
Коинфекция вич / вгс, инфекционный процесс, прогрессирующий фиброз печени, эластометрия, субпопуляции т-лимфоцитов, противовирусная терапия, индекс высокого риска, критерии риска, т-lymphocytes subpopulations
Короткий адрес: https://sciup.org/142224428
IDR: 142224428 | УДК: 616-099 | DOI: 10.21668/health.risk/2020.2.16
Procedure for predicting progressing hepatic fibrosis in patients with human immunodeficiency and hepatitis C coinfection
Our research goal was to develop a system for predicting nature of fibrosis processes in patients infected with HIV and Hepatitis C virus and to assess its efficiency bearing in mind peculiarities of anti-virus therapy applied for treating the infections. Research was performed on 459 patients with confirmed HIV/viral hepatitis C who had been treated for 1 year at Saratov Regional Center for AIDS Prevention and Elimination. Most patients were males younger than 36. 72-78 % patients had 3-4A HIV infection stages. The rest had 4B-C stages. 32 % were treated only with sets of anti-retroviruses medications made up of nucleoside and non-nucleoside inhibitors of reverse transcriptase, inhibitors of protease, and inhibitors of integrase in different combinations. 14 % patients infected with both HIV and Hepatitis C virus were treated only with antiviral medications aimed for treating hepatitis C and made up of pegylated interferon α and ribavirin or medications with direct effects such as sofosbuvir and daclatasvir...
Текст научной статьи Методика прогнозирования прогрессирующего фиброза печени у больных коинфекцией вируса иммунодефицита человека и вирусного гепатита С
Коинфекция вируса иммунодефицита человека и вирусного гепатита С (ВИЧ / ВГС) имеет не только более тяжелое течение, но и в значительной степени определяет летальность среди пациентов за счет быстрого прогрессирования поражения печени. Отмечено также, что у ВИЧ-инфицированных пациентов с гепатитом С повышается риск внепеченочных проявлений [1] и гепатотоксического эффекта антиретровирусных (АРВ) препаратов [2]. В связи с этим на первый план выступает проблема прогнозирования прогрессирующего течения фиброза печени, а также лечения хронического гепатита С (ХГС), развивающегося у больных, коинфицированных ВИЧ / ВГС. В последние годы появилась новая стратегия, касающаяся лечения ХГС именно при коинфекции ВИЧ / ВГС. До настоящего времени единственным способом противовирусной терапии ХГС служила комбинация пегилированного рекомбинантного интерферона α (ИФНα) и рибавирина, схема использования которой зависела от генотипа ВГС. Этот способ лечения связан с развитием многочисленных по- бочных эффектов. Довольно значительной когорте больных, страдающих нейропсихическими или сердечно-сосудистыми расстройствами, лечение интерферонами было противопоказано [3, 4]. Применение этой схемы приводит к развитию устойчивого вирусологического ответа примерно только у 40 %, если речь идет о пациентах, коинфицированных ВИЧ и ВГС [5].
В 2011 г. началась эра внедрения новых противовирусных препаратов прямого действия на ВГС. В инфекционную практику были введены ингибиторы NS3/4A протеаз ВГС (телапревир и боцепревир) для лечения ВГС-инфекции, вызванной генотипом 1 вирусного возбудителя, в комбинации с пегилиро-ванным интерфероном α и рибавирином [6, 7]. По мере развития этого направления появились препараты с более широким спектром механизмов воздействия на ВГС, которые позволяли их применение без использования ИФН [8]. Однако возникла новая проблема – возможность взаимодействий между антиретровирусными агентами и препаратами прямого действия для лечения ВГС-инфекции [9].
Масляков Владимир Владимирович – доктор медицинских наук, профессор, проректор по научной работе (e-mail: ; тел.: 8 (903) 023-71-69; ORCID: .
Аристанбекова Майра Садыковна – аспирантка кафедры клинической медицины (e-mail: ; тел.: 8 (4952) 74-27-21; ORCID: .
Решение всех этих проблем, чрезвычайно актуальных для современной инфектологии, поставило перед клинической медициной еще одну задачу: создание системы четкого прогнозирования прогрессирующего характера фиброза печени у больных, коинфицированных ВИЧ и ВГС. В основе – существующие диагностические методы, цель – последующая разработка показаний для назначения адекватных методов лечения. В настоящее время не вызывает сомнений, что ВГС-инфекция значительно быстрее прогрессирует у ВИЧ-инфицированных лиц [10, 11], поскольку ВИЧ-инфекция многократно (в 2–5 раз) увеличивает частоту перехода острого гепатита С в хроническую форму, способствует развитию цирроза печени, гепатоклеточной карциномы, декомпенсации печени вплоть до полной потери ее жизненно важных функций [12]. При этом около 60 % летальных исходов при коинфекции ВИЧ / ВГС связаны именно с поражением печени [13]. Сложность проблемы оценки эффективности противовирусной терапии при коинфекции ВИЧ / ВГС может быть связано и с тем обстоятельством, что антиретровирусные и анти-ВГС-препараты могут взаимодействовать между собой [9, 14–20]. Была создана система выявления высокого риска прогрессирующего течения фиброза печени у больных с коинфекций ВИЧ / ВГС, включающая разработку количественного интегрального показателя для оценки риска, а также алгоритма его расчета и использования для проведения антиретровирусной и анти-ВГС-терапии.
Цель исследования – разработать систему прогнозирования характера фиброзного процесса у больных, коинфицированных ВИЧ и ВГС, и оценить ее эффективность с позиций особенностей противовирусной терапии инфекционного процесса.
Материалы и методы. В течение года под наблюдением в Государственном учреждении здравоохранения «Саратовский областной центр профилактики и борьбы со СПИД» находились 459 больных с верифицированным диагнозом коинфекции ВИЧ / ВГС. Критериями отбора пациентов в исследование служили: верифицированный диагноз ВИЧ-инфекции и хронического гепатита С; отсутствие этиотропной терапии по поводу ВГС на момент исследования; 3–4В стадии ВИЧ-инфекции в соответствии с классификацией В.И. Покровского; наличие у больных наркотической зависимости разной степени выраженности; возраст от 25 до 57 лет; информированное согласие на обследование.
Критерии исключения пациентов из исследования: наличие тяжелых сопутствующих соматических и психических заболеваний, ожирение; сопутствующие аутоиммунные и аллергические заболевания, принадлежность к группе часто и длительно болеющих; наличие вирусных гепатитов другой этиологии (не ХГС), аутоиммунного гепатита, лекарственных поражений печени, стеатоза печени; отказ от участия в исследовании. Среди пациентов преобладали мужчины в возрастной группе моложе
36 лет. У 72–78 % больных были диагностированы стадии 3–4А ВИЧ-инфекции, остальные пациенты находились на стадиях 4Б–4В. Около 67 % поражены генотипом 1b ВГС, 1 % – генотипом 2 a , а остальные – генотипом 3. Всем пациентам в течение всего срока наблюдения проводилась транзиентная эластомет-рия печени, результаты которой выражались в кПа. Стадии фиброзного процесса оценивались в соответствии со шкалой METAVIR. По исходным данным у 40 % больных фиброзных изменений в печени не наблюдалось (стадия F0), у 20 % отмечен дебют фиброзного процесса (стадия F1), 16 % пациентов находились на стадии значимого фиброза печени (стадия F2), 8 % – на стадии выраженного фиброза (стадия F3), у 16 % больных развился цирроз печени (стадия F4). 35 % наблюдаемых пациентов противовирусной терапии не получали. 32 % больных проводилась только антиретровирусная терапия с использованием комбинации препаратов из групп нуклеозидных и ненуклеозидных ингибиторов обратной транскриптазы, ингибиторов протеазы и ингибиторов интегразы в различных сочетаниях. 14 % коинфици-рованных ВИЧ / ВГС получали только противовирусную анти-ВГС-терапию на основе пегилирован-ного интерферона α и рибавирина или препаратов прямого действия – софосбувира и даклатасвира. 19 % пациентов назначалась как противовирусная анти-ВГС, так и антиретровирусная терапия. Всем больным, помимо лабораторных исследований, подтверждающих диагноз коинфекции ВИЧ / ВГС (серологические исследования методом иммунофер-ментного анализа, иммуноблоттинг, ПЦР-диагнос-тика), на протяжении всего срока наблюдения проводился лабораторный мониторинг с использованием клинического и биохимического анализа крови, определением вирусной нагрузки ВИЧ и ВГС в крови методом ПЦР в реальном времени, иммунологических исследований методом проточной ци-тофлуориметрии.
Иммуноферментный анализ крови (ИФА) проводился для определения в сыворотке крови антител-маркеров ВИЧ-инфекции и вирусного гепатита С с использованием ридера микропланшетного Dynex MRX II (Dynex technologies, USA) на основе диагностических тест-систем Abbot (CША). Исследование выполнялось в соответствии с инструкцией по применению прибора и тест-систем. Иммуноблоттинг осуществлялся для определения в сыворотке крови белков ВИЧ-1 с использованием электрофоретического оборудования в комплекте с программным обеспечением GelDoc (Bio-Rad, USA) и тест-системы Genescreen Plus HIV Ag-AB (Bio-Rad, USA) в соответствии с инструкцией по применению прибора и тест-систем. Полимеразная цепная реакция (ПЦР) использовалась для определения наличия в крови РНК ВИЧ и РНК ВГС, вирусной нагрузки ВИЧ и ВГС, генотипа ВГС и осуществлялась на базе ПЦР-анали-затора COBAS 50 TaqMan 48 с автоматизированной станцией пробоподготовки COBAS® AmpliPrep
(Roche Diagnostic Systems, USA). Исследование состояло из следующих этапов: выделение РНК (про-боподготовка), реакция обратной транскрипции, ПЦР-амплификация к ДНК ВИЧ в режиме реального времени для количественного определения вирусной нагрузки в соответствии с инструкцией по применению прибора и реагентов. Качественное и количественное определение РНК ВГС в плазме крови проводилось с использованием тест-системы Hoffman-LaRoche при ее чувствительности 15 МЕ/мл. Транзиент-ная фиброэластометрия печени проводилась на аппарате Fibroscan (Франция). Исследование выполнялось всем пациентам до лечения и через 48 недель (по окончании лечения) с определением стадии фиброза печени, соответствующей шкале METAVIR, и измерением в кПа. Гемометрия применялась для клинического исследования периферической крови с подсчетом форменных элементов в единице объема и проводилась на автоматическом гематологическом анализаторе SWELAB Alfa Basic (Швеция). В исследовании использовался показатель числа тромбоцитов, 109/л. Биохимический анализ крови проводился на автоматическом биохимическом анализаторе FURUNO 270 (Япония) с определением: аспартатаминотрансферазы (АСТ), мкмоль/мин·л; аланин-51-аминотрансферазы (АЛТ), мкмоль/мин·л; щелочной фосфатазы (ЩФ), мкмоль/мин·л; лактатдегидрогеназы (ЛДГ), мкмоль/мин·л; общего белка, г/л; альбумина, г/л; общего и прямого билирубина, мкмоль/л; холестерина, г/л; глюкозы, г/л. Проточная цитофлуо-риметрия осуществлялась для определения иммунологических показателей с использованием FACS Calibur (Beckton Diсkinson, USA) после автоматизированной пробоподготовки крови с помощью станции BD FACS Sample Prep Assistant II (Becton Dickinson, США) в соответствии с инструкцией по применению приборов и моноклональных антител. Для обработки полученных данных применялось программное обеспечение FACS Diva. Определение проводилось на основе стандартизированного комплекта моноклональных антител BD Multitest 6-Color TBNK Reagent (BD Biosciences, США). В исследовании анализировались показатели абсолютного содержания в крови числа CD3+CD4+ лимфоцитов (Т-хелперов и CD3+CD8+ клеток (цитотоксических Т-лимфоцитов). По результатам исследования подсчитывался иммунорегуляторный индекс (ИРИ) по формуле: ИРИ = CD3+CD4+ / CD3+CD8+.
Статистическая обработка данных проводилась на основе пакета статистических программ SPSS (версия 21) в соответствии с инструкцией по его применению.
Результаты и их обсуждение. В соответствии с характером течения фиброзного процесса – прогрессирующим, стабильным, регрессирующим – проведена группировка всех обследованных, коин-фицированных ВИЧ и ВГС. Основой такого исследования послужили данные транзиентной эласто-метрии, выполненной каждому пациенту как в нача- ле наблюдения, так и по его окончании – через год. Заболевание считалось прогрессирующим, если показатели эластометрии печени возрастали через год более чем на 10 % с переходом больного на следующую стадию фиброза печени, и регрессирующим, если показатели эластометрии в течение года снижались более чем на 10 %, и больной возвращался на предыдущую стадию фиброзного процесса. Все остальные случаи расценивались как стабильное течение фиброза печени. В результате оказалось, что среди 459 наблюдаемых пациентов, коинфици-рованных ВИЧ / ВГС, у 16 % наблюдался прогрессирующий фиброз печени, у 65 % – стабильный и у 19 % – регрессирующий (таблица).
Соответствие динамики показателей эластометрии течению фиброза печени у больных, коинфицированных ВИЧ и ВГС
|
Течение фиброза печени |
Показатели эластометрии (кПа): Ме [min; max] |
р |
|
|
исходные данные |
через год |
||
|
Прогрессирующее течение, n = 73 |
6,7 [4,0; 12,9] |
7,7 [4,0; 28,0] |
< 0,001* |
|
Стабильное течение, n = 297 |
5,8 [2,8; 75,0] |
5,8 [3,0; 75,0] |
0,950 |
|
Регрессирующее течение, n = 89 |
7,7 [4,7; 22,5] |
5,8 [3,5; 15,4] |
< 0,001* |
П р и м е ч а н и е : n – число больных в группе; р – вероятность различий между исходными данными и данными, полученными через год; * – достоверность различий по критерию Манна – Уитни при р < 0,05.
Правомочность такого подхода к оценке фиброзного процесса была подтверждена статистически. Так, при прогрессирующем течении наблюдался статистически достоверный переход от исходной медианы показателя эластометрии 6,7 кПа до 7,7 кПа через год (рост примерно на 15 %). При стабильном течении медиана практически не менялась и находилась в диапазоне 5,8 кПа. При регрессирующем течении медиана достоверно снижалась с 7,7 до 5,8 кПа, то есть примерно на 13 %. Подобный подход к группировке данных был использован нами впервые и аналогов в доступной научной литературе не имеет.
Следующий этап исследования был посвящен определению инструментальных и лабораторноиммунологических критериев для идентификации группы высокого риска неблагоприятного течения фиброза печени у больных, коинфицированных ВИЧ и ВГС. В качестве количественных параметров исследовались показатели эластометрии, а также рутинные гематологические, биохимические, вирусологические и иммунологические данные, которые традиционно используются для мониторинга фиброза печени при ХГС или течения ВИЧ-инфекции, в том числе и в условиях коинфицирования: нару- шение эластичности ткани печени, кПА, число тромбоцитов, активность АЛТ, АСТ, щелочной фосфатазы, ЛДГ, уровни общего белка, альбумина, общего билирубина, холестерина, глюкозы, вирусная нагрузка ВИЧ, вирусная нагрузка ВГС, число CD3+CD4+ и CD3+CD8+ лимфоцитов, иммунорегу-ляторный индекс. Как показал статистический анализ, данные эластометрии позволяли довольно четко дифференцировать группы высокого и низкого риска. В частности, значения выше 7 кПа были характерны для группы высокого риска. Среди рутинных гематологических и биохимических данных ни один из показателей не свидетельствовал о статистически достоверных различиях у коинфицированных больных с разным характером течения фиброза печени. Что касается иммунологических показателей крови, то все они достоверно отличались от контрольных данных, но их различия в зависимости от риска прогрессирующего течения фиброзного процесса были ограничены только двумя показателями – числом Т-хелперов (CD3+CD4+) и иммунорегуляторным индексом. Статистическая оценка прогностической ценности отклонений этих показателей выявила, что при значениях ниже 400 клеток в мл число Т-хелперов позволяет прогнозировать принадлежность больного к группе высокого риска с высокой прогностической точностью (AUROC = 0,818), как и ИРИ при значениях ниже 0,45 (AUROC = 0,793).
Таким образом, к критериям риска прогрессирующего течения фиброза печени можно отнести несколько факторов: показатель эластометрии печени, число CD3+CD4+ клеток в крови, иммуноре-гуляторный индекс. На основе этих данных был разработан интегральный показатель оценки количественных критериев риска для случаев первичного обращения больного или его кратковременного наблюдения. С этой целью проводился регрессионный анализ полученных количественных данных в выделенных нами группах высокого и низкого риска прогрессирующего течения фиброза печени. При проведении регрессионного анализа в качестве независимых переменных использовались следующие данные: исходные показатели эла-стометрии печени, число Т-хелперов, иммунорегу-ляторный индекс; в качестве зависимой переменной – оценка факторов риска в баллах, а в качестве переменной отбора наблюдений – принадлежность к группе высокого риска прогрессирующего течения фиброза печени. Полученное уравнение регрессии имело следующий вид: ИВР = 4,070 + + 0,099·кПа + 0,476·CD4 – 0,518·ИРИ, где кПа – показатель исходной эластометрии, CD4+ – абсолютное число СD3+CD4+ клеток/мл крови, ИРИ – иммунорегуляторный индекс. Результат решения этого уравнения был обозначен нами как индекс высокого риска (ИВР) прогрессирующего течения фиброза печени. Определение 95%-ного доверительного интервала ИВР в группах высокого и низкого риска больных с коинфекцией ВИЧ / ВГС
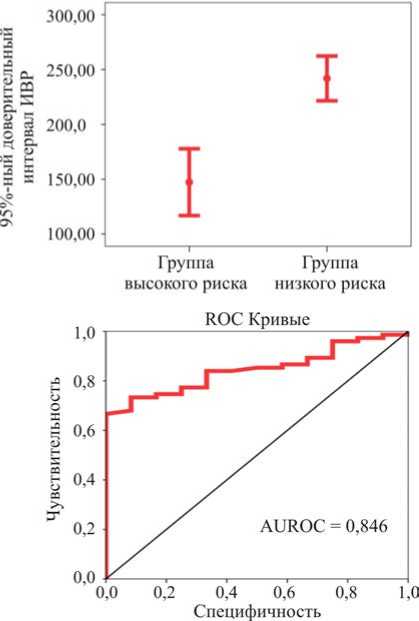
Рис. 95%-ные доверительные интервалы и ROC-кривые ИВР в группах высокого и низкого риска прогрессирующего фиброза печени у больных, коинфицированных ВИЧ / ВГС показало его высокое прогностическое значение (AUROC = 0,846) при данных ниже 180. Эта часть работы носит приоритетный характер (рисунок).
Два последних этапа исследования касались проверки значения индекса высокого риска неблагоприятного течения фиброзного процесса у больных, коинфицированных ВИЧ и ВГС, для назначения или коррекции антиретровирусной терапии, противовирусной терапии ХГС, сочетания антиретровирусной терапии и противовирусной терапии ХГС.
Приводим несколько клинических примеров из собственных наблюдений.
Клинический пример 1. Выписка из амбулаторной карты пациента с инфекцией ВИЧ / ВГС, получавшего антиретровирусную терапию, иллюстрирующая быстрое прогрессирование фиброза печени на фоне комбинации препаратов нуклеозидных ингибиторов обратной транскриптазы и ненуклеозидных ингибиторов обратной транскриптазы. Больной З., 36 лет, находится на диспансерном учете в ГУЗ «Центр СПИД» с диагнозом: ВИЧ-инфекция, стадия 4А. Хронический вирусный гепатит С, стадия репродукции вируса. Заражение произошло при внутривенном использовании ПАВ (психоактивных веществ). На момент включения больного в исследование была установлена давность выявления гепатита С – в 2002 г., а ВИЧ-инфекция ранее – в 2000 г. В настоящее время отрицает прием ПАВ, употреб- ляет – пиво 1,0–1,5 л в неделю. Ранее противовирусную терапию не принимал. При включении в исследование на осмотре 01.08.2015 г.: рост – 169 см, вес – 57 кг. Состояние удовлетворительное, жалобы на слабость, быструю утомляемость. Объективно: кожа и видимые слизистые обычной окраски, чистые. Периферические лимфоузлы: шейные, подчелюстные, подмышечные увеличены. В легких выслушивается везикулярное дыхание, хрипов нет. Тоны сердца приглушены, ритм правильный, шумов нет, ЧСС = PS = 78 уд. в мин, АД – 125/75 мм рт. ст., температура тела - 36,7 °С. Живот мягкий, безболезненный во всех отделах при пальпации, печень выступает из-под края реберной дуги на 1 см, край ровный, гладкий, поверхность эластическая. Селезенка увеличена. Симптом поколачивания отрицательный с обеих сторон. Физиологические отправления в норме. Сознание ясное. Очаговой и менингеальной симптоматики нет. В общем анализе крови: гемоглобин – 146 г/л, тромбоциты – 175,0·109 /л, лейкоциты – 7,3·109 /л. В общем анализе мочи – патологии не выявлено. В биохимическом анализе крови: АЛТ – 53 МЕ/л, АСТ – 51 МЕ/л, общий билирубин – 13,6 ммоль/л, ЛДГ – 231 МЕ/л. Показатели иммунитета: CD4+ лимфоциты – 195 клеток/мл, CD8 – 741 клеток/мл, ИРИ – 0,26. Методом ПЦР выявлена РНК ВГС 1,7·106 МЕ/мл, генотип 1б, РНК ВИЧ – 121300 копий /мл. УЗИ органов брюшной полости: гепатомегалия, диффузные изменения паренхимы печени, спленомегалия. При выполнении эластометрии печени установлен фиброз первой степени (F1) = 6,1 кПа по шкале METAVIR. Учитывая иммунологические показатели, а также показатели вирусной нагрузки, данные эластометрии печени, пациенту решением врачебной комиссии назначена антиретровирусная терапия (АРВТ) в комбинации препаратов: нуклеозидных ингибиторов обратной транскриптазы (зидовудин+ламивудин) и ненуклеозидных ингибиторов обратной транскриптазы (эфа-виренз). На фоне АРВТ в течение 6 месяцев уменьшилась вирусная нагрузка по РНК ВИЧ до неопределяемого уровня (менее 20 копий/мл), улучшились показатели иммунологические – CD4+ повысились до 240 клеток/мл, CD8+ = 857 клеток/мл, ИРИ – 0,28. Но ухудшились показатели биохимического анализа крови: АЛТ – 199 МЕ/мл, АСТ – 201 МЕ/мл, общий билирубин – увеличился до 26 ммоль/л, прямой – до 5,8 ммоль/л. В общем анализе крови количество тромбоцитов снизилось до 110·109 г/л, гемоглобин – 115 г/л. По данным эластометрии печени отмечен прогресс фиброза – F3 = 11,8 кПа по шкале METAVIR. Применив формулу индекса высокого риска неблагоприятного течения фиброзного процесса у больных, коинфицированных ВИЧ и ВГС, для назначения или коррекции антиретровирусной терапии, мы получили значение менее 180, что послужило основанием для принадлежности пациента к группе высокого риска прогрессирования фиброза печени:
ИВР = 4,070 + 0,099·11,8 кПа + + 0,476·240 клеток/мл – 0,518·0,28 = 119,33.
В связи с чем решением врачебной комиссии была изменена схема АРВТ на препараты нуклеозидных ингибиторов обратной транскриптазы (зи-довудин+ламивудин) в комбинации с препаратами ингибиторов протеазы (калетра). Находясь на динамическом наблюдении, через 6 месяцев после изменения схемы антиретровирусной терапии на вышеуказанные препараты, отмечен регресс фиброза печени до F2 = 7,4 кПа, а еще через следующие 6 месяцев – регресс фиброза до первой стадии – F1 = 6,3 кПа. Показатели иммунологические улучшились до CD4+ 38 % – 240 клеток/мл. Концентрация РНК ВИЧ – неопределяемая нагрузка (менее 20 копий/мл), вирусная нагрузка по РНК ВГС – осталась прежней – 1,5·106 МЕ/мл. Назначение противовирусной терапии гепатита С в данном случае невозможно, так как низкие иммунологические показатели крови – CD4+ менее 500 клеток/мл. Подобрав с помощью формулы ИВР оптимальную схему препаратов антиретровирусной терапии, можно в дальнейшем добиться достижения критериев, при которых возможно назначение противовирусной терапии ХГС, а следовательно, и регресса фиброза печени.
Клинический случай 2. Выписка из амбулаторной карты пациента, с инфекцией ВИЧ / ВГС, получавшего антиретровирусную терапию, иллюстрирующая регресс фиброза печени на фоне комбинации препаратов нуклеозидных ингибиторов обратной транскриптазы и ингибиторов протеазы. Больной Т., 45 лет, находится на диспансерном учете в ГУЗ «Центр СПИД» с диагнозом: ВИЧ-инфекция, стадия 4А. Хронический вирусный гепатит С, стадия репродукции вируса. Инфицирование произошло при внутривенном использовании ПАВ (психоактивных веществ). К моменту включения больного в исследование была установлена давность выявления гепатита С – в 2001 г., а ВИЧ-инфекция ранее – в 2000 г. В настоящее время отрицает прием ПАВ, алкоголя последние пять лет. Ранее, в 2006 г., назначалась антиретровирусная терапия, с которой пациент был снят из-за самовольного прекращения приема через месяц. При включении в исследование 17.12.2014 г.: рост – 178 см, вес – 67 кг. Состояние удовлетворительное, жалобы на слабость, чувство тяжести в правом подреберье, возникающее периодически при физической нагрузке и / или нарушении диеты. Объективно: кожа и видимые слизистые обычной окраски, чистые. Периферические лимфоузлы не увеличены. В легких выслушивается везикулярное дыхание, хрипов нет. Тоны сердца приглушены, ритм правильный, шумов нет, ЧСС = PS = 78 уд. в мин, АД - 120/85 мм рт. ст., температура тела - 36,7 °С. Живот мягкий, безболезненный во всех отделах при пальпации, печень выступает из-под края реберной дуги на 2 см, край ровный, гладкий, поверхность эластическая. Селезенка увеличена. Симптом поколачивания отрицательный с обеих сторон. Физиоло- гические отправления в норме. Сознание ясное. Очаговой и менингеальной симптоматики нет. В общем анализе крови: гемоглобин – 137 г/л, тромбоциты – 109,0·109 /л, лейкоциты – 6,3·109 /л. В общем анализе мочи – патологии не выявлено. В биохимическом анализе крови: АЛТ – 186 МЕ/л, АСТ – 98 МЕ/л, общий билирубин – 15,2 ммоль/л, ЛДГ – 211 МЕ/л. Показатели иммунитета: CD4+ лимфоциты – 555 клеток/мл, CD8+ – 1664 клеток/мл, ИРИ – 0,33. Методом ПЦР выявлена РНК ВГС 8,8·105 МЕ/мл, генотип 3а, РНК ВИЧ – 108231 копий /мл. УЗИ органов брюшной полости: гепатомегалия, диффузные изменения паренхимы печени, спленомегалия. При выполнении эластометрии печени установлен фиброз третьей степени (F3) = 9,6 кПа по шкале METAVIR.
Учитывая иммунологические показатели, а также показатели вирусной нагрузки, данные эла-стометрии печени, пациенту решением врачебной комиссии назначена антиретровирусная терапия (АРВТ) в комбинации препаратов: нуклеозидных ингибиторов обратной транскриптазы (абакавир+ ламивудин = кивекса) и ингибитора протеазы (пре-зиста). На фоне АРВТ в течение 6 месяцев уменьшилась вирусная нагрузка по РНК ВИЧ до неопределяемого уровня (менее 20 копий/мл), улучшились показатели иммунологические – CD4+ повысились до 680 клеток/мл, CD8+ – 1458 клеток/мл, ИРИ – 0,46, показатели биохимического анализа крови: АЛТ – 68 МЕ/мл, АСТ – 52 МЕ/мл, общий билирубин – до 10,3 ммоль/л, прямой – до 2,1 ммоль/л. В общем анализе крови количество тромбоцитов повысилось до 137·109 г/л, гемоглобин – 135 г/л. Через 6 месяцев по данным эластометрии печени отмечен регресс фиброза – с F3 = 9,6 кПа по шкале METAVIR до F1 = 7,2 кПа. Применив формулу индекса высокого риска неблагоприятного течения фиброзного процесса у больных, коинфицированных ВИЧ и ВГС, для коррекции антиретровирусной терапии, мы получили значение 323,24 (более 180), что послужило основанием для принадлежности пациента к группе низкого риска прогресса фиброза печени:
ИВР = 4,070+0,099·7,2 кПа +
+ 0,476·680 клеток/мл – 0,518·0,46 = 323,24.
Пациент не нуждается в коррекции схемы АРВТ, продолжает прием препаратов нуклеозидных ингибиторов обратной транскриптазы (абакавир + ламивудин) в комбинации с препаратом из группы ингибиторов протеазы (презиста). Находясь на динамическом наблюдении, еще через 6 месяцев отмечен регресс фиброза печени до F0 = 5,3 кПа. Показатели иммунологические улучшились до CD4+ 48 % – 720 клеток/мл. Концентрация РНК ВИЧ – неопределяемая нагрузка (менее 20 копий/мл), вирусная нагрузка по РНК ВГС – 8,5·105 МЕ/мл. В декабре 2015 г. назначена и проведена противовирусная терапия гепатита С пегилированным интерфероном и рибавирином в течение 48 недель, в результате чего достигнут устойчивый вирусологический ответ. Через 24 недели по окончании противовирусной терапии ХГС РНК HCV отрицательный, показатели эла-стометрии печени на уровне F0 = 5,1 кПа, биохимические показатели крови – АЛТ – 40 Ме/мл, АСТ – 38 Ме/мл, билирубин общий – 8,9 ммоль/л, прямой – 1,5 ммоль/л, но фоне интерферонотерапии несколько снизились иммунологические показатели крови – CD4+ – 514 клеток/мл.
Таким образом, на фоне приема АРВТ препаратами нуклеозидных ингибиторов обратной транскриптазы (абакавир + ламивудин) в комбинации с препаратом ингибитора протеазы (презиста), в дальнейшем присоединении противовирусной двойной терапии гепатита С (интерферонами+рибавирином) был достигнут полный регресс фиброза печени.
Клинический пример 3. Выписка из амбулаторной карты пациента с инфекцией ВИЧ / ВГС при отсутствии антиретровирусной терапии, иллюстрирующая прогресс фиброза печени на фоне отсутствия какой-либо терапии. Больной А., 34 г., находится на диспансерном учете в ГУЗ «Центр СПИД» с диагнозом: ВИЧ-инфекция, 3-я субклиническая стадия. Хронический вирусный гепатит С, минимальной степени активности. Инфицирование произошло при внутривенном использовании ПАВ (психоактивных веществ). К моменту включения больного в исследование была установлена давность выявления гепатита С – в 2002 г., а ВИЧ-инфекция позже – в 2015 г. В настоящее время вредные привычки: прием ПАВ, алкоголя отрицает. Ранее пациент не принимал противовирусной терапии ХГС и ВИЧ-инфекции. При первичной постановке на учет 02.04.2015 г.: рост – 171 см, вес – 59 кг. Состояние удовлетворительное, жалобы на слабость, чувство тяжести в правом подреберье, возникающее периодически при физической нагрузке и / или нарушении диеты. Объективно: кожа и видимые слизистые обычной окраски, чистые. Периферические лимфоузлы не увеличены. В легких выслушивается везикулярное дыхание, хрипов нет. Тоны сердца приглушены, ритм правильный, шумов нет, ЧСС = PS = 78 уд. в мин, АД – 120/85 мм рт. ст., температура тела - 36,7 ° С. Живот мягкий, безболезненный во всех отделах при пальпации, печень выступает из-под края реберной дуги на 2 см, край ровный, гладкий, поверхность эластическая. Селезенка не пальпируется. Симптом поколачивания отрицательный с обеих сторон. Физиологические отправления в норме. Сознание ясное. Очаговой и менингеальной симптоматики нет. В общем анализе крови: гемоглобин – 131 г/л, тромбоциты – 208,0·109 /л, лейкоциты – 6,8·109 /л. В общем анализе мочи – патологии не выявлено. В биохимическом анализе крови: АЛТ – 87 МЕ/л, АСТ – 78 МЕ/л, общий билирубин – 5,8 ммоль/л, ЛДГ – 242 МЕ/л. Показатели иммунитета: CD4+ лимфоциты – 635 клеток/мл, CD8+ – 1432 клеток/мл, ИРИ – 0,44. Методом ПЦР выявлена РНК ВГС – 8,7·103 МЕ/мл, генотип 3а,
РНК ВИЧ – 9007 копий /мл. УЗИ органов брюшной полости: гепатомегалия, диффузные изменения паренхимы печени, спленомегалия. При выполнении эластометрии печени установлен фиброз первой степени (F1) = 6,3 кПа по шкале METAVIR.
Учитывая иммунологические показатели, а также показатели вирусной нагрузки, данные эластомет-рии печени, пациент не нуждается в назначении антиретровирусной терапии (АРВТ). В соответствии со стандартами оказания медицинской помощи пациент подлежит динамическому наблюдению в ГУЗ «Центр СПИД». Через год наблюдения выросла вирусная нагрузка по РНК ВИЧ до 15 167 копий/мл, ухудшились показатели иммунологические – CD4+ снизились до 355 клеток/мл, CD8+ – 806 клеток/мл, ИРИ – 0,44, показатели биохимического анализа крови: АЛТ – 137 МЕ/мл, АСТ – 80 МЕ/мл, общий билирубин – до 20,3 ммоль/л, прямой – до 6,23 ммоль/л. В общем анализе крови количество тромбоцитов снизилось до 194·109 г/л, гемоглобин – 125 г/л, а по данным эластометрии печени отмечен прогресс фиброза – с F1 = 6,3 кПа по шкале METAVIR до F3 = 9,4 кПа. Применив формулу индекса высокого риска неблагоприятного течения фиброзного процесса у больных, коинфицированных ВИЧ и ВГС, для назначения антиретровирусной терапии, мы получили значение 173,75 (менее 180), что послужило основанием принадлежности пациента к группе высокого риска прогрессирования фиброза печени:
ИВР = 4,070 + 0,099·9,4 кПа +
+ 0,476·355 клеток/мл – 0,518·0,44 = 173,75.
Сразу же больному была предложена антиретровирусная терапия, от чего пациент отказался. В 2017 г. при плановом обследовании отмечается прогресс фиброза печени с 9,4 кПа до 10,3 кПа (F3). Пациент не дает информированного согласия для лечения ВИЧ / ВГС, низко привержен к терапии.
Таким образом, проведение АРВТ при коинфекции ВИЧ / ВГС целесообразно не только с целью лечения ВИЧ-инфекции, но и с целью влияния на фиброзный процесс при ХГС для снижения возможности активного прогрессирования фиброза печени.
Выводы:
-
1. Количественными критериями риска прогрессирующего течения фиброза печени, установленными на основе рабочих моделей высокого и низкого риска, служат: показатели исходной эла-стометрии выше 7 кПа, число CD3+CD4+ Т-лимфоцитов в крови ниже 400 клеток/мл, иммунорегуля-торный индекс ниже 0,45 при умеренной и высокой прогностической значимости этих показателей (AUROC от 0,79 до 0,83).
-
2. Наибольшей прогностической значимостью при определении неблагоприятного течения фиброза печени (AUROC = 0,846) обладал индекс высокого риска (ИВР), определяемый по формуле уравнения линейной регрессии.
-
3. Величина ИВР ≤ 180 с высокой прогностической значимостью свидетельствует о принадлежности больного, коинфицированного ВИЧ и ВГС, к группе риска неблагоприятного течения фиброза печени, а ее определение является ключевым компонентом алгоритма диагностики и лечения пациента с коинфекцией ВИЧ / ВГС.
-
4. Величина ИВР ≤ 180 у больных, коинфици-рованных ВИЧ и ВГС, служит показанием для проведения антиретровирусной терапии с назначением комбинации ингибиторов обратной транскриптазы ВИЧ и ингибиторов протеазы или интегразы ВИЧ.
Финансирование. Исследование не имело спонсорской поддержки.
Список литературы Методика прогнозирования прогрессирующего фиброза печени у больных коинфекцией вируса иммунодефицита человека и вирусного гепатита С
- Scott J.A., Chew K.W. Treatment optimization for HIV/HCV co-infected patients // Ther. Adv. Infect. Dis. - 2017. - Vol. 4, № 1. - P. 18-36. DOI: 10.1177/2049936116681279
- Nunez M., Soriano V. Hepatotoxicity of antiretrovirals: incidence, mechanisms and management // Drug. Safety. - 2005. - Vol. 28, № 1. - P. 53-66. DOI: 10.2165/00002018-200528010-00004
- Мониторинг терапии у пациентов с коинфекцией ВИЧ / ВГС, получающих противовирусную терапию гепатита С и антиретровирусную терапию / Л.Р. Шостакович-Корецька, О.П. Шевченко-Макаренко, И.В. Чухалова, О.В. Носенко // Актуальная инфектология. - 2017. - Т. 5, № 7. - С. 290-292.
- Soriano V., Labarga P., Fernandez-Montero J.V. Drug interactions in HIV-infected patients treated for hepatitis C // Expert. Opin. Drug. Metab. Toxicol. - 2017. - Vol. 13, № 8. - P. 807-816. DOI: 10.1080/17425255.2017.1351942
- Rockstroh J.K. Management of hepatitis C/HIV coinfection // Curr. Opin. Infect. Dis. - 2006. - Vol. 19, № 1. - P. 8-13. DOI: 10.1097/01.qco.0000200294.22661.e0
- Оптимизация прогнозирования темпа прогрессирования фиброза печени у ВИЧ-инфицированных пациентов с хроническим гепатитом С / Г.М. Аубинская, Т.И. Коваль, Л.М. Сизова, С.С. Руденко, Н.П. Лимаренко // Актуальная инфектология. - 2018. - Т. 6, № 5. - С. 258-259.
- Собянина С.Н., Юрганова Г.А. Обоснование и апробация применения пегилированных интерферонов в сочетании с даруновиром у больных с ХГС и ВИЧ-инфекцией // ВИЧ-инфекция и иммуносупрессии. - 2010. - Т. 2, № 3. - С. 118-122.
- Meta-analysis: increased mortality associated with hepatitis C in HIV-infected persons is unrelated to HIV disease progression / T.Y. Chen, E.L. Ding, G.R. Seage Iii, A.Y. Kim // Clin. Infect. Dis. - 2009. - Vol. 49, № 10. - P. 1605-1615.
- DOI: 10.1086/644771
- Знойко О.О. Трудный вариант с гепатитом С: что изменится с приходом безинтерфероновой терапии? // Инфекционные болезни: новости, мнения, обучение. - 2014. - № 2. - С. 60-67.
- Del Bello D., Ita Nagy F., Hand J. Direct-acting antiviral-based therapy for chronic hepatitis C virus in HIV-infected patients // J. Curr. Opin. HIV AIDS. - 2015. - Vol. 10, № 5. - P. 337-347.
- DOI: 10.1097/COH.0000000000000182
- Особенности коинфицирования ВИЧ-позитивных пациентов вирусом гепатита С / Д.В. Павлов, Д.Х. Шатрова, Н.И. Галиуллин, Ф.И. Нагимова // Казанский медицинский журнал. - 2014. - Т. 95, № 6. - С. 905-908.
- Кравченко А.В., Канестри В.Г., Куимова У.А. Современные рекомендации по применению ингибиторов протеазы вируса гепатита С у пациентов с сочетанной инфекцией (ВИЧ-инфекция/хронический гепатит С) // Инфекционные болезни. - 2012. - № 3. - С. 90-95.
- Mena A., Meijide H., Rodríguez-Osorio I. Liver-related mortality and hospitalizations attributable to chronic hepatitis C virus coinfection in persons living with HIV // HIV Med. - 2017. - Vol. 18, № 9. - P. 685-689.
- DOI: 10.1111/hiv.12502
- Кравченко А.В., Аксенова В.А., Гуркина Л.А. Ингибитор интегразы ВИЧ ралтегравир в составе схем антиретровирусной терапии у больных ВИЧ-инфекцией и гепатитом С // Инфекционные болезни. - 2015. - № 3. - С. 5-11.
- Kaur K., Gandhi M.A., Slish J. Drug-Drug Interactions Among Hepatitis C Virus (HCV) and Human Immunodeficiency Virus (HIV) Medications // Infect. Dis. Ther. - 2015. - Vol. 4, № 2. - P. 159-172.
- DOI: 10.1007/s40121-015-0061-2
- Манапова Э.Р., Фазылов В.Х., Бешимов А.Т. Эффективность противовирусной терапии хронического гепатита С у пациентов с сочетанной ВГС/ВИЧ-инфекцией в сравнительном аспекте // Инфекционные болезни: новости, мнения, обучение. - 2017. - Т. 21, № 4. - С. 51-56.
- Комбинированная терапия хронического гепатита C пегилированным интерфероном альфа-2а и рибавирином у больных с ВИЧ-инфекцией и больных с моноинфекцией HCV / Н.Д. Ющук, С.Л. Максимов, Л.М. Иванова, Е.А. Климова, О.О. Знойко, А.В. Кравченко // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. - 2009. - Т. 19, № 1. - С. 35-42.
- Протокол диагностики и лечения больных вирусными гепатитами В и С / Н.Д. Ющук, Е.А. Климова, О.О. Знойко, Г.Н. Кареткина, С.Л. Максимов, Ю.В. Мартынов, В.С. Шухов, К.Р. Дудина [и др.] // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. - 2010. - Т. 20, № 6. - С. 4-60.
- Канестри В.Г., Кравченко А.В., Ганкина Н.Ю. Гепатотоксичность антиретровирусной терапии у больных ВИЧ-инфекцией // Эпидемиология и инфекционные болезни. Актуальные вопросы. - 2015. - № 1. - С. 31-36.
- Азовцева О.В., Архипова Е.И., Архипов Г.С. Клинико-генотипическая характеристика коинфекции вирусного гепатита С и ВИЧ // ВИЧ-инфекция и иммуносупрессии. - 2010. - Т. 2, № 2. - С. 42-47.


