Мезотелиома брюшины. Циторедуктивная операция и HIPEC
Автор: Копейка С.М., Аксарин А.А., Бабенко М.Ю.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 3 т.24, 2025 года.
Бесплатный доступ
Мезотелиома брюшины представляет собой редкое и агрессивное злокачественное новообразование, которое возникает из мезотелиальных клеток, выстилающих брюшную полость. Эта опухоль отличается высокой степенью инвазивности и, как правило, имеет неблагоприятный прогноз. Хирургическое вмешательство продолжает оставаться важным методом лечения мезотелиомы. Оно позволяет удалить макроскопически видимые опухолевые массы, которые часто оказываются устойчивыми к традиционной лекарственной терапии. Тем не менее необходимость и целесообразность хирургического подхода должны оцениваться индивидуально, принимая во внимание гистологический подтип опухоли, степень ее распространения и наличие сопутствующих факторов риска. Современные исследования показывают, что наилучшие долгосрочные результаты достигаются при использовании мультимодального подхода к лечению, который может включать комбинацию хирургии, химиотерапии и радиотерапии. Такой комплексный подход позволяет более эффективно справляться с заболеванием и улучшать качество жизни пациентов. Описание клинического случая. Представляем случай успешного хирургического лечения 59-летней пациентки с мезотелиомой брюшины, дополненного интраоперационной гипертермической химиотерапией (HIPEC) с использованием цисплатина и доксорубицина. При последующем наблюдения в течение 12 мес не зафиксировано признаков прогрессирования заболевания, что свидетельствует о высокой эффективности этого подхода. Заключение. Применение циторедуктивной хирургии и HIPEC позволяет получить хорошие результаты при лечении мезотелиомы брюшины.
Мезотелиома брюшины, циторедуктивная хирургия, интраоперационная гипертермическая химиотерапия, полная циторедукция
Короткий адрес: https://sciup.org/140310587
IDR: 140310587 | УДК: 616.381-006.32-089:615.28 | DOI: 10.21294/1814-4861-2025-24-3-198-204
Peritoneal mesotheioma. Cytoreductive surgery and HIPEC
Background. Peritoneal mesothelioma is a rare, high invasive and aggressive malignant tumor that arises from the mesothelial cells lining the abdominal cavity. Surgery is a primary treatment method for mesothelioma. It allows the removal of macroscopically visible tumor masses, which are often resistant to conventional drug therapy. However, the necessity and appropriateness of a surgical approach should be assessed individually, taking into account the histological subtype of the tumor, the extent of its spread and the presence of associated risk factors. Current research shows that the best long-term results are achieved with a multimodal treatment approach, which may include a combination of surgery, chemotherapy, and radiotherapy. This comprehensive approach allows for more effective management of the disease and improved quality of life of patients. Case report. We present a clinical case of a 59year-old female patient with peritoneal mesothelioma. The patient underwent surgery with intraoperative hyperthermic intraperitoneal chemotherapy (HIPEC) using cisplatin and doxorubicin. During a 12-month follow-up, there were no signs of disease progression, which indicates the high effectiveness of the applied approach. Conclusion. The use of cytoreductive surgery and HIPEC demonstrated positive effects in the treatment of peritoneal mesothelioma.
Текст научной статьи Мезотелиома брюшины. Циторедуктивная операция и HIPEC
Мезотелиома брюшины (МБ) – редкая злокачественная опухоль, развивающаяся из мезотелиальных клеток плевры, брюшины, перикарда, оболочек яичка. Заболевание впервые было описано J. Miller и W.H. Wynn в 1908 г. В США ежегодно диагностируется от 500 до 700 новых случаев мезотелиомы [1]. Частота развития мезотелиомы в Европе составляет 18–20 случаев на миллион жителей в год. Статистические данные о заболеваемости мезотелиомой брюшины и иных локализаций в РФ отсутствуют. Мезотелиома брюшины встречается значительно реже мезотелиомы плевры и составляет 15–20 % всех новых случаев мезотелиомы [1]. Заболевание может поражать пациентов в широком возрастном диапазоне с некоторым преобладанием доли мужчин среди заболевших [2].
Этиологически возникновение мезотелиомы брюшины чаще связывают с воздействием асбестовых волокон, реже – с другими причинами: воздействием не асбестовых минеральных волокон, последствиями лучевой терапии при других злокачественных новообразованиях (с латентным периодом от нескольких лет до десятилетий) и рецидивирующим перитонитом, хроническим серозитом, связанным с болезнью Крона, эндометриозом или семейной средиземноморской лихорадкой [3–5].
Мезотелиома брюшины чаще диагностируется на поздней стадии, т. к. на ранней стадии симптомы заболевания, чаще всего, не специфичны: вздутие живота (30–80 % пациентов), боль в животе (27–58 %), редко – кишечная непроходимость и перфорация полых органов пищеварительной системы [6]. Распространение чаще диффузное, реже – локализованное.
Процесс диагностики МБ является комплексным и основан на сопоставлении анамнестических данных с результатами инструментальных (компьютерная томография, магнитно-резонансная томография, позитронно-эмиссионная томография) и лабораторных исследований, а также с результатами патологоанатомического исследования операционного или биопсийного материала с его иммуногистохимическим исследованием. Диагноз должен быть подтвержден обнаружением злокачественных клеток в асцитической жидкости и биоптате, полученном при выполнении диагностической лапароскопии либо открытой операции [6].
Мезотелиома брюшины включает три гистологических подтипа (эпителиоидный, саркоматоидный и смешанный/бифазный), определение которых имеет решающее значение для дальнейшего лечения и прогноза. Для эпителиоидного подтипа (75–90 % случаев) характерен лучший прогноз, чем для иных типов [1]. При эпителиоидном варианте клетки чаще напоминают нормальные мезотелиальные клетки с преимущественно тубу-лопапиллярным или трабекулярным рисунком [1]. Однако могут наблюдаться и микропапиллярные, светлоклеточные, децидуоподобные, перстневидные, мелкоклеточные и рабдоидные опухолевые комплексы. Митотическая активность, как правило, низкая, но в низкодифференцированных опухолях могут наблюдаться многочисленные фигуры митозов [7, 8]. Саркоматоидный подтип характеризуется плотно расположенными веретенообразными клетками. Могут наблюдаться саркомы с плеоморфными изменениями, заключающимися в наличии гигантских многоядерных атипичных клеток и многочисленных митозов. Иногда в структуре саркоматоидной мезотелиомы присутствуют гетерологичные элементы, такие как рабдомиосаркома, остеосаркома или хондросаркома. В таком случае следует использовать термин «с гетерологичными элементами». Смешанный подтип содержит как эпителиоидные, так и саркоматоидные элементы, при этом присутствует не менее 10 % гистологических признаков каждого подтипа [1]. Однако в случае небольших биоптатов, при наличии эпителиоидного и саркоматоидного компонентов, любая опухоль может быть расценена как двухфазная, вне зависимости от процентного соотношения.
Иммуногистохимическое исследование (ИГХ) при дифференциальной диагностике МБ и вторичном поражении брюшины при других злокачественных новообразованиях затруднено тем, что ни один иммуногистохимический маркер не является в полной мере чувствительным и специфичным. В связи с этим рекомендуется использовать ИГХ-панель, состоящую, как минимум, из двух маркеров, положительно реагирующих с мезотелиомой, и двух маркеров, реагирующих с мезотелиомой отрицательно. Исходя из специфич- ности и чувствительности, рекомендуемыми мезотелиальными (положительно реагирующими) маркерами являются calretinin, WT1, D2-40 (podoplanin), HBME-1 и CK5/6, тогда как в качестве отрицательно реагирующих обычно используются claudin-4, BerEP4 или MOC31, B72.3, CEA, CD15 (LeuM1) и BG8 [9].
При локализованном процессе основным методом лечения МБ является радикальное удаление опухоли. При диссеминированной МБ применяют комбинацию хирургического лечения, лучевой терапии и химиотерапии. При лечении применяют циторедуктивную хирургию в сочетании с интраоперационной фотодинамической терапией или химиотерапией. Однако прогноз при МБ остается неутешительным ввиду ранней диссеминации процесса. Медиана выживаемости составляет от одного до двух лет. Наилучший прогноз получен при эпителиоидном типе мезотелиомы, при саркоматозном и смешанном типе – наихудший. Согласно ряду исследований, использование циторедуктивной хирургии в комбинации с вну-трибрюшной гипертермической химиотерапией при эпителиоидной форме МБ с низким риском прогрессирования может привести к значительным долгосрочным результатам. Этот подход демонстрирует обнадеживающие перспективы для пациентов, обеспечивая улучшение выживаемости и качество жизни [1, 4, 5, 10].
Клинический случай
Пациентка 59 лет. Диагноз основной: Злокачественная мезотелиома брюшины с распространением на тело матки, широкую связку матки, яичник. Сопутствующий: Нефропатия смешанного генеза (гипертонческая + подагрическая + токсическая); ХБП С3а; расчетная СКФ СКD-EPI: 56 мл/мин/1,73м2; проба Реберга (9.08.23): СКФ 64,1 мл/мин А1. Кисты почек (Bosniak I). Нетоксический многоузловой зоб, клинический эутиреоз. Анемия легкой степени
Из анамнеза: в 2014 г. при плановом УЗИ органов брюшной полости и малого таза выявлено увеличение правого яичника. После дообследования, 14.05.14 выполнена плановая операция: экстирпация матки с придатками, резекция большого сальника. При срочном исследовании – подозрение на рак яичника. При плановом патогистологиче-ском исследовании верифицирована мезотелиома брюшины. В послеоперационном периоде проведено 6 курсов полихимиотерапии (ПХТ) по схеме пеметрексед + цисплатин.
Прогрессирование в апреле 2016 г., при плановой МРТ выявлен рецидив опухоли в малом тазу. 23.05.16 выполнено удаление рецидивной опухоли малого таза. После операции проведено 6 курсов II линии ПХТ по схеме пеметрексед + карбоплатин, которая была завершена 14.11.16.
При контрольной МРТ в августе 2022 г., при отсутствии клинических проявлений, выявлено прогрессирование болезни: справа в подвздошной области на уровне края подвздошной кости, за петлей кишки определялось кистозно-солидное образование, размерами 40×30 мм, с признаками ограничения диффузии на DWI и выпадением сигнала на ADC. После контрастирования образование активно накапливало контрастное вещество по периферии. Заключение: МР-признаки внеорган-ного образования в правой подвздошной области (имплантационный метастаз?)
Во время операции (06.09.22) выявлено подвижное, бугристое, кистозно-солидное образование в забрюшинном пространстве, интимно спаянное с восходящей ободочной кишкой, на 10 см проксимальнее илеоцекального угла. Другие органы брюшной полости и брюшина без патологических изменений. Опухоль удалена с плоскостной резекцией восходящей ободочной кишки. После операции проведено 6 курсов ПХТ по схеме пеметрексед + карбоплатин, в период с 3.10.22 по 1.02.23.
По данным патогистологического исследования: опухоль солидного строения в стенке толстой кишки, формирующиеся ацинарные и микроже-лезистые структуры, выполненные атипичными мезотелиальными клетками, с крупными ядрами с выраженными ядрышками. Митотическая активность умеренно выражена. Яркая экспрессия WT-1 и HBME-1. Иммуноморфологическая картина соответствует вторичному поражению восходящей ободочной кишки злокачественной мезотелиомой эпителиоидного типа. R0
Прогрессирование диагностировано в сентябре 2023 г.: рецидив опухоли в проекции слепой кишки. По данным МРТ органов брюшной полости (11.09.23): гепатоспленомегалия; в эпигастральной, мезогастральной областях единичные узловые образования до 3–4 мм (рецидив мезотелиомы?). По данным МРТ (12.09.23): внеорганное образование в правой подвздошной области (имплантационный метастаз?); справа, в подвздошной области на уровне края подвздошной кости, за петлей кишки определяется кистозно-солидное образование, размерами 40×30 мм. После контрастирования накапливает контрастное вещество по периферии. Позитронно-эмиссионная томография/ компьютерная томография (21.09.23): картина наличия лимфоузлов и депозитов с повышением метаболизма радиофармпрепарата (РФП) на уровне купола слепой кишки и в восходящем отделе ободочной кишки (больше данных за специфическое поражение). В толще брюшной стенки, по ходу послеоперационного доступа, определяются уплотнения с повышением метаболизма РФП.
Пациентка оперирована в плановом порядке 5.10.23, выполнена субтотальная перитонэк-томия + внутрибрюшная гипертермическая химиотерапия (HIPEC). Использован внебрюшинный доступ. Окончательная ревизия брюшной полости произведена после мобилизации большей части
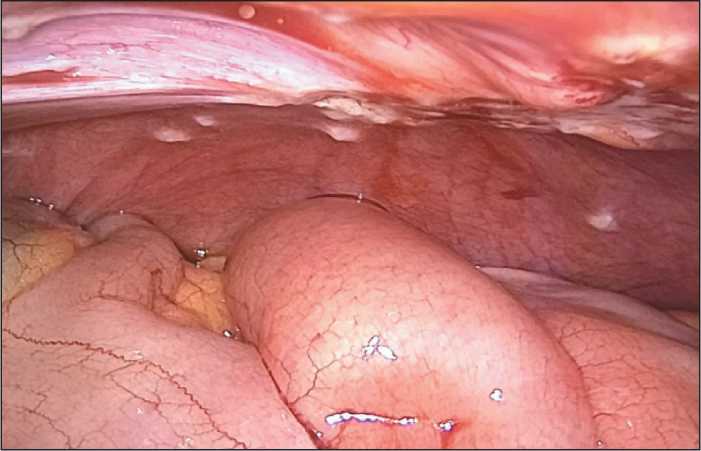
Рис. 1. Поддиафрагмальное пространство слева. Примечание: рисунок выполнен авторами Fig. 1. Subdiaphragmatic space on the left.
Note: created by the authors
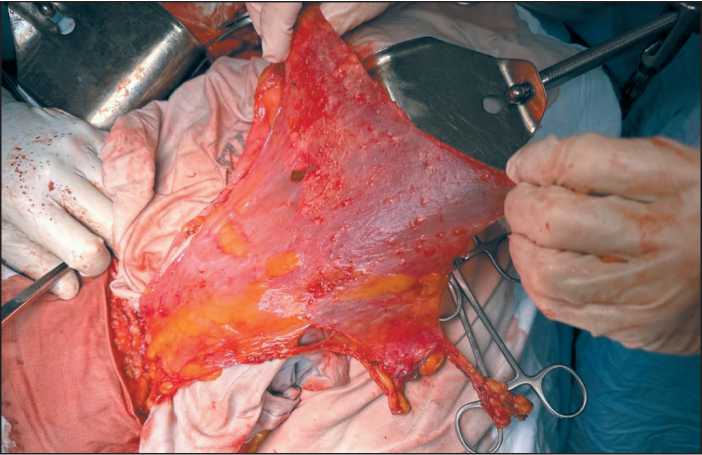
Рис. 2. Париетальная брюшина левого бокового канала с очагами мезотелиомы. Примечание: рисунок выполнен авторами Fig. 2. Parietal peritoneum of the left lateral canal with foci of mesothelioma. Note: created by the authors
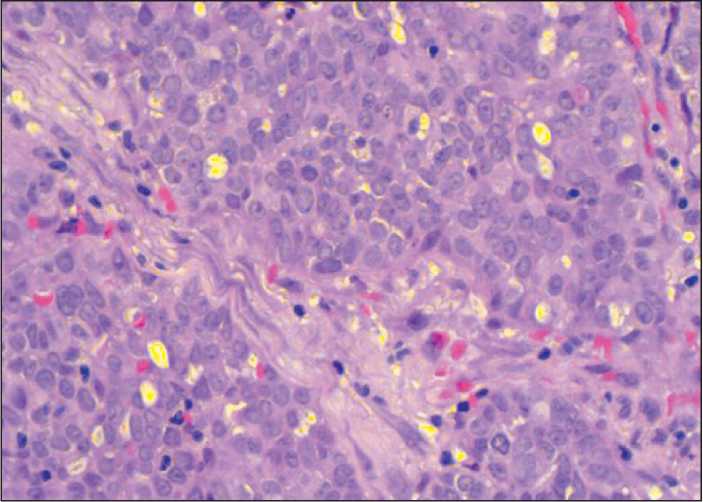
Рис. 3. Микрофото. Солидные скопления атипичных эпителиоидных клеток. Окраска гематоксилином и эозином, ×40. Примечание: рисунок выполнен авторами
Fig. 3. Microphoto. Solid clusters of atypical epithelioid cells. Hematoxylin and eosin stain, ×40. Note: created by the authors
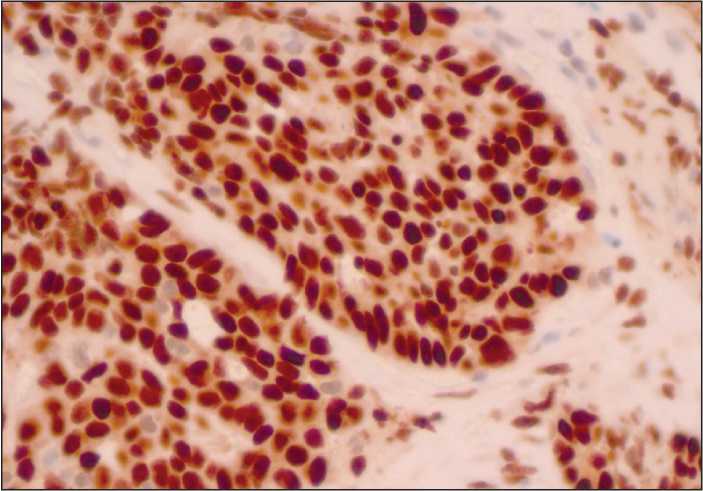
Рис. 4. Микрофото. Иммуногистохимическоре исследование. В большей части клеток опухоли отмечается яркая ядерная экспрессия антител к WT-1, ×40. Примечание: рисунок выполнен авторами
Fig. 4. Microphoto. Immunohistochemical study. Most tumor cells show strong nuclear expression of antibodies to WT-1, ×40. Note: created by the authors
париетальной брюшины, при этом выявлены единичные отсевы до 2 мм в верхнем этаже брюшной полости, поддиафрагмальном пространстве справа, подпеченочном пространстве, правом и левым боковых каналах, малом тазу, по висцеральной брюшине тонкой и толстой кишки, по брыжейке тонкой кишки (рис. 1), лимфоузлы не увеличены, в печени единичные метастазы по капсуле, до 2 мм; индекс перитонеального канцероматоза (PCI) по шкале P. Shugabacker – 13. Выделена и единым блоком удалена париетальная брюшина правой, левой половины брюшной полости, начиная от диафрагмы до малого таза (рис. 2); удалена брюшина малого таза; удалены все метастазы с серозной оболочки тонкой, толстой кишки и брыжейки. Индекс полноты циторедукции (СС) – 0.
После удаления брюшины брюшная полость дренирована через отдельные проколы трубчатыми дренажами, которые установлены в малый таз, боковые каналы и поддиафрагмальные пространства с обеих сторон. В эпигастральную область, мезогастрий и в малый таз установлены интраабдоминальные температурные датчики. Послеоперационная рана брюшной стенки ушита послойно. Подключен аппарат Performer HT. После заполнения брюшной полости 5 % раствором глюкозы, подогретым до 42,0 °С, начата циркуляция. Объем перфузата – 5 000 мл. В контур циркуляции введены циспластин в дозе 225 мг, доксорубицин в дозе 75 мг. Гипертермическая интраоперационная химиотерапия в течение 90 мин по закрытому типу. После HIPEC выполнено промывание брюшной полости. Экстубация – через 2 ч.
Послеоперационный период протекал благоприятно. Наблюдался подъем трансаминаз – АЛТ до 113 U/L, АСТ до 94 U/L – на 1-е сут после операции с нормализацией через 5 дней. Креатинин повышался в 1-е и 2-е сут до 106 мкмоль/л, мочевина – до 10,2 ммоль/л. Данные показатели нормализовались на 5-е сут после операции. На
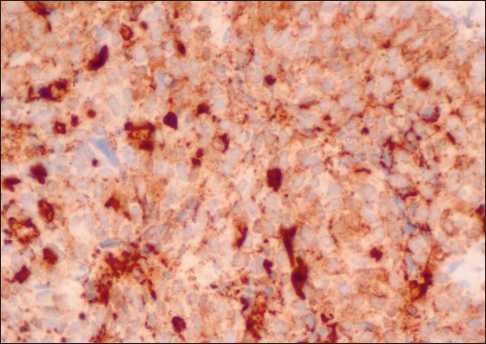
Рис. 5. Микрофото. Иммуногистохимическое исследование. Отчетливая диффузная цитоплазматическая экспрессия антител к HBME-1 в опухолевых клетках, ×40. Примечание: рисунок выполнен авторами
Fig. 5. Microphoto. Immunohistochemical study. Marked diffuse cytoplasmic expression of HBME-1 antibodies in tumor cells, ×40. Note: created by the authors
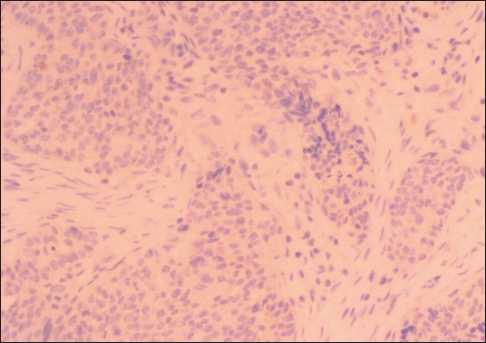
Рис. 6. Микрофото. Иммуногистохимическое исследование.
Отсутствует экспрессия опухолевыми клетками антител к
CD15, ×40. Примечание: рисунок выполнен авторами
Fig. 6. Microphoto. Immunohistochemical study. No expression of CD15 antibodies by tumor cells, ×40. Note: created by the authors
2-е сут после операции появилась перистальтика кишечника. Рана зажила первичным натяжением. Больная выписана из стационара на 10-е сут после операции.
При патоморфологическом исследовании операционного материала: опухоль представлена тубулярными, папиллярными и солидными скоплениями атипичных эпителиоидных клеток (рис. 3); в большей части опухолевых клеток отмечалась выраженная ядерная экспрессия антител к WT1 (рис. 4) и выраженная/умеренная цитоплазматическая экспрессия антител к HBME-1 (рис. 5). Кроме того, наблюдались выраженная диффузная цитоплазматическая экспрессия антител к CK-Pan, слабая/умеренная диффузная цитоплазматическая экспрессия антител к Vimentin и слабая фокальная цитоплазматическая экспрессия антител к BerEP4, наблюдалась негативная реакция с антителами к CEA и CD15 (рис. 6). Индекс пролиферативной активности (индекс мечения Ki67) – 45 %. Совокупность морфологической картины и характер экспрессии маркеров позволили сформулировать па-тогистологическое заключение – мезотелиома брюшины, эпителиоидный подтип (ICD-O code: 9052/3).
В связи с отказом пациентки от дальнейшего лечения адъювантная химиотерапия не проводилась. Наблюдается у онколога в поликлинике. При динамическом мониторинге в течение 12 мес после операции данных за прогрессирование заболевания нет. Пациентка ведет обычный образ жизни.
Заключение
Мезотелиома брюшины характеризуется диссеминированным поражением брюшной полости. Лечение мезотелиомы требует многостороннего подхода и представляет собой сложную задачу. Каждый клинический случай требует индивидуального подхода, основанного на комбинации различных методов лечения, что позволяет максимально эффективно справляться с заболеванием и улучшать качество жизни. При эпителиоидной форме мезотелиомы с местнораспространенным, но резектабельным процессом и низким риском прогрессирования оптимальным вариантом начала лечения является циторедуктивная операция с интраоперационной гипертермической химиотерапией, что может способствовать длительной ремиссии.


