Микобактериальные осложнения иммунотерапии вакциной БЦЖ рака мочевого пузыря
Автор: Зубань О.Н., Сикаев Ю.Р., Чотчаев Р.М., Авдентова В.Б.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Онкоурология
Статья в выпуске: 4 т.18, 2025 года.
Бесплатный доступ
Введение. Для лечения поверхностного рака мочевого пузыря применяется внутрипузырная иммунотерапия бациллой Кальметта-Герена (БЦЖ), частота микобактериальных осложнений при этом не превышает 1%, но они могут протекать с вовлечением мочеполовых и других органов. Цель. Изучить клинико-рентгенологические особенности туберкулеза, развившегося после внутрипузырной БЦЖ-терапии рака мочевого пузыря. Материалы и методы. Проанализировано 19 случаев туберкулеза, ассоциированного с БЦЖ-терапией рака мочевого пузыря, в период с января 2015 по август 2025 годы. Все пациенты были мужского пола, средний возраст 63 года. Результаты. Туберкулез мочеполовой системы выявлен у 15 (78,9%) пациентов, органов дыхания – у 3 (15,8%), генерализованный с поражением ЦНС, легких, почек, мочеточников и мочевого пузыря – у 1 (5,3%). У 11 (57,9%) больных выявлен туберкулез предстательной железы, с вовлечением придатков яичек – у 1 (5,3%), семенных пузырьков – также у 1 (5,3%), изолированный туберкулезный эпидидимит – у 1 (5,3%). У 3 (15,8%) пациентов развился туберкулез мочевой системы: у 2 (10,5%) – туберкулез почек, у 1 (5,3%) – мочевого пузыря и правого мочеточника. Оперировано 12 (63,2%) пациентов: выполнено 10 трансуретральных резекций предстательной железы или мочевого пузыря, 6 эпидидимэктомий и 1 илеоцистопластика. Заключение. В настоящее время при всех низкодифференцированных и некоторых высокодифференцированных не мышечно-инвазивного рака мочевого пузыря (НМИРМП) для профилактики рецидивов применяется внутрипузырная БЦЖ иммунотерапия, которая доказала свою эффективность. Однако одним из серьезных осложнений БЦЖ-терапии являются различные микобактериальные осложнения. Необходимо отметить трудности диагностики различных форм туберкулеза после БЦЖ-терапии, для подтверждения диагноза следует проводить биопсию тканей для гистопатологического исследования и обнаружения M. bovis. Больным с микобактериальными осложнениями может потребоваться комбинированная противотуберкулезная терапия в течение 3–12 месяцев, а также применение хирургического вмешательства.
Рак мочевого пузыря, иммунотерапия рака мочевого пузыря, БЦЖ, микобактериальные осложнения, туберкулез
Короткий адрес: https://sciup.org/142246976
IDR: 142246976 | DOI: 10.29188/2222-8543-2025-18-4-48-55
Mycobacterial complications of BCG immunotherapy for bladder cancer
Introduction. Intravesical immunotherapy with bacillus Calmette-Guérin (BCG) is used to treat superficial bladder cancer. The incidence of mycobacterial complications does not exceed 1%, but they can occur with the involvement of the genitourinary and other organs. Aim: to study the clinical and radiological features of tuberculosis associated with intravesical BCG therapy for bladder cancer. Materials and methods. A total of 19 cases of tuberculosis associated with BCG therapy for bladder cancer were analyzed between January 2015 and August 2025. All patients were male, the average age was 63 years. Results. Urogenital tuberculosis was detected in 15 patients (78.9%), respiratory system tuberculosis – in 3 (15.8%), miliary tuberculosis with the central nervous system, lungs, kidneys, ureters and bladder involvement – in 1 (5.3%). Tuberculosis of the prostate gland was detected in 11 patients (57.9%), with the epididymis involvement – in 1 (5.3%), seminal vesicles – also in 1 (5.3%), isolated tuberculous epididymitis – in 1 (5.3%). Tuberculosis of the urinary system developed in 3 patients (15.8%): the kidney tuberculosis in 2 (10.5%), tuberculosis of the bladder and right ureter in 1 (5.3%). A total of 12 patients (63.2%) were underwent surgery: 10 transurethral resections of the prostate gland or bladder, 6 epididymectomies and 1 ileocystoplasty were performed. Conclusion. Currently, intravesical BCG immunotherapy, which has proven effective, is used to prevent relapses in all low-grade and some high-grade NMIBC. However, various mycobacterial complications are a serious complication of BCG therapy. Difficulties in diagnosing various forms of tuberculosis after BCG therapy should be noted; to confirm the diagnosis, a tissue biopsy should be performed for histopathological examination and detection of M. bovis. Patients with mycobacterial complications may require combination antituberculosis therapy for 3–12 months, as well as surgical intervention.
Текст научной статьи Микобактериальные осложнения иммунотерапии вакциной БЦЖ рака мочевого пузыря
экспериментальная и клиническая урология № 4 2025
По данным Global cancer statistics рак мочевого пузыря занимает девятое место среди наиболее часто диагностируемых онкологических заболеваний и три надцатое место – в структуре смертности от рака. В 2022 году во всем мире было зарегистрировано 613 791 новых случаев рака мочевого пузыря (3,1% от общего числа онкологических заболеваний) и 220349 (2,3%) смертей [1]. В большинстве случаев диагностируют не мышечно-инвазивный рак мочевого пузыря рак (НМИРМП), включая карциному in situ (CIS) и стадии Ta и T1. Хотя золотым стандартом лечения НМИРМП является полное удаление всех папиллярных пораже ний посредством трансуретральной резекции (ТУР), частота рецидивов после этой операции остается вы сокой. При всех низкодифференцированных и некото рых высокодифференцированных НМИРМП применяется внутрипузырная иммунотерапия бациллой Кальметта-Герена (БЦЖ) [2]. Действующий компонент – ослабленный штамм бактерии Mycobacterium bovis в дозе 2х108 КОЕ. В ответ на введение вакцины уротелий выделяет цитокины и фактор некроза опухоли-α, ин терферон-γ. Метаанализы рандомизированных иссле дований показали, что внутрипузырная поддерживающая БЦЖ-терапия после ТУР снижает частоту реци дивов НМИРМП, а также значительно снижает риск прогрессирования мышечно-инвазивной формы забо левания [3, 4].
Известно, что иммунотерапия рака мочевого пу зыря вакциной БЦЖ противопоказана при перенесен ном ранее туберкулезе,размере местной реакции на внутрикожное введение туберкулина в дозе 2 ТЕ (проба Манту) 17 мм и более, повышенной чувствительности к компонентам препарата, тотальном недер жании мочи (невозможности удерживать препарат в мочевом пузыре). Ограничивают применение мето дики врожденный или приобретенный иммунодефи цит (СПИД, лейкемия, лимфома), лечение злокачественных новообразований (цитостатики, облучение)
или проведение иммуносупрессивной терапии, тяже лые сопутствующие заболевания в стадии декомпенса ции, беременность и период грудного вскармливания [5-7].
В клинических рекомендациях «Туберкулез у взрослых», утвержденных в 2024 году, выделяют ятрогенную форму туберкулеза мочеполовых органов вследствие инстилляции вакцины БЦЖ в мочевой пузырь [8]. Хотя частота микобактериальных осложнений не превышает 1%, они могут протекать с вовлечением не только мочевого пузыря, но и почек, половых органов, легких, центральной нервной системы (ЦНС), костей и суставов, развитием БЦЖ-сепсиса [9].
Цель исследования : изучить клинико-рентгенологические особенности туберкулеза, развившегося после внутрипузырной БЦЖ-терапии рака мочевого пузыря.
МАТЕРИАЛ И МЕТОДЫ
Проанализировано 19 случаев ятрогенного тубер кулеза, ассоциированных с БЦЖ-терапией рака моче вого пузыря, в период с 2015 по 2 024 годы. Возраст заболевших колебался от 41 до 76 лет и в среднем со ставил 63 года. Все пациенты были мужского пола. У 15 (78,9%) больных обнаружено 22 других урологиче ских заболевания:у 7 – доброкачественная гиперпла зия предстательной железы, у 6 – кисты почек, у 5 – хронический простатит, у 2 – кисты органов мошонки, у 2 – хронический пиелонефрит, у 1 – рак предстатель ной железы, у 1 – мочекаменная болезнь. Таким обра зом, в среднем на 1 больного пришлось 1,6 сопутствующих заболеваний мочеполовой системы.
РЕЗУЛЬТАТЫ
Сроки начала иммунотерапии после ТУР варьировали от 10 до 110 дней (в среднем – 26 дней), количество инстилляций вакцины БЦЖ колебалось 1 до 29 (в среднем – 9,5). На фоне внутрипузырного введения вакцины БЦЖ появилась ирритативная симптоматика в виде учащенного и болезненного мочеиспускания у 12 (63,2%) пациентов, боль различной локализации – у 3 (15,8%), из них в паховой области – у 1 (5,3%), в подреберье – у 1 (5,3%), почечная колика – у 1 (5,3%), лихорадка с ознобом – у 3 (15,8%). У 12 больных (63,2%) больных отмечена стертая клиническая картина поражения мочеполовых органов, а у 7 (36,8%) – острое начало. У всех в последствии диагностирован туберкулез различной локализации. Данные о локализации, клинической форме и распространенности туберкулеза представлены в таблице 1. Туберкулез мочеполовой системы выявлен у 15 (78,9 %) пациентов, органов дыхания – у 3 (15,8%), генерализованный туберкулез с поражением ЦНС, легких, почек, мочеточников и мочевого пузыря – у 1 (5,3%). У 11 (57,9%) больных выявлен туберкулез предстательной железы, с вовлечением придатков яичек – у 1 (5,3%), семенных пузырьков, также у 1 (5,3%) больного диагностирован изолированный туберкулезный эпидидимит. У 3 (15,8%) пациентов развился туберкулез мочевой системы без поражения мужских половых органов, из них у 2 (10,5%) – туберкулезный папиллит почек, у 1 (5,3%) – туберкулез мочевого пузыря с формированием микроцистиса и распространением на правый мочеточник.
Все пациенты получали терапию с учетом чувствительности к лекарственным препаратам с хорошим эффектом. Оперативное лечение выполнено 12 (63,2%) пациентам: 10 пациентам выполнена ТУР предстательной железы или мочевого пузыря, 6 – эпидидимэктомия и 1 – илеоцистопластика. В целом на 1 больного пришлось примерно 1,5 оперативных вмешательств.
Диагноз верифицирован у 16 (84,2%) человек: у 13 (68,4%) гистологически, из них ДНК микобактерий туберкулеза (МТБ) методом полимеразно-цепной реакции (ПЦР) обнаружена у 3 (15,8%) пациентов и еще у 3 (15,8%) – только ДНК. У оставшихся 3 (15,8%) ту- беркулез установлен на основании характерной кли нико-рентгенологической картины. Роста колоний МБТ при посеве мокроты и других биологических жидкостей не отмечено во всех случаях.
Для иллюстрации ятрогенного характера тубер кулеза после иммунотерапии рака мочевого пузыря вакциной БЦЖ приводим следующее клиническое на блюдение.
Клиническое наблюдение
Пациент Ж., 56 лет, поступил клинику №2 ГБУЗ МНПЦ борьбы с туберкулезом ДЗМ с жалобами на учащенное мочеиспускание малыми порциями (до 2 мочеиспусканий за час), тупую боль в поясничной области, жжение при мочеиспускании, ночную полла-киурию до 10 раз. Общее состояние удовлетворитель ное, артериальное давление 120/80 мм. рт. ст., частота дыхательных движений 18 в минуту, частота пульса 78 ударов в минуту, регулярный; температура тела 36,6°С
Из анамнеза известно, что рак мочевого пузыря выявлен в 1991 г., гистологически – переходно-клеточ ный без признаков инвазии в мышечный слой.С 1991 по 2023 гг. перенес 13 трансуретральных резекций мочевого пузыря, 2 курса химиотерапии адреомицином. С 2022 года переведен на внутрипузырную БЦЖ-терапию, получил 11 сеансов (индукционный курс и 5 ежемесячных вливаний в поддерживающий курс).
С августа 2022 г. стал отмечать боль в правом подреберье, общую слабость, повышение температуры тела.
Биохимические и клинические показатели крови в пределах нормы: мочевина 7,6 ммоль/л, креатинин 105 мкмоль/л, калий 4,0 ммоль/л, лейкоциты 3,2х109/л, Hb 127 г/л.
При ультразвуковом исследовании (УЗИ) вы явлена левосторонняя уретеропиело-каликоэктазия,
Таблица 1. Формы туберкулеза, развившиеся после БЦЖ-терапии рака мочевого пузыря
Table 1. Forms of tuberculosis that developed after BCG therapy for bladder cancer
|
Локализация, форма и распространенность Localization, form, and prevalence |
Количество Quantity абс. % |
Всего Total |
||
|
Туберкулез мужских гениталий Male genital organs tuberculosis |
Туберкулез предстательной железы Prostate тuberculosis |
9 |
47,4 |
12 (63,2%) |
|
Туберкулез предстательной железы + эпидидимит или везикулит Prostate Tuberculosis + epididymitis or vesiculitis |
2 |
10,5 |
||
|
Туберкулезный эпидидимит Tuberculosis epididymitis |
1 |
5,3 |
||
|
Туберкулез мочевыделительной системы Urinary system tuberculosis |
Туберкулез почек (папиллит) Kidney tuberculosis (papillitis) |
2 |
10,5 |
3 (15,8%) |
|
Туберкулез мочевого пузыря Bladder Tuberculosis |
1 |
5,3 |
||
|
Туберкулез легких Lung tuberculosis |
Диссеминированный туберкулез легких Disseminated pulmonary tuberculosis |
2 |
10,5 |
3 (15,8%) |
|
Инфильтративный туберкулез легких Infiltrative pulmonary tuberculosis |
1 |
5,3 |
||
|
Генерализованный туберкулез с вовлечением ЦНС, легких и мочеполовой системы Miliary tuberculosis with the central nervous system, lungs, genitourinary system |
1 |
5,3 |
1 (5,3%) |
|
снижение объема мочевого пузыря до 50 мл, утолще ние его стенок до 10мм.По данным компьютерной то мографии (КТ) органов дыхания картина диссемини рованного туберкулеза легких (рис. 1). На КТ органов брюшной полости с контрастным усилением двухсто ронняя уретероэктазия, более выраженная слева, мик роцистис, утолщение стенок мочевого пузыря (рис. 2) КТ головного мозга выявила мелкие гиперваскулярные очаги в левой гемисфере (рис. 3).
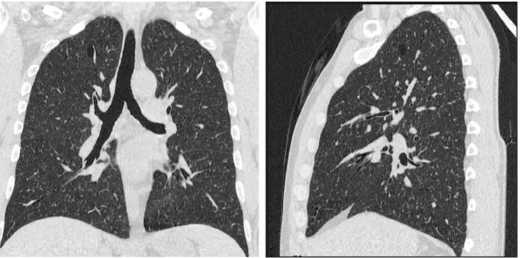
Рис. 1. Больной Ж. КТ органов грудной клетки: диссеминированный процесс в легких, киста правого легкого
Fig. 1. Patient J. Сhest CT: disseminated process in the lungs and a cyst in S1 of the right lung
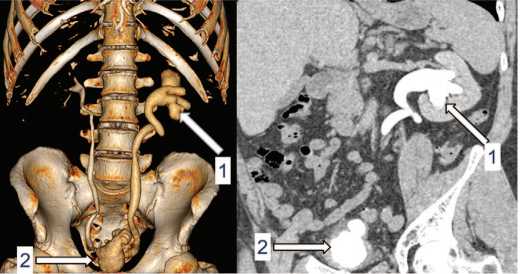
Рис. 2. Пациент Ж. КТ мочевыводящих путей с контрастным усилением: 1 – левосторонняя калико-пиелоэктазия (лоханка до 21 мм, расширение шеек чашечек до 14 мм, чашечек до 24 мм), стриктура (сужение до 1 мм) нижней трети левого мочеточника, двухсторонняя уретероэктазия, более выраженная слева; 2 – микроцистис, утолщение стенок мочевого пузыря до 12 мм
Fig. 2. Parient J. Contrast-enhanced CT of the urinary tract: 1- left-sided hydronephrosis (ureter up to 21 mm, dilatation of the calyces up to 14 mm and the calyces up to 24 mm), stricture (narrowing to 1 mm) of the lower third of the left ureter, and bilateral ureteroectasia, more pronounced on the lef; 2 - microcystis, thickening of the bladder walls up to 12 mm
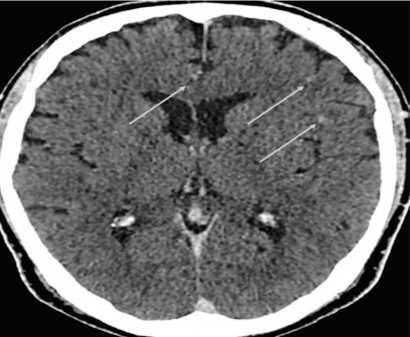
Рис. 3. Пациент Ж. КТ головного мозга: в левой гемисфере определяются гиперваскулярные очаги с перифокальным отеком размерами до 10 мм (отмечены стрелками).
Fig. 3. CT scan of the brain: hypervascular foci with perifocal edema up to 10 mm in size are detected in the left hemisphere (marked with arrows).
В мокроте кислотоустойчивых бактерий и ДНК МБТ не обнаружено. Проба с антигеном туберкулез ным рекомбинантным «Диаскинтест» от 17.11.2022 от рицательная. Тест на высвобождение интерферона-γ Т-SpotTB от 05.12.2022 отрицательный. В осадке мочи методом ПЦР обнаружена ДНК МБТ с сохраненной чувствительностью к противотуберкулезным препара там.
Решением врачебной комиссии установлен диаг ноз: «Генерализованный туберкулез: туберкулезный менингоэнцефалит; диссеминированный туберкулез легких в фазе инфильтрации, МБТ (-). Туберкулез мочеполовой системы: туберкулезный папиллит почек туберкулезный левосторонний уретерит, инфильтра тивная форма и туберкулез мочевого пузыря, с форми рованием микроцистиса МБТ(-), ДНК МБТ(+), 1 ГДН».
После проведения курса химиотерапии в количе стве 120 доз по схеме лечения лекарственно-чувстви тельного туберкулеза выполнена операция: супра тригональная резекция мочевого пузыря, илеоцисто пластика,имплантация левого мочеточника в неоци стис.
КТ мочевыводящих путей в динамике демонстри рует достаточную емкость артифициального мочевого пузыря, наличие стента в левом мочеточнике, восста новления адекватной уродинамики верхних мочевыво дящих путей (рис. 4).
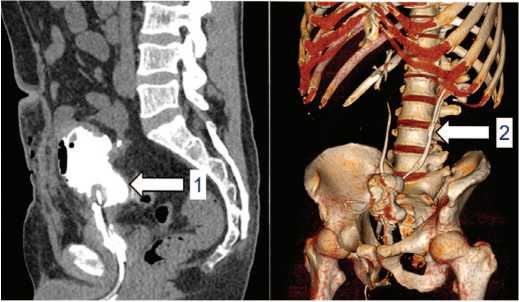
Рис. 4. Больной Ж. КТ мочевыводящих путей с контрастным усилением после операции: 1 – увеличение емкости мочевого пузыря, 2 – внутренний стент в левом мочеточнике
Fig. 4. Patient J. Contrast-enhanced CT of the urinary tract after surgery: 1– increased bladder capacity, 2 – internal stent in the left ureter
ОБСУЖДЕНИЕ
На данный момент остается неясным,коррели рует ли риск развития побочных эффектов, ассоции рованных с вакциной БЦЖ, с состоянием иммуно супрессии. В рамках исследования H.W. Herr и соавт. включавшего 45 пациентов,были проанализированы случаи применения внутрипузырной БЦЖ-терапии для лечения рака мочевого пузыря.Из общего числа пациентов 12 получали системную химиотерапию по поводу раковых заболеваний иной локализации,23 – стероидную терапию в связи с аутоиммунными заболеваниями, а 10 – не получали специфического лечения. В результате не было зарегистрировано ни одного случая БЦЖ-сепсиса, а терапия была признана хорошо переносимой [10].
В литературе зарегистрирован только один случай БЦЖ-индуцированного сепсиса через 7 лет после 6-недельного индукционного курса внутрипузырной БЦЖ-терапии и через 1,5 года после иммуносупрессии в связи с трансплантацией почки [11]. Из мочи и крови этого пациента выделена культура микобактерий штамма БЦЖ, т.е. сепсис был вызван скорее дис-семинацией микобактерий в условиях иммуносупрессивной терапии,а не системной реакцией гиперчувствительности. В связи с этим, клинические рекомендации Европейской ассоциации урологов (EAU) указывают, что БЦЖ-терапию следует использовать с осторожностью у пациентов с ослабленным иммунитетом, несмотря на сопоставимые случаи осложнений у пациентов с ослабленным иммунитетом и без него [12]. Вакцинация БЦЖ также не рекомендуется к применению у пациентов с аутоиммунными ревматическими заболеваниями, однако мало данных, доказывающих, что безопасность лечения снижается у лиц, получающих синтетические или биологические противоревматические препараты [13, 14].
При лечении пожилых пациентов возрастное ухудшение врожденного и адаптивного иммунитета и снижение работоспособности могут влиять на риск терапевтической токсичности.У пожилых пациентов потенциальные побочные эффекты и осложнения внутрипузырной иммунотерапии БЦЖ могут встречаться чаще. Отмечено повышение частоты осложнений у пациентов старше 70 лет почти в три раза по сравнению с более молодыми (48,6% против 17,6%, соответственно) после поддерживающей терапии БЦЖ [15]. В ретроспективном исследовании 200 пациентов старше 80 лет при индивидуальном режиме введения БЦЖ 1 раз в 2 недели продемонстрировано значительное снижение доли осложнений: 15% против 27% у пожилых при стандартной еженедельной терапии БЦЖ [16].
Хронические сопутствующие заболевания рассматриваются как потенциальные предрасполагающие факторы риска системных побочных эффектов [17]. Однако Pérez-Jacoiste Asín MA и соавт. провели исследование 11 пациентов с системной БЦЖ-инфекцией из общей выборки в 245 человек, получавших внутрипу-зырную иммунотерапию по поводу рака мочевого пузыря. Не было обнаружено значимых различий по демографическим показателям, сопутствующим заболеваниям или ранее установленному диагнозу активной или латентной туберкулезной инфекции между пациентами с системной БЦЖ-инфекцией и без нее. Не выявлено также существенных различий ни по среднему количеству ТУР мочевого пузыря до первой инстилляции БЦЖ,ни по среднему количеству ин-стилляций,ни по временному интервалу между последней ТУР и первой инстилляцией [18].
Введение БЦЖ начинают не ранее чем через 2 недели после ТУР мочевого пузыря,чтобы обеспечить адекватное заживление уротелия и предотвратить системную абсорбцию вакцины. Более того, внутрипу-зырное введение БЦЖ противопоказано пациентам с макрогематурией, после травматичной катетеризации или с симптоматической инфекцией мочевыводящих путей [12]. Следует учитывать потенциальное влияние некоторых антибиотиков,особенно фторхиноло-нов, на жизнеспособность БЦЖ и последующую эффективность. Сообщалось, что снижение дозы внутрипузырного введения БЦЖ приводит к снижению ее потенциальной токсичности.В рандомизированном проспективном исследовании местные проявления токсичности наблюдали у 33,3% пациентов с уменьшенной до 27 мг дозой внутрипузырной БЦЖ против 45,3% – со стандартной дозой 81 мг и аналогичными онкологическими результатами. Но различий в тяжелых системных осложнениях между этими группами обнаружено не было: 4,4% против 3,6% соответственно [19].
Профилактика осложнений эффективно используется для снижения потенциальной токсичности внутрипузырной БЦЖ.В рандомизированном проспективном, двойном слепом, многоцентровом исследовании изучены результаты лечения 120 пациентов, которым выполняли 6 еженедельных инстилляций БЦЖ. Оказалось, что местные побочные эффекты, ограниченные мочевым пузырем,были значительно ниже среди тех, кто получал 3-дневный курс изониазида 300 мг в сравнении с плацебо (35% против 48%) [20]. Напротив, в последующем более крупном рандомизированном исследовании не отмечено снижения частоты цистита, гематурии или высокой лихорадки у пациентов, лечившихся БЦЖ и изониазидом. Именно в этой группе зарегистрирован один случай легочной диссеминации, вызванной БЦЖ [21]. Проведенное проспективное рандомизированное открытое контролируемое клиническое исследование показало, что профилактический 3-дневный курс прулифокса-цина 600 мг имеет значительную эффективность в предотвращении системных, умеренных и тяжелых нежелательных явлений после инстилляций БЦЖ при промежуточном или высоком риске НМИРМП [22]. Также в рандомизированном, проспективном, двойном слепом, плацебо-контролируемом, многоцентровом исследовании отмечено, что прием офлоксацина значительно (на 18,5%) снизил частоту умеренных и тяжелых побочных эффектов, связанных с внутрипу-зырной терапией БЦЖ [23].
Надо отметить,что на сегодняшний день отсутствуют очевидные предикторы,которые могли бы по- мочь врачам выявить пациентов с риском развития БЦЖ-инфекции после внутрипузырных инстилляций БЦЖ. Учитывая многообразие клинических прояв лений этого осложнения, сохраняется высокая степень настороженности для своевременного начала проти вотуберкулезной терапии. Несмотря на то, что данное состояние имеет в целом благоприятный прогноз,су ществует неопределенность относительно безопасно сти возобновления внутрипузырных инстил ляций БЦЖ, что ставит под угрозу прогноз основного злокачественного новообразования. Для точного опре деления факторов риска этого осложнения, а также оп тимальной тактики его лечения необходимы проспек тивные многоцентровые исследования.
В настоящее время нами разработан алгоритм ди агностики и лечения пациентов с подозрением на ту беркулез после внутрипузырной БЦЖ-терапии рака мочевого пузыря (рис. 6).
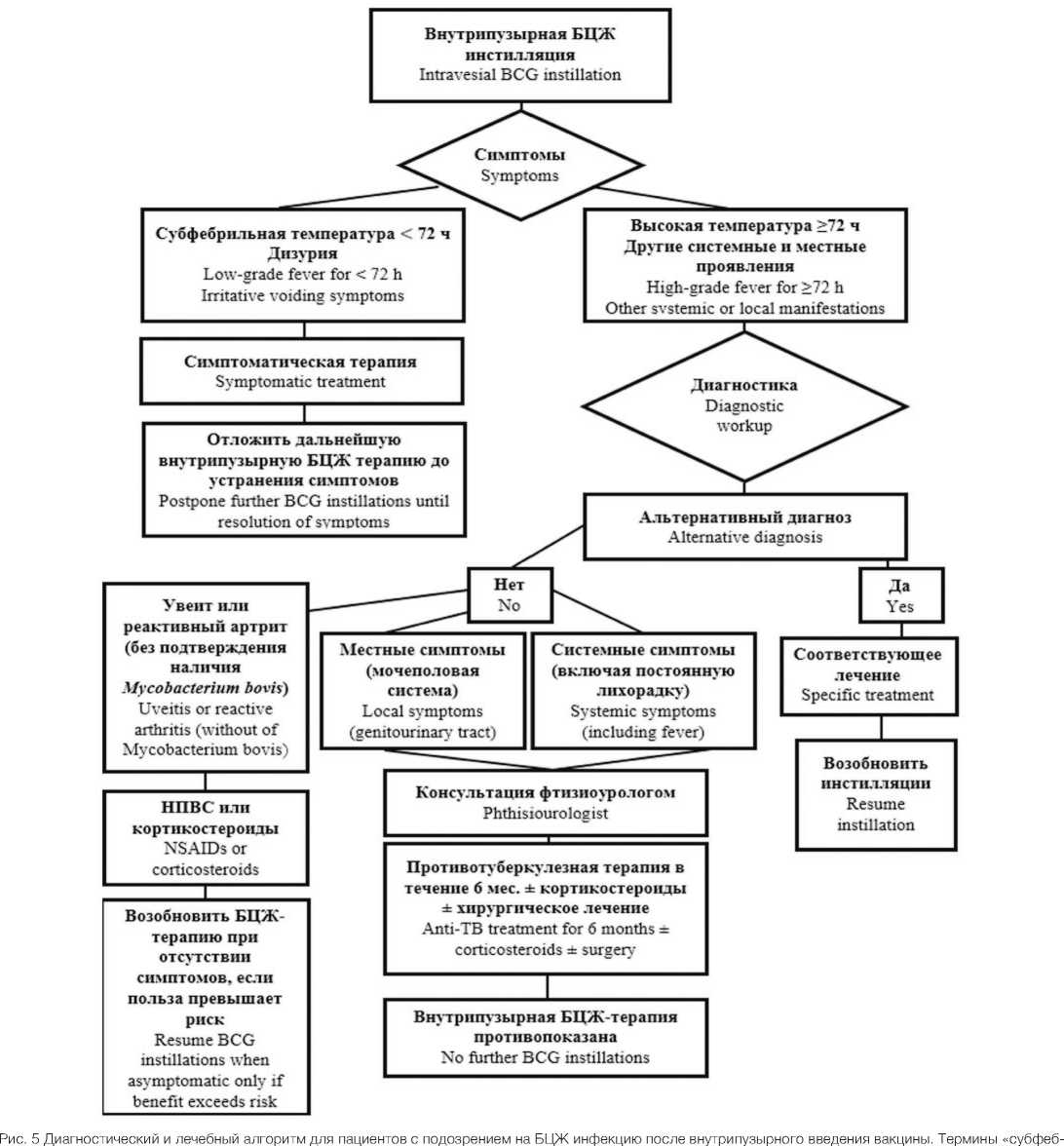
рильная» и «высокая» температура обозначают температуру тела <37,9 °C и ≥38 °C соответственно
Fig. 5 Algorithm for the diagnosis and treatment of patients with suspected BCG infection after intravesical BCG instillation. The terms «low-grade fever» and «high-grade fever» refer to body temperatures of <37.9 °C and ≥38 °C, respectively
ЗАКЛЮЧЕНИЕ
В настоящее время при всех низкодифференцированных и некоторых высокодифференцированных НМИРМП для профилактики рецидивов применяется внутрипузырная БЦЖ иммунотерапия, которая доказала свою эффективность.Однако одним из серьезных осложнений БЦЖ-терапии являются различные микобактериальные осложнения.
Необходимо отметить трудности диагностики различных форм туберкулеза после БЦЖ-терапии для подтверждения диагноза следует проводить био псию тканей для гистопатологического исследования и обнаружения M. bovis.
Больным с микобактериальными осложнениями может потребоваться комбинированная противоту беркулезная терапия в течение 3–12 месяцев, а также применение хирургического вмешательства.
nTEPAUPA/REFEREHES
Сведения об авторах:
Зубань О.Н. – д.м.н., профессор, заместитель директора по научно-клинической работе, врач-уролог ГБУЗ «Московского городского научно-практического центра борьбы с туберкулезом Департамента здравоохранения города Москвы», профессор кафедры фтизиатрии ФГБОУ ДПО «Российской медицинской академии непрерывного профессионального образования» Минздрава России; Москва, Россия;
РИНЦ Author ID 584866,
Сикаев Ю.Р. – врач-уролог туберкулезного внелегочного отделения Клиники № 2 ГБУЗ «Московского городского научно-практического центра борьбы с туберкулезом Департамента здравоохранения города Москвы»; Москва, Россия
Чотчаев Р.М. – д.м.н., заместитель главного врача по медицинской части, уролог Клиники №2 ГБУЗ «МНПЦ борьбы с туберкулезом ДЗМ», профессор кафедры фтизиатрии ФГБОУ ДПО «Российской медицинской академии непрерывного профессионального образования» Минздрава России, профессор кафедры инфекционных болезней с курсами эпидемиологии и фтизиатрии ФГАОУ ВО «Российского Университета Дружбы Народов имени Патриса Лумумбы»; Москва, Россия; РИНЦ Author ID 903985,
Авдентова В.Б. – научный сотрудник научно-клинического отдела, врач-фтизиатр ГБУЗ «Московского городского научно-практического центра борьбы с туберкулезом Департамента здравоохранения города Москвы»Москва, Россия;
РИНЦ Author ID 1061427
Вклад авторов:
Зубань О.Н. – общее руководство, идея, концепция, сбор материала, дизайн исследования, оформление, поиск литературы, написание, корректирование и утверждение текста, 45%
Сикаев Ю.Р. – сбор и обработка материала, статистическая обработка, редактирование, оформление и написание текста, 35%
Чотчаев Р.М. – общее руководство, сбор материала, редактирование, проверка и утверждение текста, 15%
Авдентова В.Б. – сбор и обработка материала, редактирование текста, 5%
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Финансирование: Статья подготовлена без финансовой поддержки.


