Микробиологические исследования клинического материалакак этап профилактики перипротезной инфекции при артропластике крупных суставов
Автор: Пчелова Н.Н., Борисова Л.В., Назарова В.В., Добровольская Н.Ю.
Журнал: Кафедра травматологии и ортопедии @jkto
Статья в выпуске: 3 (33), 2018 года.
Бесплатный доступ
Целью исследования является анализ частоты положительных посевов биоматериала у пациентов при первичном и ревизионном эндопротезировании крупных суставов; выявление расхождений результатов посева пунктатов до операции и посева интраоперационного биоматериала; сравнение результатов посева синовиальной жидкости в бактериологических лабораториях по месту жительства с данными лаборатории ФГБУ «Федеральный центр травматологии, ортопедии и эндопротезирования» Минздрава России (г. Чебоксары); проведение анализа микробиологического пейзажа возбудителей инфекционных осложнений. Материалом исследования явились результаты микробиологического исследования 12847 проб биоматериала от 5881 пациента, взятых в 2015-2017 гг. (пунктаты из полости сустава, тканевые биоптаты, смывы с удаленных компонентов протезов, спейсеров и других металлоконструкций). Группу исследования составили пациенты, нуждающиеся в первичном эндопротезировании и имеющие в анамнезе 4 и более фактора риска развития инфекционных осложнений (6433 пробы, из них положительные - 3); поступившие на ревизионное эндопротезирование (2991 проба, из них положительные - 414); имеющие металлоконструкции в области хирургического вмешательства или состояние после их удаления (1631 проба, и них положительные - 15); имеющие в анамнезе гнойный процесс в области планируемого оперативного вмешательства (1792 пробы)...
Перипротезная инфекция, микробиологическое исследование, пунктаты крупных суставов
Короткий адрес: https://sciup.org/142221765
IDR: 142221765 | УДК: 616-093-098 | DOI: 10.17238/issn2226-2016.2018.3.40-45
Microbiological studies of clinical material as a stage of prophylaxis of periprosthetic infection after arthroplasty of large joints
The purpose of the study is to analyze the frequency of positive culture of biomaterial in patients with primary and revision of large joint arthroplasty; identify discrepancies between the results of sowing of puncts before surgery and sowing of intraoperative biomaterial; comparison of the results of sowing of synovial fluid in the bacteriological laboratories at the place of residence with the data of the laboratory of Federal center for traumatology, orthopedics and endoprosthetics of the Ministry of health of Russia (Cheboksary); analysis of the microbiological landscape of pathogens of infectious complications. The material of the study was the results of microbiological examination of 12847 samples of biomaterial from 5881 patients taken in 2015-2017 (punctates from the joint cavity, tissue bioptates, washouts from remote components of prostheses, spacers and other metal structures). The study group consisted of patients who needed primary endoprosthetics and who had a history of 4 or more risk factors for the development of infectious complications (6433 samples, of them positive - 3); received for revision of the endoprosthetics (2991 samples, of them 414 were positive); having metal structures in the field of surgical intervention or condition after their removal (1631 samples, and they are positive - 15); having a history of purulent process in the field of planned surgical intervention (1792 samples)...
Текст научной статьи Микробиологические исследования клинического материалакак этап профилактики перипротезной инфекции при артропластике крупных суставов
Открытие в России федеральных центров по эндопротезированию крупных суставов в разы увеличило количество подобных операций. Это, в свою очередь, влечёт за собой рост числа инфекционных осложнений [1]. Совершенствование методов микробиологической диагностики повышает частоту выявля-емости инфекций как на нативных, так и на протезированных суставах.
Исследование синовиальной жидкости важно для выявления этиологии болевого синдрома у пациентов без явных клинических признаков воспаления перипротезной зоны, в случаях наличия в анамнезе оперативных вмешательств с использованием металлоконструкций, а также при гнойных осложнениях в области хирургического вмешательства у пациентов, которым планируется проведение артропластики [2].
По литературным данным зарубежных исследователей, инфекционные осложнения при установке ортопедических устройств для фиксации перелома встречаются в 5% случаев [3].
Зачастую решающую роль в выборе тактики хирургического лечения для травматолога-ортопеда имеют именно данные микробиологического исследования биоматериала [4].
Согласно консенсусу по перипротезной инфекции (ППИ) под руководством Parvisi J, для интерпретации и достоверности результатов посевов рекомендовано исследовать 3-6 проб биоматериала [5,6,7].
Клинически значимыми в развитии инфекции протезированных суставов считается рост высоковирулентного микроорганизма в одной пробе биоматериала или рост низковирулентного микроорганизма (например, коагулазонегативные стафилококки) в двух и более пробах [8.]
Цель исследования
-
1. Выявить частоту положительных посевов интраоперационного биоматериала у пациентов при первичном и ревизионном эндопротезировании коленных и тазобедренных суставов.
-
2. Сопоставить результаты исследования пунктатов коленных и тазобедренных суставов при ревизионных вмешательствах, взятых до операции, с результатами посевов интраоперационного биоматериала.
-
3. Провести анализ микробиологического пейзажа возбудителей инфекционных осложнений в разных клинических ситуациях.
-
4. Сравнить результаты микробиологических посевов синовиальной жидкости, проведённых на амбулаторном этапе по месту жительства, с данными лаборатории ФГБУ «Федеральный центр травматологии, ортопедии и эндопротезирования» Минздрава России (г. Чебоксары).
Материалы и методы
В ФГБУ «Федеральный центр травматологии, ортопедии и эндопротезирования» Минздрава России (г. Чебоксары), далее – Центр, проведен ретроспективный анализ результатов микробиологических исследований биологического материала пациентов с патологией крупных суставов. Центр является одним из ведущих учреждений России по артропластике крупных суставов. С 2009г. на базе учреждения выполнено 37222 эндопротезирования тазобедренных (ТБС) и коленных (КС) суставов для жителей различных регионов России, в т.ч. 16466 артропластик – за исследуемый период 2015-2017 гг.
Проанализированы результаты посева пунктатов, полученных под ультразвуковым контролем на амбулаторном этапе, а также посевов аспиратов из полости сустава, тканевых био-птатов, смывов с удаленных компонентов протезов, спейсеров и других металлоконструкций, взятых во время операции.
Исследование биоматериала проводилось пациентам, отвечающим следующим критериям:
-
- наличие в анамнезе 4 и более факторов риска развития инфекционных осложнений у пациентов при первичной артропластике;
-
- необходимость в ревизионном эндопротезировании;
-
- наличие металлоконструкций в области хирургического вмешательства или состояние после их удаления;
-
- наличие в анамнезе гнойных процессов в области планируемого оперативного вмешательства.
К факторам риска инфекционных осложнений были отнесены: возраст пациента старше 60 лет; индекс массы тела более 35 кг/м²; системные заболевания на фоне базисной терапии стероидами, иммунодепрессантами или цитостатиками; иммуносупрессия (рецидивы фурункулеза, герпеса, частые ОРВИ в анамнезе, ВИЧ-инфекция); гнойные осложнения в анамнезе или наличие очагов хронической инфекции; экстракция зубов менее чем за неделю до операции; онкологические заболевания; наличие лейкоцитоза или лейкопении в общем анализе крови; сахарный диабет; прием антибактериальных препаратов в течение последних 4-х месяцев; операции в течение 6 месяцев до настоящей; неоднократные хирургические манипуляции в области планируемого вмешательства в анамнезе; обнаружение во время операции внешне измененных тканей.
Отдельной оценке подвергался микробиологический пейзаж биоматериала, взятого у пациентов с глубокой ППИ; у пациентов с имеющимися/удалёнными металлоконструкциями в области хирургического вмешательства перед первичной артропластикой; при инфекционных артритах.
На основе анализа данных электронных медицинских карт (ЭМК) пациентов проведена оценка совпадений/расхождений результатов микробиологических посевов синовиальной жидкости, проведённых на амбулаторном этапе по месту жительства, с данными лаборатории Центра.
Для микробиологического исследования создавались условия для роста наиболее широкого спектра микроорганизмов - для аэробов, анаэробов и прихотливых микроорганизмов. Использовались высокопитательные среды: кровяной, шоколадный, Шедлер - агары, бульон со средой Шедлера, аэробные и анаэробные флаконы анализатора для стерильных в норме биологических жидкостей. Исследование смывов, полученных с помощью обработки имплантов в ультразвуковой мойке BRANSON 8510, проводили в анализаторе для стерильных в норме биологических жидкостей Bact/aLERT 3D с применением аэробных и анаэробных флаконов. Продолжительность инкубации посевов составляла не менее 14 суток.
Идентификацию выделенных микроорганизмов и определение антибиотикочувствительности проводили при помощи автоматического бактериологического анализатора Vitek-2 compact («Bio Merieux»), полуавтоматического анализатора Multiskan FC c использованием коммерческих тест-систем.
Анализ ЭМК проводился с применением медицинской информационной системы (МИС) Центра. Для формирования отчета по исследованию и интерпретации результатов анализов был разработан бланк «Направление на микробиологическое исследование» согласно форме 204/у, утвержденной Минздравом СССР от 04.10.1980 г. №1030, в которую введены дополнительные поля (рис. 1).
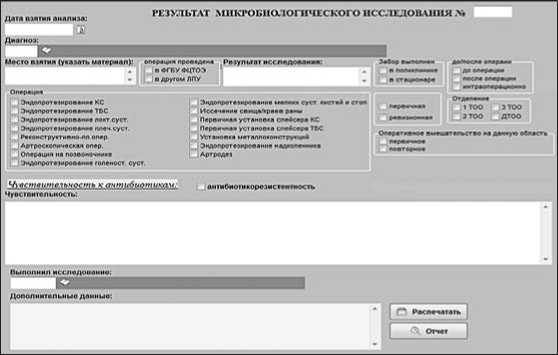
Рис.1. Экранная форма бланка «Направление на микробиологическое исследование»
Мы считали значимыми такие параметры, как место забора материала (медицинская организация по месту жительства пациента; поликлиника, стационар Центра); время забора биоматериала (до, во время или после операции); вид эндопротезирования (первичное или ревизионное); особенности оперативного вмешательства (нативный сустав, наличие металлоконструкций или состояние после их удаления, первичная или повторная установка спейсера).
Статистическую обработку полученных данных проводили с помощью пакета анализа данных программного комплекса «Microsoft EXCEL 2010». Характер вариабельности данных лабораторных исследований подчинялся законам нормального рас- пределения, что позволило отражать результаты в виде средней арифметической (М) и средней ошибки среднего значения (m).
Результаты и обсуждение
Ретроспективному анализу подверглись результаты микробиологического исследования 12847 проб биоматериала от 5881 пациента за период 2015-2017гг., из которых более 90% получено интраоперационно (табл.1).
Таблица 1
Объём проведённых микробиологических исследований проб биоматериала, 2015-2017 гг.
|
Год |
Число обследованных пациентов, n |
Число взятых проб |
||||
|
Всего, n |
в т.ч. интраоперационно, n |
% |
Амбулаторно, n |
% |
||
|
2015 |
2201 |
3964 |
3616 |
91,2 |
348 |
8,8 |
|
2016 |
2565 |
5931 |
5323 |
89,9 |
608 |
10,1 |
|
2017 |
1115 |
2952 |
2116 |
71,7 |
836 |
28,3 |
|
Итого |
5881 |
12847 |
11055 |
86,0 |
1792 |
14 |
Если в 2015 г. на 1 пациента приходилось в среднем 1,8 пробы, то в 2016г. этот показатель увеличился до 2,3 пробы, в 2017 г. этот показатель составил в среднем 3,2 пробы на одного пациента. Невысокий средний показатель кратности взятия биоматериала обусловлен большим числом микробиологических исследований нативных суставов с низкой кратностью проб (1,7 на одного пациента), что «размывает» средний показатель. Кратность проб при ревизионных операциях составила 6,2, что соответствует критериям консенсуса по ППИ.
Ежегодный анализ инфекционных осложнений показал необходимость исследования интраоперационного биоматериала у пациентов с нативными суставами, имеющих риски инфекционных осложнений в анамнезе.
При проведении протезирования на нативных КС исследованы 5772 проб от 3274 пациентов с 4 и более факторами риска. За период исследования выявлено 3 положительных результата у 2 пациентов (в среднем 0,05% от ежегодного числа проб). Резистентный эпидермальный стафилококк у одного из пациентов выделен только в одной пробе, результат расценен как контаминация и в дальнейшей тактике лечения не учитывался. У другого пациента выделен аналогичный микроорганизм, идентичный в двух пробах (в анамнезе у данного пациента имело место внутрисуставное введение лекарственных препаратов), в дальнейшем пациент длительно получал этиотропную антибактериальную терапию (табл.2).
При первичном протезировании нативных ТБС у 464 пациентов с отягощенным анамнезом, имеющих риск инфекционных осложнений, за 2015–2017 гг. положительных проб не выявлено.
В 2015 и 2016 гг., несмотря на большое число микробиологических исследований нативных суставов, выявленный процент положительных высевов достаточно низок (0,05%). Данный результат показал нецелесообразность сплошного подхода в заборе материала у этой группы пациентов. Показания для микробиологического исследования нативных суставов были определены нами на основании факторов риска инфекционных осложнений протезированных суставов: гнойно-септические процессы, системные заболевания, обнаружение во время операции внешне измененных тканей. Внедрение данных критериев привело к снижению в 2017 г. количества забора биоматериала с нативных суставов.
Анализ результатов посевов интраоперационного биоматериала у пациентов с наличием в анамнезе операций с использованием металлоконструкций в области хирургического вмешательства (ТБС и КС), в 2015 г. выявил 4 случая положительных высевов (1,4% от общего числа пациентов). Клинически значи-
Таблица 2
Результаты исследований интраоперационного биоматериала на нативных суставах, 2015-2017 гг.
В 2016 г. положительные посевы выявлены у 3-х пациентов (в 1,0% случаев). У одного – рост Staphylococcus epidermidis
MRSE в 2-х пробах, у другого - рост Staphylococcus epidermidis MRSE в одной пробе с удаленных винтов, у третьего – рост Propionibacterium granulosum в трех образцах), в 2017 г. – только у одного пациента (рост Staphylococcus lugdunensis в 2-х пробах), что составило 0,7% случаев. На амбулаторном этапе двоим пациентам перед артропластикой исследование пунктатов из суставов не проводились, несмотря на отягощенный анамнез. В одном случае в 2016 г. получен положительный посев интраоперационного материала при отрицательных результатах пункции на амбулаторном этапе (табл. 3).
Таблица 3
Результаты исследований интраоперационного биоматериала при первичном эндопротезировании с наличием в анамнезе операций в области хирургического вмешательства, 2015-2017 гг.*
|
Годы |
Коленный сустав |
Тазобедренный сустав |
||||||
|
Пробы |
Пациентов |
Пробы |
Пациентов |
|||||
|
всего n |
позитивные n (%) |
всего n |
позитивные n (%) |
всего n |
позитивные n(%) |
всего n (%) |
позитивные n(%) |
|
|
2015 |
324 |
4 (1,23%) |
195 |
2 (1,03%) |
233 |
3 (1,29%) |
88 |
2 (2,27%) |
|
2016 |
404 |
0 (0%) |
192 |
0 (%) |
304 |
6 (1,94%) |
102 |
3 (2,94%) |
|
2017 |
83 |
0 (%) |
39 |
0 (%) |
283 |
2 (0,70%) |
109 |
1 (0,91%) |
|
итого |
811 |
4 (0,49%) |
426 |
2 (0,47%) |
820 |
11 (1,34%) |
299 |
6 (2%) |
*в таблицу не включены данные о пациентах с металлоконструкциями, обследованных амбулаторно.
Помимо этого, в амбулаторных условиях нами обследовано 210 пациентов, перенесших операции по установке металлоконструкций (при этом у 11 из них, или 5,2%, выявлены клинически значимые для развития инфекции протезированных суставов микроорганизмы), что позволило рационально спланировать тактику хирургического лечения.
При ревизионных вмешательствах у пациентов с ППИ за анализируемые годы соотношение положительных посевов при
Таблица 4
Результаты исследований интраоперационного биоматериала при ревизионном вмешательстве, 2015-2017 гг.
|
Годы |
Коленный сустав |
Тазобедренный сустав |
||||||
|
Пробы |
Пациентов |
Пробы |
Пациентов |
|||||
|
всего n |
позитивные n (%) |
всего n |
позитивные n (%) |
всего n |
позитивные n (%) |
всего n |
позитивные n (%) |
|
|
2015 |
385 |
38 (9,8%) |
69 |
18 (26%) |
338 |
58 (17,1%) |
58 |
17 (29,3%) |
|
2016 |
429 |
93 (21,7%) |
79 |
19 (24,05%) |
554 |
93 (16,7%) |
76 |
18 (23,6%) |
|
2017 |
627 |
67 (10,3%) |
95 |
13 (13,6%) |
658 |
65 (9,9%) |
103 |
14 (13,5%) |
|
Итого |
1441 |
198 (13,7%) |
243 |
50 (20,6%) |
1550 |
216 (13,9%) |
237 |
49 (20,7%) |
эндопротезировании КС и ТБС выглядело как 1:1. Отрицательные пробы получены от пациентов, нуждающихся в замене компонентов эндопротеза по поводу асептической нестабильности, при износе вкладыша, перипротезных переломах, открытых вправлениях вывихов эндопротезов (табл. 4).
Обращает на себя внимание результат анализа синовиальной жидкости, взятой для контроля лечения у пациентов с установленным спейсером на амбулаторном этапе при двухэтапной санирующей ревизии по поводу инфекции. У исследованных 105 пациентов результат в 100% был отрицательным. Этот факт позволяет предположить целесообразность отказа от проведения амбулаторного исследования пунктата пациентам со спейсером перед вторым этапом ревизии.
Сравнительный анализ результатов посевов при ревизионном эндопротезировании в пунктате, взятом до операции, и в интраоперационном материале показал совпадение результатов в 281 случаях из 290 (96,9%). Характеризуя случаи расхождения (9 или 3,1%), мы отметили, что в 4-х случаях более информативным оказался интраоперационный материал (пунктаты до операции – отрицательные); в 5-ти случаях при наличии клиники ППИ при положительном результате посева синовиальной жидкости до операции получен отрицательный интраоперационный посев. Проведенный анализ показывает необходимость комплексного подхода к оценке микробиологического исследования биоматериала с учётом анамнестических и клинических данных (антибактериальная терапия, качество забора биоматериала).
Выявление ведущего возбудителя инфекционных осложнений имеет огромное значение для проведения профилактических мероприятий и выбора лечебной тактики. Изучен микробиологический пейзаж при различных нозологических формах инфекционных осложнений у пациентов, прооперированных в Центре. Среди возбудителей, выявленных у пациентов с ППИ, превалировал золотистый стафилококк (42,2%). Вторую позицию занимали коагулазонегативные стафилококки (25,5%), главным образом, эпидермальный стафилококк (84,6%), в 77% случаев представленный резистентными штаммами. Третьими по частоте были энтерококки и стрептококки (12,7%). Далее, в порядке убывания, - грамотрицательная флора, микст-флора, анаэробы и другие микроорганизмы. (рис. 2).
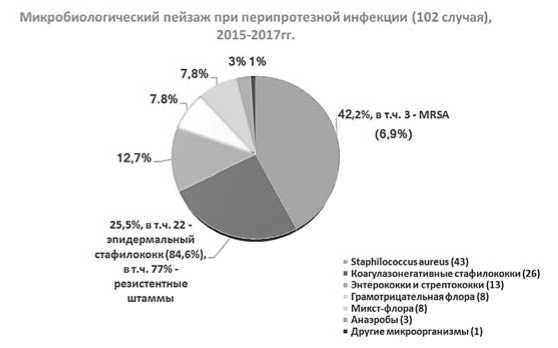
Рис. 2. Микробиологический пейзаж при перипротезной инфекции (102 случая), 2015-2017 гг.
Микробный пейзаж пациентов после остеосинтеза металлоконструкциями (n=15) отличается от пейзажа при ППИ. Здесь ведущую роль играет эпидермальный стафилококк (n=9), доля которого составляет 60% (из которых резистентные штаммы – 55%). В равном соотношении - по 13,3% (n=2) – представлены золотистый стафилококк, микст-инфекция и анаэробы.
Ведущую роль в развитии гнойных артритов (n=8), как и при ППИ, играет золотистый стафилококк (n=7), доля которого составляет 87,5% (резистентных штаммов выявлено не было), остальная флора была представлена сальмонеллой (n=1) – 12,5% случаев.
В связи с тем, что от результатов микробиологического посева зависит хирургическая тактика лечения пациента, возникла необходимость повторного исследования пунктатов до операции в лаборатории Центра и сравнения их с данными посевов, полученных по месту жительства пациентов. Анализ ЭМК пациентов показал расхождение результатов у 21 пациента из 116 обследованных, что составляет 16,8%. По месту жительства ложноположительные результаты могли быть обусловлены контаминацией. Достоверность исследований в условиях Центра подтверждалась в последующем данными интраоперационных посевов и клиническим наблюдением.
Заключение и выводы
-
1. Интраоперационное исследование нативного сустава без соответствующего отягощенного инфекционного анамнеза нецелесообразно.
-
2. Расхождение результатов посева пунктатов до операции и посева интраоперационного биоматериала показывает необходимость комплексного подхода к оценке микробиологического исследования биоматериала с учётом анамнестических и клинических данных (антибактериальная терапия, качество забора биоматериала).
-
3. Анализ микрофлоры при инфекционных осложнениях суставов выявил различия ведущего возбудителя в разных клинических ситуациях: после остеосинтеза металлоконструкциями - это коагулазонегативные стафилококки (в 55% случаев являющиеся резистентными), а при глубокой перипротезной инфекции и артритах – золотистый стафилококк.
-
4. С учетом расхождений полученных результатов посевов синовиальной жидкости, выполненных пациентам амбулаторно по месту жительства и в лаборатории Центра, целесообразно проводить контрольную пункцию перед госпитализацией в условиях Центра. Исследование пунктатов пациентам с установленными спейсерами перед вторым этапом ревизионного эндопротезирования нецелесообразно.
-
5. vВыявление микроорганизмов в биологическом материале из сустава перед проведением артропластики может профилак-тировать развитие инфекционного осложнения протезировано-го сустава.
Список литературы Микробиологические исследования клинического материалакак этап профилактики перипротезной инфекции при артропластике крупных суставов
- Yin J.M., Liu Z.T., Zhao S.C., Guo Y.J. Diagnosis, management, and prevention of prosthetic joint infections. Front Biosci (Landmark ed). 2013; Vol. 18: 1349-57
- Николаев Н.С., Николаева А.В., Пчелова Н.Н. Борисова Л.В. Комплексный подход к проблеме инфекционных осложнений после эндопротезирования крупных суставов. Вестник академии наук Молдовы. Медицина. 2017;3(55):341-347. [Nikolaev N.S., Nikolaeva A.V., Pchelova N.N. Borisova L.V. Kompleksnyj podhod k probleme infekcionnyh oslozhnenij posle ehndoprotezirovaniya krupnyh sustavov. Vestnik akademii nauk Moldovy. Medicina. 2017;3(55):341-347.]
- Diagnosis and treatment of infections associated with fracture-fixation devices Andrej Trampuz, Werner Zimmerli, Injury, Int. J. Care Injured (2006) 37, S59-S66
- Николаев Н.С., Борисова Л.В., Пчелова Н.Н., Орлова А.В., Каралин А.Н. Практические рекомендации по диагностике имплант-ассоциированной инфекции при эндопротезировании крупных суставов в современных условиях. Медицинский альманах, 2016;3(43):40-5. [Nikolaev N.S., Borisova L.V., Pchelova N.N., Orlova A.V., Karalin A.N. Prakticheskie rekomendacii po diagnostike implant-associirovannoj infekcii pri ehndoprotezirovanii krupnyh sustavov v sovremennyh usloviyah. Medicinskij al'manah, 2016;3(43):40-5.]
- Parvisi J., Gehrke T., Chen A.F. Proceedings of the International Consensus in Periprosthetic Joint Infection. Bone Joint J. 2013; 95-B: 1450-145
- Peel TN, Spelman T, Dylla BL, Hughes JG, Greenwood-Quaintance KE, Cheng AC, Mandrekar JN, Patel R. 2017. Optimal periprosthetic tissue specimen number for diagnosis of prosthetic joint infection. J Clin Microbiol 55:234-243. DOI: 10.1128/JCM.01914-16
- Федеральные клинические рекомендации. Двухэтапное ревизионное эндопротезирование в лечении перипротезной инфекции в области тазобедренного сустава. // Санкт-Петербург 2015г. ФГБУ «РНИИТО им. Р.Р. Вредена» Минздрава России. [Federal'nye klinicheskie rekomendacii. Dvuhehtapnoe revizionnoe ehndoprotezirovanie v lechenii periproteznoj infekcii v oblasti tazobedrennogo sustava. // Sankt-Peterburg 2015g. FGBU «RNIITO im. R.R. Vredena» Minzdrava Rossii.]
- Renz N.,Trampuz A. Pocet Guide to Diagnosis & Treatment of Periprosthetic joint infection.Version 4: 18.07.2016.


