Микробная ферментация субпродуктов птицы
Автор: Зинина Оксана Владимировна, Меренкова Светлана Павловна, Князева Александра Сергеевна, Марушкевич Марина Александровна, Гаврилова Карина Сергеевна
Рубрика: Биохимический и пищевой инжиниринг
Статья в выпуске: 4 т.9, 2021 года.
Бесплатный доступ
Цель работы - исследование влияния микробной ферментации субпродуктов птицы на накопление продуктов гидролиза белка и изменение микроструктуры гидролизатов. В качестве объектов исследования выбраны мышечные желудки цыплят-бройлеров и кур родительского стада, которые подвергали микробной ферментации бактериальными концентратами пропионовокислых бактерий и бифидобактерий. Ферментацию проводили при температурах 30, 35 и 40 °С в течение 16 ч. Для анализа степени гидролиза определяли содержание аминного азота через каждые 4 часа ферментации. Отмечено, что под действием ферментов микроорганизмов происходит более глубокий гидролиз молекулы белка с интенсивным накоплением аминного азота. При этом наиболее высокое накопление аминного азота наблюдается при микробной ферментации желудков пропионовокислыми бактериями при температуре 30 °С, а бифидобактериями - при температуре 40 °С. Также о степени гидролиза судили по накоплению свободных аминокислот. Установлено увеличение концентрации свободных аминокислот в контрольных и экспериментальных образцах гидролизатов после 16 часов ферментации. В гидролизатах желудков, ферментированных пропионовокислыми бактериями и бифидобактериями, наблюдалось значительное накопление незаменимых аминокислот. Содержание как незаменимых, так и заменимых аминокислот в гидролизатах субпродуктов цыплят-бройлеров в несколько раз выше, по сравнению с субпродуктами кур маточного стада. Исследования микроструктуры гидролизатов желудков с помощью сканирующей электронной микроскопии показали, что под действием бактерий происходит значительное изменение структуры мышечных и коллагеновых волокон, их диссоциация на многочисленные тонкие фибриллы и формирование ретикулярной структуры в сочетании с глобулярными белками и минеральными компонентами сыворотки. Образцы, обработанные бактериальными ферментами, имели более открытую микроструктуру и большую пористость. В результате проведенных исследований установлено, что микробная ферментация приводит к глубокому гидролизу белков, входящих в состав мышечных желудков птицы. При благоприятных для каждого вида бактерий температурных режимах ферментации гидролиз происходит более интенсивно.
Мышечный желудок, микробная ферментация, бактериальный концентрат, микроструктура, гидролизат
Короткий адрес: https://sciup.org/147236420
IDR: 147236420 | УДК: 637.5.03 | DOI: 10.14529/food210409
Microbial fermentation of poultry by-products
The aim of this research is to analyze the effect of microbial fermentation of poultry by-products on the accumulation of protein hydrolysis products and changes in the microstructure of hydrolysates. The objects of the study were the gizzards of broilers and hens of the parent flock, which were subjected to microbial fermentation with bacterial concentrates of propionic acid bacteria and bifidobacteria. Fermentation was carried out at temperatures of 30, 35 and 40 °C for 16 hours. To analyze the degree of hydrolysis, the content of amine nitrogen was determined every 4 hours of fermentation. It was noted that under the action of microbial enzymes, a deeper hydrolysis of the protein molecule occurs with an intensive accumulation of amine nitrogen. At the same time, the highest accumulation of amine nitrogen is observed during microbial fermentation of gizzards by propionic acid bacteria at a temperature of 30 °C, and by bifidobacteria at a temperature of 40 °C. In addition, the degree of hydrolysis has been assessed by the accumulation of free amino acids. An increase in the concentration of free amino acids in the control and experimental samples of hydrolysates after 16 hours of fermentation was found. In the hydrolysates of gizzards fermented with propionic acid bacteria and bifidobacteria a significant accumulation of the essential amino acids was observed. The content of both essential and nonessential amino acids in the hydrolysates of broiler chicken by-products was several times higher than in hen’s by-products. The study of the microstructure of hydrolysates using scanning electron microscopy has shown that under the action of microorganisms there have been significant changes in the structure of muscle and collagen fibers, their dissociation into numerous thin fibrils and the formation of a reticular structure in combination with globular proteins and mineral components of serum. Samples treated with bacterial enzymes had a more open microstructure and greater porosity. As a result of the study performed, it was established that the microbial fermentation promotes a deep hydrolysis of proteins in the by-products of chickens and hens. When the temperature conditions of fermentation are suitable for each type of bacteria, hydrolysis occurs more intensively.
Текст научной статьи Микробная ферментация субпродуктов птицы
Актуальность исследований
Во всем мире промышленное птицеводство представляет крупную специализированную отрасль, которая имеет перспективы развития.
В разных странах появляются комплексы различной мощности, оснащенные современными технологическими линиями, где внедряются новые технологии по переработке птицы; расширяется ассортимент выпускаемой продукции [1, 2]. Мясо птицы в настоящее время является наиболее важным источником животного белка во многих странах мира, и эта тенденция подчеркивает важность птицеводческой промышленности и стимулирует ее дальнейший рост [3, 4].
Коллаген, входящий в состав субпродуктов птицы, является потенциальным источником для получения не только животных кормов, но и пищевого белка [9, 10]. Нерациональное использование в полном объеме бе- локсодержащего сырья является причиной существующих экологических проблем предприятий отрасли, а также нехватки продовольственных ресурсов. Расширенное использование коллагенсодержащих продуктов птицеводства в производстве продуктов питания путем изменения их свойств способствует развитию предприятий по переработке птицы и увеличивает их доходность благодаря выпуску продукции с добавленной стоимостью. Ферментативная обработка вторичных продуктов переработки птицы является экологичной альтернативой традиционной кислотной или щелочной модификации сырья [11].
Потенциал субпродуктов птицы отмечен в качестве субстратов для получения белковых гидролизатов с различными функциональными свойствами и биологической активностью [12]. Белки, которые в настоящее время используются в качестве корма для животных, могут быть модифицированы и улучшены для потребления человеком [13]. Гидролиз субпродуктов может происходить разными способами [7]. Ферментативная обработка является более физиологичной, ее можно проводить как с использованием протеолитических ферментов, так и с использованием живых культур бактерий. Микробная ферментация происходит под действием набора ферментов, вырабатываемых микроорганизмами [14]. При выборе способа гидролиза учитываются следующие критерии: простота экстракции и выделение белков; белки предпочтительно должны находиться в неденатуриро-ванном состоянии; отсутствие сопутствующих соединений; высокая растворимость гидролизата в широком диапазоне рН; сбалансированный аминокислотный профиль [13].
Процесс гидролиза белка направлен на разрыв связей между пептидами в полипеп-тидной цепи белка с целью получения низкомолекулярных компонентов и свободных аминокислот, которые способны эффективно усваиваться в организме человека [15]. Биоактивные пептиды образуются при гидролизе белка под действием протеаз, синтезируемых ферментирующими организмами [16]. Биоактивные пептиды, помимо высокой пищевой ценности, обладают антимикробной, антиоксидантной и иммуномодулирующей активностью, способствуют лечению и профилактике значительному перечню заболеваний человека.
Таким образом, целью работы является исследование влияния микробной фермента- ции субпродуктов птицы на накопление продуктов гидролиза белка и изменение микроструктуры гидролизатов.
Материалы и методы
Сырье и материалы
-
– «Пропионикс» – концентрированную микробную массу штамма Propionibacterium freudenreichii subsp. shermanii – КМ 186 с активностью 1010–1011 КОЕ/см3;
-
– бактериальный концентрат Bifidobacterium longum B379M с активностью 1011–1012 КОЕ/см3.
Изготовление опытных образцов гидролизатов
У измельченных субпродуктов определяли физико-химические показатели по стандартным методикам (массовая доля белка, жира, влаги, золы).
Полученные после ферментации гидролизаты фильтровали через мембранные фильтры с диаметром пор 0,45 нм и высушивали методом сублимации. В сухих гидролизатах определяли аминокислотный состав и микроструктуру.
Исследование образцов гидролизатов
Для определения несвязанных аминокислот использовали жидкостный хроматограф Agilent 1260 Infinity LC (США). Для приготовления образцов проводилась жидкостная экстракция. Пять граммов образца гидролизата помещали в эпендорф и добавляли 4 мл 20 % трихлоруксусной кислоты для осаждения белков и пептидов. Объем доводили до 30 мл подкисленным буфером соляной кислоты с pH 2,2 и выдерживали в течение 8 мин, поддерживая гомогенат в условиях охлаждения. Полученную смесь центрифугировали (20 мин, 4 °C, 10000 об/мин) и супернатант пропускали через шприцевой фильтр в виалу. После провели предколоночную дериватиза-цию в автосамплере системы ВЭЖХ с использованием реагентов: ортофталевый альдегид для первичных аминокислот и 9-фторметил-хлорформиат для вторичных аминокислот. Соотношение дериватов к отобранному объему пробы 1:10.
Хроматографическое деление осуществляли на колонке ZORBAX C18 PA, 3,5 мкм, 4,6×150 мм (Agilent, США) в режиме градиентного элюирования в течение 25 мин. Для первичных аминокислот измерения проводили в УФ-детекторе при длине волны λ = 338 нм, для вторичных аминокислот λ = 262 нм. Использовали подвижную фазу А: ацетонитрил: метанол: вода (45:45:10); подвижная фаза B с pH 8,2: Na2HPO4 1,42 г и Na2B4O7 2,1 г pH 8,2. Скорость потока составляла 1 мл/мин. Температура колонки 40 °С. Содержание не- связанных (свободных) аминокислот выражали в мг аминокислот на 100 г жидких гидролизатов.
Каждое измерение проводили трехкратно. Значения вероятности р ≤ 0,05 были взяты для указания статистической значимости. Данные были проанализированы с помощью One-way ANOVA [17].
Результаты исследований и обсуждение
Таблица 1
Примечание: Средние значения в столбце без общего надстрочного индекса имеют достоверные различия (p < 0,05) при анализе с помощью однофакторного дисперсионного анализа и TUKEY-теста.
представленных Abdullah и др. (2016): содержание белка – 17,34 %, содержание жира – 0,76 %, содержание влаги – 78,60 %, зола – 0,97 % [19].
При гидролизе белков мяса образуются полипептиды, которые в дальнейшем могут расщепляться на более мелкие пептиды и свободные аминокислоты [20, 21]. Как отмечено некоторыми авторами, такая деградация может быть вызвана эндогенными и микробными ферментами [22, 23]. El. Adab и др. (2015) показали, что в колбасах, ферментированных S. xylosus и L. plantarum , в результате протеолиза содержание свободных аминокислот увеличилось с 2059,82 мг / кг до 3461,07 мг / кг. Эту разницу в общем накоплении свободных аминокислот авторы связывают с протеолитической активностью микробных ферментов [24]. Таким образом, по накоплению аминного азота и свободных аминокислот в субстрате можно судить об интенсивности гидролиза белка [12].
Для оценки степени гидролиза белка определяют содержание не только структурных, но и свободных аминокислот в субстрате.
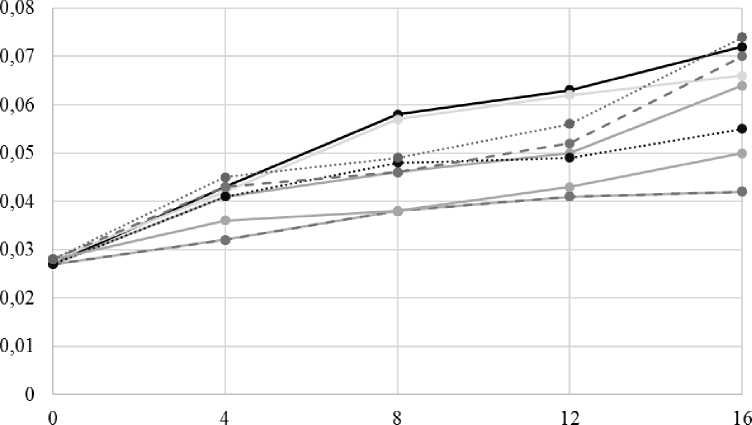
Время ферментации, ч
—•—контр. (30°С)
—•—ферментированный пропионовокислыми бактериями(ЗО°С)
ферментированный бифидобактериями (30°С)
-
- • - контр. (35°С)
ферментированный пропионовокислыми бактериями (35°С)
-
- --• •— ферментированный бифидобактериями (35°С)
-
— •— контр. (40°С)
-
- • - ферментированный пропионовокислыми бактериями (40°С)
-
■ ■■■•■■■ ферментированный бифидобактериями (40°С)
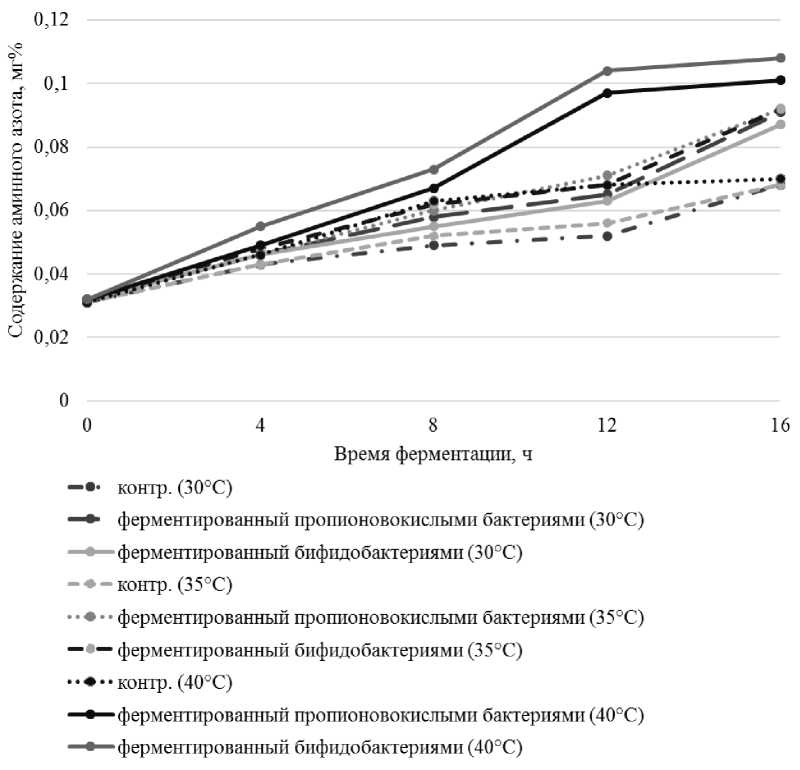
док, содержат большое количество пролина, гидроксипролина и глицина, а также низкие уровни триптофана и тирозина [27].
Таблица 2
Таблица 3
Выводы
Полученные данные могут быть использованы при получении белковых гидролизатов из субпродуктов птицы для дальнейшего включения в состав пищевых продуктов как источника полноценного белка.
Контр. в начале ферментации

Контр. через 16 ч
Ферментированный пропио-

новокислыми бактериями рментации
Ферментированный бифидобактериями


Увеличение ×200
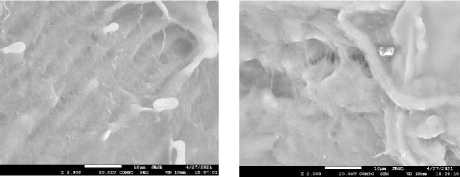
Увеличение ×2000





Увеличение ×5000
Ферментированный
Контр. в начале

Контр. через 16 ч ферментации

Ферментированный пропио- новокислыми бактериями

бифидобактериями
Увеличение ×200


Увеличение ×2000

Увеличение ×5000

Исследование выполнено при финансовой поддержке РФФИ и Челябинской области в рамках научного проекта № 20-416-740002.
Список литературы Микробная ферментация субпродуктов птицы
- Глотова, И.А. Исследование процессов дегидратации биополимерных систем в составе птицепродуктов / И.А. Глотова, А.Н. Литовкин, Е.С. Артемов // Политематический сетевой электронный научный журнал Кубанского государственного аграрного университета. – 2016. – № 121. – С. 801–812.
- Бектасова, С.С. Совершенствование технологии переработки цыплят-бройлеров / С.С. Бектасова, Г.Т. Салкинбаева, Т.М. Турарбек, Ж.М. Атамбаева // Международная научно-практическая конференция, посвященная памяти Василия Матвеевича Горбатова. – 2016. – № 1. – С. 57–59.
- Peña-Saldarriaga, L.M. Quality of chicken fat by-products: Lipid profile and colour proper-ties / L.M. Peña-Saldarriaga, J. Fernández-López, J.A. Pérez-Alvarez // Foods. – 2020. – № 9. – Р. 1046.
- Гущин, В.В. Сырьевая база побочного сырья, получаемого при убое птицы, и ее использование / В.В. Гущин, В.Г. Волик // Птица и птицепродукты. – 2018. – №3. – С. 18–21.
- Денисюк, Е.А. К вопросу безотходной переработки сырья птицеперерабатывающих производств и пути ее интенсификации / Е.А. Денисюк, И.А. Носова, К.Т. Гусейнов, А.С. Ерахтин // Вестник Нижегородской гос. сель-скохоз. академии. – 2013. – Т. 3. – С. 323–328.
- Roiter, L.M. Poultry by-products, reserve for growth of export potential of the industry / L.M. Roiter, L.A. Zazykina, N.A. Eremeeva // IOP Conf. Ser. Earth Environ. Sci. – 2019. – № 341. – 012209.
- Фисинин, В.И. Глубокая переработка вторичных продуктов птицеводства для разных направлений использования / В.И. Фиси-нин, Д.Ю. Исмаилова, В.Г. Волик, В.С. Лукашенко, И.П. Салеева // Сельскохозяйственная биология. – 2017. – Т. 52, № 6. – С. 1105–1115.
- Курчаева, Е.Е. Особенности переработки вторичных ресурсов мясной промышленности с использованием микробной ферментации / Е.Е. Курчаева, В.Л. Пащенко, И.В. Максимов // Технологии и товароведение сельскохозяйственной продукции. – 2018. – № 2(11). – С. 131–138.
- Процан, А.Г. Рациональное использование малоценных частей тушек птицы / А.Г. Процан, А.Н. Нургазезова, Б.К. Асенова // Международная научно-практическая конференция, посвященная памяти Василия Матвеевича Горбатова. – 2015. – № 1. – С. 376–379.
- Волик, В.Г. Современные технологии переработки белоксодержащего сырья / В.Г. Волик // Птицепром. – 2017. – № 1(35). – С. 66.
- Polaštíková, A. Preparation of protein products from collagen-rich poultry tissues / A. Polaštíková, R. Gál, P. Mokrejš, J. Orsavová // Potravin. Slovak J. Food Sci. – 2020. – № 14. – Р. 713–720.
- Гармашов, С.Ю. Выбор условий ферментативного гидролиза коллагенсодержащего сырья / С.Ю. Гармашов // Вестник Крас-ГАУ. – 2018. – № 3. – С. 268–273.
- Boland, M.J. The future supply of ani-mal-derived protein for human consumption / M.J. Boland, A.N. Rae, J.M. Vereijken, M.P.M. Meuwissen, A.R.H. Fischer, M.A.J.S. van Boekel, S.M. Rutherfurd, H. Gruppen, P.J. Moughan, W.H. Hendriks // Trends Food Sci. Technol. – 2013. – № 29. – Р. 62–73.
- Smid, E.J. Microbe-microbe interactions in mixed culture food fermentations / E.J. Smid, C. Lacroix // Curr. Opin. Biotechnol. – 2013. – № 24. – Р. 148–154.
- Saadi, S. Recent advances in food biopeptides: Production, biological functionali-ties and therapeutic applications / S. Saadi, N. Saari, F. Anwar, A.A. Hamid, H. Mohd-Ghazali // Biotechnol. Adv. – 2015. – № 33. – Р. 80–116.
- Chai, K.F.; Hui Voo, A.Y.; Chen, W.N. Bioactive peptides from food fermentation: A comprehensive review of their sources, bioactivi-ties, applications, and future development / K.F. Chai, A.Y. Hui Voo, W.N. Chen // Compr. Rev. Food Sci. Food Saf. – 2020. – № 19. – Р. 3825–3885.
- Assaad, H. Rapid publication-ready MS-Word tables 597 for one-way ANOVA / H. Assaad, L. Zhou, R.J. Carroll, G. Wu // Springer Plus. – 2014. – № 3. – P. 474.
- Zhumanova, G. Prospects of Using Poul-try by-Products in the Technology of Chopped Semi-Finished Products / G. Zhumanova, M. Rebezov, B. Assenova, E. Okuskhanova // Inter-national Journal of Engineering & Technology. – 2018. – № 7(3.34). – P. 495–498.
- Abdullah, FAA. Comparison of qualita-tive and quantitative properties of the wings, necks and offal of chicken broilers from organic and conventional production systems / FAA. Ab-dullah, H. Buchtova // Veterinarni Medicina. – 2016. – № 61. – P. 643–651.
- Lorusso, A. Use of Selected Lactic Acid Bacteria and Quinoa Flour for Manufacturing Novel Yogurt-Like Beverages / A. Lorusso, R. Coda, M. Montemurro, C.G. Rizzello // Foods. – 2018. – № 7. – P. 51.
- Mirzaei Teshnizi, Z. Optimization of the Enzymatic Hydrolysis of Poultry Slaughterhouse Wastes using Alcalase Enzyme for the Prepara-tion of Protein Hydrolysates / Z. Mirzaei Teshnizi, S.M. Robatjazi, J. Mohammadian Mosaabadi // Appl Food Biotechnol. – 2020. – № 7(3). – Р.153–160.
- Hughes, M.C. Characterization of prote-olysis during the ripening of semi-dry fermented sausages/ M.C. Hughes, J.P. Kerry, E.K. Arendt, P.M. Kenneally, P.L.H. McSweeney, E.E. O’Neill // Meat Science. – 2002. – № 62. – P. 205–216.
- AroAro, J.M. The effect of starter cul-tures on proteolytic changes and amino acid con-tent in fermented sausages / J.M. AroAro, P. Nyam-Osor, K. Tsuji, K.I. Shimada, M. Fuku-shima, M. Sekikawa // Food Chemistry. – 2010. – № 119. –Р. 279–285.
- El Adab, S. Microbiological, biochemi-cal and textural characteristics of a Tunisian dry fermented poultry meat sausage inoculated with selected starter cultures / S. El Adab, I. Essid, M. Hassouna // Journal of Food Safety. – 2015. – № 35. – Р. 75–85.
- Sarbon, N.M. Purification and character-ization of antioxidative peptides derived from chicken skin gelatin hydrolysates / N.M. Sarbon, F. Badiia, N.K. Howell // Food Hydrocolloids. – 2018. – № 85. – Р. 311–320.
- Haq, M. Biofunctional properties of bac-terial collagenolytic protease-extracted collagen hydrolysates obtained using catalysts-assisted subcritical water hydrolysis / M. Haq, T.C. Ho, R. Ahmed, A.T. Getachew, Y.-J. Cho, J.-S. Park, B.-S. Chun // Journal of Industrial and Engineer-ing Chemistry. – 2020. – № 81. – Р. 332–339.
- Jayathilakan, K. Utilization of byprod-ucts and waste materials from meat, poultry and fish processing industries: a review / K. Jayathilakan, K. Sultana, K. Radhakrishna, A.S. Bawa // Journal of Food Science and Tech-nology. – 2012. – №49 (3). – P. 278–293.
- Arihara, K. Bioactivities generated from meat proteins by enzymatic hydrolysis and the Maillard reaction / K. Arihara, I. Yokoyamaa, M. Ohatab // Meat Science. – 2021. – №180. – 108561.
- Unsal, M. Fractionation and characteri-zation of edible sheep tail fat / M. Unsal, N. Aktas // Meat Sci. – 2003. – № 63(4). – Р. 235–239.
- Alemán, A. Contribution of Leu and Hyp residues to antioxidant and ACE-inhibitory activities of peptide sequences isolated from squid gelatin hydrolysate / A. Alemán, B. Giménez, E. Pérez-Santin, M. C. Gómez-Guillén, P. Montero // Food Chemistry. – 2011. – № 125. – P. 334–341.
- Akram, A.N. Extraction of collagen-II with pepsin and ultrasound treatment from chick-en sternal cartilage; physicochemical and func-tional properties / A.N. Akram, C. Zhang // Ultrason Sonochem. – 2020. – № 64. – 105053.


