Микрофлора желудочно-кишечного тракта в патогенезе цирроза печени и осложнений портальной гипертензии
Автор: Ковтун А.В., Аникина Е.В., Яковенко А.В., Гиоева И.З., Яковенко Эмилия Прохоровна
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.9, 2014 года.
Бесплатный доступ
В исследование было включено 85 пациентов с циррозом печени (ЦП). Для выявления избыточного бактериального роста (ИБР) в тонкой кишке всем пациентам был выполнен лактулозный водородный дыхательный тест, в диагностике толстокишечного дисбактериоза - микробиологический анализ кала. ИБР и толстокишечный дисбактериоз был выявлен у 82,4% пациентов с одинаковой частотой при алкогольных и вирусных ЦП. Установлено, что дисбактериоз кишечника является фактором риска нарастания тяжести ЦП и печеночной дисфункции, а также развития осложнений портальной гипертензии. Установлено, что формирование синдрома кишечной диспепсии у пациентов ЦП сопряжено с наличием дисбиотических нарушений кишечника.
Алкогольный цирроз печени, вирусный цирроз печени, осложнения портальной гипертензии, биохимические пробы печени, толстокишечный дисбактериоз, синдром избыточного бактериального роста в тонкой кишке
Короткий адрес: https://sciup.org/140188368
IDR: 140188368 | УДК: 616.36-004-092
Текст научной статьи Микрофлора желудочно-кишечного тракта в патогенезе цирроза печени и осложнений портальной гипертензии
ЦП в экономически развитых странах входит в число шести основных причин смерти пациентов от 35 до 60 лет, составляя 14–30 случаев на 100 тыс. населения [4, 6]. В связи с усовершенствованием методов диагностики и лечения продолжительность жизни данных пациентов существенно возросла. В течение последних лет уточняются факторы риска прогрессирования и дестабилизации ЦП, и разрабатываются методы их терапии. Одним из таких факторов является дисбиоз кишечника, который играет роль не только в формировании симптомов диспепсии, но и в прогрессировании ЦП [2, 5, 9].
Основными причинами развития дисбиоза кишечника при ЦП являются замедление гастроинтестинальной моторики, снижение секреции желчи и изменение ее качества, в частности, падение бактерицидности, нарушение гидролиза компонентов пищи с образованием избыточного количества нутриентов для кишечных бактерий [2]. Современные клинические и экспериментальные исследования свидетельствуют о том, что наличие нарушения кишечной микробиоты, транслокация кишечных бактерий и их токсинов в систему портальной вены, контакт липополисахаридов кишечных бактерий с печеночными макрофагами (клетки Купфера), способствуют продукции провоспалительных цитокинов, которые участвуют в формировании некрозов гепатоцитов, воспалительных реакций и прогрессировании фиброза печени [6, 7, 8].
В исследование включено 85 пациентов с ЦП, из них 60 мужчин и 25 женщин в возрасте от 29 до 75 лет (средний возраст 54,3 года). ЦП алкогольной этиологии был выявлен у 66, вирусной – 19 пациентов, из них у 9 (47,4%), ассоциированный с вирусом гепатита В и у 10 (52,6%) – с вирусом гепатита С.
Критерии включения пациентов в исследование: ЦП алкогольной и вирусной этиологии; воздержание от приема алкоголя в течение 6 и более месяцев до включения в исследование; информированное согласие на участие в исследовании. Из исследования исключались больные с наличием ЦП другой этиологии; самостоятельных заболеваний кишечника, заболеваний других органов и систем, которые могут сопровождаться моторно-секреторными нарушениями желудочно-кишечного тракта с развитием диспепсических нарушений и абдоминального болевого синдрома, опухолевых процессов любой локализации.
Диагноз ЦП устанавливался на основании данных анамнеза, результатов физикального и лабораторноинструментального и, в ряде случаев, гистологического исследования биоптатов печени. Вирусная этиология ЦП была подтверждена наличием сывороточных маркеров вирусов гепатита В, С с использованием метода ПЦР. Для выявления портальной гипертензии использовались ультразвуковые и эндоскопические исследования, а также компьютерная томография органов брюшной полости.

Степень тяжести (компенсации) ЦП оценивалась по шкале Чайльда-Пью [14].
Лабораторные исследования включали клинический анализ крови с акцентом на наличие анемии, лейкопении и тромбоцитопении и комплекс биохимических тестов, позволяющих оценить снижение синтетической функции гепатоцитов (гипоальбуминемия), наличие активности процесса (повышение уровня АЛТ, АСТ), выявить холестаз (повышение уровня щелочной фосфатазы (ЩФ) и гаммаглютамилтрасферазы (ГГТП), и иммунологические (гипергаммаглобулинемия) нарушения.
При анализе жалоб и физикальном исследовании помимо синдромов, характерных для ЦП, оценивалось также наличие клинических проявлений, связанных с нарушением функций кишечника. По аналогии с Римскими критериями III, применяемыми для классификации функциональных нарушений желудочно – кишечного тракта, при наличии у пациентов симптомов, характерных для синдрома раздраженной кишки (СРК), использовался термин «СРК – подобные нарушения» [13]. При этом в зависимости от характера нарушения стула выделялись СРК – подобные нарушения с запором, диареей и смешанного типа. Болевой абдоминальный синдром и синдром метеоризма, если они не сочетались с изменениями частоты стула и консистенции кала, анализировались самостоятельно. Отдельно выделялся также синдром функциональной желудочной диспепсии: эпигастральные боли или постпрандиальный дистресс-синдром [12]. В ходе исследования оценивались частота выявления клинических проявлений в зависимости от состояния кишечного биоценоза.
Для выявления ИБР в тонкой кишке всем пациентам был выполнен лактулозный водородный дыхательный тест с использованием анализатора концентрации ионов водорода в выдыхаемом воздухе EC60 Gastrolyzer (Bedfont Tech. Inst., Великобритания). ИБР в тонкой кишке считался доказанным, если концентрация ионов водорода в выдыхаемом воздухе при базальном исследовании или в двух последовательных измерениях после приема лактулозы превышал 20 ppm [15]. Бактериологическое исследование кала проводилось по общепринятой методике, а интерпретация полученных результатов – в соответствии с Российским отраслевым стандартом [3]. При оценке степени выраженности нарушений состава микрофлоры толстой кишки использовалась классификация В.М. Бондаренко [1]. При анализе посевов кала основное внимание уделяли выявлению условно-патогенной микрофлоры, наличие которой, несомненно, свидетельствует о толстокишечном дисбактериозе. При статистической обработке полученных результатов для анализа количественных признаков использовался критерий Стьюдента, качественных – χ 2.
С учетом клинико–лабораторных показателей из 85 пациентов, включенных в исследование, у 23 (27,0%) был установлен ЦП класс А, у 39 (45,3%) – В и у 23 (26,7%) – С. Нарушение нормального состава кишечной микро- флоры было выявлено у 70 (82,4%) больных, из них у 57 (86,3%) из 66 пациентов ЦП алкогольной и у 13 (68,4%) из 19 – вирусной этиологии. Из 70 больных с наличием кишечного дисбиоза у 23 (32,9%) был выявлен толстокишечный дисбактериоз, у 47 (67,1%) имел место ИБР в тонкой кишке, из них у 13 (18,6%) – изолированный и у 34 (48,6%) – сочетанные дисбиотические расстройства. Характер нарушений кишечной микрофлоры у пациентов алкогольным и вирусным ЦП существенно не различался.
Состояние кишечного микробиоценоза в зависимости от степени компенсации ЦП и наличия осложнений портальной гипертензии представлены в таблице 1. Результаты исследования свидетельствуют о том, что по мере нарастания тяжести ЦП увеличивается количество пациентов с сочетанными нарушениями кишечной микрофлоры. Так, у пациентов ЦП класса В и С выявляли преимущественно сочетанный кишечный дисбиоз, при этом при осложнениях портальной гипертензии частота его выявления существенно возрастала.
При анализе показателей клинических и биохимических анализов крови были выявлены анемия – у 20 (23,5%), лейкопения – у 19 (22,4%), тромбоцитопения – у 35 (41,2%), повышение уровня сывороточных трансаминаз – у 78 (91,8%), билирубина с преобладанием коньюги-рованной фракции у 42 (49,4%), ЩФ – у 21 (24,7%), ГГТП – 32 (37,6%), гаммаглобулинов – у 29 (34,1%), креатинина – у 11 (12,9%), гипоальбуминемия – у 43 (50,6%) исследу-
Табл. 1. Состояние кишечного биоценоза в зависимости от степени компенсации ЦП и наличия осложнений ПГ
|
Признаки (n - количество пациентов) |
Состояние кишечной микробиоты |
|||||
|
Норма n - 15 |
ИБР в тонкой кишке и толстокишечный дисбактериоз n - 47 |
Изолированный толстокишечный дисбактериоз n - 23 |
||||
|
n |
% |
n |
% |
n |
% |
|
|
Номер графы |
1 |
2 |
3 |
|||
|
ЦП класс А N – 23 |
132 |
86,7 |
1 1,3 |
2,1 |
92 |
39,1 |
|
ЦП класс В n – 39 |
1 2,3 |
6,7 |
241 |
51,1 |
141 |
60,9 |
|
ЦП класс С n – 23 |
12 |
6,7 |
22 1,3 |
46,8 |
02 |
0 |
|
ЦП алкогольный n – 66 |
9 |
60 |
38 |
80,9 |
19 |
82,6 |
|
ЦП вирусный n – 19 |
6 |
40 |
9 |
19,1 |
4 |
17,4 |
|
Печеночная энцефалопатия 2–3 степень n – 53 |
32 |
20 |
381,3 |
80,9 |
122 |
52,2 |
|
Асцит n – 44 |
52 |
33,3 |
301 |
63,8 |
9 |
39,1 |
|
Асцит перитонит n – 7 |
0 |
0 |
7 |
14,9 |
0 |
0 |
|
Гепаторенальный синдром n – 10 |
0 |
0 |
9 |
19,1 |
1 |
4,3 |
Примечание: данной и последующих таблицах верхний индекс обозначает номера граф, с показателями которых имеются статистически достоверные различия.
емых пациентов. Показатели клинического и биохимического анализа крови в зависимости от состава кишечной микрофлоры представлены в таблице 2.
Полученные данные свидетельствуют о том, что у пациентов с наличием ИБР в тонкой кишке имели место наиболее выраженные нарушения в клиническом анализе крови и биохимических пробах печени. Так, признаки гиперспленизма, повышение уровня трансаминаз в сочетании с гипербилирубинемией, синдром холестаза и гипергаммаглобулинемия значительно чаще были выявлены у пациентов с наличием ИБР в тонкой кишке.
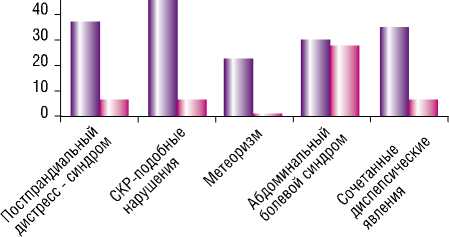
Симптомы желудной и кишечной диспепсии были обнаружены у 67 (78,8%) из 85 наблюдаемых пациентов, из них у 52 (78,8%) из 66 алкогольной и у 15 (78,9%) из 19 вирусной этиологии (р > 0,05). Из 67 больных у 26 (30,6%) имели место проявления функциональной диспепсии по типу постпрандиального дистресс – синдрома, у 32 (37,6%) – СРК-подобные нарушения, из них у 12 (14,1%) –с диареей, у 13 (15,3%) – с запором и у 7 (8,2%) – смешанного типа. Метеоризм и абдоминальный болевой синдром без нарушения частоты стула и формы кала выявлялены у 16 (14,1%) и у 24 (28,2%) пациентов соответственно, у 25(25,9%) – отмечались сочетанные проявления диспепсических явлений (рис. 1).
Результаты исследования показали, что клинические проявления желудочной и кишечной диспепсии значительно чаще представлены у пациентов с нарушением нормальной кишечной микрофлоры, и только частота обнаружения абдоминального болевого синдрома оказалась идентичной у пациентов с наличием и отсутствием кишечного дисбиоза. При этом следует отметить, что при наличии ИБР в тонкой кишке в клинической картине преобладали СРК-подобные нарушения с диареей и метеоризм, в то время как при толстокишечном дисбиозе обнаруживали СРК-подобные нарушения различных типов с одинаковой частотой.
Установлена высокая частота выявления нарушений кишечного биоценоза у пациентов ЦП (82,4%) и ее связь со степенью компенсации заболевания и наличием осложнений портальной гипертензии. У наблюдаемых пациентов преобладали сочетанные нарушения кишечной микрофлоры, включающие наличие ИБР в тонкой кишке и толстокишечный дисбактериоз. По мере нарастания тяжести ЦП увеличивалась частота их выявления. Из 70 пациентов ЦП с наличием кишечного дисбиоза у 47 (67,1%) выявлены сочетанные нарушения кишечной микрофлоры и у 23 (32,9%) – толстокишечный дисбактериоз (р < 0,001). Частота выявления ИБР в тонкой кишке в проведенном нами исследовании совпадает с литературными данными [8, 9, 10, 11]. В то же время имеются лишь единичные работы, в которых были представлены результаты комплексного исследования тонкокишечной и толстокишечной микрофлоры у пациентов ЦП и связь сочетанных дисбиотических нарушений со степенью компенсации и клинико-лаботаторными проявлениями заболевания [2].
Табл. 2. Результаты лабораторных исследований в зависимости от состояния кишечного биоценоза
|
Показатели (n–количество пациентов) |
Состояние кишечного биоценоза |
|||||
|
Норма n – 15 |
ИБР в тонкой кишке и толстокишечный дисбактериоз n – 47 |
Изолированный толстокишечный дисбактериоз n – 23 |
||||
|
n |
% |
n |
% |
n |
% |
|
|
Номер графы |
1 |
2 |
3 |
|||
|
Анемия n – 20 |
02 |
0 |
17 1,3 |
36,2 |
32 |
13,0 |
|
Лейкопения n – 19 |
12 |
6,7 |
16 1,3 |
34,0 |
2 2 |
8,7 |
|
Тромбоцитопения n– 35 |
2 2 |
13,3 |
27 1,3 |
57,4 |
6 2 |
26,1 |
|
Повышение уровня трансаминаз n – 78 |
8 2,3 |
53,3 |
471 |
100 |
231 |
100 |
|
Гипербилирубинемия n – 42 |
0 2 |
0 |
35 1,3 |
74,5 |
7 2 |
30,4 |
|
Повышение уровня ЩФ n – 21 |
02 |
0 |
191,3 |
40,4 |
22 |
8,7 |
|
Повышение уровня ГГТП n – 32 |
22 |
13,3 |
251,3 |
53,2 |
52 |
21,7 |
|
Гипергаммаглобули-немия n – 29 |
12 |
6,7 |
231,3 |
48,9 |
52 |
21,7 |
|
Гиперкреатинине-мия n – 11 |
02 |
0 |
11 1,3 |
23,4 |
02 |
0 |
|
Гипоальбуминемия n – 43 |
32 |
20 |
311,3 |
65,95 |
92 |
39,1 |
I ■ Нормальная микрофлора
I ■ Наличие дисбиозакишечника
Рис. 1. Диспепсические нарушения у больных ЦП в зависимости от состояния кишечного биоценоза
Полученные нами результаты свидетельствуют, что у пациентов с сочетанными нарушениями кишечного дисбиоза преобладали больные ЦП класса В и С (51,1% и 46,8%, соответственно) с наличием осложнений портальной гипертензии (печеночная энцефалопатия, асцит-перитонит и гепаторенальный синдром). У данных пациентов значительно чаще выявляли гематологические нарушения, свидетельствующие о развитии гиперспле-низма, биохимические признаки печеночно-клеточной недостаточности, холестаза, гипергаммаглобулинемия,
свидетельствующая о включении в патогенез прогрессирования заболевания аутоиммунных реакций, а также цитолитический синдром с гипербилирубинемией. Полученные данные подтверждают, что сочетанное нарушение кишечной микрофлоры является несомненным фактором, утяжеляющим течение ЦП и способствующим развитию основных осложнений портальной гипертензии.
Подтверждена роль кишечного дисбиоза в формировании симптомов желудочной и кишечной диспепсии у пациентов ЦП. Полученные результаты позволяют считать, что наличие у пациентов ЦП диспепсических нарушений с большой долей вероятности может служить диагностическим тестом кишечного дисбиоза, что необходимо учитывать при разработке тактики их ведения.
Заключение
При ЦП нарушения кишечного микробиоценоза были выявлены у 82, 4% пациентов с одинаковой частотой при вирусной и алкогольной этиологии. У большинства из них имелось сочетанное нарушение микрофлоры тонкой и толстой кишки. У пациентов с сочетанными нарушениями кишечной микрофлоры тяжесть ЦП и частота развития осложнений ПГ существенно возрастали. У пациентов ЦП с наличием сочетанного кишечного дисбиоза чаще выявляли гематологические нарушения, биохимические признаки высокой активности заболевания, синтетической недостаточности, внутрипеченочного холестаза и включения аутоиммунных реакций.
Список литературы Микрофлора желудочно-кишечного тракта в патогенезе цирроза печени и осложнений портальной гипертензии
- Бондаренко В.М. Дисбактериозы желудочно-кишечного тракта/Бондаренко В.М. Боев Б.В., Лыкова Е.А., Воробьёв А.А.//Рос. журн. гастроэнтерол. гепатол. колопроктол. -1998. -Т. 8, № 1. -С. 66-70.
- Жданов К.В. Особенности микроэкологии кишечника у больных циррозом печени/Жданов К. В., Захаренко С. М., Гусев Д. А.//Лечение и профилактика. -2012. -Т. 3 № 4 -C. 36-49.
- Приказ Министерства здравоохранения Российской федерации. № 231 от 9 июня 2003 года утвержден отраслевой стандарт. Протокол ведения больных. Дисбактериоз кишечника (ОСТ 91500.11.0004-2003).
- Шерлок Ш. Заболевания печени и желчных путей. Практическое руководство: Пер. с англ. Под редакцией З.Г. Апросиной, И.А. Мухина./Шерлок Ш., Дули Д. -М.: Гэотар медицина; 1999. -864 с.
- Яковенко Э.П. Нарушение состава кишечной микрофлоры в механизмах формирования функциональных расстройств кишечника у больных циррозом печени/Яковенко Э.П., Каграманова А.В., Яковенко А. В. и др.//Тер. архив. -2012. № 2. -С. 41-45.
- Яковенко Э.П. Цирроз печени, клинико-патогенетические аспекты./Яковенко Э.П., Яковенко А.В.//Фарматека. -2012. -№ 13 -С. 32-36.
- Albillos A. Serum lipopolysaccharide-binding protein prediction of severe bacterial infection in cirrhotic patients with ascites/Albillos A., De-la-Hera A., Alvarez-Mon M.//The Lancet. -2004. -№ 363 -P. 1608-1610.
- Alexander J. The process of microbial translocation/Alexander J. W., Boyce S. T., Babcock G. F. et al.//Ann Surg. -1990. -№ 212 -P. 496-512.
- Almeida J. Gut flora and bacterial translocation in chronic liver disease/Almeida J., Galhenage S.Yu J. et al.//World J Gastroenterol. -2006. -Vol. 12, № 10 -P. 1493-1502.
- Bares J. Small intestinal bacterial overgrowth syndrome/Bares J., Cvranv J., Kohoutova D. et al.//World J. Gastroenterol. -2010. -№ 16. -P. 2978-2990.
- Bauer T.M. Small intestinal bacterial overgrowth in human cirrhosis is associated with systemic endotoxaemia/Bauer T.M., Schwacha H., Steinbruckner B., Brinkmann F.E., Ditzen A.K., Aponte J.J., Pelz K., Berger D., Kist M., Blum H.E.//Am J Gastroenterol -2002. -№ 97 -P. 2364-2370.
- Drossman D.A. The Functional Gastrointestinal Disorders and the Rome III Process/Drossman D. A.//Gastroenterology -2006. -Vol. 130, N 5 -P. 1377-1390.
- Farrokhyar F. Functional Gastrointestinal Disorders and Mood Disorders in Patients with Inactive Inflammatory Bowel Disease: Prevalence and Impact on Health/Farrokhyar F., Marshall J.K., Easterbrook B. et al.//Inflamm Bowel Dis. -2006. -Vol.12, № 1 -P. 38-45.
- Pugh R.N. Transection of the esophagus for bleeding esophageal varices/Pugh R. N., Murray-Lyon I.M., Dawson J.L., et al.//BrJSurg. -1973. -Vol. 60, № 8 -P. 646-649.
- Walters B. Detection of bacterial overgrowth in IBS using the lactulose H2 breath test: comparison with 14C-Dxylose and healthy controls/Walters B., Vanner S.J.//Am J Gastroenterol. -2005. -№ 100 -P. 1566-1570.


