Множественная фиброаденома молочной железы в сочетании с аномалией развития внутренних половых органов у девочки-подростка (клинический случай)
Автор: Федюшина А.О., Трушина О.В., Хворостухина Н.Ф., Новичков Д.А., Покалицина Ю.А., Суханов С.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Акушерство и гинекология
Статья в выпуске: 1 т.17, 2021 года.
Бесплатный доступ
Фиброаденома — наиболее частое доброкачественное новообразование молочных желез. В большинстве случаев опухоль встречается в виде единичных узлов, диаметр которых не превышает Зсм. Описан клинический случай множественной фиброаденомы молочной железы больших размеров у девочки-подростка в сочетании с аномалией развития внутренних половых органов. Представленное наблюдение акцентируют внимание на важном аспекте ювенильной маммологии и показывает целесообразность динамического наблюдения за ростом и развитием молочных желез в детском и подростковом возрастах, что позволит не допустить случаев поздней диагностики иногда столь очевидных заболеваний.
Фиброаденома, подростки, молочные железы, дети, аномалия развития половых органов
Короткий адрес: https://sciup.org/149134973
IDR: 149134973 | УДК: 618.19
Multiple fibroadeno-ma of the breast in combination with abnormal development of internal genitalia in a teenage girl (clinical case)
Fibroadenoma is the most common benign neoplasm of the mammary glands. In most cases, the tumor occurs in the form of single nodes, the diameter of which does not exceed 3 cm. A clinical case of multiple large breast fibroadenoma in a teenage girl, combined with an abnormality in the development of internal genitalia, is presented. The presented observation focuses on an important aspect of juvenile mammology and shows the feasibility of dynamic monitoring of the growth and development of mammary glands in childhood and adolescence adolescence, which will prevent cases of late diagnosis of such obvious diseases.
Текст научной статьи Множественная фиброаденома молочной железы в сочетании с аномалией развития внутренних половых органов у девочки-подростка (клинический случай)
возрастах. Многие аспекты проблемы ювенильной маммологии — от терминологии до диагностического и лечебного алгоритмов — остаются предметом активных дискуссий [1]. М. Л. Травиной и соавт. предложена клинико-морфологическая классификационная система, в которой выделены четыре варианта оценки состояния молочных желез у детей и подрост- ков [2]. В первую группу авторы включили физиологические состояния молочных желез, соответствующие возрастным нормам развития. Вторая группа — это временные отклонения от нормального развития молочных желез, которые носят преходящий характер и не провоцируют стойких патологических изменений в маммарной ткани. В третью группу внесены патологические процессы, сопровождаемые структурными изменениями в маммарной ткани — фибрознокистозная мастопатия, новообразования, масталгия и мастодиния, воспалительное поражение, внутрипротоковая патология. Четвертая группа — это пороки развития (дисморфии) молочных желез.
В структуре доброкачественных новообразований молочных желез, в том числе в подростковом возрасте, особое место занимает фиброаденома [3, 4]. Фиброаденома молочных желез (ФМЖ) представляет собой доброкачественную опухоль из стромальной и эпителиальной (протоковой) тканей. Этиология ФМЖ до настоящего времени остается предметом научных дискуссий. Ключевую роль отводят влиянию половых стероидных гормонов, в первую очередь гиперэстрогенной стимуляции.
Морфологически ФМЖ не имеют истинной капсулы, представлены пролиферацией эпителиальных и стромальных элементов терминальной протоково-дольчатой единицы, гистологически различаются по пролиферации пери- или интраканаликулярной стром. Размер узлов ФМЖ обычно не превышает 3 см. В случае если размер узлов превышает 5 см (или имеют массу более 500,0 граммов, или замещают 80% ткани молочной железы), то используют термин «гигантские» [5]. В то же время G. Doğan и соавт. представлены случаи спонтанного регресса новообразований в подростковом возрасте на 10-15% наблюдений [6].
Наряду с классическими ФМЖ предложено выделять гистологический подтип — ювенильную (клеточную) фиброаденому, характеризующуюся быстрым ростом и способностью достигать больших размеров. Например, S. Islam и соавт. представили клиническое наблюдение ювенильной ФМЖ у 16-летней девочки с размерами узла 28×25 см [7]. Морфологическими особенностями ювенильной ФМЖ являются более выраженная, чем у классической фиброаденомы, эпителиальная и стромальная гиперплазия с протоковым, дольчатым или комбинированным протоково-дольчатым рисунком. Ювенильные формы составляют 0,5-2% всех ФМЖ у подростков и могут демонстрировать локальную агрессию, вызывая фиброзный ответ в прилегающих тканях, что приводит к физическому и психологическому дискомфорту и может стать причиной формирования нарушения осанки [7, 8]. N. Rafeek и соавт. сообщили об уникальном случае билатеральных гигантских ювенильных фиброаденом — общая масса удаленных опухолей (21 кг) составила практически половину собственного веса 13-летней пациентки [9]. Чаще всего ФМЖ представлена одиночным узлом и пальпируется в виде эластичного безболезненного образования овальной формы с четкими контурами. Литературные данные указывают, что верхний наружный квадрант молочных желез — это наиболее распространенная локализация ФМЖ, при этом отсутствуют значимые различия в частоте поражения правой и левой молочных желез [5, 8]. В 10-25% случаев наблюдается билатеральное поражение молочных желез [10]. Важными компонентами клинической оценки состояния молочных желез является их визуальный осмотр и пальпаторное исследование, которое должно быть неотъемлемой частью физикального обследования девочек любого возраста [3, 8].
Основным методом визуализации патологии молочных желез у детей и подростков является ультразвуковое исследование, которое демонстрирует высокую информативность и безопасность при многократном применении [11]. Цветовое допплеровское картирование выявляет различную по степени выраженности интранодозную васкуляризацию. Стандартом для описания и разделения поражений молочных желез на категории, коррелирующие с вероятностью злокачественного новообразования, принята лексика системы отчетов и данных визуализации молочной железы — Breast Imaging Reporting and Data Systemlexicon (BI-RADS). Однако в настоящее время валидность этой системы у подростков остается предметом дискуссий [12].
Согласно позиции большинства авторов, опубликованные стратегии ведения юных пациенток с новообразованиями молочных желез демонстрируют сходство с алгоритмом ведения категории 3 BI-RADS для взрослых, но различаются с точки зрения включения размера опухоли в показания для хирургического лечения [13]. Следует отметить, что размеры узлов ФМЖ иногда затрудняют их клиническую и сонографическую оценку как дискретного образования. Повысить информативность дифференциации доброкачественного и злокачественного характера образований может использование соноэластографии, позволяющей не только визуализировать, но и измерить эластичности тканей опухоли.
Магнитно-резонансную томографию чаще применяют для уточнения результатов, полученных при ультрасонографии, дифференциации сосудистых поражений от нормальной ткани молочной железы, определения многодольчатых поражений [1, 14]. Вместе с тем возрастные особенности молочных желез, характеризующиеся преобладанием фиброгландулярной ткани по отношению к жировой, и потенциальное неблагоприятное действие на чувствительную маммарную ткань ионизирующего излучения ограничивают использование у детей и подростков маммографии — стандартного скринингового метода диагностики патологии молочных желез у взрослых [8, 14]. Компьютерная томография также не нашла широкого применения в педиатрической практике для первичной оценки новообразований молочных желез, но патологические изменения в маммарной ткани могут быть случайно обнаружены на томограммах, полученных по другим показаниям.
Важным моментом остается и тот факт, что схожие с фиброаденомами вариабельные пальпаторные и ультрасонографически выявляемые признаки имеют и другие новообразования молочных желез. Это, в свою очередь, ограничивает возможности до-морфологической верификации опухоли.
Подходы к тактике ведения девочек с новообразованиями молочных желез остаются проблематичными. В научной литературе представлена ограниченная информация о критериях мониторинга и показаниях к хирургическому вмешательству [8, 13]. Существует мнение о том, что с учетом редкости злокачественных морфологических вариантов новообразований молочных желез у юных пациенток, потенциальной хирургической травмы, наносимой развивающейся маммарной ткани и указаниям о возможном спонтанном регрессе опухолей, при типичных клинических и ультрасонографических признаках ФМЖ целесообразно выбрать тактику динамическо- го наблюдения [15], с одной стороны. С другой стороны, гарантированное исключение злокачественных форм до морфологической верификации невозможно. Кроме того, наличие патологии молочных желез — это тревожное событие как для юной пациентки, так и для семьи, провоцирующее психологические проблемы [16, 17]. Цитологическое исследование материала, полученного при тонкоигольной аспирации или биопсии стержневой иглой, может дать дополнительную информацию для характеристики образования (доброкачественного или злокачественного), но данный метод существенно уступает в информативности эксцизионной биопсии [18]. Наряду с этим, с точки зрения большинства исследователей, своевременно выполненное хирургическое вмешательство позволяет добиться более благоприятного эстетического эффекта и снижает психосоциальную коморбидность, тогда как наличие гигантских или многоузловых опухолей может потребовать проведения мастэктомии и последующей реконструктивно-пластической коррекции [4, 19].
Описание клинического случая . На публикацию представляемых данных из истории болезни получено добровольное информированное согласие пациентки.
Пациентка в возрасте 16 лет обратилась в клинику в плановом порядке с жалобами на случайно выявленное при самообследовании безболезненное уплотнение в левой молочной железе, которое за четыре месяца увеличилось в размере. Девочка-подросток с неотягощенным перинатальным анамнезом. В раннем детстве перенесла ветряную оспу, редкие респираторные заболевания. Страдает дискинезией желчевыводящих путей на фоне аномалии развития желчного пузыря и миопией слабой степени. Наследственность по патологии органов репродуктивной системы, эндокринопатиям, онкологическим заболеваниям по линии матери и отца не отягощена. По данным гинекологического анамнеза установлено физиологическое течение пубертата. В течение года после менархе (в возрасте 11 лет) установился менструальный цикл продолжительностью от 26 до 29 дней. Менструации до семи дней, субъективно оцениваемые как умеренные и безболезненные. Масталгию не отмечает. До настоящего обращения инструментального обследования органов репродуктивной системы не проходила. Состояние пациентки при поступлении в клинику удовлетворительное. По результатам соматоскопии отмечено среднее гармоничное физическое развитие (рост 168 см; SDS роста +0,76; масса тела 51 кг; ИМТ 18,11 кг/м2; SDS ИМТ –0,56). При осмотре на коже спины и верхних конечностей выявлены множественные пигментные невусы без визуальных признаков активности. Молочные железы визуально с умеренно выраженной асимметрией (sin>dex), кожа не изменена, но с более выраженной венозной сетью слева (рис. 1).
В правой молочной железе объемные образования не пальпируются. В левой молочной железе при пальпации обнаружено несколько плотных безболезненных образований округлой формы с четкими контурами, не спаянных с окружающими тканями — в верхневнутреннем квадранте размерами 5,0×4,0 см и 2,0×3,0 см, в верхненаружном квадранте — 5,0×3,0 см, в нижненаружном квадранте — 5,0×6,0 см и 7,0×4,0 см. С обеих сторон сосково-ареолярные комплексы не изменены, выделений из сосков нет. Надключичные, подключичные и ак-силлярные лимфатические узлы не определяются.
По данным наружного гинекологического осмотра: наружные половые органы изосексуального типа; большие половые губы сформированы правильно, не прикрывают малые половые губы, которые гипертрофированы, асимметричны (dex>sin); клитор нормальных размеров, топография наружного отверстия уретры не изменена; hymen типичной анатомической формы, имеет одно отверстие; слизистая преддверия влагалища розовая, без патологических элементов; выделения из влагалища физиологические.
Пациентке проведено лабораторно-инструментальное обследование в соответствии с действующими стандартами. По данным ультразвукового исследования (аппарат «Samsung Medison Accuvix XG», датчик 7,5 Мгц): в правой молочной железе эхоплотность железисто-стромального комплекса не изменена, млечные протоки диаметром 1,5 мм. В левой молочной железе лоцированы семь гипо-эхогенных образований с четкими контурами диаметром от 2,3 см до 5,7 см и одно многоузловое образование общим размером 7,9×3,2 см, содержащее гиперэхогенные включения диаметром 0,2– 0,3 см и анэхогенные участки диаметром до 0,4 см (рис. 2). При цветовом допплеровском картировании в образованиях зарегистрированы единичные сигналы по периферии.
При проведении трансабдоминального ультразвукового исследования визуализированы два тела мат-
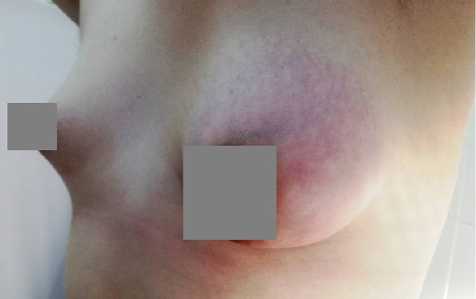
Рис. 1. Асимметрия молочных желез при первичном визуальном осмотре пациентки
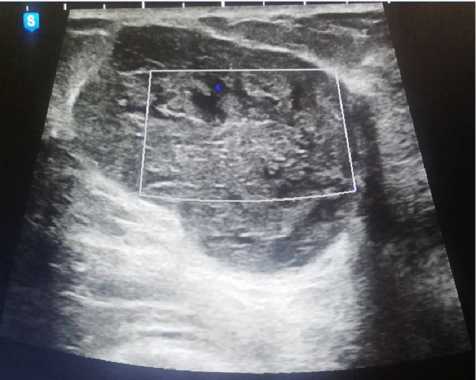
Рис. 2. Структура самого крупного очагового образования в левой молочной железе пациентки (ультрасонография, «Samsung Medison Accuvix XG»)
ки размерами 4,1×2,3×3,4 см и 4,2×2,3×3,8 см и одна шейка матки; структура миометрия не изменена, два М-эхо 0,6 см и 0,7 см на 8-й день менструального цикла; яичники в типичном месте, объем левого 6,7 см3, объем правого 7,1 см3, структура типичная. Вариант впервые диагностированного порока развития внутренних гениталий (двурогая матка) был уточнен данными магнитно-резонансной томографии, проведенной на 8-й день менструального цикла. На серии МР-томограмм, взвешенных по Т1 и Т2 в трех взаимно перпендикулярных плоскостях с подавлением МР-сигнала от жировой ткани с применением DWI ИП установлено: матка расположена в anteflexio , имеет два отклоненных по вертикальной оси рога: правый 5,4×3,0×2,7 см, левый 5,1×2,6×3,1 см, грушевидной формы, с четкими, ровными контурами, сохраненной зональной архитектоникой стенок, однородной структурой миометрия, эндометрий толщиной в правом роге до 1,1 см и до 0,8 см в левом роге, имеет однородный МР-сигнал, контуры на границе с миометрием четкие, ровные; шейка матки размерами 3,6×2,8 см, цервикальный канал не расширен, перегородок не определяется, толщина эндоцервикса 0,4см. Яичники: правый 7,6см3, левый 7,7см3 обычной формы, положения и структуры. Таким образом, получено подтверждение выявленного порока развития внутренних половых органов без нарушения оттока менструальной крови — двурогой матки.
По результатам лабораторного обследования клинически значимых отклонений не выявлено. Клинический анализ крови: WBC 6,89*109/л, RBC 4,05*1012/л, HGB 118 г/л, Ht 37,3%, MCH 29,1 пг, МСНС 316,0 г/л, MCV 92,2 фл, PLT 306 х 109/л, сегментоядерные нейтрофилы 58%, палочкоядерные нейтрофилы 1%, эозинофилы 2%, лимфоциты 34%, моноциты 5%, СОЭ 9 мм/час. Показатели биохимического анализа крови в пределах возрастной нормы: C-реактивный белок менее 6,0 мг/л, общий белок 76,8 г/л, креатинин 82,0 мкмоль/л, мочевина 4,16 ммоль/л, билирубин общий 10,8 мкмоль/л, холестерин 4,13 ммоль/л, HDL 1,3 ммоль/л, LDL 1,74 ммоль/л, триглицериды 1,32 ммоль/л, железо 31,7 мкмоль/л, ферритин 33,3 нг/мл, ЛДГ 342,0 U/l, щелочная фосфотаза 166,0 U/l, АлТ 11,1 U/l, АсТ 18,2 U/l, фосфор неорганический 1,5 ммоль/л. При исследовании системы гемостаза клинически значимых отклонений не выявлено: время свертывания крови по Ли — Уайту 11 мин 06 сек, протромбиновое время 14,7 сек, тромбиновое время 17,9 сек, МНО 1,02, фибринолитическая активность 4 мин 45 сек, РФМК 6,0 мг/%, фибриноген 2,95 г/л, АЧТВ 37,6 сек. Не выявлено повышения уровня фетальных
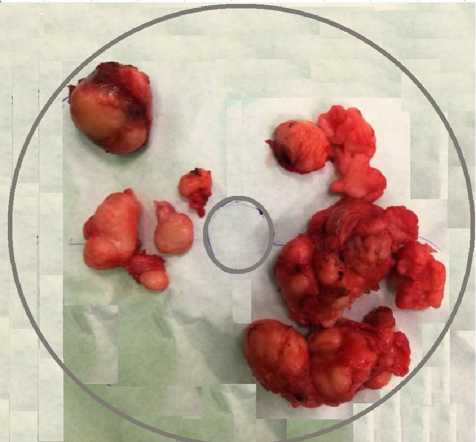
Рис. 3. Множественные узлы фиброаденомы молочной железы (макропрепарат)
онкомаркеров в сыворотке крови (АФП 0,01 МЕ/л; в—ХГЧ 0,01 МЕ/л). При исследовании уровня гормонов в сыворотке крови диагностирован эутиреоз (Т4 св. 12,6 пмоль/л, ТТГ 2,8 мкЕД/мл), функциональная гиперпролактинемия (750 мМЕ/л), нормогонадотро-пинемия и нормоэстрогенемия при исследовании на 5-й день менструального цикла (ФСГ 7,13 мМЕ/мл, ЛГ 5,3 мМЕ/мл, эстрадиол 76,0 пг/мл), нормальный уровень 17-ОН прогестерона (1,57 нг/мл), ДГЭА-С: (2,9 мкмоль/л), общего тестостерона (3,0 нмоль/л), кортизола (7:00 791,0 нмоль/л; 23:00114,0 нмоль/л) и АКТГ (37,7 пг/мл).
Учитывая наличие множественного очагового поражения левой молочной железы у девочки-подростка, в плановом порядке проведено оперативное лечение — энуклеация множественных узловых новообразований левой молочной железы из полуовального разреза, окаймляющего наружный край ареолы. Операция выполнена под интраоперационным ультразвуковым контролем, с интраоперационным экспресс-цитологическим исследованием удаленных тканей. Общая масса удаленных узлов составила 580 г (рис. 3).
Макроскопически узлы имели четкие контуры, на разрезе представлены тканью бледно-сероватого цвета, слегка дольчатого строения, местами с кистозными полостями диаметром 0,2–0,3 см, в одном из узлов — с мелкими кровоизлияниями (рис. 4).
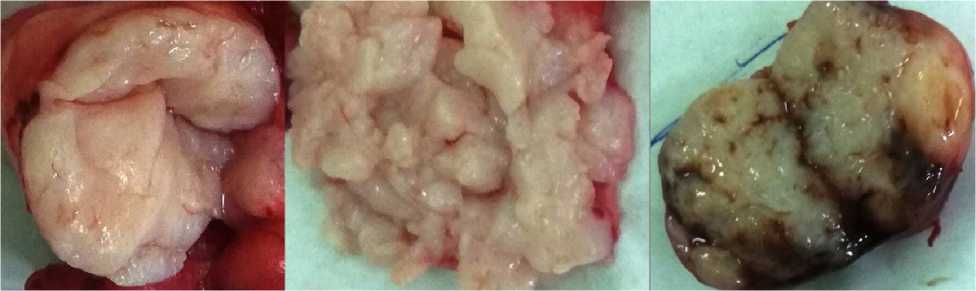
Рис. 4. Структура узлов фиброаденомы (макропрепараты)
При патоморфологическом исследовании во всех удаленных узлах верифицирована интраканалику-лярная форма фиброаденомы — на фоне преобладающей фиброзной ткани редкие щелевидные протоки с внутрипротоковой пролиферацией кубического эпителия. Течение послеоперационного периода — без осложнений. Заживление послеоперационных швов — первичным натяжением.
При катамнестическом наблюдении через три, шесть и девять месяцев после операции у девочки-подростка сохранялся клинически физиологический менструальный цикл, без проявлений дисменореи. Субъективно оцениваемая интенсивность менструальной кровопотери как физиологическая, подтверждена отсутствием гипохромных изменений в анализе крови. Асимметрия молочных желез не прогрессирует, масталгии нет. При динамическом ультрасонографическом контроле через три, шесть и девять месяцев после операции изменений в правой молочной железе не выявлено. В левой молочной железе через три месяца после операции в проекции ложа одного из удаленных узлов фиброаденомы лоцированы два участка средней эхогенности и гипоэхогенным ободком размерами 0,7×0,5 см и 0,9×0,7 см, аваску-лярные при цветовом допплеровском картировании; через шесть месяцев — при цветовом допплеровском картировании аваскулярный гипоэхогенный участок с четкими ровными контурами размерами 0,7×0,7 см; через девять месяцев — позади ареоляр-но-анэхогенные образования размерами 1,1×0,6 см; 0,7×0,5 см и 0,6×0,3 см. Динамическое наблюдение продолжено.
Обсуждение. Представленный клинический случай демонстрирует редкое сочетание множественной фиброаденомы молочной железы и порока развития внутренних половых органов у девочки-подростка. В доступной научной литературе мы не встретили аналогичного варианта коморбидности. Отметим, что у пациентки, несмотря на наличие двурогой матки, отсутствовали клинические проявления дисменореи и субъективные ощущения аномальной менструальной кровопотери. Именно этот факт, на наш взгляд, и стал причиной выявления порока развития половых органов при практически случайном обследовании. Согласно данным литературы, только у 12,2% девочек с ФМЖ имеется сопутствующая менструальная дисфункция и только в 7,3% наблюдений — масталгия [6], что подтверждается сведениями, представленными в нашем клиническом случае. Как известно, клинические проявления патологических изменений молочных желез у подростков разнообразны, среди них наиболее распространенные проявления — увеличение молочных желез, чаще — асимметричное пальпируемое образование имастал-гия [1, 8, 20]. Крайне редко при спонтанном кровоизлиянии в ткани узла возле протока или вовлечении в патологический процесс параареолярной области могут наблюдаться кровяные выделения из сосков. Во время пубертатного периода прогрессирующее увеличение размеров молочных желез часто связано с их естественным развитием, а не с наличием новообразования [8, 20]. Как одну из причин ювенильной агрегированной гипертрофии молочных желез у девочек-подростков рассматривают повышенную чувствительность органа-мишени к половым стероидным гормонам. В каждом третьем случае поводом для обращения за медицинской помощью становится пальпируемое в молочной железе образование [14, 17, 20]. Обстоятельства обнаружения объемных образований в маммарной ткани — важный фактор, который необходимо учитывать при оценке достоинств обучения девочек-подростков процедурам самообследования молочных желез. По данным исследований, до 80,0% новообразований молочных желез подростки обнаруживают самостоятельно [8]. В нашем случае пациентка также обнаружила уплотнение (наиболее крупный из имеющихся узлов) при самообследовании. В представленном нами клиническом случае показанием для хирургического лечения стало одностороннее многоузловое поражение ткани молочной железы, быстрый рост и большие размеры опухоли, что согласуется с существующими требованиями и мнением многих ученых.
Заключение . Представленный клинический случай акцентирует внимание на важном аспекте ювенильной маммологии. Знание основ возрастной маммологии и активная просветительская работа по обучению девочек-подростков навыкам самооб-следования молочных желез должны стать неотъемлемой составляющей врача — акушера-гинеколога и врачей смежных специальностей при работе в рамках амбулаторного приема независимо от причины обращения. Динамическое наблюдение за ростом и развитием молочных желез у девочек отвечает требованиям превентивной медицины, поскольку большинство заболеваний репродуктивной системы манифестируют у взрослых на неблагоприятном пре-морбидном фоне, сформировавшемся в детском и подростковом возрастах. Такой подход позволит своевременно заподозрить патологический процесс и определить маршрутизацию юных пациенток для проведения диагностических и лечебных мероприятий.
Список литературы Множественная фиброаденома молочной железы в сочетании с аномалией развития внутренних половых органов у девочки-подростка (клинический случай)
- Gao Y, Saksena MA, Brachtel EF, et al. How to approach breast lesions in children and adolescents. Eur J Radiol 2015; 84 (7): 1350-64.
- Травина М.Л., Попов А. Г., Попов С.А., Куликова Е.В. Клиническая классификация заболеваний и состояний молочных желез у детей и подростков. Вопросы современной педиатрии 2016; 15 (4): 385-90.
- Elsedfy Н. A clinical approach to benign breast lesions in female adolescents. Acta Biomed 2017; 88 (2): 214-21.
- Knell J, Koning JL, Grabowski JE. Analysis of surgically excised breast masses in 119 pediatric patients. Pediatr Surg Int 2016; 32(1): 93-6.
- Ciftci I, Sekmenli T, Ozbek S, et al. Inframammarial Giant Fibroadenoma Removing and a Nipple-sparing Breast Reconstruction in an Adolescent: A Case Report. Prague Med Rep 2015; 116(2): 161-6.
- Dogan G, Soyer T, Ekinci S, et al. Evaluation of surgically treated breast masses in children. Turk J Pediatr 2017; 59 (2): 177-83.
- Islam S, Saroop S, Bheem V, et al. Largest giant juvenile fibroadenoma of the breast. BMJ Case Rep 2019; 12 (1): e227277.
- Karaayvaz S. Clinical Evaluation of Breast in Childhood. Eur J Breast Health 2019; 15 (3): 137-40.
- Rafeek N, Rangasami R, Dhanraj K, et al. Multimodality approach in the diagnosis and management of bilateral giant juvenile breast fibroadenoma. BMJ Case Rep 2016; 2016: bcr2016217588.
- Laitano FF, Neto FL, Zerwes FP Bilateral giant juvenile fibroadenomas of the breasts-a rare indication for bilateral skin reducing mastectomy. Gland Surg 2016; 5 (4): 435-8.
- Valeur NS, Rahbar H, Chapman T. Ultrasound of pediatric breast masses: what to do with lumps and bumps. Pediatr Radiol 2015; 45 (11): 1584-99; quiz 1581-3.
- Cohen O, Avinadav E, Sharon E, et al. Pediatric and Adolescent Surgical Breast Clinic: Preliminary Experience. J Pediatr Adolesc Gynecol 2020; 33 (1): 23-6.
- Omar L, Gleason MK, Pfeifer CM, et al. Management of palpable pediatric breast masses with ultrasound characteristics of fibroadenoma: a more conservative approach. Am J Roentgenol 2019; 212 (2): 450-5.
- Durmaz E, Oztek MA, Arioz Habibi H, et al. Breast diseases in children: the spectrum of radiologic findings in a cohort study. Diagn Interv Radiol 2017; 23 (6): 407-13.
- McLaughlin CM, Gonzalez-Hernandez J, Bennett M, et al. Pediatric breast masses: an argument for observation. J Surg Res 2018; (228): 247-52.
- Brownstone ND, Celie KB, Spigland NA, et al. Pediatric Breast Fibroadenomas: A Systematic Review and Algorithm for Treatment. Ann Plast Surg 2019; 83 (5): 601-5.
- Michala L, Tsigginou A, Zacharakis D, et al. Breast disorders in girls and adolescents. Is there a need for a specialized service? J Pediatr Adolesc Gynecol 2015; 28 (2): 91-4.
- Shirian S, Daneshbod Y, Haghpanah S, et al. Spectrum of pediatric tumors diagnosed by fine-needle aspiration cytology. Medicine (Baltimore) 2017; 96 (6): e5480.
- Javed A, Jenkins SM, Labow B, et al. Intermediate and long-term outcomes of fibroadenoma excision in adolescent and young adult patients. Breast J 2019; 25 (1): 91-5.
- Harth S, Behrens C, Roller FC, et al. Breast Ultrasonography: Findings in Pediatric Patients. Ultraschall Med 2017; 38 (5): 500-7.


