Мочеточниковые стенты: в поисках рационального выбора
Автор: Нестеров С.Н., Ханалиев Б.В., Тевлин К.П., Барсегян А.Г., Косарев Е.И., Авакян С.К.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Обзоры литературы
Статья в выпуске: 2 т.15, 2020 года.
Бесплатный доступ
Стентирование мочеточников широко применяется в качестве способа временного и постоянного отведения мочи при обструкции верхних мочевыводящий путей. Цель: обзор литературы о видах мочеточниковых стентов, их преимуществах и недостатках, показаниях к установке, а также о ранних и поздних осложнениях, связанных с их применением. Материалы и методы: В статье представлены данные обзоров литературы и оригинальных статей из базы данных PubMed, Web of Science, Scopus и Elibrary по ключевым словам: мочеточниковые стенты, стентирование мочеточника, виды мочеточниковых стентов, показания мочеточниковых стентов. Заключение: Мочеточниковые стенты различаются по длине, диаметру, количеству петель, материалу, а также покрытию. В связи с преимуществами силиконовых стентов, они предпочтительны в большинстве случаев. Установка мочеточниковых стентов возможна при обширном количестве урологических и неурологических нозологий, а также перед оперативными вмешательствами в качестве профилактики повреждения мочеточника. Большое количество возможных осложнений, требует от врача наблюдения за пациентом с установленным мочеточниковым стентом в течение некоторого времени. Сегодня материалы, покрытия и конструкции мочеточниковых стентов меняются в соответствии с клиническими требованиями. Идеальный мочеточниковый стент - это стент, обладающий следующими характеристиками: простота установки, замены и удаления, отсутствие стент-ассоциированных симптомов, отсутствие ранних и поздних осложнений (в том числе аллергических реакций), хорошая визуализация при рентгеновском и УЗ-исследовании, а также низкая стоимость. К сожалению, несмотря на достаточно долгий период использования мочеточниковых стентов в урологической практике идеальных стентов, отвечающих данным критериям, до сих пор нет. Поэтому знание показаний, а также преимуществ и недостатков различных видов мочеточниковых стентов может помочь урологам принять решение об установке более подходящего стента в зависимости от клинической ситуации. Цель же последних инноваций в разработке стентов - создание мочеточникового стента, максимально отвечающего современным требованиям.
Мочеточниковые стенты, стентирование мочеточника, виды мочеточниковых стентов, показания мочеточниковых стентов
Короткий адрес: https://sciup.org/140259996
IDR: 140259996 | DOI: 10.25881/BPNMSC.2020.24.98.021
Ureteral stents: in search of a rational choice
Background: Over the past decades, ureteral stenting has been widely used as a method of temporary or permanent urine diversion while obstruction of the upper urinary tract. This article is aimed at studying the rational choice of the ureteral stent depending on the clinical situation. Objective: To review the literature of currently available data on the types of ureteral stents, their advantages and disadvantages, indications for their installation, as well as on early and late complications. Methods: The article presents data from literature reviews and original articles from the PubMed, Web of Science, Scopus, and Elibrary databases by keywords: ureteral stents, ureteral stenting, types of ureteral stents, indications for ureteral stents. Conclusions: Ureteral stents vary in length, diameter, number of loops, material, and coating. Due to the advantages of silicone stents, they are preferred in most cases. Ureteral stents may be installed in a large number of urological and non-urological diseases, as well as a prophylaxis of iatrogenic ureteral injury before surgical interventions as. A large number of possible complications requires the doctor to observe a patient with an installed ureteral stent for some time. Today, the materials and designs of the ureteral stents are changing in accordance with clinical requirements. An ideal ureteral stent is a stent with the following characteristics: ease installation, replacement and removal, absence of stent-associated symptoms, absence of early and late complications (including allergic reactions), good visualization with x-ray and ultrasound examination and a low price. However, despite of the long period of use of the ureteral stents in urological practice still doesn`t exist ideal stents that meet these criteria. The goal of recent innovations in stent development is to create this ideal ureteral stent.
Текст обзорной статьи Мочеточниковые стенты: в поисках рационального выбора
Актуальность
Установка мочеточниковых стентов один из первых навыков, которым начинающий уролог должен овладеть в процессе своего обучения. Стентирование мочеточника является высокоэффективным и относительно простым способом внутреннего дренирования мочи из почки. Значение данного умения определяется, в первую очередь, высокой частотой применения стентов в урологической практике. Например, мочекаменная болезнь, при которой в половине случаев требуется проведения стентирования, имеет заболеваемость в мире 3,5–9,6%, в структуре урологический заболеваний — 30–40% и является наиболее распространенным заболеваниям у пациентов, поступающих в экстренном порядке в урологический стационар [1].
В большинстве стационаров России устанавливается лишь несколько видов стентов, в то время как на рынке медицинского оборудования на сегодняшний день представлено огромное количество разнообразных мочеточниковых стентов, каждый из которых обладает теми или иными преимуществами и недостатками, в связи с чем показания к применению, а также частота развития осложнений будет разной и от правильного выбора зависит эффективность стентирования. В связи с этим актуальность данной темы невозможно переоценить.
История
Достижения в области химии после I и II мировых войн стали предпосылкой для быстрого развития

нового медицинского оборудования. Многочисленные материалы для стентов были исследованы в том числе на животных, однако, большинство из них в конечном итоге оказались неэффективны в результате таких проблем, как: инкрустация стента (полиэтилен, поливинил), размягчение стента при температуре тела (гуттаперча), жесткость и хрупкость с тенденцией к фрагментации (полиэтилен) и высокий реакционный ответ организма (политетрафторэтилен) [2]. Для преодоления этих ограничений была использована смесь полиэтилена и полиуретана [3]. Позже силикон вытеснил остальные материалы, так как в сравнении с ними подходил гораздо больше. Он был достаточно жестким и при этом устойчивым к инкрустации [2].
В 1976 г. P.D. Zimskind и соавт. значительно усовершенствовали мочеточниковые стенты и сообщили о продолжительном внутреннем дренировании мочеточника с помощью силиконового стента, установленного при цистоскопии с целью дренирования верхних мочевых путей при опухолевой обструкции [4]. В связи с отсутствием фиксаторов эти стенты легко мигрировали, поэтому Хепперлен в 1978 г. описал новую конструкцию мочеточникового стента, который удерживался в лоханке благодаря специальному завитку типа pig tale («поросячий хвост»), представляющие современные одно- и двухпетлевые стенты, что значительно снизило частоту миграции стента [5]. В настоящее время существуют металлические стенты, изготовленные из никель-титанового сплава (нитинола). Этот материал обладают памятью формы, что позволяет ему размягчаться при температуре ниже 7–13 °С и восстановить свою форму при температуре выше 55 °C, что помогает при установке и удалении стентов [6].
Классификация мочеточниковых стентов
-
1) Количество петель.
Выделяют одно- и двухпетлевые мочеточниковые стенты (Рис. 1), последние устанавливаются гораздо чаще. Однопетлевые стенты с фиксацией лишь в почке рекомендованы беременным для предупреждения миграции стента и сдавления мочеточника в результате роста плода и увеличения матки [7].
-
2) Длина и диаметр.
Диаметр мочеточниковых стентов измеряется в Шарьерах или Френчах (Ch, Fr) и варьирует от 3 до 34 Ch/Fr, чаще 6-9 Ch/Fr. В проспективном рандомизированном исследовании 45 пациентов Erturk и соавт., а также в исследовании Candela и Bellman на 60 пациентах устанавливались стенты 4.8-Fr Hydroplus, 6-Fr Percuflex и 6-Fr Hydroplus сравнивалась частота развития стент-ассоциированных симптомов (боль в области почки или мочевого пузыря, учащенное мочеиспускание, ноктурия, недержание мочи, ложные позывы, ощущение неполного опорожнения мочевого пузыря, гематурия) при помощи опросника в зависимости от вида и диаметра мочеточни-

Рис. 1. Двухпетлевой мочеточниковый стент.
кового стента. В ходе исследований выявлено, что такая зависимость статистически незначима, однако у пациентов со стентами с меньшим диаметров наблюдалось большее количество миграций [8; 9].
Длина мочеточниковых стентов варьирует от 12 до 90 см (длина однопетлевых стентов, дистальный конец которых выводится наружу), в среднем 26–28 см. В проспективном исследовании 87 пациентов Hо и со-авт. изучалось влияние длины мочеточниковых стентов (22, 24 и 26 см) на возникновение стент-ассоциированных симптомов при помощи опросника. Анализ результатов показал, что более длинный стент связан со значительно более высокой частотой учащенного мочеиспускания, однако не было статистически значимого различия в частоте развития гематурии и боли в области почки или мочевого пузыря [10].
В исследовании Rane и соавт. и в исследовании Al-Kandari и соавт. оценивалось влияние положения и длины стента на частоту возникновения стент-ассоцииро-ванных симптомов у 60 пациентов с помощью опросника. Результаты показали, что стенты, петли которых после установки пересекали среднюю линию мочевого пузыря, а также стенты с не полностью сформированными петлями на дистальном конце приводили к более частому возникновению стент-ассоциированных симптомов (77,8% пациентов против 33,4% пациентов, P<0,01) [11; 12].
-
3) Материал.
Существует два основных типа биосовместимых материалов которые используются для изготовления мочеточниковых стентов: полимеры и металлы [6]. Каждый материал имеет свои достоинства и недостатки [13]. Полимерные представлены полиуретановыми и силиконовыми стентами. Полимерные материалы реже вызывают аллергические реакции, менее склоны к инкрустациям, вызывают меньшую интенсивность болевого синдрома, безопасны для беременных, помимо этого могут быть биоразлагаемыми, что может не требовать их удаления. Преимуществом металлических стентов является их устойчивостью к сильному сжатию, и поэтому они эффективны при опухолевом сдавлении и/или прорастании мочеточника в качестве паллиативной помощи пациентам. Недостатками же металлических стентов является сложность их установки и высокая стоимость [14].
-
4) Специальные стенты.1. Мочеточниковые стенты с антирефлюксным клапаном.
-
2. Стент с памятью формы Мемокат. Представляет собой спиральную проволоку из никель-титанового сплава (нитинола), обладающего свойством «памяти формы» (спираль при нагревании трансформируется). Для удаления стента необходимо в мочевыводящие пути ввести охлажденный до 5 °C физиологический раствор и стент Мемокат при тракции превращается в прямую проволоку [15].
-
3. Allium стент. Это саморасширяющийся сетчатый стент компании Allium Medical (Caesarea Industrial Park South, Israel), разработанный с целью уменьшения раздражения мочевыводящих путей и, соответственно, развития стент-ассоциированных симптомов, а также для увеличения потока мочи в стенте и, следовательно, уменьшения вероятности обструкции мочеточника. Такие стенты могут применяться для лечения врожденного стеноза лоханочно-мочеточникового сегмента и ятрогенного стеноза мочеточника. Диаметр стента варьирует от 24 до 30 Fr и состоит из саморасширяюще-гося металла, который покрыт тонкой полиуретановой пленкой для предотвращения врастания стента в слизистую. Установка данных стентов произведена Leonardo и соавт. для лечения 12 взрослых пациентов с 2010–2013 гг. с гидронефрозом из-за врожденной обструкции чашечно-лоханочной системы или ятрогенного стеноза мочеточника. Стеноз был скомпенсирован, послеоперационный период протекал без осложнений, рецидивов во время наблюдения не было. Стент является съемным и не разработан для постоянной установки [16].
-
4. Vortek. Это запатентованный материал компании Coloplast, рассчитанный на срок использования до 12 месяцев. Самый популярный материал для стентов длительного стояния. Vortek имеет двухслойную структуру: наружный слой мягкий для комфорта пациента, внутренний — жесткий для удобства установки. Это термопластичный биополимер, поэтому в организме человека он становится мягче, что снижает частоту стент-ассоциированных симптомов.
-
5. Tail-стенты. Очень похожи на традиционные двухпетлевые стенты, разница заключается лишь в том, что дистальный конец стента имеет вид косичек для уменьшения раздражение мочевого пузыря. К таким стентам относятся: Inlay® (Bard® medical, USA) и Polaris ™ (Boston® scientific, USA) [6].
-
6. Стенты dual durometer. Такие стенты имеют аналогичную конструкцию, как и tail-стенты. Но состоят из двух материалов с разными физическими свойствами: твердого на проксимальном конце стента (для предотвращения дистальной миграции) и мягкого на дистальном конце (для увеличения переносимости стента). К таким стентам относятся: Sof-Curl (ACMI, Southborough, MA) и Polaris (Boston Scientific) [6; 17].
-
7. Стент с магнитным концом. Такой стент был впервые
представлен Maculuso и соавт. в 1989 г., и был разработан в основном для уменьшения дополнительных расходов, связанных с удалением стента [18]. Taylor и соавт. подтвердили успешное удаление таких стентов в 29 из 30 случаев. Для данного типа стентов также не требуется проведение цистоскопии при их удаления [19].
-
8. Двухпросветные стенты. Подобные стенты имеют два дренажных канала для возможности компенсации в случае обструкции одного из них. Эта конструкция была протестирована в исследовании J. Hafron и со-авт., которые сообщили об улучшении дренажа мочи с течением времени по сравнению с однопросветным стентом [20].
-
9. Стент на гелевой основе. Rosman и соавт. описали новый стент на гелевой основе из производного полиакрилонитрила. Гелевый стент представлен педиатрическим стентом AguaMedicina компании Q Urological. Авторы in vitro брали несколько срезов длиной 1 см данного стента и полимерного стента компании Boston Scientific и оценивали рост бактерий через каждые 3 суток в течение 15 суток. Анализ результатов показал, что рост бактерий на гелевых стентах был ниже на 43–71% чем на контрольных [21] .
-
10. Спиральный стент. Спиральный стент Percuflex компании Boston Scientific изготовлен из материала Percu-flex и характеризуется наличием спирального разреза по всей длине прямой части стента. Стент разработан для уменьшения стент-ассоциированных симптомов благодаря лучшему соответствию мочеточнику за счет увеличения гибкости стента без снижения дренажной способности стента. Однако, Mucksavage и соавт. в исследовании на свиньях определили, что нет никакой разницы в частоте гидронефроза, миграции стента, инфицировании мочевыводящих путей и инкрустации стента при использовании данного стента по сравнению со стандартными [22].
-
11. Микростент. При острой закупорке мочеточника вследствие мочекаменной болезни необходимо создать максимальную дилатацию мочеточника, занимая как можно меньше места в просвете мочеточника, чтобы облегчить прохождение камня через мочевые пути. Микростент компании PercSys — стент с диаметром 3 Fr. Потенциальный риск использования такого стента состоит в том, что он может не обеспечивать адекватного дренажа мочи. Для определения дренажной способности данного стента Lange и соавт. провели исследование на свиньях in vitro и ex vivo и определили, что микростент с 3 Fr продемонстрировал дренирование эквивалентное стандартному стенту 4.7 Fr. Поэтому этот новый микростент может оказаться полезным для устранения острой обструкции, вызванной камнями мочеточника [23].
-
12. Биоразлагаемые мочеточниковые стенты. «Забытый» стент — это осложнение, которого опасаются все урологи, так как оно сопряжено с высокими рисками,

не только для здоровья пациента, но и для его жизни. Биоразлагаемый стент может устранить эти риски и необходимость пациента в повторной госпитализации для удаления стента. В 2008 г. Hadaschik и соавт. провели исследование на свиньях in vivo и сравнивали эффективность дренирования, степень гидронефроза, дилатации мочеточника и частоту инфицирования мочевыводящих путей разлагаемого стента (Uriprene, Poly-Med Inc., Anderson, SC) и стандартного биоста-бильного стента. Результаты показали, что стенты Uriprene начали разлагаться спустя 3 недели и были полностью разрушены на 10 неделе. Эффективность дренирования мочи была одинаковой, однако стенты Uriprene показали меньшую дилатация мочеточника и меньшее количество бактериурии. Однако возникли некоторые сложности с установкой стента в связи с его мягкостью [24].
Второе поколение биоразлагаемых стентов было разработано для более быстрого разложения. Согласно результатам исследования Chew и соавт. на свиньях 80% таких стентов разрушились в течение 2-3 недель, а 100% стентов — уже к 4-й неделе [25].
-
5) Покрытие стентов.Стенты бывают покрытые и непокрытые.
Мочеточниковые стенты могут быть покрыты фармакологическими средствами, которые со временем постепенно высвобождаются, обеспечивая местное действие. Если стенты с лекарственным покрытием в кардиологии уже активно используются, то данных за их использовании в урологической практике довольно мало. Стенты могут быть покрыты антибиотиками, анальгетиками, спазмолитиками или другими фармакологическими соединениями [17].
Триклозан — антимикробный препарат широкого спектра действия, является первым соединением, которое одобрено для клинического применения в качестве покрытия для мочеточниковых стентов. В исследовании Cadieux и соавт. частота бактериурии в группе пациентов со стентами, выделяющими триклозан и группе контроля была одинаковой, тем не менее частота инфицирования мочевыводящих путей и потребность в антибиотиках для их лечения были значительно ниже в группе с три-клозаном [26].
Minardi и соавт. изучили действие комбинации двух антибиотиков, рифампина и тигециклина на энтерококков in vitro и in vivo на крысах. Мочеточниковые стенты были покрыты рифампицином, а тигециклин вводился внутрибрюшинно в крыс, зараженных энтерококком. Сочетание двух антибиотиков было более эффективным против бактерий, чем каждый из антибиотиков в отдельности [27]. Израильская группа оценила материал C-flex компании Cook Medical, покрытый медленно высвобождаемым хлоргексидиновым лаком для борьбы с энтерококком, Escherichia и Pseudomonas и показали его эффективность, благодаря предотвращаю колонизации [28].
Компания Cook Medical производит также мочеточниковый стент Endo-Sof Radiance, покрытый гепариноподобным веществом. Данное покрытие позволяет снизить степень инкрустации стента и, соответственно, снизить частоту замены стента (срок стентирования до 12 месяцев). Стент обладает термочувствительными свойствами: исходная жесткость обеспечивает легкость при установке, а затем происходит размягчение стента, что улучшает его переносимость пациентами.
Показания к установке мочеточниковых стентов
Стенты устанавливаются при различных урологических и неурологических заболеваниях. К урологическим заболеваниям, при которых возможно применение мочеточниковых стентов, относят:
-
1. Мочекаменная болезнь;
-
2. Опухоли мочеточника, мочевого пузыря;
-
3. Обструкция мочеточника кровяными свёртками;
-
4. Чрезмерный отек слизистой оболочки мочеточника;
-
5. Образование рубцов и спаек вследствие инфекционновоспалительных процессов;
-
6. Травма мочеточника.
К неурологическим заболеваниям относят:
-
1. Сдавление и прорастание опухоли других локализаций (шейки матки или яичника, лимфомы) в мочеточник;
-
2. Болезнь Ормонда.
Другие причины:
-
1. Ятрогенные причины (осложнение хирургического лечения, лучевой терапии или дистанционной ударно-волновой литотрипсии). Для исключения повреждения мочеточника в абдоминальной хирургии и оперативной гинекологии. Такое использование стента является безопасным, и улучшает интраоперационное выявление повреждений мочеточника, поэтому должно рассматриваться при операциях с высоким риском повреждения мочеточника [29].
-
2. В исследовании Gomes и соавт. рекомендуется применение мочеточниковых стентов в качестве профилактики развития урологических осложнений (стеноза и свища) после трансплантации почки [частота развития осложнений после установки стента — 5,4% против 8,4% — без стента (P<0,005)] [31].
-
3. Металлические стенты могут применяться в клинической практике в качестве активного электрода при проведении радиочастотной абляции [32].
В своем исследовании Chandhoke и соавт. сравнивали два разных диаметра стента (4.7F и 7F) у пациентов, которым показана ударно-волновая литотрипсия с контрольной группой не стентированных пациентов. У стентированных пациентов значительно чаще возникали ирритативные симптомы (учащенное мочеиспускание, недержание мочи, ноктурия), чем у не стентированных пациентов, разница же в диаметра стента была статистически незначима. Но при этом в группе стентированных пациентов (особенно со стентами 4,7 Fr) количество случаев экстренных госпитализаций по поводу почечной колики и лихорадки было меньше чем в группе пациентов без стентов (7% против 22%). По мнению авторов, более хорошие показатели у стентов с меньшим диаметром связаны с тем, что между стентом и стенкой мочеточника остается больше пространства для миграции камня. В связи с этим авторы рекомендуют у пациентов, которым показана установка стента при дистанционной

ударно-волновой литотрипсия, использовать стенты с меньшим диаметром (4,7F) [30].
Осложнения установки мочеточниковых стентов
Ранние осложнения
-
1. Стент-ассоциированные симптомы (боль в области почки или мочевого пузыря, учащенное мочеиспускание, ноктурия, недержание мочи, ложные позывы, ощущение неполного опорожнения мочевого пузыря, гематурия);
-
2. Пузырно-мочеточниково-лоханочный рефлюкс;
-
3. Инфекционные осложнения;
-
4. Почечная колика;
-
5. Сужение просвета из-за отека слизистой мочеточника;
-
6. Повреждение стенок мочеточника;
-
7. Ретропульсия камня.
Поздние осложнения
-
1. Инкрустация стента (Рис. 2), что происходит в связи с наличием таких бактерий, как Proteus mirabilis, которые производят уреазу, что повышает рН мочи и приводит к образованию кристаллов [33];
-
2. Гидронефроз;
-
3. Проксимальная либо дистальная миграция стента;
-
4. Фрагментация стента;
-
5. Узлообразование;
-
6. Уретеро-артериальные и уретеро-кишечные фистулы;
-
7. «Забытый» стент;
-
8. Пролежень мочеточника;
-
9. Аллергическая реакция на материал стента.
Данный обзор литературы не содержит информации о частоте развития тех или иных осложнениях и о возможных способах их лечения, так как мы считаем, что изучение данного вопроса невозможно в рамках одного обзора и заслуживает внимания уже в отдельной статье.
Заключение
Мочеточниковые стенты различаются по длине, диаметру, количеству петель, материалу, а также покрытию. В связи с преимуществами силиконовых стентов, они предпочтительны в большинстве случаев. Установка мочеточниковых стентов возможна при обширном количестве урологических и неурологических нозологий, а также перед оперативными вмешательствами в качестве профилактики повреждения мочеточника.
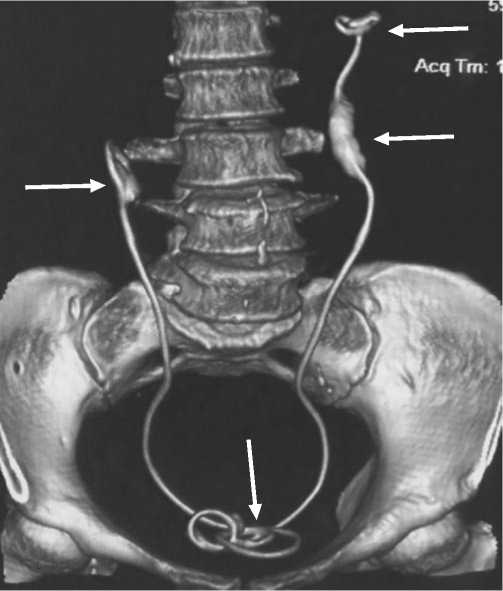
Рис. 2. Инкрустация проксимальных и дистальных концов обоих мочеточниковых стентов (белые стрелки). МСКТ с 3D-реконструкцией.
Большое количество возможных осложнений, требует от врача наблюдения в течение некоторого времени за пациентом с установленным мочеточниковым стентом. Сегодня в соответствии с клиническими требованиями разрабатываются новые материалы, покрытия и конструкции мочеточниковых стентов [34]. Многочисленные антимикробные покрытия были применены на мочеточниковых стентах и мочевых катетерах в попытке уменьшить адгезию бактерий, но, к сожалению, это часто сопровождалось развитием резистентности. Необходимы дальнейшие научные и клинические исследования, прежде чем антимикробные покрытия могут быть введены в клиническую практику[3].
Идеальный мочеточниковый стент — это стент, обладающий следующими характеристиками: легкая установка, отсутствие миграции, отсутствие дискомфорта у пациента, биосовместимость, устойчивость к инкрустации солями, хорошая визуализация при УЗ-исследо-вании, простота замены или удаления, а также низкая стоимость [3]. Несмотря на достаточно долгий период использования мочеточниковых стентов в урологической практике идеальных стентов, отвечающих данным критериям, до сих пор нет [3]. Поэтому знание показаний, а также преимуществ и недостатков различных видов мочеточниковых стентов может помочь урологам принять решение об установке более подходящего стента в зависимости от клинической ситуации. Цель последних
инноваций в разработке стентов — создание идеального мочеточникового стента [34].
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Doi: 10.1016/j.juro.2008.05.003.
Doi: 10.1089/end.2008.0437.
Список литературы Мочеточниковые стенты: в поисках рационального выбора
- Борисов В.В., Дзеранов Н.К. Мочекаменная болезнь. Терапия больных камнями почек и мочеточников. Учебное пособие. — Москва; 2011. — 96 с. [Borisov VV, Dzeranov NK. Mochekamennaya bolezn'. Terapiya bol'nykh kamnyami pochek i mochetochnikov. Uchebnoe posobie. Moscow; 2011. 96 p. (In Russ).]
- Donahue RP, Stamm AW, Gibbons RP, et al. Evolution of the ureteral stent: the pivotal role of the gibbons ureteral catheter. Urology. 2018;115:3-7. Doi: 10.1016/ j.urology.2018.02.007.
- Золотухин О.В., Мадыкин Ю.Ю., Федоров А.А. Эволюция метода дренирования верхних мочевых путей // Вестник экспериментальной и клинической хирургии. — 2019. — Т.12. — №3. — С. 199-202. [Zolotukhin OV, Madykin YuYu, Fedorov AA. Evolution of upper urinary tract drainage method. Journal of Experimental and Clinical Surgery. 2019;12(3):199-202. (In Russ).] Doi: 10.18499/2070-478X-2019-12-3-199-202.
- Zimskind PD, Fetter TR, Wilkerson JL. Clinical use of long-term indwelling silicone rubber ureteral splints inserted cystoscopically. J Urol. 1967;97(5):840-844.
- Hepperlen TW, Mardis HK, Kammandel H. Self-retained internal ureteral stents: a new approach. J Urol. 1978;119(6):731-734. Doi: 10.1016/s0022-5347(17)57613-2.
- Mosayyebi A, Manes C, Carugo D, Somani BK. Advances in Ureteral Stent Design and Materials. Curr Urol Rep. 2018;19(5):35. Doi: 10.1007/s11934-018-0779-y.
- kidneystoners.org [Internet]. How is a ureteral stent placed? [cited 2020 Apr 29]. Available at: https://www.kidneystoners.org/surgery/how-is-a-ureteral-stent-placed/.
- Erturk E, Sessions A, Joseph JV. Impact of ureteral stent diameter on symptoms and tolerability. JEndourol. 2003;17(2):59-62. Doi: 10.1089/08927790360587342.
- Candela JV, Bellman GC. Ureteral stents: impact of diameter and composition on patient symptoms. J Endourol. 1997;11(1):45-47. Doi: 10.1089/end.1997.11.45.
- Ho CH, Chen SC, Chung SD, et al. Determining the appropriate length of a double-pigtail ureteral stent by both stent configurations and related symptoms. J Endourol. 2008;22(7):1427-1431. Doi: 10.1089/end.2008.0037.
- Rane A, Saleemi A, Cahill D, et al. Have stent-related symptoms anything to do with placement technique? J Endourol. 2001;15(7):741-745. Doi: 10.1089/ 08927790152596352.
- Al-Kandari AM, Al-Shaiji TF, Shaaban H, et al. Effects of proximal and distal ends of double-J ureteral stent position on postprocedural symptoms and quality of life: a randomized clinical trial. J Endourol. 2007;21(7):698-702. Doi: 10.1089/ end.2007.9949.
- Sali GM, Joshi HB. Ureteric stents: overview of current clinical applications and economic implications. Int J Urol. 2019;27(1):7-15. Doi: 10.1111/iju.14119.
- Dellis A, Joshi HB, Timoney AG, et al. Relief of stent related symptoms: review of engineering and pharmacological solutions. J Urol. 2010;184(4):1267-1272. Doi: 10.1016/j.juro.2010.06.043.
- Глыбочко П.В., Аляев Ю.Г., Газимиев М.А., и др. Стенты мемокат в лечении обсутрктивных заболеваний мочевых путей // Медицинский вестник Башкортостана. — 2011. — Т.6. — №2. — С. 227-231. [Glybochko PV, Aliayev YuG, Gazimiyev MA, et al. Memokath stents in the treatment of urinary tract obstructive diseases. Meditsinskii vestnikBashkortostana. 2011;6(2):227-231. (In Russ).]
- Brotherhood H, Lange D, Chew BH. Advances in ureteral stents. Transl Androl Urol. 2014;3(3):314-319. Doi: 10.3978/j.issn.2223-4683.2014.06.06.
- Duvdevani M, Chew BH, Denstedt JD. Minimizing symptoms in patients with ureteric stents. Curr Opin Urol. 2006;16(2):77-82. Doi: 10.1097/01. mou.0000193375.29942.0f.
- Rao NP, Preminger GM, Kavanagh JP, editors. Urinary tract stone disease. London: Springer; 2011. Doi: 10.1007/978-1-84800-362-0.
- Taylor WN, McDougall IT. Minimally invasive ureteral stent retrieval. J Urol. 2002;168(5):2020-2023. Doi: 10.1097/01.ju.0000033964.15384.e2.
- Hafron J, Ost MC, Tan BJ, et al. Novel dual-lumen ureteral stents provide better ureteral flow than single ureteral stent in ex vivo porcine kidney model of extrinsic ureteral obstruction. Urology. 2006;68(4):911-915. Doi: 10.1016/j.urology.2006.05.025.
- Rosman BM, Barbosa JA, Passerotti CP, et al. Evaluation of a novel gel-based ureteral stent with biofilm-resistant characteristics. Int Urol Nephrol. 2014;46(6):1053-1058. Doi: 10.1007/s11255-013-0636-3.
- Mucksavage P, Pick D, Haydel D, et al. An in vivo evaluation of a novel spiral cut flexible ureteral stent. Urology. 2012;79(3):733-737. Doi: 10.1016/ j.urology.2011.10.062.
- Lange D, Hoag NA, Poh BK, Chew BH. Drainage characteristics of the 3F MicroStent using a novel film occlusion anchoring mechanism. J Endourol. 2011;25(6): 1051-1056. Doi: 10.1089/end.2010.0722.
- Hadaschik BA, Paterson RF, Fazli L, et al. Investigation of a novel degradable ureteral stent in a porcine model. J Urol. 2008;180(3):1161-1166. Doi: 10.1016/j.juro.2008.05.003.
- Chew BH, Lange D, Paterson RF, et al. Next generation biodegradable ureteral stent in a yucatan pig model. J Urol. 2010;183(2):765-771. Doi: 10.1016/j.juro.2009.09.073.
- Cadieux PA, Chew BH, Nott L, et al. Use of triclosan-eluting ureteral stents in patients with long-term stents. J Endourol. 2009;23(7):1187-1194. Doi: 10.1089/end.2008.0437.
- Minardi D, Cirioni 0, Ghiselli R, et al. Efficacy of tigecycline and rifampin alone and in combination against Enterococcus faecalis biofilm infection in a rat model of ureteral stent. J Surg Res. 2012;176(1):1-6. Doi: 10.1016/j.jss.2011.05.002.
- Zelichenko G, Steinberg D, Lorber G, et al. Prevention of initial biofilm formation on ureteral stents using a sustained releasing varnish containing chlorhexidine: in vitro study. J Endourol. 2013;27(3):333-337. Doi: 10.1089/end.2012.0193.
- da Silva G, Boutros M, Wexner SD. Role of prophylactic ureteric stents in colorectal surgery. Asian JEndosc Surg. 2012;5(3):105-110. Doi: 10.1111/j.1758-5910.2012.00134.x.
- Chandhoke PS, Barqawi AZ, Wernecke C, Chee-Awai RA. A randomized outcomes trial of ureteral stents for extracorporeal shock wave lithotripsy of solitary kidney or proximal ureteral stones. J Urol. 2002;167(5):1981-1983. Doi: 10.1016/s0022-5347(05)65067-7.
- Gomes G, Nunes P, Castelo D, et al. Ureteric stent in renal transplantation. Transplant Proc. 2013;45(3):1099-1101. Doi: 10.1016/j.transproceed.2013.02.086.
- LaBerge JM. The 27th annual Charles T. Dotter lecture: Data integration in in-terventional radiology: the pressing challenge of our time. J Vasc IntervRadiol. 2011;22(8):1061-1067. Doi: 10.1016/j.jvir.2011.04.007.
- Darlington D, Anitha FS. Single session endoscopic removal of bilateral ureteric stents retained for three decades: a case report. Cureus. 2019;11(3):e4294. Doi: 10.7759/cureus.4294.
- Forbes C, Scotland KB, Lange D, Chew BH. Innovations in ureteral stent technology. Urol Clin North Am. 2019;46(2):245-255. Doi: 10.1016/j.ucl.2018.12.013.


