Моделирование направленного транспорта лекарственных веществ. Часть I. Однократное введение
Автор: Заборовский Андрей Владимирович, Гуревич Константин Георгиевич
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 1 т.16, 2017 года.
Бесплатный доступ
В онкологической практике, несмотря на развитие методов ранней диагностики, хирургии, лучевой терапии и др., химиотерапия вряд ли потеряет свою актуальность в ближайшее время. В этой связи разработка новых противоопухолевых препаратов является одной из актуальных задач современной онкологии. При всей значимости поиска новых соединений с противоопухолевой активностью воз-можности «старых» средств полностью не исчерпаны. Направленный транспорт противоопухолевых средств может подарить им «вторую жизнь» в клинике. При разработке направленного транспорта лекарственных средств и их дальнейшем внедрении в практику особое значение имеет изменение их фармакодинамики и фармакокинетики. В работе описана формальная фармакокинетическая модель направленного транспорта лекарственных веществ. Сформулированы условия, при которых для ис-ходного действующего вещества имеет смысл искать средство доставки. Исходя из основных предпо-ложений модели проведен первичный скрининг противовопухолевых средств с целью их модификации для направленного транспорта.
Лекарственные вещества, направленный транспорт, ткани-мишени, противоопухолевые препараты
Короткий адрес: https://sciup.org/140254095
IDR: 140254095 | УДК: 615.277.3 | DOI: 10.21294/1814-4861-2017-16-1-59-65
Simulation of targeted transport for drug substances. Part 1: a single administration
In oncology practice, despite advances in methods for early detection, surgery, radiotherapy, laser therapy, targeted therapy, etc., chemotherapy is unlikely to lose its relevance in the near future. In this context, the development of new antitumor drugs is one of the urgent problems of modern conservative oncology. Despite the importance of the search for new compounds with antitumor activity, the clinical potential of the «old» agents does not yet seem to be exhausted. The transport of antitumor agents can give them a «second life» in the clinic. When developing the targeted transport for chemotherapeutic drugs, the changes in their pharmacodynamics and pharmacokinetics are of great importance. A pharmacokinetic model of targeted transport of drug substances has been described in this paper. There have been described conditions under which it is worth to search for facility of transport for the initial active agent. Primary screening of antitumor agents have been undertaken to modify them for the targeted transport based on underlying assumptions of the model.
Текст научной статьи Моделирование направленного транспорта лекарственных веществ. Часть I. Однократное введение
Направленный транспорт лекарственных веществ – способ модификации для улучшения их поступления в ткани-мишени [1]. Кроме того, стоимость разработки направленного транспорта известных антибактериальных и противоопухолевых препаратов в разы уступает стоимости разработки новых лекарственных средств. Это объясняется двумя причинами: во-первых, тем, что обычно в качестве носителей используются мицеллы (липосомы) [2], наночастицы [3], биополимеры [4, 5], для большинства которых вопросы биобезопасности хорошо изучены [6]; во-вторых, «старые» препараты имеют мощное доклиническое и клиническое досье. Именно поэтому для модифицированного лекарственного средства («старый» препарат плюс носитель) чаще всего достаточно проведения ограниченного изучения токсичности и эффективности [7–9].
При этом достаточно часто за рамками исследований остаются вопросы изучения фармакокинетики модифицированных лекарственных средств [10]. Хотя именно показатели фармакокинетики осново-полагающи в подборе режимов дозирования [11].
Кроме того, с нашей точки зрения, имеются фармакокинетические ограничения в выборе исходных веществ, которые имеет смысл модифицировать для целей направленного транспорта. Подобный вопрос практически не изучался; есть лишь описательная (но не аналитическая) модель направленного транспорта антибиотиков [12, 13]. Все это обосновывает необходимость создания аналитической фармакокинетической модели направленного транспорта, в первую очередь, с целью изучения модифицированных противоопухолевых препаратов. Это и определило актуальность настоящего исследования.
Материал и методы
Моделирование изменения концентрации лекарственного вещества (ЛВ) в крови и тканях осуществляли, используя описанные линейные фармакокинетические модели [14]. Основные предположения модели:
-
1. Введение ЛВ в кровь осуществляется одномоментно, в конъюгированном виде.
-
2. ЛВ может находиться в крови в свободном и конъюгированном виде. Конъюгированное
-
3. Из крови почками (печенью) элиминируется только неконъюгированная форма ЛВ. Константа элиминации меньше любой константы поступления ЛВ в ткани.
-
4. Константа поступления неконъюгированной формы ЛВ в ткани одинакова.
-
5. Константа поступления конъюгированной формы ЛВ в ткань 1 существенно превосходит все остальные ткани организма (ткань 2). Поступление конъюгированной формы ЛВ в ткань 2 осуществляется не быстрее, чем свободной.
-
6. Поступление конъюгированной формы ЛВ в ткань по сути означает сочетание 2 процессов: взаимодействия носителя ЛВ и высвобождения ЛВ. Таким образом, в ткани всегда оказывается неконъюгированная форма ЛВ.
-
7. Скорость выведения ЛВ из ткани не зависит от типа ткани.
-
8. Скорость любого процесса пропорциональна концентрации ЛВ.
-
9. Объем крови (тканей) неизменен.
вещество может только распадаться и не может синтезироваться de novo .
При построении модели были использованы следующие основные обозначения:
Ск – концентрация конъюгированной формы ЛВ; к
Ссв – концентрация свободной формы ЛВ в крови;
С1 и С2 – концентрации ЛВ в камерах 1 и 2 соответственно;
kд – константа деструкции конъюгированной формы ЛВ;
kэл – константа экскреции ЛВ печенью или почками;
-
k1 – константа поступления свободной формы ЛВ в ткани из крови;
-
k1’ – константа поступления конъюгированной формы ЛВ в ткань 1;
-
k1” – константа поступления конъюгированной формы ЛВ в ткань 2;
-
k2 – константа поступления ЛВ из ткани в кровь.
Соотношение между константами, следующее из постулатов модели:
-
k 1 ’ > k 1 ≥ k 1 ”.
Исходя из представленных предположений, концентрация ЛВ описывается следующей системой линейных дифференциальных уравнений:
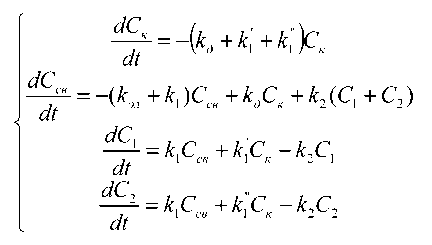
Теоретически данная система уравнений методом преобразований Лапласа может быть на комплексной плоскости сведена к системе линейных алгебраических уравнений, что позволит ее решить в аналитическом виде. Однако получаемое решение является громоздким. Поэтому в работе использовали численное решение методом Рунге-Куты. Решение проводили в программе Excel на основании написанного алгоритма. Шаг по времени - 0,01 ч. Исходную концентрацию конъюгированного препарата предполагали 1 ммоль/мл, свободного - 0 ммоль/мл. к 1 =0,1 ч-1; к 1 ’=0,5 ч-1; к 1 ”=0,01 ч-1; кд =0,005 ч-1; к эл =0,4 ч-1; к 2 =0,2 ч-1. Выбор констант основан на литературных данных для доксорубицина [15] и цисплатины [16, 17]. В дальнейшем осуществляли вариацию констант.
Результаты исследования
Ск – концентрация конъюгированной формы ЛВ; Ссв – концентрация свободной формы ЛВ в крови; С1 и С2 – концентрации ЛВ в камерах 1 и 2 соответственно. Динамика изменений концентраций ЛВ в крови (свободная и конъюгированная формы), таргетной ткани (ткань 1) и других тканях (ткань 2) представлена на рис. 1. Выбранные
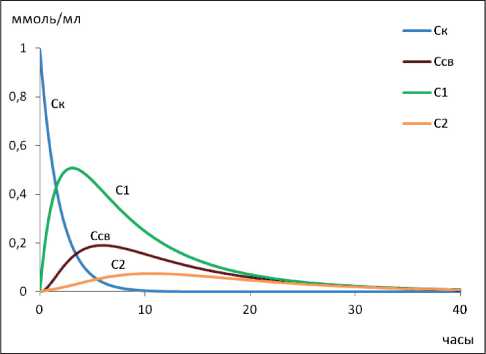
Рис. 1. Динамика изменений концентраций ЛВ
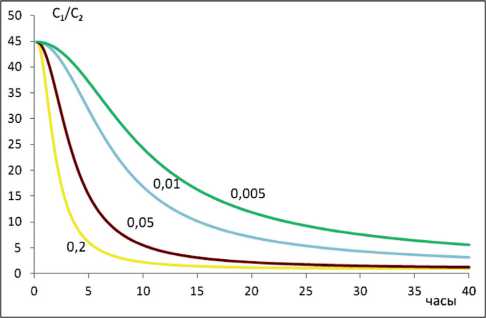
Рис. 2. Изменение соотношения концентраций ЛВ в камерах 1 и 2 в зависимости от времени таблица
Фармакокинетические параметры противоопухолевых средств [18–22]
|
ЛВ |
Время полувыведения |
Связывание |
Выведение |
Способность |
|
(быстрая; медленная фаза) |
с белками крови |
с мочой |
накапливаться в тканях |
|
|
Абраксан |
27 ч |
95 % |
0 % |
Да |
|
Азацитидин* |
41 мин |
Нет данных |
50–85 % |
Да |
|
Актиномицин Д |
36 ч |
Нет данных |
10 % |
Да |
|
Амифостин* |
10 мин для исходного вещества |
Нет данных |
100 % |
Да |
|
Анастразол |
50 ч |
40 % |
0 % |
Нет |
|
Апротитин* |
150 мин; 7–10 ч |
Нет данных |
100 % |
Да |
|
Бендамустин* |
28,3 мин |
95 % |
20 % |
Да |
|
Блеомицин |
2-3 ч |
5 % |
60–70 % |
Нет |
|
Бусульфан* |
2,5 ч |
Нет данных |
40–60 % |
В больших дозах – да |
|
Винбластин |
25 ч |
99 % |
Менее 5 % |
Да |
|
Винкристин |
85 ч |
75 % |
0 % |
Да |
|
Винорелбин |
35 ч |
80 % |
0 % |
Да |
|
Гексаметилметианин |
0,5–3 ч; 4,7–10,2 ч |
50 % |
Порядка 99 % |
Нет данных |
|
Гемцитабин* |
1–7 ч |
5 % |
10–60 % |
Да |
|
Гефитиниб |
35 ч |
90 % |
0 % |
Да |
|
50 % исходное |
||||
|
Гидроксимочевина* |
3–4 ч |
Нет данных |
вещество; 80 % |
Да |
|
метаболиты |
||||
|
10–36 ч для исходного веще- |
97 % исходное веще- |
|||
|
Идарубицин |
ства; 33–60 ч для активного |
ство; 94 % активный |
До 50 % |
Да |
|
метаболита |
метаболит |
|||
|
Имидазол* |
19 мин; 5 ч |
5 % |
40 % |
Частично |
|
Иринотекан |
9 ч |
45 % |
Не более 10 % |
Да |
|
Ирнатиниб |
18 ч |
95 % |
До 20 % |
Да |
|
Ифосфармид |
7 ч |
20 % |
Около 100 % |
Нет |
|
Дакабазин |
5 ч |
20 % |
Около 10 % |
нет |
|
Даунорубицин* |
35–45 мин; 46–54 ч |
Нет данных |
10–25 % |
Да |
|
Доксорубицин* |
1 ч; 20–48 ч |
74–76 % |
40 % |
Да |
|
Доцетаксел* |
4 мин; 11,4 ч |
95 % |
6 % |
Да |
|
Иринотекан |
12 мин |
65 % |
20–25 % |
Нет данных |
|
Капецитабин |
0,6–0,9 ч |
54 % |
84–96 % |
Нет |
|
Карбоплатин |
144 ч |
0 % |
Около 100 % |
Нет |
|
Кармустин* |
0,33 ч |
80 % |
Около 100 % |
Да |
|
Лизомустин |
12 ч |
Нет данных |
40 % |
Нет данных |
|
Ломустин |
16–48 ч; 72 ч |
50 % |
50 % |
Да |
|
Мелфотан |
90 мин |
50–60 % |
50 % |
Нет данных |
|
6–меркаптопурин* |
45 мин; 2,5 ч; 10 ч |
Нет данных |
7–40 % |
Да |
|
Метотрексат |
3–17 ч |
50 % |
80–95 % |
Нет |
|
Митоксантрон |
75 ч |
80 % |
0 % |
Да |
|
Митомицин С |
17 мин |
Нет данных |
10 % |
Нет |
|
Нимустин* |
1 ч |
Нет данных |
Нет данных |
Да |
|
Нитромедазолмоче-вина* |
6–7 мин; у части больных – 17 мин |
Нет данных |
Нет данных |
У части больных – да |
|
Оксалиплатин* |
0,28 ч |
98 % |
58 % |
Да |
|
Ормустин* |
3,5 мин; 109,4 ч |
Нет данных |
Около 100 % |
Да |
|
Паклитаксел* |
3 мин; 52,7 ч |
89–98 % |
10 % |
Да |
|
Пеметрексед* |
20 мин–3,5 ч |
80 % |
Около 100 % |
Да |
|
Пралатрексед |
12–18 ч |
67 % |
30–40 % |
Нет |
|
Прокарбазин |
1 ч |
Нет данных |
100 % |
Нет данных |
|
Ралтитрексед |
32–99 мин |
Мало |
80–95 % |
Нет (при неизмененной функции почек) |
|
Стрептозоцин |
6 мин; 40 мин |
Нет данных |
20 % |
Нет |
Продолжение таблицы
|
ЛВ |
Время полувыведения (быстрая; медленная фаза) |
Связывание с белками крови |
Выведение с мочой |
Способность накапливаться в тканях |
|
Сунитиб |
50 ч |
95 % |
0 % |
Да |
|
Тамоксифен |
240 ч |
99 % |
Менее 5 % |
Да |
|
Тегафур* |
10–25 мин |
Нет данных |
25 % |
Да |
|
Темозоломид* |
2 ч |
15 % |
100 % |
Да |
|
Тиогуанин |
80 мин |
Нет данных |
Более 90 % |
Нет |
|
Тиофосфамид |
20 ч |
Нет данных |
85 % |
Нет данных |
|
Топотекан* |
3 ч |
25 % |
90 % |
Да |
|
Трабектедин* |
175 мин |
97 % |
До 10 % |
Да |
|
1,5 ч для исходного вещества, |
||||
|
Хлорамбуцил |
2,5 ч для активного метабо- |
99 % |
Менее 1 % |
Нет |
|
лита |
||||
|
Циклофосфамид |
2-3 ч для исходного препарата, 65 ч для метаболитов |
12-14 %; ряд метабо-литов до 60 % |
Около 100 % |
Нет |
|
Цисплатин* |
25–49 мин; 58–73 ч |
90–95 % |
27–43 % |
Да |
|
Цитозин* |
10 мин; 1–3 ч |
15 % |
80 % |
Да |
|
Флударабин фосфат* |
30 мин для исходного препарата; 2 ч и более для актив- |
0 % |
40–80 % |
Да |
|
ных метаболитов |
||||
|
Фотомустин* |
7 мин |
25–30 % |
50–60 % |
Да |
|
5–фторурацил |
8–22 мин |
10 % |
20 % |
Нет |
|
Эверолимус |
30 ч |
75 % |
Менее 5 % |
Нет данных |
|
Эксеместран |
24 ч |
90 % |
Менее 10 % |
Нет |
|
Эстрамустин |
20 ч |
Нет данных |
Менее 10 % |
Нет данных |
|
Эпирубицин |
35 ч |
80 % |
0 % |
Да |
|
Эрлотиниб |
36,2 ч |
95 % |
10 % |
Да |
|
Этопозид |
1,5–7 ч |
90–95 % |
40–60 % |
Нет |
Примечание. * – ЛВ, которые по фармакокинетическим параметрам являются перспективными для разработки средств направленного транспорта.
константы позволяют достичь в камере 1 более высокой концентрации ЛВ по сравнению с камерой 2 и сохранять ее таковой в течение некоторого времени. Полученный результат соответствует целям направленного транспорта, так как позволяет повысить доставку ЛВ в ткань-мишень и уменьшить в других тканях, что увеличивает эффективность терапии и снижает вероятность развития побочных эффектов.
Так как через некоторое время после введения концентрации ЛВ в камерах 1 и 2 выравниваются, то для целей направленного транспорта имеет смысл оценить соотношение концентраций ЛВ в этих камерах ( C 1 / C 2 ). Изменение этого соотношения в зависимости от времени при вариации констант представлено на рис. 2. С нашей точки зрения, направленный транспорт ЛВ имеет смысл тогда и только тогда, когда соотношение C 1 / C 2 больше единицы.
Из приведенных рисунков можно сделать следующий вывод. Разница C 1 / C 2 тем дольше сохраняется по времени, чем больше значения kэл , меньше значения кд , к 1 , к 2 и больше отношение к 1 ’ к к 1 ”. То есть ЛВ должно обладать следующими свойствами для того, чтобы имело смысл разрабатывать его направленные формы:
-
- Медленное выведение из тканей (т.е. способность накапливаться в них).
– Быстрое выведение из организма (хотя бы одна из фаз выведения). Заметим, что при построении системы уравнений (1) мы предполагали, что выведение ЛВ - простой процесс, пропорциональный его концентрации. На самом деле из-за поступления и накопления ЛВ в ткани динамика убывания Ссв будет описываться, как минимум, двумя экспонентами. Как показывает численный эксперимент, для целей увеличения соотношения C 1 / C 2 достаточно, чтобы кэл первой фазы было достаточно велико. Это эквивалентно требованию малой величины времени полувыведения первой фазы ЛВ из крови (не более нескольких часов).
-
– Медленное поступление в ткани свободной формы.
– Стабильность получаемого конъюгата ЛВ с носителем. Не имеет смысла использовать для таргетной терапии нестабильные конъюгаты. Увеличение kд приводит к снижению соотношения C/C 2.
В соответствии с приведенными фармакокинетическими параметрами нами был проведен скрининг противоопухолевых ЛВ, чтобы выявить, для каких из них имеет смысл разрабатывать средства направленной доставки (таблица). Как следует из данных, приведенных в таблице, таковыми могут быть азацитидин, амифостин, апротинин, бендаму-стин, бусульфан, гентацабин, гидроксимочевина, даунорубицин, имидазол, доксорубицин, доцетаксел, кармустин, 6-меркаптопурин, ормустин, оксиплатин, паклитаксел, пеметрексед, нимустин, нитромедазолмочевина, тегафур, темозоломид, топотекан, трабектидин, цисплатин, цитозин, флу-дарабин фосфат, фотомустин.
Заключение
Разработка средств направленного транспорта ЛВ – задача медицины будущего. Она позволяет снизить затраты на разработку новых лекарственных препаратов; уменьшить время, необходимое для их разработки; повысить ценовую доступность лекарственной терапии для потребителя и, наконец (что самое главное), повысить эффективность проводимой терапии при снижении потенциального риска развития ее осложнений [23].
В онкологической практике, несмотря на развитие методов ранней диагностики, хирургии, радиотерапии, лазерной терапии, таргетной терапии и т. д., химиотерапия вряд ли потеряет свою актуальность в ближайшее время. В этой связи разработка новых противоопухолевых препаратов является одной из актуальных задач современной консерва- тивной онкологии. При всей значимости процесса поиска новых соединений с противоопухолевой активностью возможности «старых» средств исчерпаны далеко не полностью. Направленный транспорт противоопухолевых средств может подарить им «вторую жизнь» в клинике [24].
Список литературы Моделирование направленного транспорта лекарственных веществ. Часть I. Однократное введение
- Ивонин А.Г., Пименов Е.В., Оборин В.А., Девришов Д.А., Копылов С.Н. Направленный транспорт лекарственных препаратов: современное состояние вопроса и перспективы. Известия Коми научного центра УрО РАН. 2012; 9: 46-55.
- Березов Т.Т., Яглова Н.В., Дмитриева Т.Б., Жирков Ю.А., Чехонин В.П. Направленный транспорт лекарственных средств с помощью липосом. Вестник Российской академии медицинских наук. 2004; 5: 42-47.
- Санжаков М.А., Игнатов Д.В., Кострюкова Л.В., Дружиловская О.С., Медведева Н.В., Прозоровский В.Н., Ипатова О.М. Изучение свойств лекарственных композиций доксорубицина в составе коллоидных наночастиц с адресным фрагментом в экспериментах in vivo. Биомедицинская химия. 2016; 62 (2): 150-153.
- Яббаров Н.Г., Посыпанова Г.А., Воронцов Е.А., Попова О.Н., Северин Е.С. Направленный транспорт доксорубицина: система доставки на основе pamam дендримеров. Биохимия. 2013; 78 (8): 1128-1140.
- Пятаев Н.А., Гуревич К.Г., Заборовский А.В., Кокорев А.В., Минаева О.В., Зырняева Н.А., Кладиев А.А., Бычковский П.П., Ревмтович М.Ю. Эффективность комбинации свободной и полимерсвязанной форм проспидина с доксорубицином у крыс с асцидной гепатомой Зайдела. Химико-фармацевтический журнал. 2014; 48 (11): С.18-22


