Модифицированная коллаген-ламининовая матрица в лечении ожоговой болезни. Клинический пример
Автор: Саганов Владислав Павлович, Бутуханов Сергей Борисович, Балханов Юрий Содномович, Башкуев Булат Романович, Хитрихеев Владимир Евгеньевич
Журнал: Вестник Бурятского государственного университета. Медицина и фармация @vestnik-bsu-medicine-pharmacy
Статья в выпуске: 3, 2019 года.
Бесплатный доступ
Значительное улучшение результатов отделения гнойной хирургии ГАУЗ«РКБСМП им. В. В. Ангапова» в лечении обожженных стало возможно благодаря разработке и внедрению Байкальским центром биотехнологий модифицированной коллаген-ламининовой матрицы (аналог живой кожи) в клиническую практику. МИП «Байкальский центр биотехнологий» образован на базе медицинского центра «Диамед» и ФГБОУ ВО «Бурятский государственный университет им. Д. Банзарова». В состав аналога живой кожи входят биологически активные вещества коллаген и ламинин - производные клеток кожи. Коллаген обладает и лечебным свойством. Ламинин воспроизводят клетки, которые затем ликвидируются. Ранозаживляющий материал по сравнению с аналогами не содержит чужеродные клетки, отличается простотой изготовления, длительностью срока хранения не менее 12 месяцев.В исследуемой работе отражены положительные результаты лечения пациентов с последствиями термических травм в отделении гнойной хирургии БСМП им. В. В. Ангапова г. Улан-Удэ в 2018 г. Основой лечения являлась аллопластика с применением модифицированной коллаген- ламининовой матрицы.Внедрение биотехнологических методов восстановления кожных покровов способствовало ускоренному выздоровлению пациентов с термическойтравмой и проведению более ранней реабилитации с последующим снижением инвалидизации.
Коллаген, ламинин, живая кожа, термическая травма, аллопластика, биотехнологический метод, ранняя реабилитация
Короткий адрес: https://sciup.org/148316826
IDR: 148316826 | УДК: 617-089.844 | DOI: 10.18101/2306-1995-2019-3-3-14
Modified collagen-laminin matrixin the treatment of burn disease. Clinical example
A significant improvement in the results of treating the burned in the Department of Purulent Surgery GAU "RK BSMP V. V. Angapova", became possible due to the development and implementation of MIP "Baikal center of biotechnology" in the clinical practice of Modified collagen-laminin matrix (analogue of "natural skin"). MIP "Baikal center of biotechnology" was formed through the joint work of the medical center "Diamed" and Buryat State University named after D. Banzarov. The composition of the analogue of the natural skin has biologically active substances-derivatives of skin cells: collagen and laminin. Collagen has a therapeutic factor. Laminin reproduces cells, which are then eliminated. The wound-healing material, in comparison with analogues, does not contain foreign cells, it differs in comparative simplicity of production and duration of storage - not less than 12 months.The study presents positive results of treatment of patients with the consequences of thermal injuries in the Department of Purulent Surgery GAU RK BSMP named after V. V. Angapova, Ulan-Ude in 2018. The basis of treatment was alloplasty using a modified collagen-laminin matrix. The introduction of biotechnological methods of skin restoration allowed accelerated recovery of patients with thermal trauma and earlier rehabilitation with subsequent reduction of disability.
Текст научной статьи Модифицированная коллаген-ламининовая матрица в лечении ожоговой болезни. Клинический пример
Ожоги представляют глобальную проблему в области здравоохранения. В мире ежегодно происходит 195 000 случаев смерти от ожогов [1]. На протяжении последних трех десятилетий частота ожогов во всем мире непрерывно возрастает. По данным Всемирной организации здравоохранения, термические поражения занимают третье место среди прочих травм [2]. Это объясняется высокой энерговооруженностью современного производства, транспорта, широким использованием токов высокого напряжения, агрессивных химических жидкостей и взрывоопасных газов. По данным отечественных авторов, ожоги формируют 8 - 12% общего травматизма [3].
Несмотря на определенные успехи, достигнутые за последние годы в лечении пациентов с обширным ожогом, проблема термических поражений сохраняет свою актуальность. Необходимость дальнейшего изучения всех ее аспектов связана с тем, что число пострадавших от ожогов во всем мире, особенно в промышленно развитых странах, неуклонно растет, а результаты их лечения оставляют желать лучшего [4].
Основной целью при лечении обожженных пациентов является максимально быстрое восстановление целостности кожного покрова [5]. Однако при обширных глубоких ожогах, поражающих более 30% поверхности тела, возникает дефицит донорских ресурсов кожи и в совокупности с развитием осложнений травмы часто приводит к летальному исходу [6]. В связи с этим актуальность развития, область применения и процесс внедрения модифицированной коллаген-ламининовой матрицы в современные методы лечения высока, так как она не содержит человеческих клеток, тем самым не противоречат современному законодательству и в разы уменьшает риски развития осложнений, патологических реакций организма [7].
Материал и методы
Модифицированная коллаген-ламининовая матрица (аналог живой кожи) — результат деятельности Байкальского центра биотехнологий, созданного на базе медицинского центра «Диамед» и Бурятского государственного университета им. Д. Банзарова.
Аналог «живой кожи» — это тонкая пленка, в основе которой лежат коллаген и ламинин. В состав данного продукта не входят донорские человеческие клетки. Представляет собой прозрачную желеобразную пленку различной величины, помещенную в чашку Петри (рис. 1).
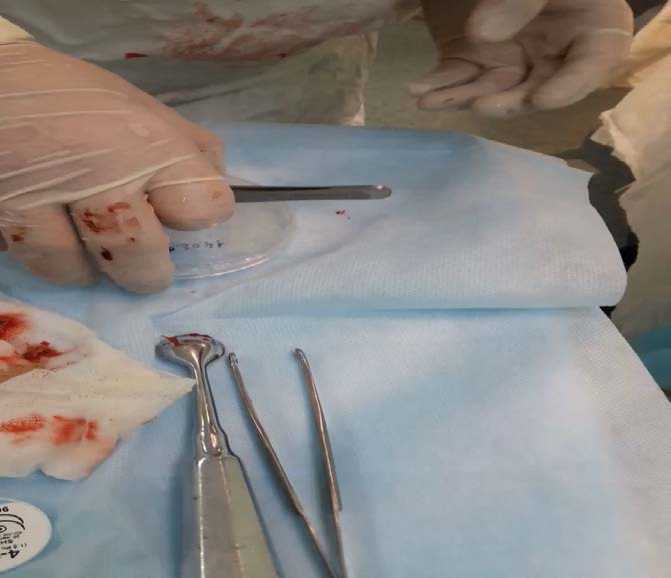
Рис. 1. Аналог «живой кожи» перед применением
Материалом аналога «живой кожи» служит соединительная ткань (сухожилия) лабораторных крыс. Коллаген — самый распространенный белок в нашем теле, основной компонент соединительных тканей, который в том числе входит в состав кожи. Коллаген выполняет ряд важных функций, включая обеспечение кожи структурой и упругостью. Ламинин, в свою очередь, стимулирует и ускоряет физиологический процесс заживления ран. Данный продукт может сохранять свои свойства до 12 месяцев. Материал может быть использован не только при лечении ожоговых ран, но и при отморожениях, трофических язвах, длительно незаживающих ранах, пролежнях.
Аллопластика модифицированной коллаген-ламининовой матрицей использована при лечении пациента с последствием термического ожога правого плеча и области плечевого сустава, полученного в июле 2018 г. и имевшего характер вялогранулирующих, длительно незаживающих постожоговых ран.
Материал хранился в соответствующих условиях, рекомендованных биотехнологами. Пациенту проводилась аллопластика «живой кожи» в условиях операционной и в связи с риском инфицирования проводилось ведение ран закрытым методом на протяжении от 2-х до 4-х суток. Максимальная площадь закрытия дефектов кожного покрова составила 3%.
Результаты
Пациент Г., 14.04.1965 г. р., поступил в ОГХ БСМП им. В. В. Ангапова с диагнозом: последствия термического ожога от июля 2018 г. Осложнения: Вялогранулирующие постожоговые раны правого плеча и области правого плечевого сустава.
Из анамнеза: пациент получил ожог кипятком в быту в июле 2018 г. Находился на лечении в ОГХ БСМП, где проводилось консервативное и оперативное лечение путем некрэктомии и аутодермопластики. Частично ожоговые раны имели признаки спонтанной эпителизации. Выписан на медицинскую паузу. В течение последних семи суток, перед повторной госпитализацией для этапного оперативного лечения, отмечаются повышение температуры тела и слабость.
Локально: в области плечевого сустава и правого плеча имелись постожоговые вялогранулирующие раны площадью до 3%, с налетом фибрина и серозным отделяемым. Повторно госпитализирован в ОГХ для этапного оперативного лечения с целью закрытия оставшегося дефекта кожного покрова. Проводились:
-
• консервативное лечение (антибактериальная терапия: р-р Цефтриаксона 2,0 два раза, р-р Метрогила 100,0 три раза); инфузионная, обезболивающая и симптоматическая терапия, ежедневная санация раневой поверхности растворами антисептиков;
-
• оперативное лечение: 23.10.18 г. — расширенная перевязка вялограну-лирующих ран под общим обезболиванием; 24.10.18 г. — пластика вялограну-лирующих ран модифицированной коллаген-ламининовой матрицей. В послеоперационном периоде признаков лизиса аутотранплантата не было;
-
• бактериологические анализы раневого отделяемого в динамике: от 24.10.18 г. — еnterobacter hormaechei-pseudomonasaeruginosa. Чувствительность к антибиотикам: амикацин-S, цефоперазон/сульбактам-S, цифтазидим-R, имипе-нем/циластатин-S, меропенем-S; от 26.10.18 г. — роста нет; от 29.10.18 г. — enterobacter hormaechei 10^5: амикацин-S, ципрофлоксацин-R, цефотаксим-R, цефоперазон/сульбактам-S, цефтриаксон-R, цефепим-I, имипенем/циластатин-S, меропенем-S; от 30.10.18 г. — acinetobacter baumannii 10л5-1; enterobacter cloacae ssp. 10Л5-2: амикацин — 1-R, 2-S; ципрофлоксацин —1-R, 2-R; цефотаксим-2-R; цефоперазон/сульбактам — 1-R, 2-S; цефтриаксон — 2-R; цефепим-1-R; имипе-нем/циластатин — 1-R, 2-S; меропенем — 1-R, 2-S.
-
7 ноября 2018 г. после полного приживления трансплантанта пациент выписан на дальнейшее наблюдение и лечение у хирурга поликлиники по месту жительства.
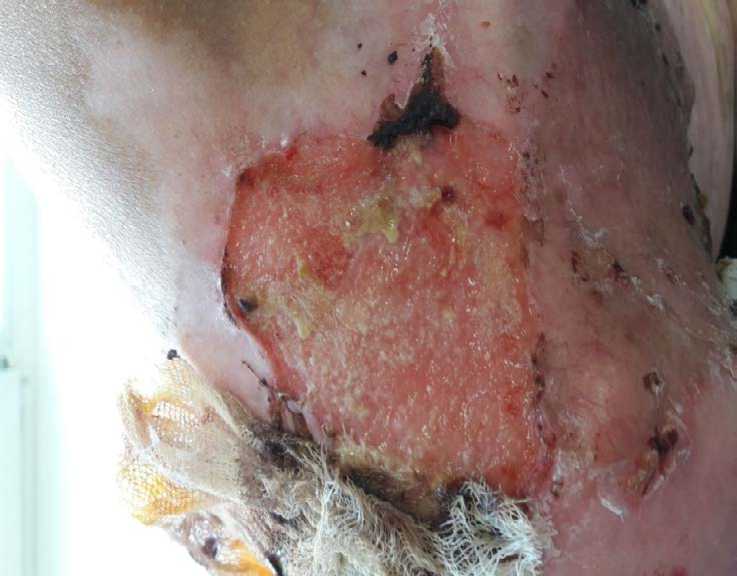
Рис. 1. Первые сутки после пересадки «живой кожи»
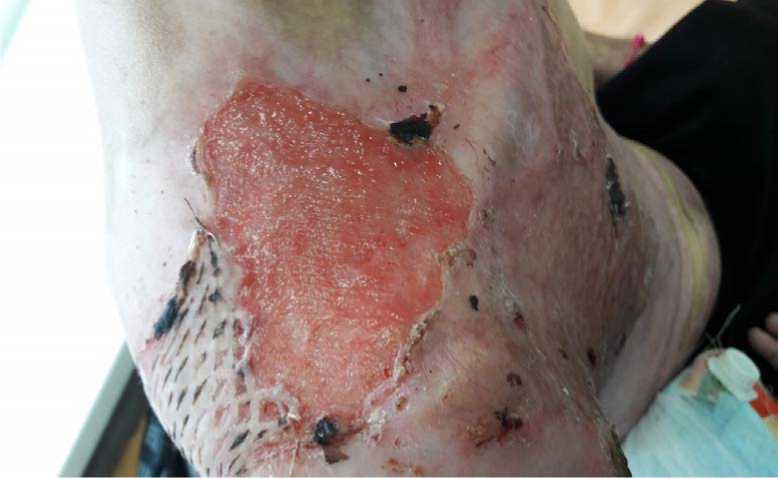
Рис. 2. Третьи сутки
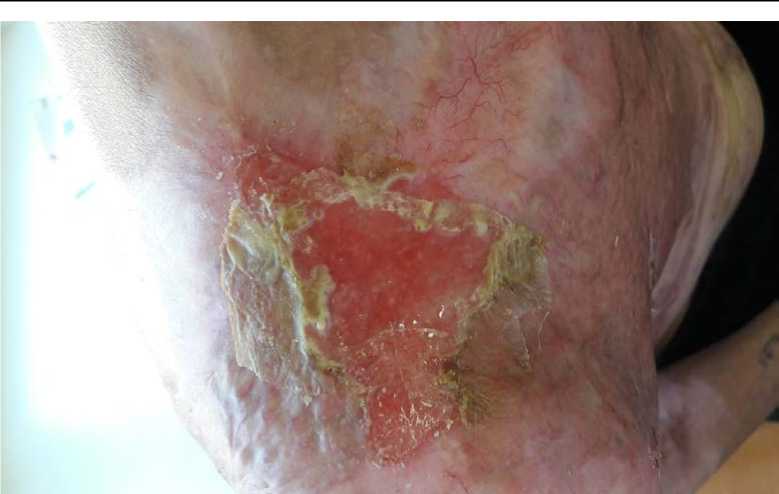
Рис. 3. Седьмые сутки
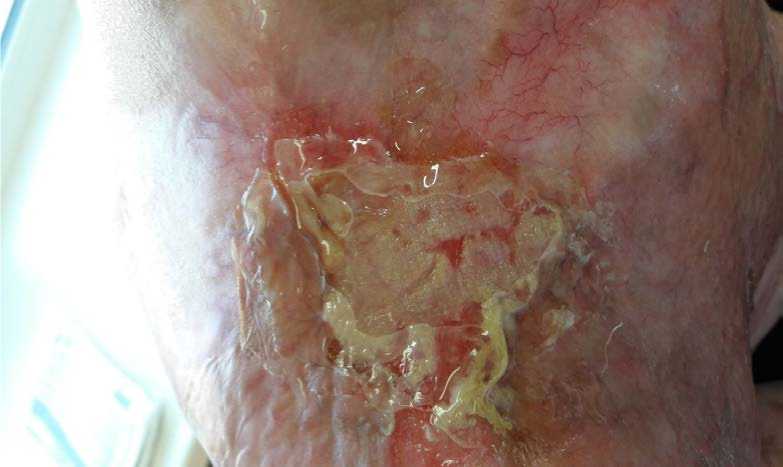
Рис. 4. Десятые сутки
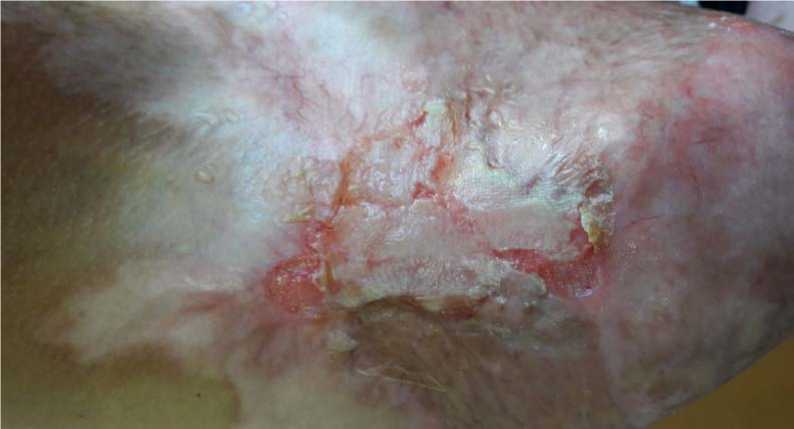
Рис. 5. Четырнадцатые сутки
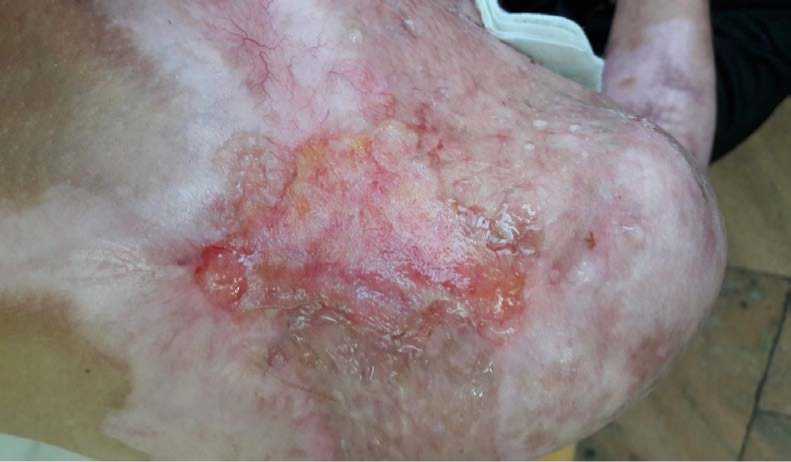
Рис. 6. Двадцатые сутки
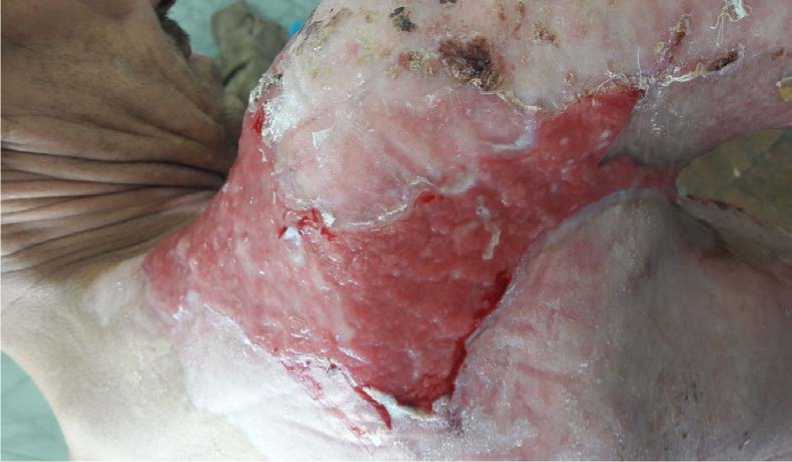
Рис. 7. Больной Г. в начале лечения
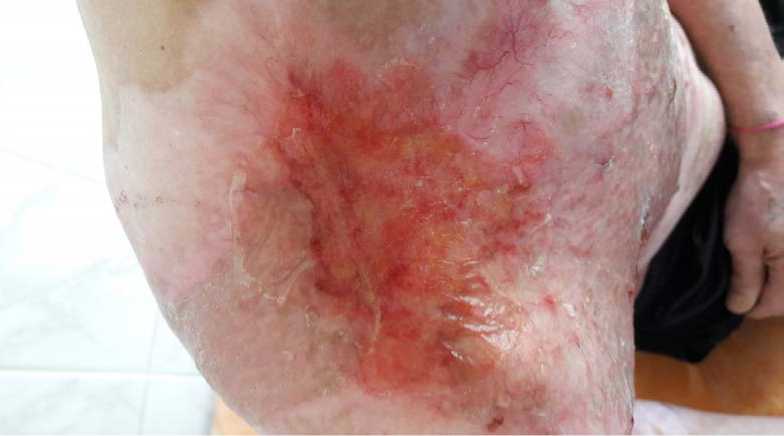
Рис. 8. В конце лечения
Через 6 недель результат оказался положительный.
Таким образом, при аллопластике модифицированной коллагенламининовой матрицей достигается более полное приживление, ускоряется краевая эпителизация даже в присутствии патогенной микрофлоры. Внедрение и совершенствование биотехнологических методов восстановления кожных покровов приведут к качественно новому уровню развития комбустиологии, что, несомненно, приведет к уменьшению смертности при тяжелых ожогах, уменьшению случаев инвалидизации, ускорению выздоровления и ранней реабилитации.
Список литературы Модифицированная коллаген-ламининовая матрица в лечении ожоговой болезни. Клинический пример
- Абаев Ю. К. Биология заживления острой и хронической раны // Медицинские новости. 2003. № 6. С. 3-10.
- Алексеева Н. Т., Глухов А. А., Остроушко А. П. Роль клеток фибропластического дифферона в процессе заживления ран // Вестник экспериментальной и клинической хирургии. 2012. Т. 5, № 3. С. 601-608.
- Аничков И. П., Волкова К. Г., Гаршин В. Г. Морфология заживления ран. М.: Медгиз, 1951. 123 с.
- Болдырев А. А., Кяыйвяряйнен Е. И., Илюха В. А. Биомембранология: учебное пособие для студентов высших учебных заведений, специализирующихся в области биологии, медицины и психологии. Петрозаводск: КНЦ РАН, 2006. 225 с.
- Глухов А. А., Аралова М. В. Патофизиология длительно незаживающих ран и современные методов стимуляции раневого процесса // Новости хирургии. 2015. Т. 23, № 6. С. 673-679.
- Клиническая хирургия: национальное руководство: в 3 т. / под ред. В. С. Савельева, А. И. Кириенко. М.: ГЭОТАР-Медиа, 2008. Т. 1. 864 с.
- Копылов В. А., Никитенко И. Е. Применение фактора роста фибробластов в медицине // Вестник ОГУ. 2010. № 4. C. 95.


