Модификация противоопухолевой химиотерапии антиоксидантными препаратами в эксперименте
Автор: Зорькина А.В., Скопин П.И.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 1 (43), 2011 года.
Бесплатный доступ
Комбинированное применение препаратов антиоксидантного действия - эмоксипина и α-токоферола ацетата - с про- тивоопухолевыми лекарственными средствами (циклофосфан, 5-фторурацил, рубомицин) на модели перевиваемого рака крыс РС-1 выявило снижение показателей интоксикации в организме опухоленосителей, ограничение лейкопении и актив- ности процессов перекисного окисления липидов в тканях печени и почек. В опухолевой ткани в этих условиях наблюдался рост содержания малонового диальдегида и угнетение антиокислительной активности. Эмоксипин (17 мг/кг, 25 мг/кг) повысил индекс торможения роста опухоли циклофосфаном, 5-фторурацилом и рубомицином при комбинированном при- менении в условиях роста холангиоцеллюлярного рака РС-1 в эксперименте в большей степени, чем α-токоферола ацетат в изомолярных дозах.
Противоопухолевая химиотерапия, перекисное окисление липидов, эмоксипин, перевиваемый холангиоцеллюлярный рак рс-1
Короткий адрес: https://sciup.org/14055878
IDR: 14055878 | УДК: 615.277.3+577.115]-092.9
Modification of antitumor therapy with antioxidant drugs in experimental studies
We investigated ability of broad spectrum antioxidants - emoxipinum (3-oxy-6-metyl-2-etyl-piridin hydrochloridum) and alphatocopheryl acetate, to control the oxidative damage induced by some antitumor drugs (cyclophosphamide, 5-fluorouracil, rubomycine). Studies were performed on rats with transplantable cholangiocellular RS-1 carcinoma. Biochemical methods were used for this investigation. The rats that were subjected to combination antioxidants and antitumor drug had normalized of lipid peroxidation in the liver and renal tissue compared the group treated with antitumor drug only. Also, emoxipinum inhibited chemotherapy-induced leucopenia. The activity of tumor antioxidative enzymes was significantly decreased and tumor malondialdehyde (MDA) level was increased in the study group compared to the group only treated with antitumor drug (р
Текст научной статьи Модификация противоопухолевой химиотерапии антиоксидантными препаратами в эксперименте
Современная интенсивная противоопухолевая химиотерапия сопровождается многочисленными побочными эффектами. Образующиеся на фоне противоопухолевой химиотерапии, в организме больного свободные радикалы и инактивация ферментов антиоксидантной защиты усиливают интоксикацию, вызывают токсическое повреждение клеток внутренних органов и зачастую оказываются лимитирующим фактором для продолжения лечения [9, 13]. Также важно учитывать, что химиотерапия проводится у больных в условиях уже активированных злокачественной опухолью процессов перекисного окисления липидов (ПОЛ) [8, 11, 15].
Относительно взаимодействия противоопухолевых препаратов и веществ с антиоксидантной активностью в литературе имеются многочисленные, но довольно противоречивые сведения. Большинство авторов указывают на способность антиоксидантов улучшать переносимость химиотерапии и отдаленные результаты лечения [7, 12, 14, 16], сторонники иной точки зрения считают, что антиоксиданты ингибируют противоопухолевый эффект химиопрепаратов [10]. Однако все эти исследования касаются применения нутрицевтиков с мягким антиоксидантным действием (β-каротин; витамины А, С, Е; селен; мелатонин, цистеин; витамины группы В; витамин D3; витамин K3; глютатион, коэнзим Q10).
Целью исследования явилось изучение воздействия отечественного синтетического производного 3-оксипиридина с мощным антиоксидантным действием – эмоксипина – на эффективность и токсичность некоторых противоопухолевых препаратов в условиях роста холангиоцеллюлярного рака РС-1.
Материал и методы
На 228 белых нелинейных крысах мужского пола с перевиваемой опухолью – холангиоцел-люлярным раком крыс РС-1 (НИИ экспериментальной диагностики и терапии опухолей РОНЦ им. Н.Н. Блохина РАМН) проведено изучение возможности применения синтетических препаратов антиоксидантного действия на фоне противоопухолевой химиотерапии. Для проведения эксперимента использованы следующие фармакологические препараты: эмоксипин (ФГУП «Московский эндокринный завод») в ампулах по 1 мл 1 % раствора, α-токоферола ацетат – 10 % масляный раствор в ампулах (АО «АЙ СИ ЭН ОКТЯБРЬ», г. Санкт-Петербург). В качестве препарата сравнения при исследовании корригирующего влияния антиоксидантов на процессы ПОЛ в организме опухоленосителя нами применялся α-токоферола ацетат, так как он обладает доказанным наибольшим антиоксидантным действием из всех веществ природного происхождения [1].
Для моделирования курса противоопухолевой химиотерапии использованы препараты, наиболее широко применяемые в клинической практике, с разным механизмом противоопухолевого действия: циклофосфан – противоопухолевый препарат из группы алкилирующих цитостатиков (ОАО «Биохимик», г. Саранск) во флаконах по 200 мг сухого вещества (растворялся в стерильном 0,9 % растворе натрия хлорида), в дозе 20 мг/кг, внутримышечно (в/м), через день № 5; 5-фторурацил – цитостатик из группы антиметаболитов нуклеинового обмена, по 10 мг/кг внутримышечно через день № 5; рубо-мицин – противоопухолевый антрациклиновый антибиотик (ЗАО «Брынцалов-А», г. Москва) во флаконах по 20 мг сухого вещества (растворялся в стерильном 0,9 % растворе натрия хлорида) в дозе 4 мг/кг, внутрибрюшинно через день № 4.
Эмоксипин вводился внутримышечно в дозах 3,4, 6,8, 17, 25 мг/кг – условно соответствующих 1 % от LD50, 2, 5 и 8 % от LD50; α-токоферола ацетат применялся в/м в дозах 9,5, 19, 47,5 мг/кг, изомолярно соответствующих изучаемым дозам эмоксипина (3,4; 6,8 и 17 мг/кг). У трех групп моделировалась противоопухолевая химиотерапия циклофосфаном, 5-фторурацилом и рубо-мицином, а также изучались комбинации этих цитостатиков с α-токоферола ацетатом в дозе 47,5 мг/кг и эмоксипином 17 и 25 мг/кг. Корригирующие препараты вводились с 21 по 35-е сут роста опухоли ежедневно; интактную группу составили 12 животных, животным контрольной группы вводился физиологический раствор в/м. Животных всех опытных серий забивали путем декапитации под эфирным наркозом на 35-е сут после перевивки опухолевого штамма.
В плазме крови, эритроцитах, гомогенатах печени, почек, ткани сердца и кишечника, а также ткани опухоли определяли содержание вторичного продукта перекисного окисления липидов – малонового диальдегида (МДА) и железом индуцированного МДА (Fe-МДА) (Конюхова С.Г., 1989), рассчитывали антиокислительную активность (АОА) (Клебанов Г.И., 1999), определяли активность ферментов антиокислительной защиты – каталазы (Королюк М.А., 1988) и супероксиддисму-тазы (СОД) по методу С. Чевари (1981) [3–6]. Для оценки изменений в метаболическом звене гомеостаза определяли уровень креатинина, мочевины, активность АлТ и АсТ, содержание глюкозы, молекул средней массы (МСМ), общую (ОКА) и эффективную (ЭКА) концентрации альбумина. По полученным значениям ЭКА, ОКА и МСМ рассчитывали: резерв связанного альбумина (РСА), индекс токсичности (ИТ) и критерии интоксикации (КИ) [2]. Производили общий анализ крови, рассчитывали индекс лейкоцитарной интоксикации (ИЛИ). Оценивали массу животных-опухоленосителей, массу и индекс массы опухоли (ИМО), рассчитанный как отношение массы опухоли к массе животного. Противоопухолевый эффект оценивали по индексу торможения роста опухоли (ИТРО): ИТРО = 100 – (средняя mконтр/mопыт×100), где средняя mконтр – средняя масса опухоли в контрольной группе, mопыт – масса опухоли в опытной группе.
Статистическую обработку проводили с использованием критерия Стьюдента (t). Изменения считали статистически значимыми при р<0,05.
Результаты и обсуждение
Рост холангиоцеллюлярного рака РС-1 в организме животных сопровождался резким усилением процессов ПОЛ на фоне выраженного истощения антиоксидантной защиты организма-опухоленосителя по сравнению с интактными животными. Это проявлялось повышением содержания вторичных продуктов ПОЛ – МДА и Fe-МДА в плазме крови, тканях печени и почек, угнетением активности каталазы и СОД в плазме крови и ткани печени. На фоне роста опухоли отмечено снижение ЭКА на 75 % (р<0,001), снижение РСА – на 64 % (р<0,001) и увеличение индекса токсичности в 5 раз (р<0,001). Увеличение СОЭ произошло в 4,6 раза (р<0,001) по сравнению с уровнем интактных животных. В плазме крови происходило значительное увеличение содержания молекул средней массы, мочевины и креатинина, развивались гипогликемия, анемия и лейкопения.
Полученные результаты полностью согласуются с литературными данными, по которым на фоне роста опухоли в организме происходит смещение прооксидантно-оксидантного равновесия, развивается дефицит антиоксидантных ферментов первой линии защиты – СОД, глутатионпероксидазы и каталазы [11, 15]. Подобное состояние объясняют развивающимся гипогликемическим давлением опухоли на метаболизм нормальных тканей, что, в свою очередь, приводит к мобилизации тканями в качестве энергетических ресурсов жирных кислот. Данное обстоятельство плюс развивающаяся на фоне роста опухоли тканевая гипоксия приводят к выраженному усилению процессов ПОЛ в организме.
При противоопухолевом лечении дефицит антиоксидантных ферментов усугубляется, в ряде случаев отмечается истощение механизмов антиоксидантной защиты, что приводит к снижению резистентности организма и к повреждению жизненно важных органов и систем. В нашем эксперименте применение химиопрепаратов вызывало торможение роста опухоли, так, при введении циклофосфана ИТРО составил 40,2 %, при использовании рубомицина ИТРО – 33,5 ± 7,05 %. В условиях применения 5-фторурацила ИМО уменьшился на 45 % (р<0,05). В связи с уменьшением опухолевой массы под влиянием цитостатиков в организме опухоленосителей несколько ограничивались показатели эндотоксикоза – наблюдалось снижение содержания МДА во внутренних органах, повышение РСА, снижался уровень гипогликемии, однако происходило усиление лейкопении, сохранялось угнетение АОА в крови и внутренних органах. Отрицательные эффекты специфического противоопухолевого лечения диктуют необходимость поиска и разработки новых подходов для получения оптимального лечебного эффекта при уменьшении токсических эффектов цитостатической терапии.
При комбинированном применении противоопухолевых химиопрепаратов и α-токоферола ацетата не происходило изменений весовых показателей опухоли по сравнению с таковыми у животных, получавших только цитостатик, и сохранялись изменения процессов ПОЛ, вызванные введением противоопухолевых препаратов. Кроме того, в крови животных и в тканях внутренних органов происходило усиление активности каталазы, повышение АОА по сравнению с уровнем этих показателей у животных, получавших монотерапию цитостатиками. В ткани опухоли применение циклофосфана с α-токоферола ацетатом проявилось ростом уровня МДА на 36 % (р<0,05) по сравнению с этим показателем у животных, получавших монотерапию циклофосфаном. Кроме того, происходило снижение содержания в плазме крови МСМ, увеличение количества лейкоцитов и содержания гемоглобина по сравнению с показателями у животных, получавших монотерапию цитостатиками. Таким образом, комбинация α-токоферола ацетата в максимальной из изученных доз – 47,5 мг/кг, не уменьшая противоопухолевую эффективность цитостатиков, несколько ограничивала показатели эндотоксикоза в организме исследуемых животных.
При комбинированном использовании противоопухолевых препаратов и эмоксипина отмечено усиление противоопухолевого эффекта цитостатиков. Это наблюдалось при введении эмоксипина в дозах 17 и 25 мг/кг (табл. 1). Так, у животных, получавших комбинацию циклофос-фана и эмоксипина в дозе 17 мг/кг, масса опухоли уменьшилась на 44 % (р<0,01) по сравнению с животными, получавшими только циклофосфан.
Индекс массы опухоли в этой группе был на 73 % (р<0,001) ниже контрольного уровня, а индекс торможения роста опухоли составил 66,3 %. Введение эмоксипина в дозе 17 мг/кг на фоне применения рубомицина способствовало снижению массы опухоли на 39 % и на 55 % – при использовании эмоксипина в дозе 34 мг/кг, при этом индекс массы опухоли уменьшился на 50 % и 63 % соответственно в сравнении с группой животных, получавшей рубомицин.
Применение эмоксипина на фоне моделирования химиотерапии холангиоцеллюлярного рака оказывало выраженное дезинтоксикаци-онное действие на организм опухоленосителей: наблюдалось увеличение ОКА и ЭКА, снижение концентрации МСМ в плазме крови, уменьшение критериев интоксикации, нормализация активности АлТ и АсТ, снижение содержания креатинина, а также увеличение содержания лейкоцитов и концентрации гемоглобина по отношению к уровню показателей у животных, получавших цитостатик в режиме монотерапии (рис. 1). Комбинация циклофосфана с эмоксипи-ном в дозах – 3,4 и 6,8 мг/кг вызывала умеренное ограничение процессов ПОЛ в организме опу-холеносителя, с увеличением дозы эмоксипина до 17 мг/кг выраженность эффектов нарастала, и при использовании максимальной из изученных доз (25 мг/кг), наблюдался наибольший корригирующий эффект.
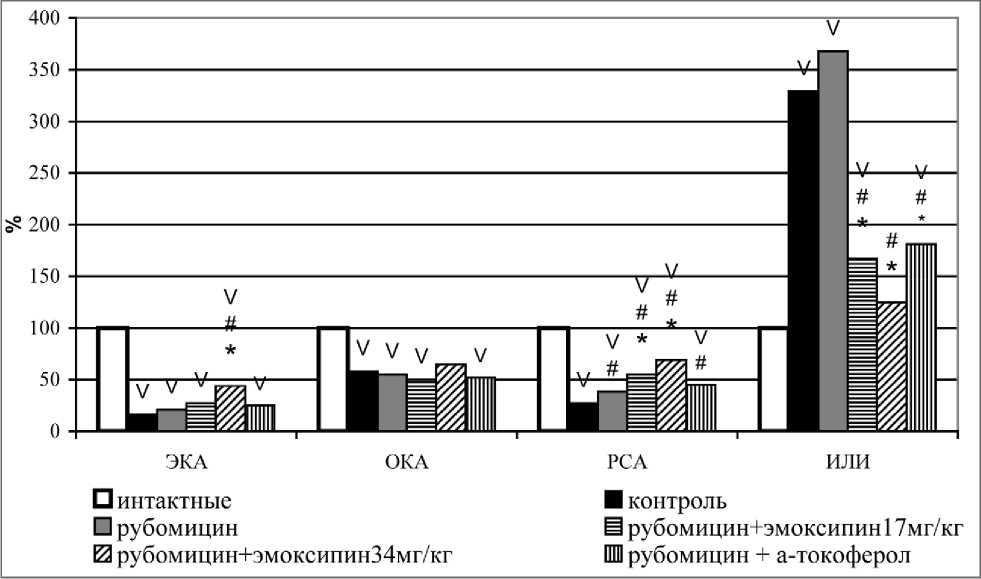
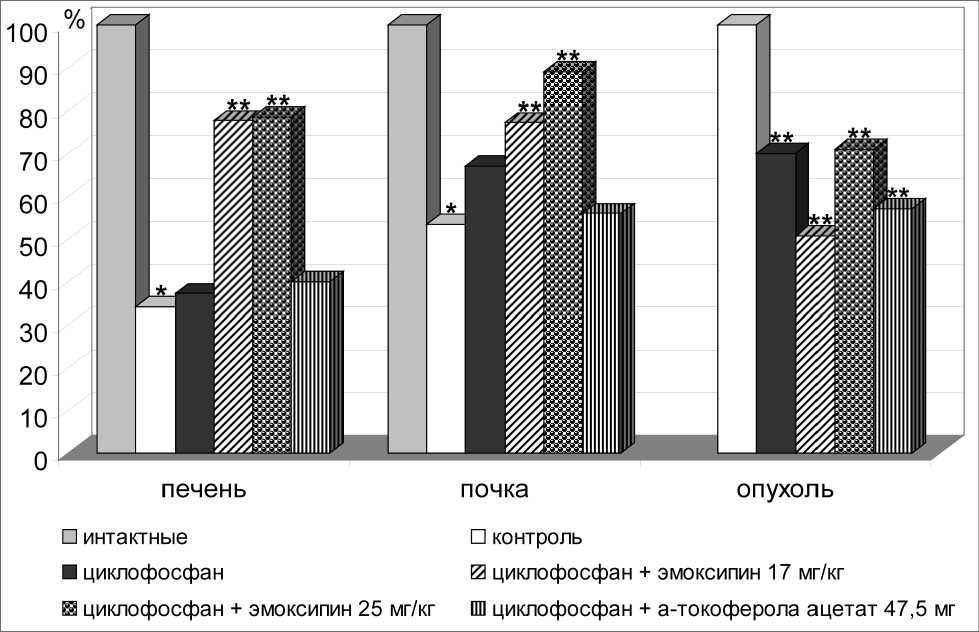
Рис. 1. Влияние комбинированного применения рубомицина с эмоксипином и α-токоферолом на некоторые показатели эндогенной интоксикации (в % к данным интактной группы животных, v – достоверность различия р<0,05 с данными интактной группы, # – достоверность различия р<0,05 с данными контрольной группы, * – достоверность различия р<0,05 с данными группы, получавшей рубомицин)
Рис. 2. Влияние эмоксипина и α-токоферола ацетата на антиокислитель-ную активность (в %) в органах экспериментальных животных и ткани холан-гиоцеллюлярного рака РС-1 в условиях моделирования химиотерапии циклофос-фаном в дозе 20 мг/кг. * – достоверность отличия с данными интактной группы, р<0,05; ** – достоверность отличия с данными контрольной группы, р<0,05
Таблица 1
Влияние α-токоферола ацетата и эмоксипина в комбинации с циклофосфаном на весовые характеристики холангиоцеллюлярного рака РС-1 (М±m)
|
Группы животных |
Масса крысы с опухолью, г |
Масса крысы без опухоли, г |
Масса опухоли, г |
Индекс массы опухоли |
ИТРО |
|
Контроль |
140,0 ± 16,41 |
105,3 ± 12,67 |
37,54 ± 7,05 |
30,85 ± 1,54 % |
- |
|
Циклофосфан 20 мг/кг |
188,3 ± 21,04 р>0,05 |
155,6 ± 12,35 р<0,05 |
22,47 ± 2,61 р>0,05 |
9,42 ± 1,25 % р<0,001 |
40,24 ± 4,73 % |
|
Циклофосфан + эмоксипин 17 мг/кг |
129,2 ± 14,44 р>0,05; р’<0,05 |
114,8 ± 6,79 р>0,05; р’<0,05 |
12,56 ± 1,78 р<0,01; р’<0,01 |
8,47 ± 2,11 % р<0,001; р’>0,05 |
66,31 ± 3,36 % р’<0,001 |
|
Циклофосфан + эмоксипин 25 мг/кг |
138 ± 6,63 р>0,05; р’<0,05 |
125,3 ± 9,72 р>0,05; р’>0,05 |
14,54 ± 1,22 р<0,01; р’>0,05 |
10,27 ± 1,73 % р<0,001; р’>0,05 |
61,13 ± 2,51 % р’<0,01 |
|
Циклофосфан + α-токоферола ацетат 47,5 мг/кг |
172 ± 11,94 р>0,05; р’>0,05 |
152,1 ± 9,41 р<0,05; р’>0,05 |
17,9 ± 2,59 р<0,05; р’>0,05 |
10,5 ± 1,18 % р<0,001; р’>0,05 |
52,46 ± 4,04 % р’>0,05 |
Примечание: р – уровень значимости различий с данными контрольной группы; р’– уровень значимости различий с данными группы «Циклофосфан».
Таблица 2
Влияние применения эмоксипина и α-токоферола ацетата на показатели перекисного окисления липидов в ткани холангиоцеллюлярного рака РС-1 при моделировании химиотерапии циклофосфаном в дозе 20 мг/кг (М±m)
|
Группы животных |
Каталаза, мКат/ с х л |
Fe-MДA, ммоль/л |
MДA, ммоль/л |
AOA, ммоль/л |
СОД, усл. ед. |
|
Контроль |
0,65 ± 0,07 |
5,381 ± 0,269 |
0,963 ± 0,062 |
4,419 ± 0,267 |
53,759 ± 1,574 |
|
Циклофосфан 20 мг/кг |
0,29 ± 0,04 р<0,001 |
5,53 ± 0,276 р>0,05 |
1,898 ± 0,22 р<0,01 |
3,093 ± 0,301 р<0,01 |
38,814 ± 1,178 р<0,001 |
|
Циклофосфан + эмок-сипин 17 мг/кг |
0,36 ± 0,037 р<0,01; р*>0,05 |
4,46 ± 0,194 р<0,05; р*<0,05 |
2,221 ± 0,209 р<0,001; р*>0,05 |
2,239 ± 0,386 р<0,001; р*>0,05 |
18,019 ± 2,333 р<0,001; р*<0,001 |
|
Циклофосфан + эмок-сипин 25 мг/кг |
0,357 ± 0,075 р<0,05; р*>0,05 |
6,789 ± 0,184 р<0,001; р*<0,001 |
3,646 ± 0,109 р<0,001; р*<0,001 |
3,143 ± 0,247 р<0,01; р*>0,05 |
21,793 ± 2,893 р<0,001; р*<0,001 |
|
Циклофосфан + α-токоферол 47,5 мг/кг |
0,407 ± 0,04 р<0,05; р*>0,05 |
5,108 ± 0,215 р>0,05; р*>0,05 |
2,577 ± 0,142 р<0,001; р*<0,05 |
2,531 ± 0,229 р<0,001; р*>0,05 |
32,825 ± 2,233 р<0,001; р*<0,05 |
Примечание: р – уровень значимости различий с данными контрольной группы; р* – уровень значимости различий с данными группы «циклофосфан».
Так, при использовании эмоксипина в дозе 25 мг/кг на фоне применения циклофосфана в плазме крови содержание МДА уменьшилось на 44 % (р<0,001), АОА увеличилась на 166 % (р<0,001), активность каталазы выросла на 45 % (р<0,001) (рис. 2). В ткани печени на 41 % (р<0,001) уменьшилась концентрация МДА, АОА увеличилась на 111 % (р<0,001). Активность СОД снизилась на 26 % (р<0,05), а активность каталазы выросла на 45 % (р<0,05) по сравнению с уровнем показателей у животных, получавших монотерапию циклофосфаном. Сходные изменения наблюдались и в других внутренних органах, при комбинированном применении 5-фторурацила и эмоксипина 17 мг/кг
МДА в почках снижался на 43 % (р<0,001) по сравнению с данными у животных, получавших только 5-фторурацил, а АОА возросла на 31 % (р<0,01).
В ткани опухоли комбинация противоопухолевых препаратов и эмоксипина, напротив, приводила к активации процессов ПОЛ. Дополнительное применение эмоксипина в дозе 25 мг/кг на фоне терапии 5-фторурацилом вызвало бóльшую активацию процессов ПОЛ в опухолевой ткани, чем 5-фторурацил в виде монотерапии, что проявилось повышением концентрации МДА в ткани опухоли на 35 % (р<0,01). При комбинированном применении эмоксипина в дозе 25 мг/кг и циклофосфана активность СОД в ткани опухоли уменьшилась на 44 % (р<0,001), а содержание МДА выросло на 92 % (р<0,001) (табл. 2). Аналогичный эффект наблюдался при применении рубомицина с эмоксипином. Так, комбинированное применение рубомицина и эмоксипина в дозе 17 мг/кг в опухолевой ткани вызывало угнетение активности каталазы и СОД на 56 % (р<0,005) и 76 % (р<0,05) соответственно (р<0,05). Повышение дозы эмоксипина до 25 мг/кг приводило к еще большему угнетению активности ферментов антиоксидантной защиты, при этом содержание МДА увеличилось на 79 % (р<0,05), а АОА снизилась на 33 % (р<0,01) в сравнении с группой, получавшей только рубомицин.
Таким образом, применение эмоксипина (17 мг/кг, 25 мг/кг) на фоне моделирования химиотерапии холангиоцеллюлярного рака РС-1, во-первых, повысило противоопухолевую эффективность циклофосфана, 5-фторурацила и рубомицина. Во-вторых, эмоксипин в большей степени, чем токоферола ацетат в изомолярных дозах, снижал выраженность нежелательных побочных эффектов противоопухолевых препаратов в условиях роста РС-1, что проявлялось корригирующим воздействием на процессы ПОЛ в тканях печени и почек опухоленосите-лей, ограничением лейкопении. Следует особо отметить, что на фоне применения эмоксипина в ткани опухоли развивалась противоположная картина – усиление окислительных процессов, на фоне снижения активности антиокислитель-ных ферментов. Раскрытие механизма этого феномена требует дальнейших исследований.


