Молекулярно-генетический анализ трансгенных клеточных линий мягкой пшеницы с использованием IRAP ПЦР
Автор: Бавол Андрей Васильевич, Дубровная Оксана Васильевна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Биотехнология
Статья в выпуске: 3-5 т.15, 2013 года.
Бесплатный доступ
Методом IRAP ПЦР с праймером к LTR последовательностям ретротранспозона SIRE1, у трех трансгенных линий мягкой пшеницы обнаружено появление новых, относительно высокомолекулярных (длиной более 1000 п.н.) ампликонов, что свидетельствует о транспозиции данного мобильного элемента. Полученные данные могут служить доказательством того, что индукция транспозиции SIRE 1 обусловлена геномным стрессом, вызванным встраиванием чужеродной ДНК или стрессом, непосредственно связанным с процессом трансформации (микропоранение, культивирование на селективных средах).
Мягкая пшеница, биолистическая трансформация, каллусные линии, ретротранспозон sire 1, irap пцр
Короткий адрес: https://sciup.org/148202042
IDR: 148202042 | УДК: 581.143.6:58.085
Analysis of tranagenic cell lines of bread wheat using IRAP PCR
By IRAP PCR with primers to LTR of SIRE 1 retrotransposon, at the three transformed lines showed the emergence of new, relatively high (more than 1000 bp) amplicons, which indicating of the TE transposition. As new DNA fragments were detected in three of seven studied lines and were absent in the control callus, it may indicate that the induction of transposition SIRE 1 may be due to genomic stress, caused by inserting foreign DNA (plasmid pAHC25) or stress associated with the transformation process (mechanical wounding, cultivation on selective media).
Текст научной статьи Молекулярно-генетический анализ трансгенных клеточных линий мягкой пшеницы с использованием IRAP ПЦР
Технология генетической трансформации имеет большие перспективы в селекции растений для улучшения хозяйственно полезных признаков, в частности урожайности, повышения качества, устойчивости к патогенам и вредителям [1]. Для пшеницы перспективным методом генетической инженерии является биолистическая трансформация, поскольку ткани этой культуры имеют низкую чувствительность к агробактериальной инфекции [2]. На сегодняшний день большинство протоколов получения генетически модифицированных организмов предполагает использование культуры in vitro , в том числе этапы образования каллуса и регенерации растений. Следует учитывать, что при этом может возникать значительное число мутаций, известных под общим названием сомакло-нальной изменчивости [3]. Однако кроме мутагенного эффекта культуры тканей, процесс трансформации сопровождается дополнительным стрессом, связанным как с механическим поранением (при использовании бомбардировки микрочастицами), так и с встраиванием генетической конструкции в геном реципиента [4].
Несмотря на то, что темпы получения и выращивания генетически модифицированных культур постоянно возрастают, все еще остается вопрос насколько точно современные методы генетической инженерии могут обеспечить перенос в геном чужеродных генов и сколько непредсказуемых генетических и эпигенетических эффектов при этом может возникать [5]. Следствием переноса чужеродной ДНК может быть нарушение стабильности генома трансформированного растения, однако данной проблеме уделяется недостаточно внимания, хотя такие исследования связаны не только с фундаментальными вопросами организации и функционирования генома в целом, но также с проблемой безопасности употребления трансгенных растений.
Показано, что интеграция чужеродной ДНК в ядерный геном может вызвать как эпигенетические изменения, в частности изменения уровня метилирования ДНК, так и активацию транскрипции мобильных генетических элементов (МГЭ) [6]. Matzke и сотрудники [7] получили данные, которые убедительно свидетельствуют о том, что в присутствии трансгенов в геноме реципиента наблюдается повышение частоты генетических перестроек и активация МГЭ. Явление транспозиции представляет значительный интерес, поскольку показана его роль как в изменении экспрессии структурных генов, так и индукции хромосомных аберраций [8].
IRAP-анализ (Inter-Retrotransposon Amplified Polymorphism) - метод амплификации геномной ДНК между близко расположенными последовательностями ретротранспозонов. Одним из преимуществ этого метода является возможность одновременного анализа многих локусов в различных участках генома, что особенно важно при культивировании in vitro . Широкое присутствие в геноме растений мобильных генетических элементов и их способность к самостоятельному копированию позволяет методом IRAP-анализа идентифицировать относительно недавние изменения генома, в том числе вызванные действием стрессовых факторов. Одним из мобильных элементов, который используется для анализа генома растений является соевый ретротранспозон SIRE 1, относящийся к семейству Ty1-copia -подобных ретроэлементов. Он присутствует в геноме многих видов растений, в том числе и пшеницы, имеет длину примерно 12 т.п.н. В данной работе был использован праймер, родственный к длинным концевым повторам (LTR-последовательностям) SIRE-1. Этот участок содержит низкокопийные последовательности нуклеотидов и является одним из самых консервативных. Именно поэтому изменения в длине между последовательностями ретротранспозонов, которые можно зафиксировать, как появление/исчезновение или изменение размера IRAP-ампликона, могут служить объективным критерием изменчивости генома.
В связи с этим, целью данной работы был молекулярно-генетический анализ трансгенных клеточных линий мягкой пшеницы с использование IRAP ПЦР с праймером к LTR последовательностям ретротранспозона SIRE 1.
Каллусные культуры были получены из апекса побега 3-суточных стерильных растений пшеницы сорта Зимоярка по разработанной нами методике [9]. Исходный каллус разделяли на 2 части. Одна часть была использована для проведения генетической трансформации, другая параллельно пассировалась на питательной среде МС. Генетическую трансформацию осуществляли биолистическим методом, используя самодельную пушку типа particle inflow gun (PIG). В исследованиях была использована векторная конструкция pAHC25 [10], содержащая селективный ген фосфинотрицин-N-ацетилтрансферазы (bar), который обеспечивает устойчивость к фосфинотрицину и репортерный ген β-глюкуронидазы (GUS). Способ получение и анализ трансгенных клеточных линий описан в работе [11].
ДНК из каллусных культур выделяли по методике Делапорта [12] с определенными модификациями, концентрацию и чистоту определяли спектрофотометрически. Для амплификации ДНК конечный объем реакционной смеси составлял 25 мкл: 10 мM TRIS-HCl, 50 мM KCl, 1,5 мM хлорида магния, 2 мM каждого дезоксинуклеотидтрифосфата (дНТФ), 0,2 мкл праймера, 1 ед. акт. Taq ДНК полимеразы (Thermo Scientific) и 100-120 нг исследуемой ДНК. Амплификация проводилась по следующей программе: начальная денатурация при 94 °С 5 мин, 37 циклов (денатурация 94 °С - 30 с, отжиг 58 °С - 90 с, элонгация 72 °С - 2 мин) и финальная элонгация 72 °С 10 мин. Для проведения ПЦР был использован единичный праймер к LTR
M 1
ретротранспозона SIRE 1, имеющий следующую нуклеотидную последовательность: 5'-GCACTTATGCAAGTGGGATCAGC-3 [13]. Продукты амплификации разделяли методом электрофореза в 1,6% агарозном геле с добавлением бромистого этидия. Спектры продуктов ПЦР визуализировали под УФ лучами. Для оценки размеров ампликонов применяли маркер 100 bp DNA Ladder (Thermo Scientific). Размер продуктов ПЦР определяли с помощью пакета прикладных программ TotalLab v.2.01 (Nonlinear Dynamics) [14]. Для количественной оценки полученных результатов данные были представлены в виде бинарных матриц в которых наличие/отсутствие одинаковых по размеру ампликонов соответствовало значение 1 или 0. Проверку стабильности ПЦР реакции, осуществляли путем трехкратного повторения амплификации с одним и тем же праймером на том же растительном материале.
Известно, что в процессе совместной эволюции сформировались механизмы, защищающие геном хозяина от чужеродной транспозиции, в частности описано ее подавление на транскрипционном (сайленсинг путем метилирования ДНК) и посттранскрипционном (сайленсинг за счет РНК-интерференции) уровнях [15]. Поэтому в обычных условиях активность ретротранспозонов отсутствует или наблюдается на незначительном уровне [16]. В условиях эксперимента нам не удалось зафиксировать транспозицию у исходных и контрольных форм. В целом, у нетрансформированного первичного каллуса, а также каллуса 3-го и 6-го пассажей обнаружено 10 четких ампликонов, размером от 407 до 1360 п.н. У всех исследуемых объектов выявлен идентичный спектр продуктов ПЦР. На рис. 1 представлено по одному образцу из каждой исследуемой выборки.
-
2 3
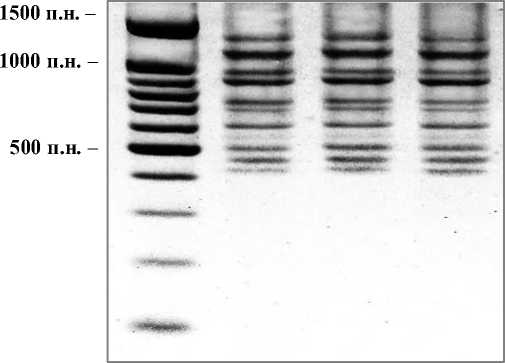
Рис. 1. Спектр продуктов амплификации ДНК контрольного нетрансформированного каллуса: М - маркер молекулярных масс (100 bp DNA Ladder), 1 – первичный каллус (0 пассаж); 2 - каллус 3 пассажа; 3 - каллус 6-го пассажа
Следующим этапом исследований было выявление полиморфизма ДНК у трансформированных форм. Для этого отбирали образцы каллусных линий LТ1-LТ7. Полученные результаты представлены на рис. 2.
М 1 2
3 4 5 6
1500 п.н. –
1000 п.н. –
500 п.н. –
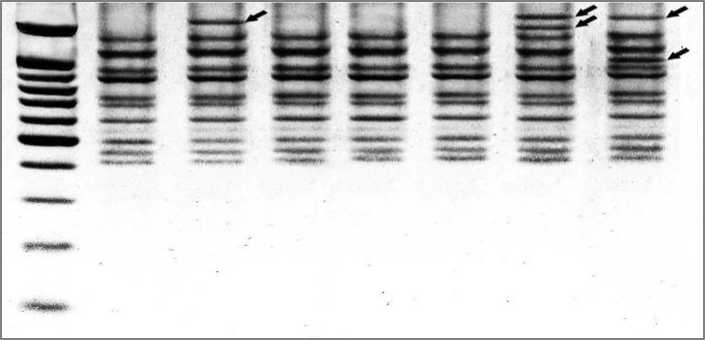
Рис. 2. Спектр продуктов амплификации ДНК трансформированных каллусных линий: М - маркер молекулярных масс (100 bp DNA Ladder), 1 - клеточная линия LТ1, 2 - клеточная линия LТ2, 3 - клеточная линия LТ3, 4 -клеточная линия LТ4, 5 - клеточная линия LТ5, 6 - клеточная линия LТ6, 7 - клеточная линия LТ7. Стрелками показаны новые ампликоны
На полученных электрофореграммах продуктов ПЦР каждый ампликон соответствует анонимному локусу между двумя близко расположенными копиями SIRE-1, поскольку применен праймер, родственный к LTR-последовательности, а общая длина этого ретротраспозона составляет около 12 тыс. п.н., что делает невозможным синтез фрагментов в пределах одной копии. Таким образом, каждый но- вый выявленный ампликон фиксирует возникновение нового межретранспозонного локуса, то есть свидетельствует о событии транспозиции. Нами отмечено появление новых, относительно высокомолекулярных (длиной более 1000 п.н.) ампликонов у трех трансгенных линий - LТ2, LТ6 и LТ7 (табл.). В частности, у двух последних обнаружено по два новых фрагмента.
Таблица. Длина новых, выявленых у трансгенных линий, ампликонов
|
Линия |
Количество новых ампликонов, шт. |
Длина амликона, п.н. |
|
LТ2 |
1 |
1567 |
|
LТ6 |
2 |
1491, 1660+* |
|
LТ7 |
2 |
1075, 1660+* |
Прим. * - При расчете длины ампликона на пакете прикладных программ TotalLab v.2.01 получено значение 1660 п.н. (линия LТ6) и 1651 п.н. (линия LТ7), однако поскольку разница между этими значениями меньше инструментальной погрешности метода (включающей разрешающую способность электрофоретического метода и погрешность вычисления), фрагменты нами условно обозначены как 1660+, что может свидетельствовать как об их идентичности, так и о несхожести по нуклеотидному составу (межретранспозонному локусу)
Появление нескольких новых ампликонов, а также то, что они были обнаружены у трех из семи исследуемых клеточных линий, может свидетельствовать об относительно высокой частоте события транспозиции в ДНК трансформированных клеточных линий. В исследуемых локусах, фланкированных LTR ретротранспозона SIRE-1, нами не выявлено точечных мутаций в сайтах связывания с праймером и/или делеций, которые могли бы приводить к исчезновению ампликона в ДНК- профилях ПЦР.
Следует отметить, что в литературе была описана транспозиционная активность ретротранспозонов Tos17 у трансгенных растений риса [4] и Tag1 у арабидопсиса [17]. Авторы также отмечают отсутствие такой активности у контрольных форм. Хотя использованный нами метод не позволяет непосредственно выявить транскрипционную и транспозиционную активность ретротранспозонов, однако он может быть быстрым и эффективным инструментом исследования изменений генома при генетической трансформации и подтверждения транспозиции МГЭ.
Таким образом, нами проведен молекулярногенетический анализ трансгенных клеточных линий мягкой пшеницы с использование IRAP ПЦР с праймером к LTR последовательности ретротранспозона SIRE 1. У трех трансформированных линий
-
- LТ2, LТ6 и LТ7 обнаружено появление новых, относительно высокомолекулярных (длиной более 1000 п.н.) ампликонов, что свидетельствует о транспозиции данного мобильного генетического элемента. Поскольку эти фрагменты отсутствовали в спектрах продуктов амплификации ДНК контрольного нетрансформированного каллуса, это дает основания считать индукцию транспозиции SIRE 1 связанной с геномным стрессом, вызванным встраиванием чужеродной ДНК (векторной конструкции pAHC25) или стрессом непосредственно связанным с процессом трансформации (микропоранение, культивирование на селективных средах).
-
1. Clive J. Global Status of Commercialized Biotech // GM Crops. 2011. ISAAA Brief. N. 43. P. 1-8.
-
2. Rakszegi M., Tamas S., Szucs P. et al. Current status of wheat transformation // J. Plant Biotechnology. 2001. V. 3. P. 67-81.
-
3. Gaspar T., Franck T., Bisbis B. et al. Concepts in plant stress physiology. Application to plant tissue cultures // Plant Growth Regul. 2002. V. 37. P. 263-285.
-
4. Wu R., Guo W.L., Wang X.R., et al. Unintended consequence of plant transformation: biolistic transformation caused transpositional activation of an endogenous retrotransposon Tos17 in rice ssp. japonica cv. Matsumae // Plant Cell Reports. 2009. V. 28. N 7. P. 1043-1051.
-
5. Lu B.R., Snow A.A. Gene flow from genetically modified rice and its environmental consequences // Bio. Sci. 2005. V. 55. P. 669–678.
-
6. Muller K., Heller H., Doerfier W . Foreign DNA integration. Genome-wide perturbations of methylation and transcription in the recipient genomes // J. Biol. Chem. 2001. V. 276. P. 14271-14278.
-
7. Matzke M.A., Mette M.F., Matzke A.J.M. Transgene silencing by the host genome defense: implications for the evolu-
tion of epigenetic control mechanisms in plants and vertebrates // Plant Mol. Biol. 2000. V. 43. P. 401-415.
-
8. Kumar A., Bennetzen J.L. Plant retrotransposons // Annu. Rev. Genet. 1999. V. 33. P. 479-532.
-
9. Бавол А.В., Дубровна О.В., Лялько І.І. Регенерація рослин із експлантів верхівки пагона проростків пшениці // Вісник Українського товариства генетиків і селекціоне-рів. 2007. Т .5. № 1-2. С. 3-10.
-
10. Christensen A.H., Quail P.H. Ubiquitin promoter-based vectors for high-level expression of selectable and/or screenable marker genes in monocotyledonous plants // Transgenic Res. 1996. V .5. N 3. Р. 213-218.
-
11. Бавол А.В., Моргун Б.В. Нітовська І.О., та ін. Генетична трансформація пшениці з використанням калюсних культур, отриманих з апікальної меристеми пагона // Дося-гнення і проблеми генетики, селекції та біотехнології: збірник наук. праць. 2012. Т .4. С. 411-416.
-
12. Delporte F., Mostadel O., Jacquemin J. Plant regeneration through callus initiation from thin mature embryo fragments of wheat // Plant Cell, Tissue and Organ Culture. 2001. V. 67. N 2. P. 73-80.
-
13. Календарь Р.В., Глазко В.И. Типы молекулярногенетических маркеров и их применение // Физиология и биохимия культурных растений. 2002. Т. 34. № 4. С. 279-296.
-
14. Nei M., Li W.H . Mathematical model for studying genetic variation in terms of restriction endonucleases // Proc. Natl. Acad. Sci. 1979. V. 76. Р. 5269-5273.
-
15. Casacuberta J.M., Santiago N. Plant LTR-retrotransposons and MITEs: control of transposition and impact on the evolution of plant genes and genomes // Gene. 2003. V. 311. P. 1-11.
-
16. Vicient C.M. Transcriptional activity of transposable elements in maize // BMC Genomics. 2010. V. 11. N. 601. P. 1-10.
-
17. Bhatt A.M., Lister C., Crawford N., Dean C. The transposition frequency of Tag1 elements is increased in transgenic Arabidopsis lines // Plant Cell. 1998. V. 10. P. 427–434.
ANALYSIS OF TRANAGENIC CELL LINES OF BREAD WHEAT USING IRAP PCR
Список литературы Молекулярно-генетический анализ трансгенных клеточных линий мягкой пшеницы с использованием IRAP ПЦР
- Clive J. Global Status of Commercialized Biotech//GM Crops. 2011. ISAAA Brief. N. 43. P. 1-8.
- Rakszegi M., Tamas S., Szucs P. et al. Current status of wheat transformation//J. Plant Biotechnology. 2001. V. 3. P. 67-81.
- Gaspar T., Franck T., Bisbis B. et al. Concepts in plant stress physiology. Application to plant tissue cultures//Plant Growth Regul. 2002. V. 37. P. 263-285.
- Wu R., Guo W.L., Wang X.R., et al. Unintended consequence of plant transformation: biolistic transformation caused transpositional activation of an endogenous retrotransposon Tos17 in rice ssp. japonica cv. Matsumae//Plant Cell Reports. 2009. V. 28. N 7. P. 1043-1051.
- Lu B.R., Snow A.A. Gene flow from genetically modified rice and its environmental consequences//Bio. Sci. 2005. V. 55. P. 669-678.
- Muller K., Heller H., Doerfier W. Foreign DNA integration. Genome-wide perturbations of methylation and transcription in the recipient genomes//J. Biol. Chem. 2001. V. 276. P. 14271-14278.
- Matzke M.A., Mette M.F., Matzke A.J.M. Transgene silencing by the host genome defense: implications for the evolution of epigenetic control mechanisms in plants and vertebrates//Plant Mol. Biol. 2000. V. 43. P. 401-415.
- Kumar A., Bennetzen J.L. Plant retrotransposons//Annu. Rev. Genet. 1999. V. 33. P. 479-532.
- Бавол А.В., Дубровна О.В., Лялько I.I. Регенерацiя рослин iз експлантiв верхiвки пагона проросткiв пшеницi//Вiсник Українського товариства генетикiв i селекцiонерiв. 2007. Т.5. № 1-2. С. 3-10.
- Christensen A.H., Quail P.H. Ubiquitin promoter-based vectors for high-level expression of selectable and/or screenable marker genes in monocotyledonous plants//Transgenic Res. 1996. V.5. N 3. Р. 213-218.
- Бавол А.В., Моргун Б.В. Нiтовська I.О., та iн. Генетична трансформацiя пшеницi з використанням калюсних культур, отриманих з апiкальної меристеми пагона//Досягнення i проблеми генетики, селекцiї та бiотехнологiї: збiрник наук. праць. 2012. Т.4. С. 411-416.
- Delporte F., Mostadel O., Jacquemin J. Plant regeneration through callus initiation from thin mature embryo fragments of wheat//Plant Cell, Tissue and Organ Culture. 2001. V. 67. N 2. P. 73-80.
- Календарь Р.В., Глазко В.И. Типы молекулярно-генетических маркеров и их применение//Физиология и биохимия культурных растений. 2002. Т. 34. № 4. С. 279-296.
- Nei M., Li W.H. Mathematical model for studying genetic variation in terms of restriction endonucleases//Proc. Natl. Acad. Sci. 1979. V. 76. Р. 5269-5273.
- Casacuberta J.M., Santiago N. Plant LTR-retrotransposons and MITEs: control of transposition and impact on the evolution of plant genes and genomes//Gene. 2003. V. 311. P. 1-11.
- Vicient C.M. Transcriptional activity of transposable elements in maize//BMC Genomics. 2010. V. 11. N. 601. P. 1-10.
- Bhatt A.M., Lister C., Crawford N., Dean C. The transposition frequency of Tag1 elements is increased in transgenic Arabidopsis lines//Plant Cell. 1998. V. 10. P. 427-434.


